亚胺是含有碳氮双键的有机化合物,可以通过还原、加成、缩合、环化、氮杂环化等有机反应获得,目前被广泛应用于制药、香料、染料和杀虫剂等行业[1-3]。N-苄叉苯胺作为一种极具代表性的亚胺化合物,在制药、化妆以及食品添加剂等领域均有重要应用[4-5]。为满足化学、化工等行业对N-苄叉苯胺日益增长的需求,需要开发一种低成本、高效的合成方法来合成N-苄叉苯胺。当前,通过将苯甲醇与苯胺进行氧化偶联反应(醇胺偶联法)来制备N-苄叉苯胺的方法吸引了研究者的广泛关注[6-7]。该方法具有反应物易得、反应条件温和、反应迅速和环境友好等优点。醇胺偶联法制备N-苄叉苯胺的关键在于研发一种具有高活性的多相催化剂。在众多材料当中,锰基催化剂在苯甲醇与苯胺偶联制备N-苄叉苯胺的反应中表现出潜在的催化活性[8-9]。因此,研究一种制备方法简单、成本低廉,并在醇胺偶联反应中具有高活性的锰基催化剂具有重要意义。
锰基催化剂在醇胺氧化偶联反应中的催化活性主要取决于其提供的表面活性位数量以及氧化能力。研究结果表明,铁物种的引入可以显著改善锰基材料的氧化能力,并提高其晶格氧的迁移能力[10-12]。例如,Zhao等[10]的研究结果表明,将Fe引入至Mn/γ-Al2O3中,可以增大Mn/γ-Al2O3的比表面积以及Mn3+的相对含量,而且Fe3+和Mn3+在催化剂表面的共存也有利于氧物种的迁移,从而提升其催化分解甲苯的活性。Li等[12]利用氧化还原反应制备了一种介孔氧化锰铁氧化物,结果表明,相较于MnOx和Fe2O3,MnxFeOy-70具有更强的氧化能力,这使其在完全氧化苯的催化反应中表现出更强的催化活性。Said等[11]通过在α-MnO2结构中掺杂Fe3+,提高了其选择性催化氧化苯甲醇制苯甲醛的活性,这是由于Fe3+的掺杂提高了α-MnO2的晶格氧活性。根据以上研究结果的启发,在锰基材料的结构中引入铁离子(如Fe3+),有助于提高其在醇胺氧化偶联反应中的催化活性。
本文采用共沉淀法制备了锰铁双金属氧化物,并将其应用于醇胺偶联法制备N-苄叉苯胺,研究了锰源与铁源的投料比对产物催化活性的影响。通过多种表征方式,研究了所得产物的晶体结构、形貌,并探讨了催化剂的相关物化性质与其醇胺偶联法制备N-苄叉苯胺性能之间的关系。
1 实验部分 1.1 催化剂的制备依次向烧杯中加入a mmol的Mn(CH3COO) 2、b mmol的Fe(NO3) 3•9H2O和50 mL的去离子水,在匀速搅拌1 h之后,向混合溶液中逐滴滴加NH3•H2O至pH = 9.0后,再继续搅拌5 h,然后将沉淀进行抽滤分离,并用大量去离子水冲洗,直至滤液为中性,最后将所得沉淀转移至烘箱中恒温(100 ℃)干燥24 h,即可得到目标产物,将化学式简写为MnaFebOx(a与b之和为20 mmol),将锰源与铁源的投料比(即a与b的比值)为9:1、7:3、1:1、3:7和1:9所制备的产物分别命名为Mn0.9Fe0.1Ox、Mn0.7Fe0.3Ox、Mn0.5Fe0.5Ox、Mn0.3Fe0.7Ox和Mn0.1Fe0.9Ox;将a = 0 mmol、b = 20 mmol和a = 20 mmol、b = 0 mmol所得到的产物分别命名为Mn0Fe1Ox和Mn1Fe0Ox。此外,将等摩尔量的Mn1Fe0Ox和Mn0Fe1Ox进行物理研磨后得到的样品命名为Mn0.5Fe0.5Ox-M,其中,控制Mn1Fe0Ox 中Mn的摩尔量与Mn0Fe1Ox中Fe的摩尔量相等。
1.2 物化性质表征采用广角X射线衍射仪(XRD,荷兰帕纳科)分析产物的物相,管电流和管电压分别设置为15 mA和40 kV;采用场发射扫描电子显微镜(FESEM,日立)与场发射透射电子显微镜(FETEM,德国赛默飞)研究产物的形貌与微观结构;采用全自动比表面积及孔隙分析仪(美国康塔)测定样品的N2吸−脱附等温线以及孔径分布曲线;采用X射线光电子能谱(XPS,德国赛默飞)表征材料的表面化学性质;采用化学吸附仪(美国麦克)进行样品的氢气程序升温还原测试(H2-TPR)。
1.3 催化活性测试催化反应测试在三颈烧瓶(装有冷凝管)中进行,分别在三颈烧瓶中加入30 mg样品、10 mL甲苯、158 μL苯甲醇、92 μL苯胺和 230 μL十二烷(内标物)。反应条件:反应温度为90 ℃(空气氛围),反应时间为30 h。待反应结束后,使用注射器抽取200 μL上层清液,并用甲苯稀释至2 mL。采用配备有氢火焰离子化检测器的气相色谱仪(Agilent 7890A型)对产物进行定量分析。
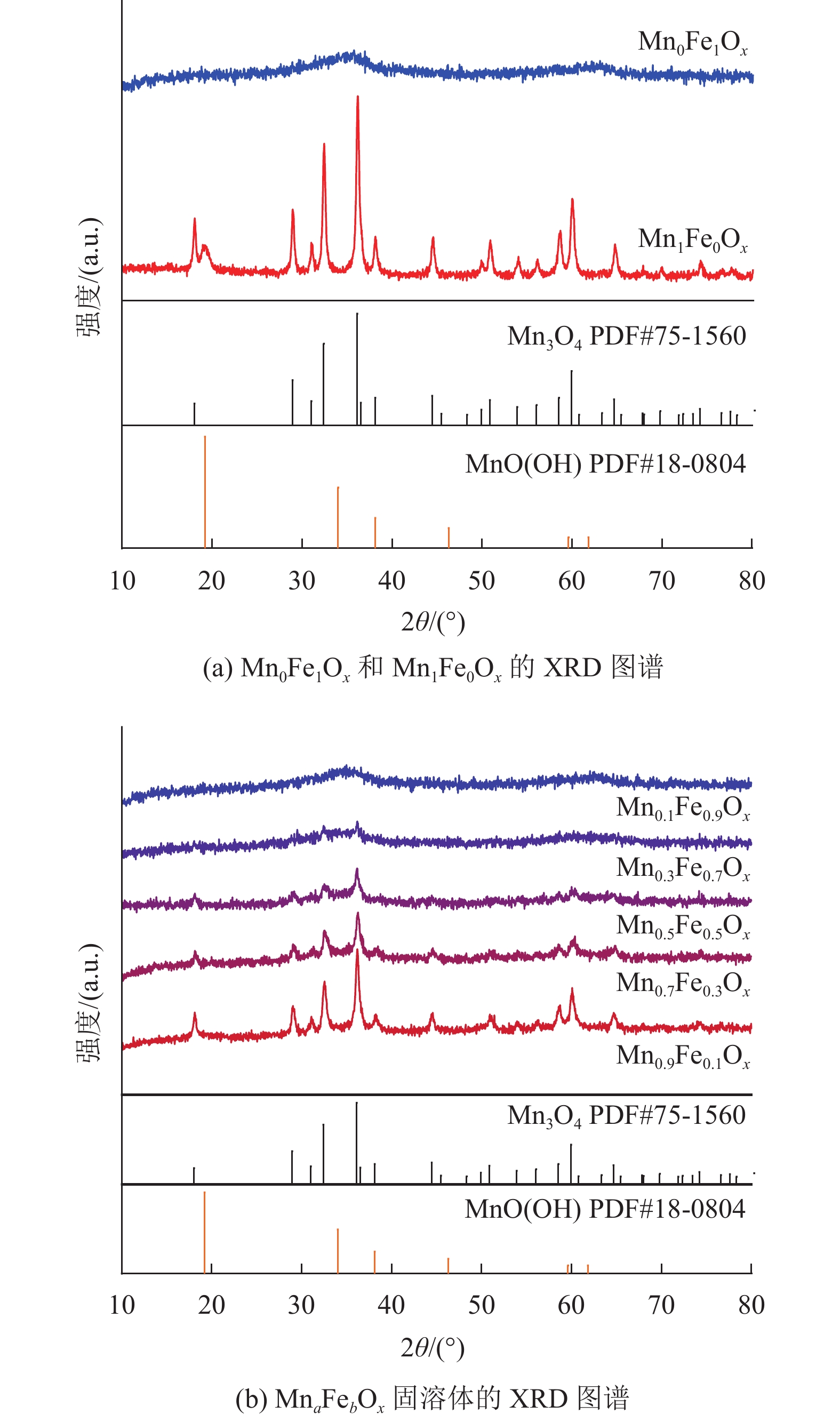
2 结果与讨论 2.1 物相分析采用XRD研究不同的Mn/Fe投料比对产物晶相的影响。如图1(a) 所示,当不加入锰盐时(即a = 0 mmol,b = 20 mmol),Mn0Fe1Ox的XRD谱图在35°左右出现一个大包峰,其强度较弱,峰形较宽,这表明Mn0Fe1Ox为无定形结构;当不加入铁盐时(即a = 20 mmol,b = 0 mmol),Mn1Fe0Ox的XRD谱图可以观察到明显的衍射峰,其中,19.2°的衍射峰对应MnOOH的(002)晶面(JCPDS 18-0804),其他位置的衍射峰均与Mn3O4的标准卡(JCPDS 75-1560)相匹配,这说明产物的主要组分为Mn3O4。如图1(b) 所示,当投料比为9:1时,Mn0.9Fe0.1Ox为纯的Mn3O4结构,但是其结晶性较Mn1Fe0Ox弱;当增加铁盐的加入量时(即投料比为7:3和1:1),Mn0.7Fe0.3Ox和Mn0.5Fe0.5Ox仍均为纯的Mn3O4结构,并且其结晶性进一步减弱;当继续增加铁盐的加入量(即投料比为3:7和1:9),Mn0.3Fe0.7Ox和Mn0.1Fe0.9Ox已无明显的Mn3O4衍射峰,而是在35°附近出现一个较弱的宽峰,这2个样品的图谱与Mn0Fe1Ox的XRD结果一致。以上结果表明,Fe3+对Mn2+的沉淀反应具有较大影响,在额外加入铁盐之后,Fe3+可以进入Mn3O4的晶格,从而影响产物的结构与结晶性。随着Fe3+加入量的提高,产物的结晶性不断变弱,这有助于其形成丰富的表面氧空位,从而有利于多相催化反应的进行[13]。
|
图 1 不同催化剂的广角 XRD图谱 Figure 1 Wide-angle XRD patterns of different catalysts |
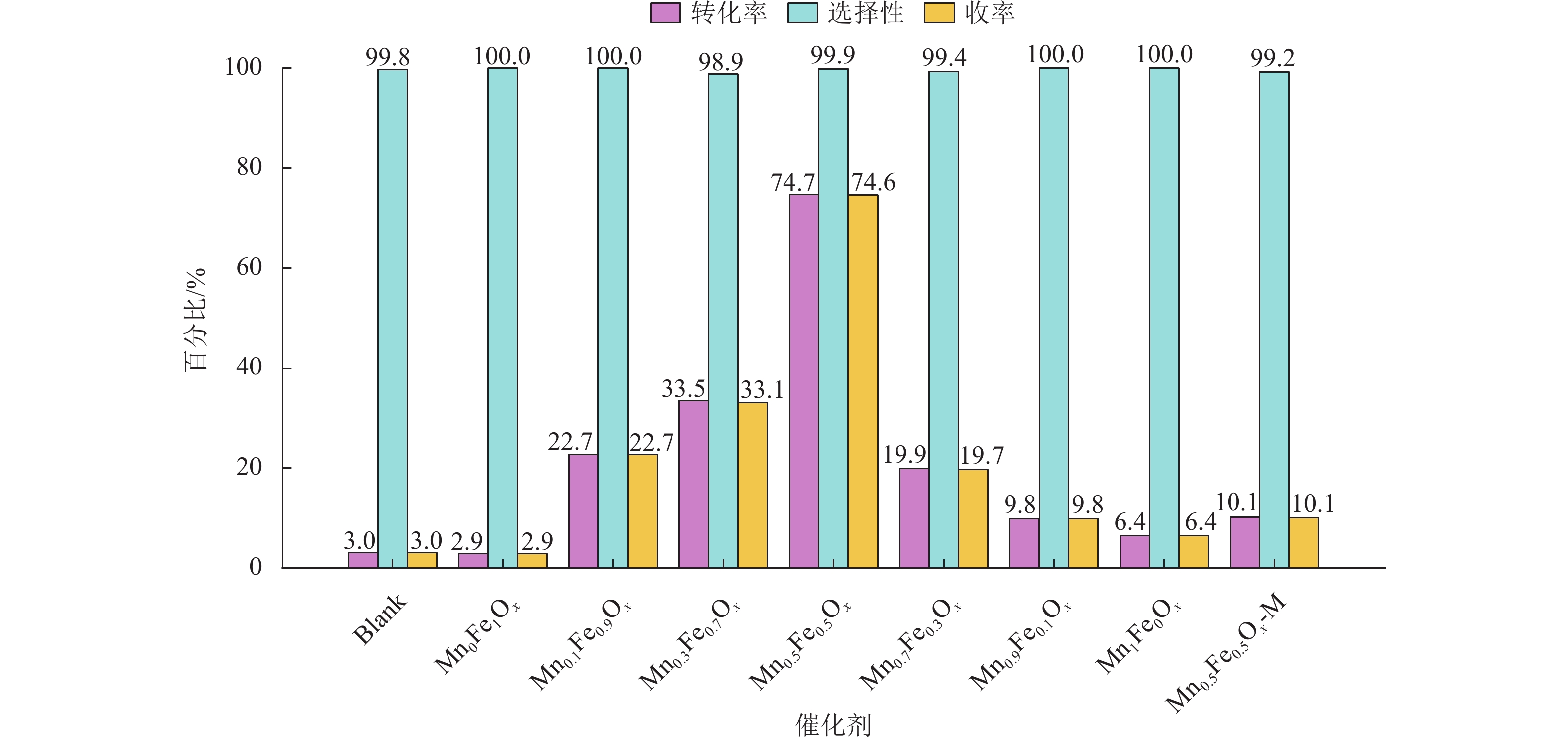
将所得产物应用于苯甲醇与苯胺氧化偶联合成N-苄叉苯胺的催化反应,其结果如图2所示。测试结果表明,所有测试组别均对该催化反应表现出较高的选择性(≥ 98.9%),这表明N-苄叉苯胺的收率与苯胺的转化率几乎一致,因此,后续比较催化反应活性时以N-苄叉苯胺的收率作为标准。
|
图 2 不同催化剂对苯甲醇与苯胺氧化偶联的催化性能 Figure 2 Catalytic performance of different catalysts for oxidative coupling of benzyl alcohol with aniline |
首先,无催化剂时的N-苄叉苯胺收率为3%,这说明在不加入催化剂的情况下,苯甲醇与苯胺氧化偶联合成N-苄叉苯胺的反应难以自发进行。在加入催化剂之后,只存在单一金属组分的Mn0Fe1Ox和Mn1Fe0Ox的N-苄叉苯胺收率分别为2.9%与6.4%,而存在锰、铁双组分的样品的N-苄叉苯胺收率均大于Mn0Fe1Ox和Mn1Fe0Ox的收率。进一步研究发现,锰铁双金属氧化物的N-苄叉苯胺收率随着铁源加入量的增大而提高,当铁源加入量大于锰源加入量时,催化剂的N-苄叉苯胺收率开始下降,其中,投料比为1:1时所制备的Mn0.5Fe0.5Ox样品的收率最高(74.6%)。此外,通过物理混合所得到的Mn0.5Fe0.5Ox-M样品的N-苄叉苯胺收率仅有10.1%。
由上述结果可知,铁源的加入可以显著提高催化剂(即锰铁双金属氧化物)的醇胺氧化偶联反应的催化活性,这表明锰离子和铁离子在催化反应过程中存在协同催化作用,从而可以显著提高N-苄叉苯胺的收率[14-15]。另外,与结晶性更强的Mn0.9Fe0.1Ox和Mn0.7Fe0.3Ox相比,Mn0.5Fe0.5Ox的N-苄叉苯胺收率更大,这是由于Mn0.5Fe0.5Ox具有更丰富的表面缺陷以及表面活性氧物种,从而更有利于促进其对反应物分子的吸附与活化[16-17]。
2.3 形貌与微观结构由于Mn0.5Fe0.5Ox具有最佳的催化反应活性,因此,本文在后续研究中将以Mn0.5Fe0.5Ox样品为主要研究对象。图3(a)和(b)为Mn0.5Fe0.5Ox的FESEM图。从图3(a) 中可以看出,Mn0.5Fe0.5Ox具有规整的球状形貌,其粒径约为1.3 μm。通过高倍数的FESEM图可以看出(见图3(b)),Mn0.5Fe0.5Ox微球具有粗糙的表面,其表面由大量纳米颗粒堆积组成,其直径较为均一,约为20 nm。

|
图 3 Mn0.5Fe0.5Ox催化剂的场发射扫描电镜图 Figure 3 Field emission scanning electron microscope image of the Mn0.5Fe0.5Ox catalyst |
通过FETEM研究Mn0.5Fe0.5Ox 微球中Mn、Fe这两种元素的分布情况,如图4所示。图4(a)为Mn0.5Fe0.5Ox样品的高角度环形暗场像。图4(b)和(c)的结果表明,Mn和Fe这两种元素在Mn0.5Fe0.5Ox微球中分布较为均匀,这有利于Mn0.5Fe0.5Ox表面活性位点的均匀分散。

|
图 4 Mn0.5Fe0.5Ox 催化剂的高角环形暗场像及 Mn、Fe元素分布图 Figure 4 High-angle annular dark field image and Mn, Fe element distribution of the Mn0.5Fe0.5Ox catalyst |
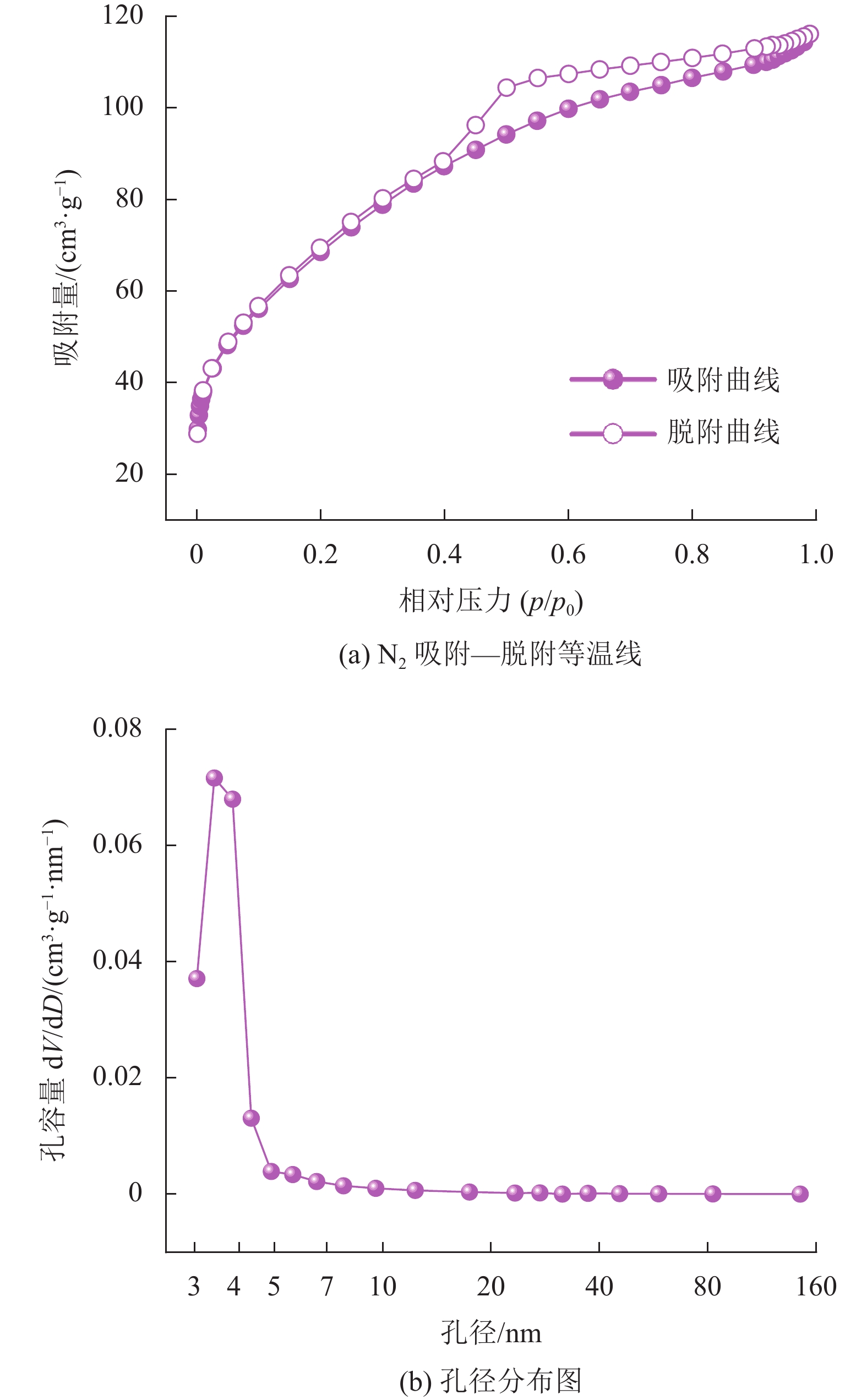
Mn0.5Fe0.5Ox的N2吸−脱附等温曲线和孔径分布如图5所示。根据国际纯粹与应用化学联合会的分类标准,Mn0.5Fe0.5Ox的N2吸−脱附等温曲线为IV型等温线(见图5(a)),这表明Mn0.5Fe0.5Ox具有介孔结构。Mn0.5Fe0.5Ox的孔径分布图(见图5(b))表明其平均孔径约为3.4 nm。此外,通过Brunauer-Emmett-Teller(BET)容量法可算出Mn0.5Fe0.5Ox的比表面积为287.5 m2/g。Mn0.5Fe0.5Ox的高比表面积和介孔结构有利于其暴露更多的活性位点,从而使其在醇胺偶联反应中获得更优异的催化活性。
|
图 5 Mn0.5Fe0.5Ox 催化剂的N2吸附-脱附等温线及孔径分布图 Figure 5 Isotherms of nitrogen adsorption-desorption and pore diameter distribution of the Mn0.5Fe0.5Ox catalyst |
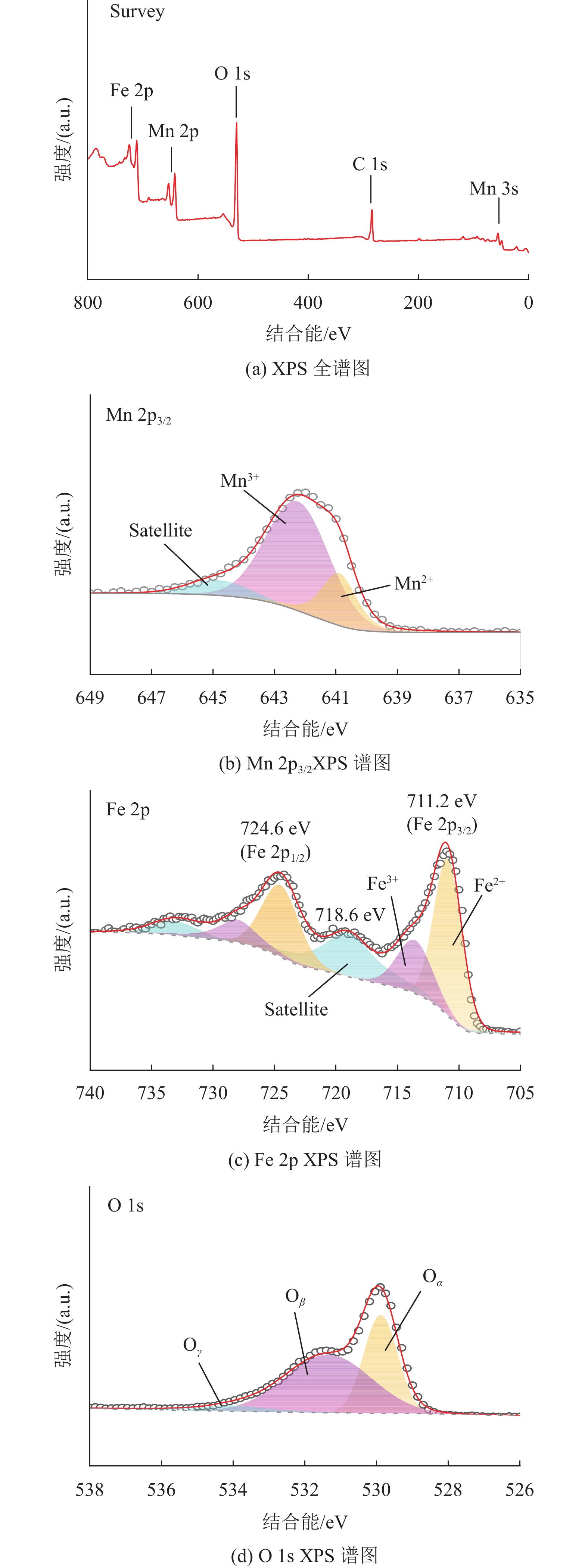
采用XPS分析Mn0.5Fe0.5Ox样品表面的元素种类及价态,结果如图6所示。图6(a) 为Mn0.5Fe0.5Ox的XPS全谱图,从该图可以看出,除了284.8 eV处是用于荷电校正的碳峰外,在54.0、530.1、642.1和711.2 eV处分别观察到归属于Mn 3s、O 1s、Mn 2p和Fe 2p的特征峰,这确认了Mn0.5Fe0.5Ox存在锰、铁和氧3种元素。
|
图 6 Mn0.5Fe0.5Ox 催化剂的的XPS谱图 Figure 6 XPS patterns of the Mn0.5Fe0.5Ox catalyst |
图6(b) 是Mn0.5Fe0.5Ox样品Mn 2p3/2的XPS谱图。通过对该谱图进行分峰拟合,可以在640.9,642.3和644.8 eV这3处得到3个子峰,并依次归属为Mn2+、Mn3+和卫星峰[18]。根据各自峰面积的计算结果可知,Mn0.5Fe0.5Ox样品中的Mn2+和Mn3+的相对摩尔含量分别为23.89%和76.11%,即Mn3+的相对摩尔含量是Mn2+的3.19倍,因此,Mn0.5Fe0.5Ox表面具有丰富的Mn3+物种。图6(c) 为Mn0.5Fe0.5Ox样品的Fe 2p谱图。通过该图可以发现,Mn0.5Fe0.5Ox的Fe 2p谱图在711.2 eV和724.6 eV处出现2个主峰,分别对应Fe 2p3/2和Fe 2p1/2的两种自旋轨道[19]。另外,在718.6 eV和733.3 eV处出现2个次峰,均属于Fe 2p的卫星峰。Fe 2p3/2可以分为2个子峰,710.9 eV的子峰归于Fe2+,713.7 eV的子峰归于Fe3+。通过比较Fe2+和Fe3+的峰面积可知,Mn0.5Fe0.5Ox样品中的Fe3+/Fe2+的比例为44.8%。Mn0.5Fe0.5Ox结构中具有丰富的变价的锰物种(Mn3+/Mn2+)和铁物种(Fe3+/Fe2+),这有利于醇胺偶联反应过程中的电子转移。
图6(d) 是Mn0.5Fe0.5Ox样品O 1s的XPS谱图。该光谱可以拟合出3个氧物种,分别位于529.9,531.4,和534.3 eV,依次归属为晶格氧(Oα)、表面吸附氧(Oβ)和表面吸附水(Oγ)[20-21]。利用氧物种的峰面积计算可知,Oβ/(Oα+Oβ) 的比值为59.9%,这表明Mn0.5Fe0.5Ox样品具有丰富的表面吸附氧。通过脱氢作用,表面吸附氧可以将苯甲醇氧化为苯甲醛[22],从而促进醇胺偶联反应的进行。因此,丰富的表面吸附氧物种可以显著提升Mn0.5Fe0.5Ox 的催化反应活性。
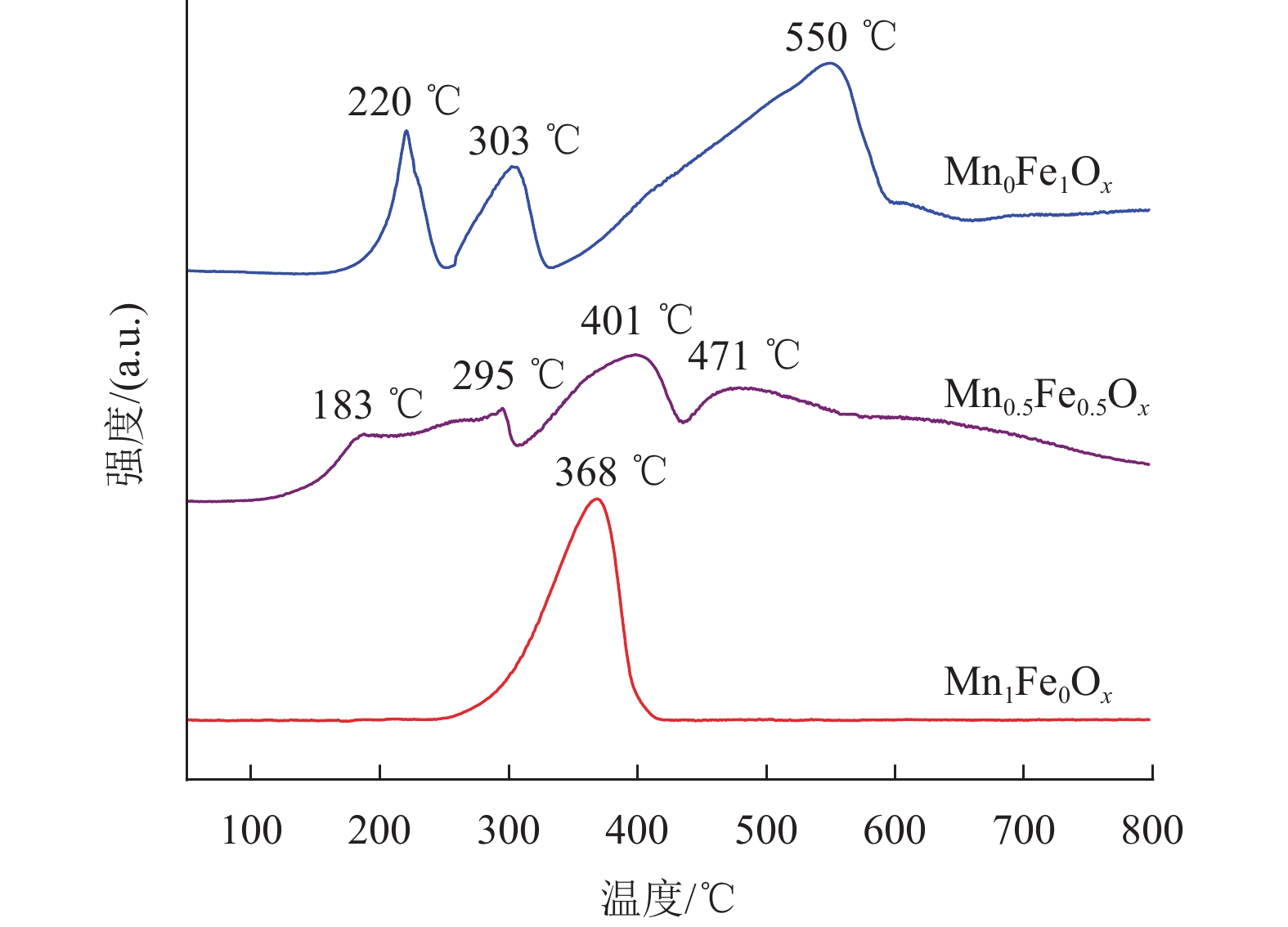
采用H2-TPR比较了Mn0.5Fe0.5Ox、Mn1Fe0Ox和Mn0Fe1Ox这3个样品的氧化能力,结果如图7所示。催化剂的低温还原峰温度顺序为:Mn0.5Fe0.5Ox < Mn0Fe1Ox < Mn1Fe0Ox。
|
图 7 催化剂的H2-TPR曲线 Figure 7 H2-TPR curves of the catalysts |
Mn1Fe0Ox样品在368 ℃处出现唯一的还原峰,该还原峰可归因于Mn3O4被还原为 MnO的过程[23]。Mn0Fe1Ox样品分别在220、303和550 ℃处出现3个还原峰,此结果与Fe2O3被还原为Fe单质的路径相对应,这表明无定型Mn0Fe1Ox的被还原过程为Fe2O3 → Fe3O4 → FeO → Fe [24]。与Mn1Fe0Ox和Mn0Fe1Ox的H2-TPR曲线相比,Mn0.5Fe0.5Ox的结果发生了明显变化,其H2-TPR曲线具有4个还原峰。首先,Mn0.5Fe0.5Ox样品在183 ℃和295 ℃处出现2个峰,可归因于Fe2O3 → Fe3O4 → FeO的还原过程;其次,在401 ℃出现的还原峰对应Mn3O4被还原为MnO的过程;最后,在471 ℃处出现的还原峰可归因为FeO → Fe。
以上结果表明,Mn0.5Fe0.5Ox较Mn1Fe0Ox和Mn0Fe1Ox具有更低的低温还原峰,这表明Mn0.5Fe0.5Ox具有更强的氧化能力,这与其催化反应测试的结果一致。由于Mn0.5Fe0.5Ox结构中的锰离子和铁离子之间的相互作用提高了其氧化能力和晶格氧的流动性,从而显著降低了其低温可还原温度,这有助于提高Mn0.5Fe0.5Ox在醇胺偶联反应中的催化活性 [25]。
3 结论本文采用共沉淀法制备出不同锰铁比的介孔锰铁双金属氧化物,并比较了其在醇胺氧化偶联合成亚胺反应中的催化活性。采用XRD、FESEM、FETEM、N2吸−脱附、XPS和H2-TPR分析了介孔锰铁双金属氧化物的物化性质。研究结果表明,Fe3+的加入对锰铁双金属氧化物的结晶性具有重要影响,提高Fe3+加入量可以降低产物的结晶度,这有助于其表面形成丰富的氧空位。与其他制备的铁锰双金属氧化物相比,Mn0.5Fe0.5Ox具有最佳的催化活性,这是因为其具有丰富的介孔结构和表面吸附氧物种,以及优良的氧化能力。
| [1] |
WANG Y, ZHANG Q, LI F, et al. Donor/acceptor maleimide and itaconimide dyes: synthesis, fluorescence and electrochemical properties[J].
Dyes and Pigments, 2020, 172: 107823.
DOI: 10.1016/j.dyepig.2019.107823. |
| [2] |
HAN Y, XING K, ZHANG J, et al. Application of sulfoximines in medicinal chemistry from 2013 to 2020[J].
European Journal of Medicinal Chemistry, 2021, 209: 112885.
DOI: 10.1016/j.ejmech.2020.112885. |
| [3] |
SU S, CHEN L, HAO L, et al. Preparation of p-amino salicylic acid-modified polysuccinimide as water-based nanocarriers for enhancing pesticide stability and insecticidal activity[J].
Colloids and Surfaces B:Biointerfaces, 2021, 207: 111990.
DOI: 10.1016/j.colsurfb.2021.111990. |
| [4] |
GUO X, LI M, ZHAO P, et al. Vanadium doped OMS-2 catalysts for one-pot synthesis of imine from benzyl alcohol and aniline: effects of vanadium content and precursor[J].
Catalysis Communications, 2022, 172: 106540.
DOI: 10.1016/j.catcom.2022.106540. |
| [5] |
MA J, YU X, LIU X, et al. The preparation and photocatalytic activity of Ag-Pd/g-C3N4 for the coupling reaction between benzyl alcohol and aniline[J].
Molecular Catalysis, 2019, 476: 110533.
DOI: 10.1016/j.mcat.2019.110533. |
| [6] |
OLIVEIRA R L, LEDWA K A, CHERNYAYEVA O, et al. Cerium oxide nanoparticles confined in doped mesoporous carbons: a strategy to produce catalysts for imine synthesis[J].
Inorganic Chemistry, 2023, 62(33): 13554-13565.
DOI: 10.1021/acs.inorgchem.3c01985. |
| [7] |
ALCAMAND H A, OLIVEIRA H D S, BALENA J G, et al. Synthesis, characterization, and use of nanocast LaMnO3 perovskites in the catalytic production of imine by the gas-phase oxidative coupling of benzyl alcohol to aniline[J].
Catalysis Communications, 2023, 175: 106606.
DOI: 10.1016/j.catcom.2023.106606. |
| [8] |
CHEN F, YANG T, ZHAO S, et al. Highly selective oxidation of amines to imines by Mn2O3 catalyst under eco-friendly conditions[J].
Chinese Chemical Letters, 2019, 30(12): 2282-2286.
DOI: 10.1016/j.cclet.2019.09.007. |
| [9] |
WU S, ZHANG H, CAO Q, et al. Efficient imine synthesis via oxidative coupling of alcohols with amines in an air atmosphere using a mesoporous manganese-zirconium solid solution catalyst[J].
Catalysis Science & Technology, 2021, 11(3): 810-822.
|
| [10] |
QIN L, HUANG X, ZHAO B, et al. Iron oxide as a promoter for toluene catalytic oxidation over Fe-Mn/γ-Al2O3 catalysts[J].
Catalysis Letters, 2020, 150(3): 802-814.
DOI: 10.1007/s10562-019-02975-5. |
| [11] |
SAID S, RIAD M. Oxidation of benzyl alcohol through eco-friendly processes using Fe-doped cryptomelane catalysts[J].
Solid State Sciences, 2019, 94: 145-154.
DOI: 10.1016/j.solidstatesciences.2019.05.020. |
| [12] |
CHEN C, LI Y, YANG Y, et al. Unique mesoporous amorphous manganese iron oxide with excellent catalytic performance for benzene abatement under UV-vis-IR and IR irradiation[J].
Environmental Science:Nano, 2019, 6: 1233-1245.
DOI: 10.1039/C9EN00180H. |
| [13] |
YANG S, QI Z, WEN Y, et al. Generation of abundant oxygen vacancies in Fe doped δ-MnO2 by a facile interfacial synthesis strategy for highly efficient catalysis of VOCs oxidation[J].
Chemical Engineering Journal, 2023, 452(4): 139657.
|
| [14] |
WEN Z, LU J, ZHANG Y, et al. Simultaneous oxidation and immobilization of arsenite from water by nanosized magnetic mesoporous iron manganese bimetal oxides (Nanosized-MMIM) : synergistic effect and interface catalysis[J].
Chemical Engineering Journal, 2020, 391: 123578.
DOI: 10.1016/j.cej.2019.123578. |
| [15] |
MASTALIR M, GLATZ M, GORGAS N, et al. Divergent coupling of alcohols and amines catalyzed by isoelectronic hydride Mn-I and Fe-II PNP pincer complexes[J].
Chemistry-a European Journal, 2016, 22(35): 12316-12320.
DOI: 10.1002/chem.201603148. |
| [16] |
HUANG N, QU Z, DONG C, et al. Superior performance of α@β-MnO2 for the toluene oxidation: active interface and oxygen vacancy[J].
Applied Catalysis A:General, 2018, 560: 195-205.
DOI: 10.1016/j.apcata.2018.05.001. |
| [17] |
LI P, ZHAN S, YAO L, et al. Highly porous alpha-MnO2 nanorods with enhanced defect accessibility for efficient catalytic ozonation of refractory pollutants[J].
Journal of Hazardous Materials, 2022, 437: 129235.
DOI: 10.1016/j.jhazmat.2022.129235. |
| [18] |
ZHANG C, CAO Y, WANG Z, et al. Insights into the sintering resistance of sphere-like Mn2O3 in catalytic toluene oxidation: effect of manganese salt precursor and crucial role of residual trace sulfur[J].
Industrial & Engineering Chemistry Research, 2022, 61(19): 6414-6426.
|
| [19] |
TAHIR A A, WIJAYANTHA K U, SAREMI-YARAHMADI S, et al. Nanostructured α-Fe2O3 thin films for photoelectrochemical hydrogen generation[J].
Chemistry of Materials, 2009, 21(16): 3763-3772.
DOI: 10.1021/cm803510v. |
| [20] |
QIU J, WANG W, WANG J, et al. Efficient monolithic MnOx catalyst prepared by heat treatment for ozone decomposition[J].
Environmental Science and Pollution Research, 2022, 29: 44324-44334.
DOI: 10.1007/s11356-021-18261-0. |
| [21] |
LIU Y, ZHANG P. Catalytic decomposition of gaseous ozone over todorokite-type manganese dioxides at room temperature: effects of cerium modification[J].
Applied Catalysis A:General, 2017, 530: 102-110.
DOI: 10.1016/j.apcata.2016.11.028. |
| [22] |
SHI J, QI T, SUN B-C, et al. Catalytic oxidation of benzyl alcohol over MnO2: structure-activity description and reaction mechanism[J].
Chemical Engineering Journal, 2022, 440: 135802.
DOI: 10.1016/j.cej.2022.135802. |
| [23] |
WANG H, CHEN H, WANG Y, et al. Performance and mechanism comparison of manganese oxides at different valence states for catalytic oxidation of NO[J].
Chemical Engineering Journal, 2019, 361: 1161-1172.
DOI: 10.1016/j.cej.2018.12.159. |
| [24] |
ALBRECHT M, RODEMERCK U, SCHNEIDER M, et al. Unexpectedly efficient CO2 hydrogenation to higher hydrocarbons over non-doped Fe2O3[J].
Applied Catalysis B:Environmental, 2017, 204: 119-126.
DOI: 10.1016/j.apcatb.2016.11.017. |
| [25] |
QIN J, LONG Y, GOU G, et al. Tuning effect of amorphous Fe2O3 on Mn3O4 for efficient atom-economic synthesis of imines at low temperature: improvingtransfer cycle of Mn3+/Mn2+ in Mn3O4[J].
Catalysis Science & Technology, 2020, 10: 5628-5640.
|
 2023, Vol. 40
2023, Vol. 40

