乙烯是世界上产量最大的化学品之一,其产量是衡量一个国家石油化工发展水平的重要标杆之一[1]。由于乙烷储量较大,且价格较低,其已成为制备乙烯的主要原料之一[2]。使用乙烷作为原料制备乙烯的传统方法主要有以下两种:乙烷蒸汽裂解法和乙烷氧化催化脱氢法[3]。这两种方法的乙烷转化率和乙烯的生成率都较高[4-5],但也存在一些亟需解决的问题,如反应受到热力学平衡限制、工作温度较高、能耗大、大量排放二氧化碳及存在积碳等[6]。
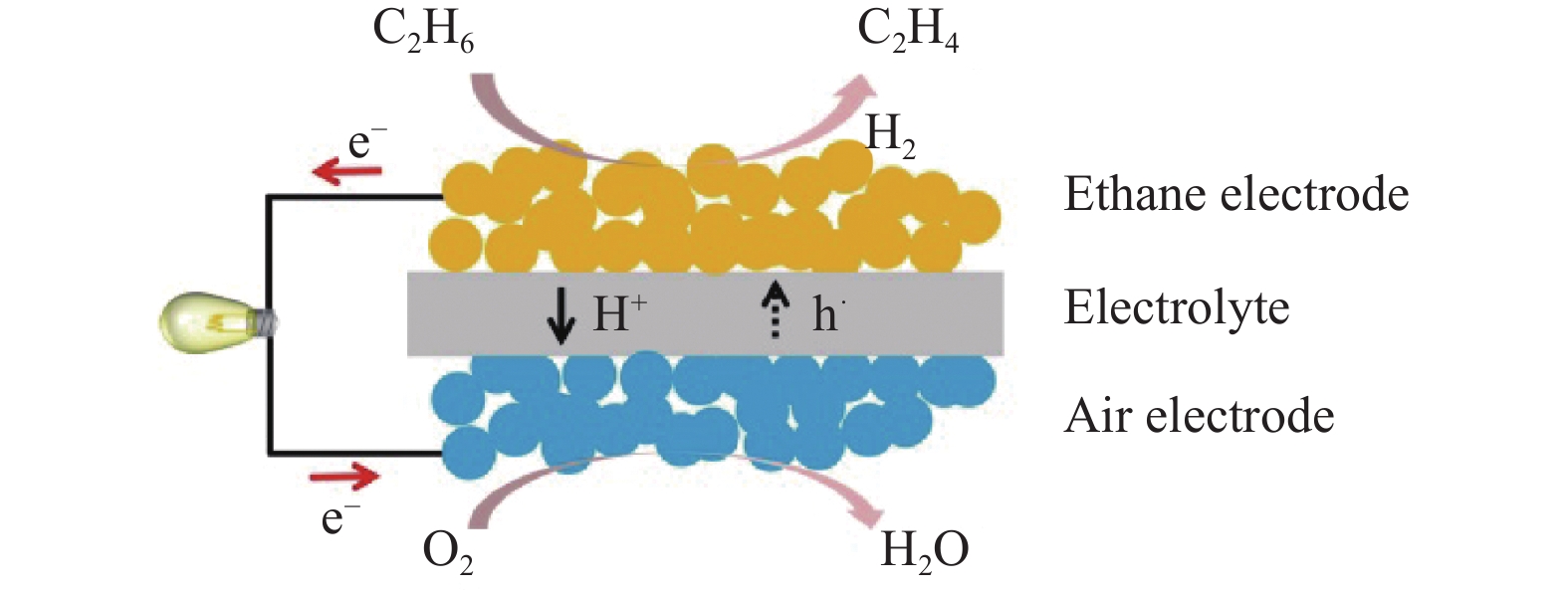
相比于传统的制备方法,基于质子导体固体氧化物燃料电池(H-SOFCs) 的电化学法制备乙烯不受热力学平衡限制且具有能耗低和环保的特点,因此该方法具有较大的发展前景,是目前的研究热点[6-7]。基于H-SOFCs制备乙烯的工作原理如图1所示。在乙烷电极侧通入乙烷,随后被热分解生成乙烯和氢气,乙烯被收集利用,而氢气被电化学氧化生成质子及电子。生成的质子穿过电解质层到达空气电极侧,随后与氧气反应生成水,电子通过外电路由乙烷电极传输至空气电极,向外部负载提供电能。
|
图 1 基于质子导体固体氧化物燃料电池制备乙烯的原理图 Figure 1 Schematic of ethylene production based on proton conducting solid oxide fuel cells |
基于H-SOFCs制备乙烯的研究主要聚焦在电解质材料和乙烷电极催化剂材料。Luo课题组[8]研究了Y掺杂的BaCeO3,发现Y的掺杂量为15%时,合成的电解质BaCe0.85Y0.15O3-δ(BCY15) 电化学性能最好。为了提高电解质材料的质子电导率及在二氧化碳气氛中的化学稳定性,Lin等[9]研究了Y、Nd、Zr多元掺杂BaCeO3。
乙烷电极催化剂材料的催化活性也会影响电池H-SOFCs的性能。前期,科研工作者使用Pt作为催化剂材料。Pt金属虽然具有较好的催化活性,但是其价格较昂贵,性价比不高[8, 10]。因此,研究者开始寻找催化活性好且性价比高的乙烷电极催化剂。2011年,Luo课题组[11]使用纳米颗粒Cr2O3作为乙烷电极催化剂,发现该材料的抗焦化能力可与Pt金属媲美,催化活性也较高,是Pt金属的理想替代品。随后,该课题组围绕Cr金属展开了一系列的研究,如研究了Cu-Cr2O3[12]、Cr3C2[13]、FeCr2O4[10]、Co2CrO4[14]等,使得乙烷电极催化剂材料的抗焦化能力、催化活性和脱氢催化性能都得到不同程度的提高。
目前,基于H-SOFCs制备乙烯的研究以实验研究为主[12, 15-19],相关的理论模型还没有被报道。因此,本文搭建用于制备乙烯的H-SOFCs的电化学模型,研究其电化学性能、法拉第效率和能量效率等,可为H-SOFCs的设计和优化提供理论指导。
1 模型的建立 1.1 质子电导率和电子空穴电导率目前,最常用的H-SOFCs电解质材料是钙钛矿型质子导体,其质子导电性与水的分压有直接关系。质子导体中的质子电导率与工作气氛中水分压的关系可表示为[20]
| $ {\sigma }_{{\mathrm{H}}^+}={\sigma }_{{\mathrm{H}}^+}^{0}\frac{\sqrt{{P}_{{\mathrm{H}}_{2}\mathrm{O}}}}{T}{\mathrm{e}}^{-\tfrac{{E}_{{\mathrm{H}}^+}}{{K}_{\mathrm{B}}T}} $ | (1) |
式中:
在本文中,由于乙烷电极侧和空气电极侧的水分压相等,因此假设电解质中的质子电导率恒定不变。
电子空穴缺陷(
| $ {{V}_{\mathrm{O}}^{\cdot \cdot }+\frac{1}{2}\mathrm{O}_{2}}\rightleftharpoons {\mathrm{O}}_{\mathrm{O}}^{\mathrm{X}}+2{h}^{.} $ | (2) |
式中:
结合反应(1) ,电子空穴电导率(
| $ {\sigma }_{{h}^{\cdot }}={\sigma }_{{h}^{\cdot }}^{0}\frac{{P}_{{\mathrm{O}}_{2}}^{\tfrac{1}{4}}}{T}{\mathrm{e}}^{-\tfrac{{E}_{{h}^{\cdot }}}{{K}_{\mathrm{B}}T}}$ | (3) |
式中:
在本文中,由于乙烷电极侧和空气电极侧的氧分压相差较大,因此引入了有效电子空穴电导率的概念,其含义是电子空穴电导率沿电解质层轴向曲线分布的平均值,其表达式如下[22]:
| $ {\sigma }_{{h}^{.},\mathrm{e}\mathrm{f}\mathrm{f}}=\frac{{\sigma }_{{h}^{.},{\rm{c}}}-{\sigma }_{{h}^{.},{\rm{a}}}{\mathrm{e}}^{-\lambda }}{1-{\mathrm{e}}^{-\lambda }}{\left(1+\frac{1}{\lambda }\mathrm{l}\mathrm{n}\frac{{\sigma }_{{h}^{.},{\rm{c}}}}{{\sigma }_{{h}^{.},{\rm{a}}}}\right)^{-1} } $ | (4) |
式中:
| $ \lambda =\frac{F}{RT}\left({V}_{\mathrm{o}\mathrm{u}\mathrm{t}}+\frac{\mathrm{\Delta }{\mu }_{{\rm{e}}}}{F}\right) $ | (5) |
式中:
电解质中载流子的传输可通过能斯特-普朗克方程描述[23]:
| $ {J}_{\mathrm{m},\mathrm{k}}=-{D}_{\mathrm{k}}\nabla {c}_{\mathrm{k}}-\frac{{\sigma }_{\mathrm{k}}}{{z}_{\mathrm{k}}q}\nabla \varphi $ | (6) |
式中:
| $ {J}_{{{h}}^{.}}=\frac{\left(\dfrac{RT}{2F}\mathrm{l}\mathrm{n}\dfrac{{P}_{{\mathrm{H}}_{2}}^{{\rm{a}}}}{{P}_{{\mathrm{H}}_{2}}^{{\rm{c}}}}-{J}_{\mathrm{e}\mathrm{x}\mathrm{t}}\dfrac{{\tau }_{\mathrm{e}\mathrm{l}\mathrm{e}\mathrm{c}}}{{\sigma }_{{\mathrm{H}}^+}}\right) }{\left(\dfrac{{\tau }_{\mathrm{e}\mathrm{l}\mathrm{e}\mathrm{c}}}{{\sigma }_{{h}^{.},\mathrm{e}\mathrm{f}\mathrm{f}}}+\dfrac{{\tau }_{\mathrm{e}\mathrm{l}\mathrm{e}\mathrm{c}}}{{\sigma }_{{\mathrm{H}}^+}}\right) }$ | (7) |
式中:
质子导体固体氧化物燃料电池的输出电压
| $ {V}_{\mathrm{o}\mathrm{u}\mathrm{t}}={E}_{\mathrm{e}\mathrm{q}}-{\eta }_{\mathrm{o}\mathrm{h}\mathrm{m}\mathrm{i}\mathrm{c}}-{\eta }_{\mathrm{a}\mathrm{c}\mathrm{t}}-{\eta }_{\mathrm{c}\mathrm{o}\mathrm{n}}$ | (8) |
式中:
理论平衡电压
| $ {E}_{\mathrm{e}\mathrm{q}}=\frac{RT}{2F}\mathrm{l}\mathrm{n}\frac{{P}_{{\mathrm{H}}_{2}}^{\mathrm{a},0}}{{P}_{{\mathrm{H}}_{2}}^{\mathrm{c},0}} $ | (9) |
式中:
欧姆过电势、活化过电势及浓差过电势可分别通过欧姆定律、Butler-Volmer方程及尘气模型(Dusty Gas Model,DGM) 来描述。在之前的研究工作有给出详细的推导过程[26],在这里不再赘述。
1.3 所需的能耗及效率法拉第效率
| $ {\omega }_{\mathrm{F}\mathrm{a}}=\frac{{J}_{\mathrm{e}\mathrm{x}\mathrm{t}}}{\left|{J}_{{\mathrm{H}}^+}\right|} $ | (10) |
基于H-SOFCs制备乙烯的过程中,需要向外界吸收的能量为可逆热能(
| $ {Q}_{\mathrm{h}\mathrm{e}\mathrm{a}\mathrm{t}}=T\mathrm{\Delta }S $ | (11) |
式中:
系统能量效率
| $ {\omega }_{\mathrm{e}\mathrm{n}\mathrm{g}}=\frac{{Q}_{\mathrm{e}\mathrm{l}\mathrm{e}}+{Q}_{{\mathrm{C}}_{2}{\mathrm{H}}_{4}}}{{Q}_{{\mathrm{C}}_{2}{\mathrm{H}}_{6}}+{Q}_{\mathrm{h}\mathrm{e}\mathrm{a}\mathrm{t}}}=\frac{{V}_{\mathrm{o}\mathrm{u}\mathrm{t}}{J}_{\mathrm{e}\mathrm{x}\mathrm{t}}+{N}_{{\mathrm{C}}_{2}{\mathrm{H}}_{4}} \times \mathrm{L}{\mathrm{H}\mathrm{V}}_{{\mathrm{C}}_{2}{\mathrm{H}}_{4}}}{{N}_{{\mathrm{C}}_{2}{\mathrm{H}}_{6}} \times {\mathrm{L}\mathrm{H}\mathrm{V}}_{{\mathrm{C}}_{2}{\mathrm{H}}_{6}}+{Q}_{\mathrm{h}\mathrm{e}\mathrm{a}\mathrm{t}}} $ | (12) |
式中:LHV为低热值,N为气体摩尔通量。
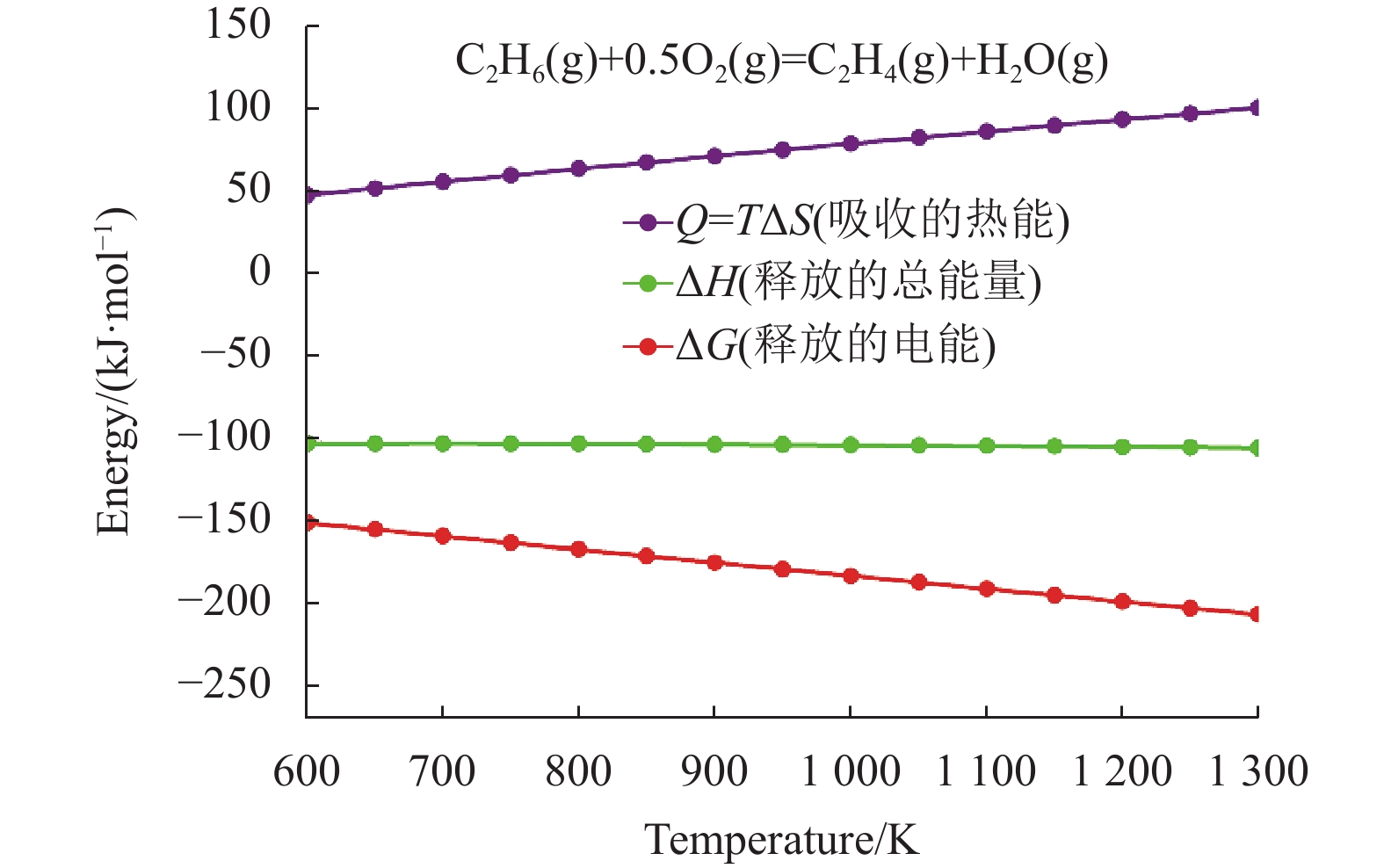
2 结果与讨论 2.1 热力学分析图2显示了不同温度下基于H-SOFCs制备乙烯的热力学计算结果。由图可知,在所示的工作温度区间内,反应的吉布斯自由能(
|
图 2 基于质子导体固体氧化物燃料电池制备乙烯的热力学计算结果 Figure 2 Thermodynamic calculation results for ethylene production based on proton conducting solid oxide fuel cells |
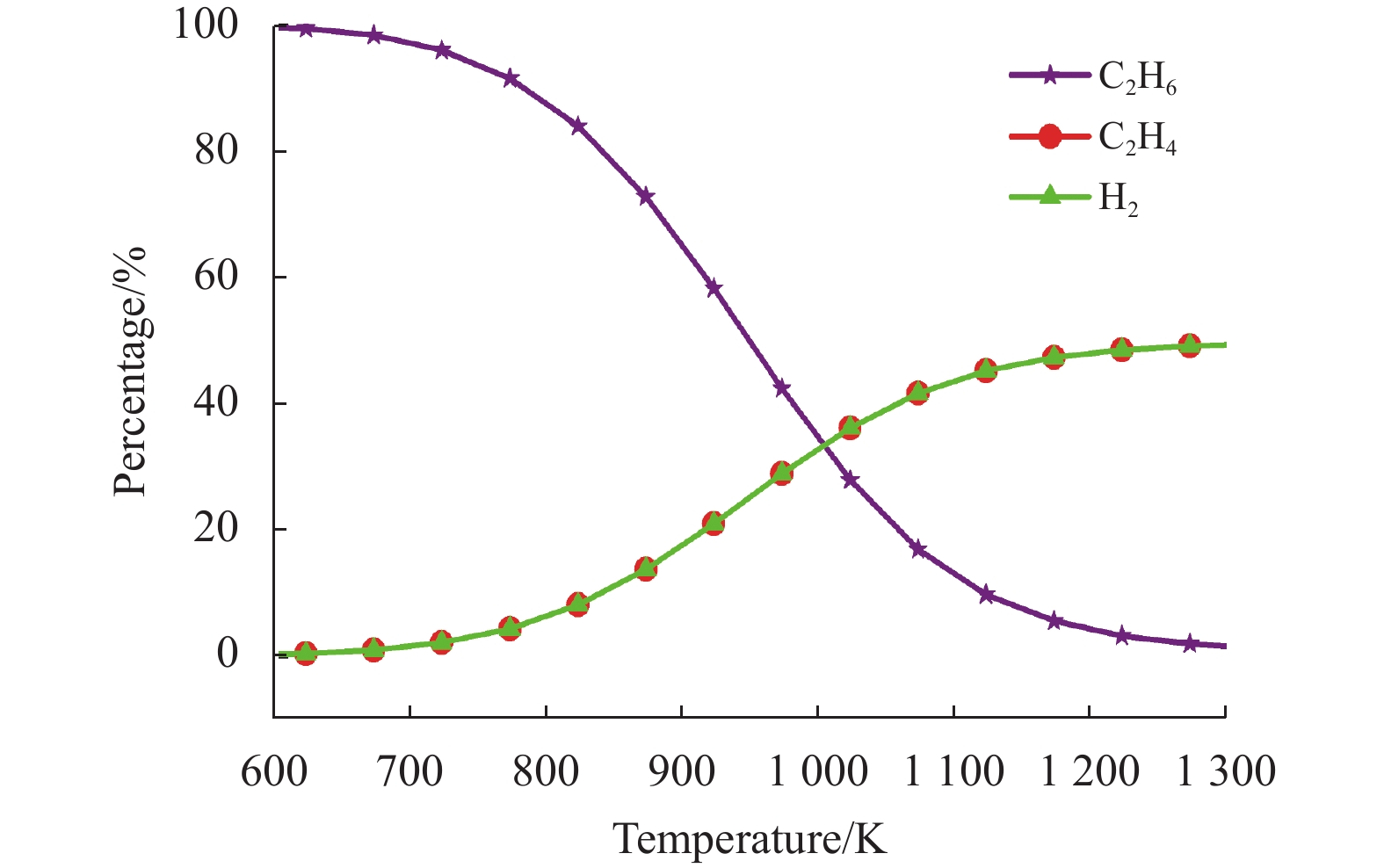
图3描述了乙烷热分解为乙烯和氢气的热力学平衡组分图。随着温度的升高,乙烷的分解程度逐渐增大,尤其是在1000~1200 K的工作温度区间。典型H-SOFCs的工作温度也处在该温度区间。相应地,在这个温度区间,乙烯和氢气的组分随温度的升高而增大。此时H-SOFCs的乙烷电极侧含有大量的氢气。另外,有研究表明氢气比乙烷更易进行电化学氧化[6, 27],因此可以合理地假设在H-SOFCs的乙烷电极发生氢气的电化学氧化反应,而不是乙烷的电化学氧化反应。
|
图 3 不同温度下,乙烷热分解的热力学平衡组分图(乙烯的选择性=100%) Figure 3 Thermodynamic equilibrium of ethane thermal cracking at various temperatures (ethylene selectivity=100%) |
表1汇总了电化学模型所使用的基本参数,这些参数的准确性已经得到了验证[26]。
| 表 1 用于模型计算的H-SOFCs参数 Table 1 Parameters of H-SOFCs used for modeling calculation |
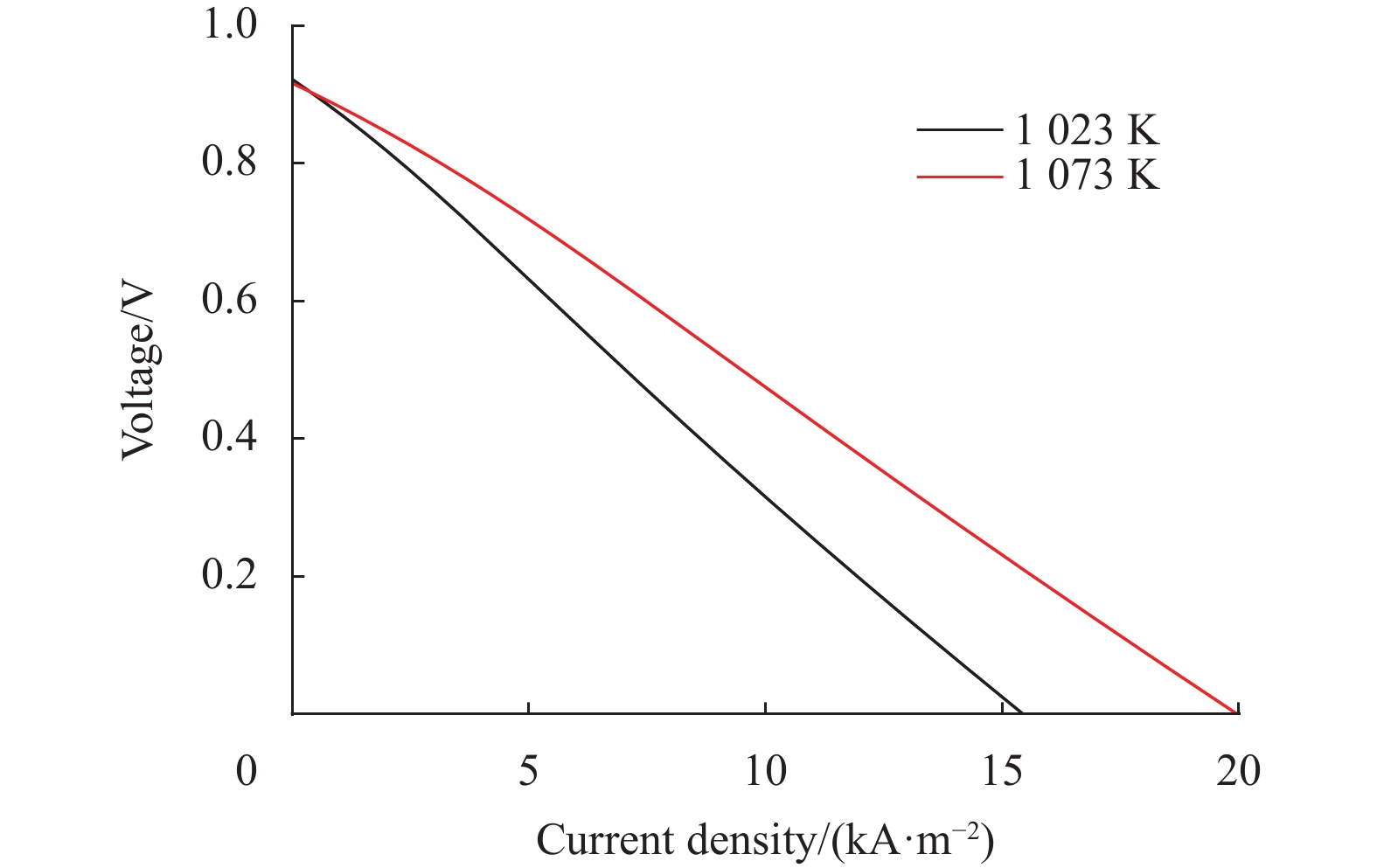
图4展示了模型预测的电流密度−输出电压曲线。由图可知,输出电压随电流密度的增大而减小,这是因为电流密度的增大导致了过电势的增大。另外,在相同的输出电压下,1073 K时的电流要明显大于1023 K时的,这主要与欧姆、活化及浓差过电势有关,后面将详细分析。
|
图 4 模型预测的电流密度−输出电压曲线 Figure 4 Model-predicted current density-output voltage curves |
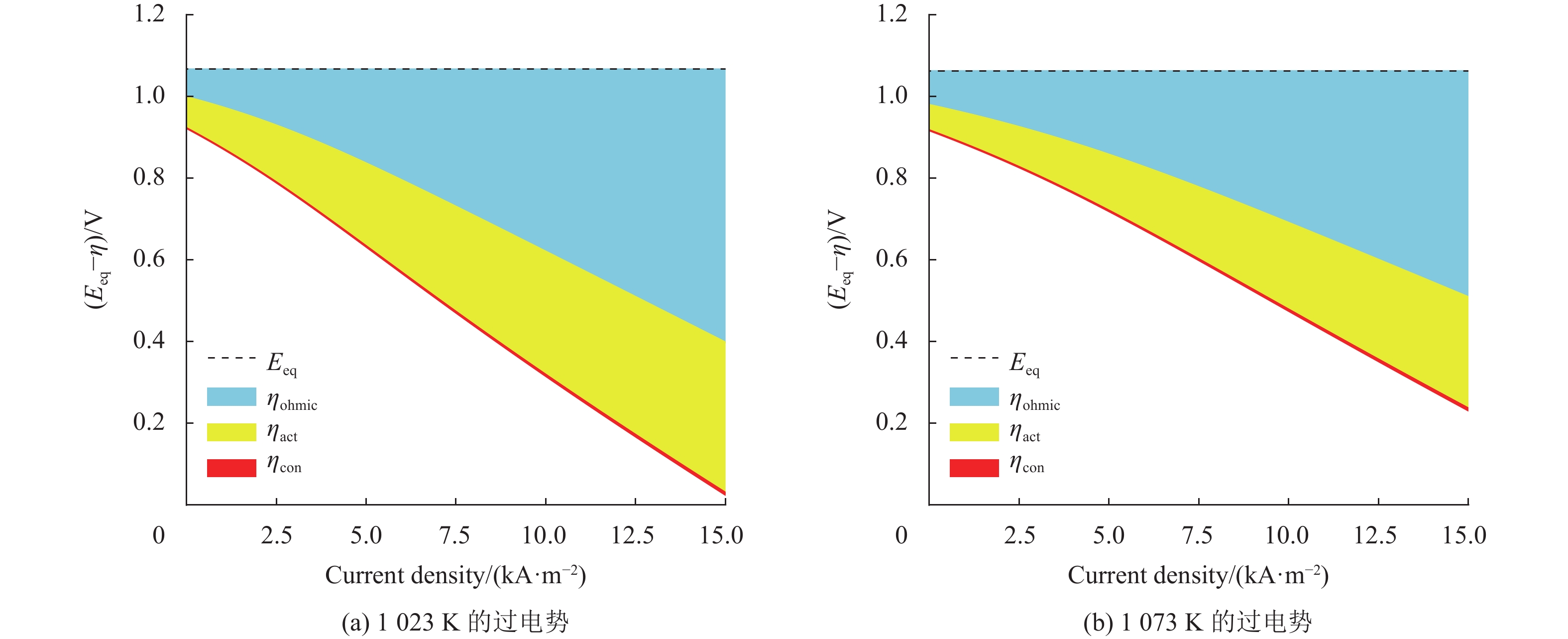
图5展示了模型预测的过电势随电流密度变化的关系曲线。在图5中,红色部分代表浓差过电势,黄色部分代表活化过电势,浅蓝色部分代表欧姆过电势。由图可知,H-SOFCs在1023 K及1073 K的工作温度下,欧姆过电势和活化过电势占主导地位,而浓差过电势几乎可忽略不计。如当H-SOFCs的工作温度为1023 K及电流密度为10000 A/m2时,欧姆过电势为0.45 V,活化过电势为0.30 V,浓差过电势为0.004 V。此外,随着电流密度的增大,三种过电势不断地增大,因此输出电压随着电流密度的增大而减小,如图4所示。在相同电流密度下,如当电流密度为7500 A/m2时,过电势由1023 K的0.59 V减小至1073 K的0.45 V。过电势的减小主要体现在欧姆过电势和活化过电势上。这是由于升高温度增大了质子电导率(如式(1)所示) ,从而降低欧姆过电势;另外,升高温度还可以提高电化学反应速率,进而降低活化过电势。
|
图 5 模型预测的过电势 Figure 5 Model-predicted overpotentials |
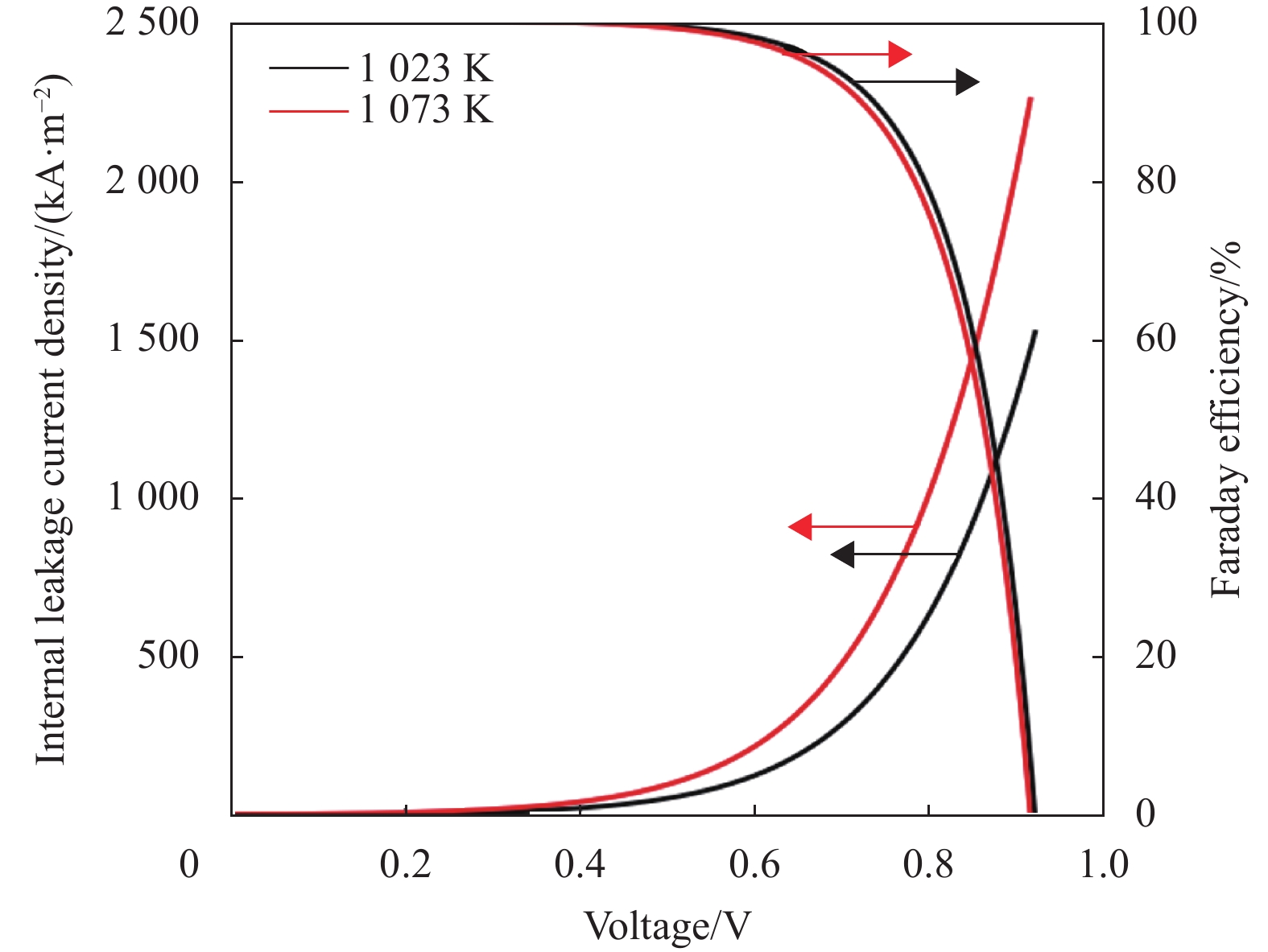
图6给出了工作温度为1023 K和1073 K时模型预测的泄漏电流密度。在开路电压处H-SOFCs的泄漏电流密度大于2200 A/m2(1073 K) ,由此可知电池存在明显的内部短路。此外,泄漏电流密度随着输出电压的减小而急剧减小,这是由于电解质内电子电流(泄漏电流) 的驱动力之一是电势梯度,此外泄漏电流与外电流的关系如式(7) 所示,外电流的增大会使泄漏电流减小。1023 K时的泄漏电流密度明显小于1073 K的,原因在于电解质层电子空穴电导率的减小(如式(3)所示) 。再从图6中模型预测的法拉第效率可以看出,在两个工作温度下,法拉第效率均随输出电压的增大而减小,这主要与泄漏电流密度的增大有关。虽然泄漏电流密度随工作温度的升高而增大,但质子电流也随工作温度的升高而增大。因此,法拉第效率对工作温度的依赖性较小。
|
图 6 模型预测的泄漏电流密度和法拉第效率 Figure 6 Model-predicted internal leakage current densityand Faraday efficiency |
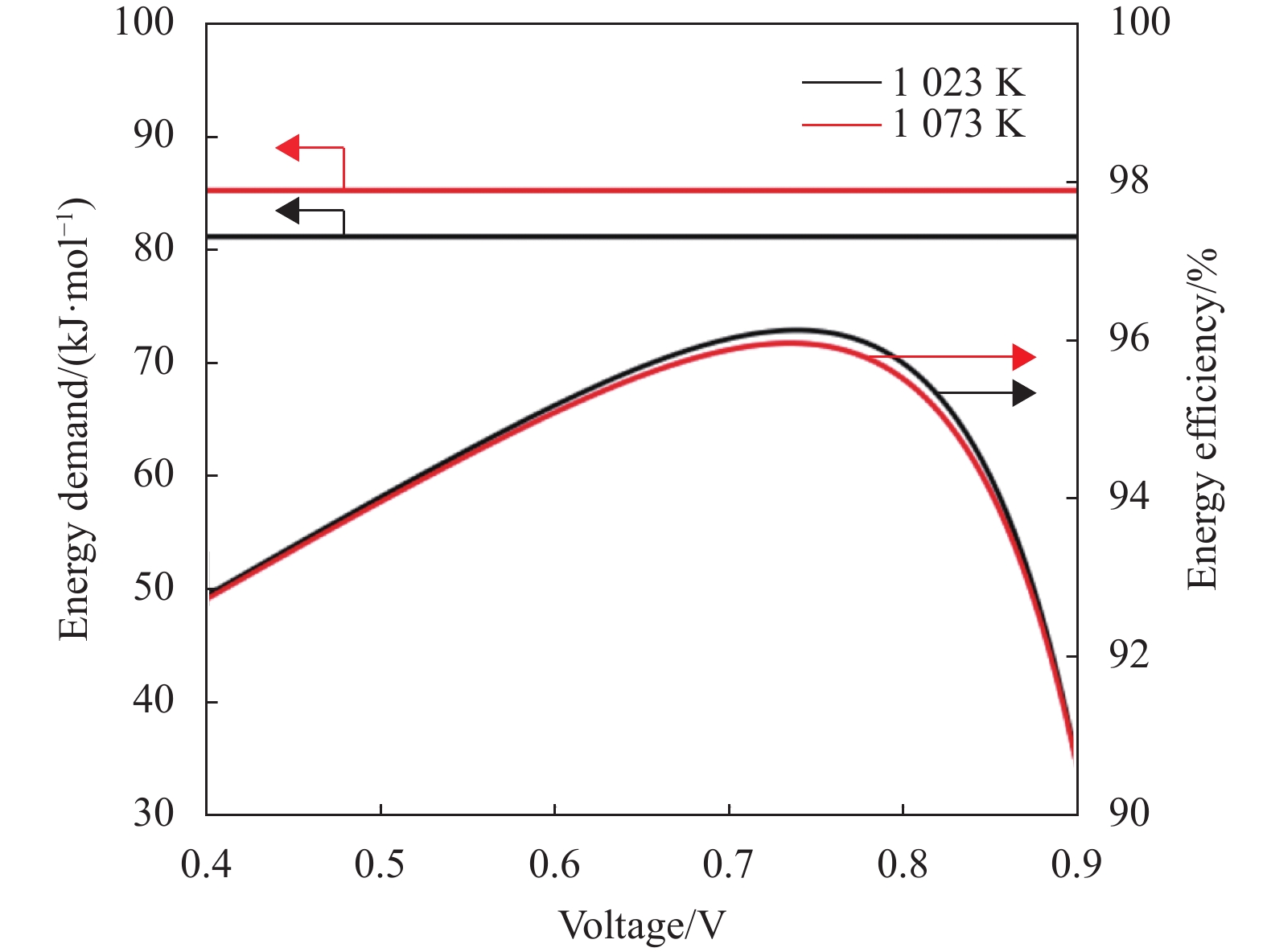
图7展示了模型预测的基于H-SOFCs产生1 mol乙烯的能量需求以及系统能量效率随输出电压的变化曲线。由图可知,产生1 mol乙烯的能量需求不随输出电压的改变而改变。这是因为基于H-SOFCs制备乙烯的反应仅需要向外界吸收可逆热能,在2.1小节热力学分析部分已经阐述。另外,产生1 mol乙烯的能量需求从1023 K的81.27 kJ/mol增长至1073 K的85.25 kJ/mol。再从图7中系统能量效率随输出电压的变化曲线可以看出,系统能量效率随输出电压的增大先增大后减小。输出电压在0.75 V附近,系统能量效率曲线出现了拐点,这是由于输出电压接近开路电压时,法拉第效率显著下降,导致输出电能下降。另外,1073 K的系统能量效率要稍小于1023 K的。在相同的工作电压及温度高的条件下,H-SOFCs释放出更多的电能,所需吸收的热能也随之增大,且温度对吸收热能的影响程度大于对释放电能的影响程度,结合公式(12) ,使得H-SOFCs在高温的系统能量效率要稍小于在低温的系统能量效率。
|
图 7 模型预测的产生1 mol乙烯的能量需求及能量效率与输出电压的关系 Figure 7 Model-predicted energy demand to produce 1 mole ethylene and energy efficiency as a function of output voltage |
本文建立基于H-SOFCs制备乙烯的电化学模型,通过电化学模型分析了电能和乙烯共生的H-SOFCs的电化学性能、法拉第效率、系统能量效率等,得出以下结论:
(1) 根据热力学分析可知,基于H-SOFCs制备乙烯的过程中需要向外界吸收可逆热能,且工作温度越高所需要吸收的可逆热能越多;在反应过程中还有电能的释放;另外,适当地提高工作温度有助于乙烷的热分解,增大乙烯的生成率。
(2) 由于质子导体电解质存在不可忽略的电子电导,造成电池内部短路,形成泄漏电流,在开路电压处的泄漏电流密度高达2200 A/m2(1073 K) ,泄漏电流密度随着输出电压的减小而急剧减小。因此,在运行H-SOFCs时,设计合适的输出电压可以有效地减小泄漏电流的影响。
(3) 法拉第效率随输出电压的增大而下降;系统能量效率随输出电压的增大先增大后减小,在输出电压为0.75 V处,系统能量效率达到最大值;产生1 mol乙烯的能量需求不随输出电压的改变而改变;因此,在设计H-SOFCs的输出电压时,需要综合考虑以上几个性能指标。
| [1] |
温翯, 郭晓莉, 苟尕莲. 乙烷裂解制乙烯的工艺研究进展[J].
现代化工, 2020, 40(5): 47-51.
WEN H, GUO X L, GOU G L, et al. Process research advances in ethane cracking to ethylene[J]. Modern Chemical Industry, 2020, 40(5): 47-51. DOI: 10.16606/j.cnki.issn0253-4320.2020.05.011. |
| [2] |
DING D, ZHANG Y, WU W, et al. A novel low-thermal-budget approach for the co-production of ethylene and hydrogen via the electrochemical non-oxidative deprotonation of ethane[J].
Energy & Environmental Science, 2018, 11(7): 1710-1716.
|
| [3] |
SAITO H, SEKINE Y. Catalytic conversion of ethane to valuable products through non-oxidative dehydrogenation and dehydroaromatization[J].
RSC Advances, 2020, 10(36): 21427-21453.
DOI: 10.1039/D0RA03365K. |
| [4] |
WU W, WANG L C, HU H, et al. Electrochemically engineered, highly energy-efficient conversion of ethane to ethylene and hydrogen below 550 °C in a protonic ceramic electrochemical cell[J].
ACS Catalysis, 2021, 11(19): 12194-12202.
DOI: 10.1021/acscatal.1c03351. |
| [5] |
SHI L, YAN B, SHAO D, et al. Selective oxidative dehydrogenation of ethane to ethylene over a hydroxylated boron nitride catalyst[J].
Chinese Journal of Catalysis, 2017, 38(2): 389-395.
DOI: 10.1016/S1872-2067(17)62786-4. |
| [6] |
ZHANG X, YE L, LI H, et al. Electrochemical dehydrogenation of ethane to ethylene in a solid oxide electrolyzer[J].
ACS Catalysis, 2020, 10(5): 3505-3513.
DOI: 10.1021/acscatal.9b05409. |
| [7] |
GAO Y, NEAL L, DING D, et al. Recent advances in intensified ethylene production—areview[J].
ACS Catalysis, 2019, 9(9): 8592-8621.
DOI: 10.1021/acscatal.9b02922. |
| [8] |
FU X Z, LUO J L, SANGER A R, et al. Y-doped BaCeO3−δ nanopowders as proton-conducting electrolyte materials for ethane fuel cells to co-generate ethylene and electricity
[J].
Journal of Power Sources, 2010, 195(9): 2659-2663.
DOI: 10.1016/j.jpowsour.2009.10.069. |
| [9] |
LIN J Y, SHAO L, SI F Z, et al. Multiple-doped barium cerate proton-conducting electrolytes for chemical-energy cogeneration in solid oxide fuel cells[J].
International Journal of Hydrogen Energy, 2018, 43(42): 19704-19710.
DOI: 10.1016/j.ijhydene.2018.08.204. |
| [10] |
LI J H, FU X Z, ZHOU G H, et al. FeCr2O4nanoparticles as anode catalyst for ethane proton conducting fuel cell reactors to coproduce ethylene and electricity
[J].
Advances in Physical Chemistry, 2011, 2011: 1-6.
|
| [11] |
FU X Z, LUO X X, LUO J L, et al. Ethane dehydrogenation over nano-Cr2O3 anode catalyst in proton ceramic fuel cell reactors to co-produce ethylene and electricity
[J].
Journal of Power Sources, 2011, 196(3): 1036-1041.
DOI: 10.1016/j.jpowsour.2010.08.043. |
| [12] |
LIU S, BEHNAMIAN Y, CHUANG K T, et al. A-site deficient La0.2Sr0.7TiO3−δ anode material for proton conducting ethane fuel cell to cogenerate ethylene and electricity
[J].
Journal of Power Sources, 2015, 298: 23-29.
DOI: 10.1016/j.jpowsour.2015.08.032. |
| [13] |
LI J H, FU X Z, LUO J L, et al. Evaluation of molybdenum carbide as anode catalyst for proton-conducting hydrogen and ethane solid oxide fuel cells[J].
Electrochemistry Communications, 2012, 15(1): 81-84.
DOI: 10.1016/j.elecom.2011.11.031. |
| [14] |
LIN J Y, SHAO L, SI F Z, et al. Co2CrO4nanopowders as an anode catalyst for simultaneous conversion of ethane to ethylene and power in proton-conducting fuel cell reactors
[J].
The Journal of Physical Chemistry C, 2018, 122(8): 4165-4171.
DOI: 10.1021/acs.jpcc.7b11680. |
| [15] |
LI M, HUA B, WANG L C, et al. Switching of metal–oxygen hybridization for selective CO2 electrohydrogenation under mild temperature and pressure
[J].
Nature Catalysis, 2021, 4(4): 274-283.
DOI: 10.1038/s41929-021-00590-5. |
| [16] |
LI J, HOU J, XI X, et al. Cogeneration of ethylene and electricity in symmetrical protonic solid oxide fuel cells based on a La0.6Sr0.4Fe0.8Nb0.1Cu0.1O3−δ electrode
[J].
Journal of Materials Chemistry A, 2020, 8(48): 25978-25985.
DOI: 10.1039/D0TA08974E. |
| [17] |
YANG X, WEI T, CHI B, et al. Lanthanum manganite-based perovskite as a catalyst for co-production of ethylene and hydrogen by ethane dehydrogenation[J].
Journal of Catalysis, 2019, 377: 629-637.
DOI: 10.1016/j.jcat.2019.08.008. |
| [18] |
WANG L C, ZHANG Y, XU J, et al. Non-oxidative dehydrogenation of ethane to ethylene over ZSM-5 zeolite supported iron catalysts[J].
Applied Catalysis B:Environmental, 2019, 256: 117816.
DOI: 10.1016/j.apcatb.2019.117816. |
| [19] |
LIU S, CHUANG K T, LUO J L. Double-layered perovskite anode with in situ exsolution of a Co–Fe alloy to cogenerate ethylene and electricity in a proton-conducting ethane fuel cell[J].
ACS Catalysis, 2015, 6(2): 760-768.
|
| [20] |
PUTILOV L P, DEMIN A K, TSIDILKOVSKI V I, et al. Theoretical modeling of the gas humidification effect on the characteristics of proton ceramic fuel cells[J].
Applied Energy, 2019, 242: 1448-1459.
DOI: 10.1016/j.apenergy.2019.03.096. |
| [21] |
HAN D, TOYOURA K, UDA T. Protonated BaZr0.8Y0.2O3−δ: impact of hydration on electrochemical conductivity and local crystal structure
[J].
ACS Applied Energy Materials, 2021, 4(2): 1666-1676.
DOI: 10.1021/acsaem.0c02832. |
| [22] |
ZHANG Q, GUO Y, DING J, et al. Comprehensive models for evaluating electrolyte hole conductivity and its impacts on the protonic ceramic fuel cell[J].
Journal of Power Sources, 2020, 472: 228232.
DOI: 10.1016/j.jpowsour.2020.228232. |
| [23] |
SHEN S, GUO L, LIU H. A polarization model for solid oxide fuel cells with a Bi-layer electrolyte[J].
International Journal of Hydrogen Energy, 2016, 41(5): 3646-3654.
DOI: 10.1016/j.ijhydene.2015.12.162. |
| [24] |
ZHANG J H, LEI L B, LIU D, et al. Mathematical modeling of a proton-conducting solid oxide fuel cell with current leakage[J].
Journal of Power Sources, 2018, 400: 333-340.
DOI: 10.1016/j.jpowsour.2018.08.038. |
| [25] |
NAKAMURA T, MIZUNUMA S, KIMURA Y, et al. Energy efficiency of ionic transport through proton conducting ceramic electrolytes for energy conversion applications[J].
Journal of Materials Chemistry A, 2018, 6(32): 15771-15780.
DOI: 10.1039/C8TA05373A. |
| [26] |
QIU R M, LIAN W C, OU Y Z, et al. Multifactor theoretical analysis of current leakage in proton-conducting solid oxide fuel cells[J].
Journal of Power Sources, 2021, 505: 230038.
|
| [27] |
XIAO J, XIE Y, LIU J, et al. Deactivation of nickel-based anode in solid oxide fuel cells operated on carbon-containing fuels[J].
Journal of Power Sources, 2014, 268: 508-516.
DOI: 10.1016/j.jpowsour.2014.06.082. |
 2023, Vol. 40
2023, Vol. 40

