2. 深圳职业技术学院 建筑与环境工程学院,广东 深圳 518055;
3. 深圳信息职业技术学院 交通与环境学院,广东 深圳 518172
2. Department of Building and Environmental Engineering, Shenzhen Polytechnic Institute, Shenzhen 518055, China;
3. School of Traffic and Environment, Shenzhen Institute of Information Technology, Shenzhen 518172, China
药品和个人护理品(Pharmaceuticals And Personal Care Products,PPCPs)在全球范围内大规模地使用,其残留物对水生环境和人类健康的潜在危害引起了广泛关注,成为环境领域的研究热点[1-2]。美托洛尔(Metoprolol,MTP)作为常用的β-受体阻滞剂用于治疗各种心血管疾病,是一种典型的PPCPs[3]。然而,美托洛尔在人类摄入后不能被完全代谢,过期和未使用的也可能经下水道进入污水处理系统。而常规污水处理工艺对美托洛尔的去除率并不高[4]。近年来由于其广泛应用、抗水解性和有限的生物代谢作用,美托洛尔在天然水体中被频繁地检测到[5-7]。有试验显示美托洛尔对许多鱼类、藻类、无脊椎动物等多种水生生物都具有毒害作用[4]。
美托洛尔在传统污水处理厂中去除率较低,通常在0~36%之间[8-10]。Vieno等[11]研究表明粒状活性炭去除MTP的效果十分有限,去除率仅为11%。Behera等[12]利用污泥吸附美托洛尔,对MTP的去除率约为30%。金玲[13]采用膜生物反应器对MTP的去除率只有50%左右。
UV/Cl2作为高级氧化领域的典型工艺,利用紫外线照射氯产生羟基自由基 (•OH)和氯自由基(•Cl)[14-17],两者结合能够有效去除多种有机污染物,UV/Cl2对阿特拉津、卡马西平、非那西丁、三氯生等典型PPCPs类污染物表现出良好的去除效果[18-21],但对MTP的研究报道较少,且都以紫外汞灯作为光源。与传统紫外汞灯相较,紫外发光二极管(Ultraviolet LightEmitting Diode,UV-LED)作为一种新型紫外光源具有电压低、寿命长、绿色无汞、结构简便、波长可调节等优势[22]。
本研究首次采用UV-LED/Cl2高级氧化工艺降解MTP,考察MTP初始质量浓度、UV-LED辐照度、氯剂量、溶液pH、自由基抑制剂等因素对MTP降解效果的影响,以期为水环境中MTP的去除提供理论依据。
1 材料与方法 1.1 实验试剂美托洛尔(CAS#81024-43-3,C15H25NO3,纯度98%),购于TRC(加拿大),实验所配置的储备液质量浓度为10 mg/L,于4 ℃恒温室避光保存备用。甲醇、乙腈、冰醋酸(CH3COOH)、磷酸(H3PO4)均为色谱纯;醋酸铵(CH3COONH4)为优级纯;其余试剂,如次氯酸钠溶液(质量分数6%~14%)、硫代硫酸钠(Na2S2O3)、叔丁醇(Tert Butyl Alcohol,TBA)、硫酸和氢氧化钠等均为分析纯。所有溶液均使用超纯水(Milli-Q超纯水仪,USA)制备。
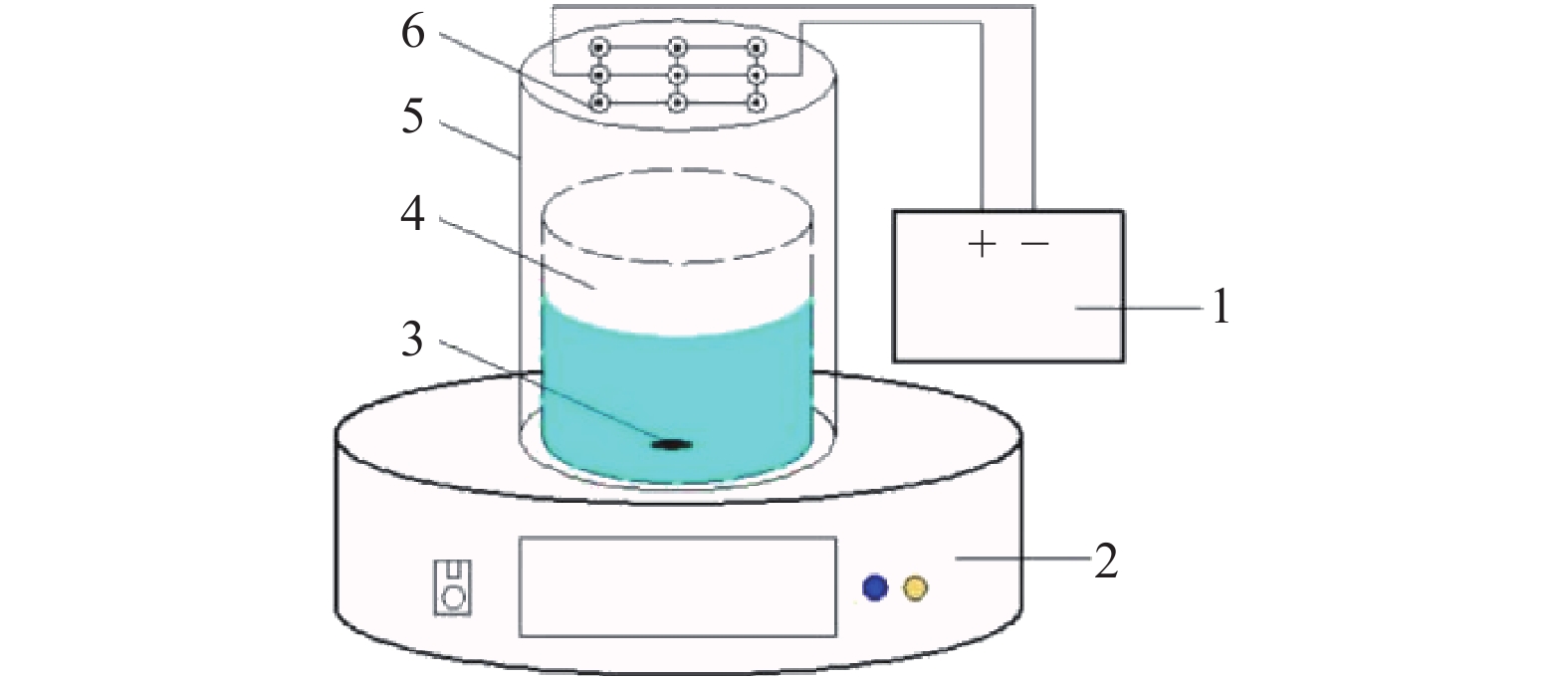
1.2 实验装置实验装置如图1所示,铝制反应器盖内径为50 mm,其顶部内侧以三串三并的方式安装了9个相同的UV-LED灯珠,波长为275 nm。铝制反应器盖内侧套内径为46 mm、高度为30 mm的石英容器,并将磁力搅拌转子置于石英容器底部。LED光源距离实际液面10 mm。紫外线辐照强度由深圳市蓝巨科技有限公司用Light Tools结合积分球测定,单颗灯珠辐照度测得值为0.3 mW/cm2。为了提高紫外光的利用率,反应装置外部用铝箔纸包裹,同时可保证整个反应只受单一光源的影响。所有实验均进行3次,相对标准偏差保持在10%以内。
|
图 1 装置示意图 Figure 1 Schematic diagram of the device 1. 电源;2. 磁力搅拌器;3. 磁力搅拌转子;4. 石英容器;5. 铝制反应器盖;6. UV-LED灯珠模组 |
本实验采用的氯溶液现场配制,以分析纯的次氯酸钠溶液(质量分数为6%~14%)作为储备液。降解实验前,用超纯水稀释至设定好的氯质量浓度,余氯使用哈希公司的便携式余氯仪N,N-二乙基对苯二胺(N,N-diethyl-p-phenylenediamine,DPD)分光光度法进行测定[23]。将已配好一定质量浓度的美托洛尔溶液和氯消毒剂倒入上述反应器中,配置成30 mL含有一定质量浓度氯的美托洛尔反应液,并在烧杯外包裹一层锡箔纸,用磁力搅拌器进行搅拌。MTP的质量浓度由高效液相色谱仪(Waters e2695型)进行测定。所用色谱柱为C18柱(4.6 mm×150 mm,ϕ=5 μm)。流动相由乙腈和10 mM醋酸铵缓冲液组成,两流动相体积比为40/60,流速为1.0 mL/min,检测波长为222 nm,柱温设定为40 ℃。在设定时间点用移液枪吸取反应液0.8 mL,所取样品经针头过滤器(孔径为0.22 µm)注入含有过量Na2S2O3的高效液相色谱(High Performance Liquid Chromatography,HPLC)进样小瓶中,送入高效液相色谱仪测定样品中MTP的质量浓度,计算降解率。
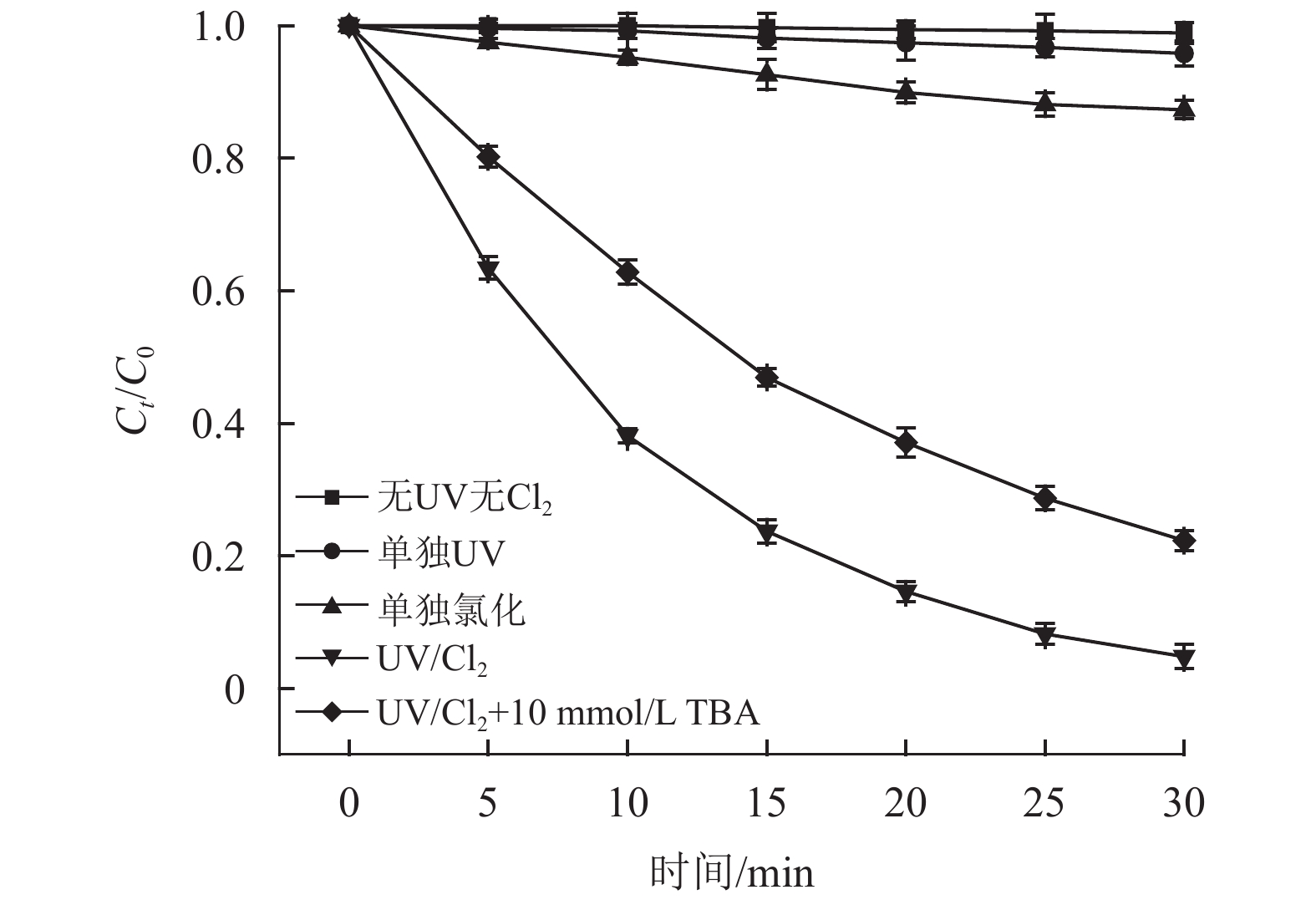
2 结果与讨论 2.1 MTP在不同工艺中的降解效果比较在MTP初始质量浓度为1.0 mg/L、辐照度为2.7 µW/cm2、氯剂量为3.0 mg/L、pH为9.0、温度25 ℃的实验条件下,比较了MTP在无UV无Cl2、单独UV、单独氯化、UV/Cl2、UV/Cl2+10 mmol·L–1 TBA等5种处理工艺中的降解效果。结果如图2所示,无UV无Cl2直接水解和单独UV直接光解这两种方式对MTP的去除率分别为1.1%和4.2%,表明美托洛尔在水中可稳定存在,可以忽略水解及光解的影响。单独氯化对MTP有一定的降解效果,反应30 min后降解率为12.7%。UV/Cl2对MTP有较好的降解效果,反应30 min后MTP的去除率达到95.2%,是单独氯化时的7.5倍,说明在降解MTP过程中UV/Cl2具有明显的协同作用。这是因为NaClO在紫外辐照条件下会促使溶液中的HClO/ClO–发生光分解反应,生成了比自由氯具有更强氧化能力的自由基如羟基自由基(•OH)和氯自由基(•Cl)[24]、(•Cl2–)、(•ClO–)等[25]。羟基自由基(•OH)是活跃性、进攻性最强的活性氧分子,具有非常高的反应速率常数、电负性和极强的氧化电极电位[26]。UV/Cl2反应体系中的•Cl、•Cl2–和•OH等的氧化还原电位较高,可通过单电子氧化、抽H或C—C不饱和键取代加成等反应有效去除芳香族、酚类和苯胺等有机化合物[27-29]。为了进一步证明自由基的作用,向反应体系中加入TBA,TBA是一种很好的自由基抑制剂,它能与MTP竞争大部分高活性自由基[30]。与UV/Cl2相比,UV/Cl2+10 mmol·L–1TBA对MTP的去除率减少12.7%,说明TBA在一定程度上抑制了UV/Cl2对MTP的降解,从而证明•OH和•Cl在降解MTP的过程中起到了一定的作用。
|
图 2 多种降解方式效果对比 Figure 2 Comparison of the effects of various degradation methods |
对MTP的降解进行拟一级反应动力学分析可知,不同工况下其降解过程均遵循准一级动力学规律,准一级动力学常数即降解速率kobs(min–1),也是ln(Ct/C0)与t拟合后的斜率。拟合方程及降解速率如表1所示,降解速率根据式(1)计算:
| $ - \ln \left[ {{C_t} / {C_0}} \right] = {k_{{\rm{obs}}}}t$ | (1) |
其中,C0和Ct分别为MTP初始时刻和t时刻的质量浓度,mg/L;t为反应时间,min。
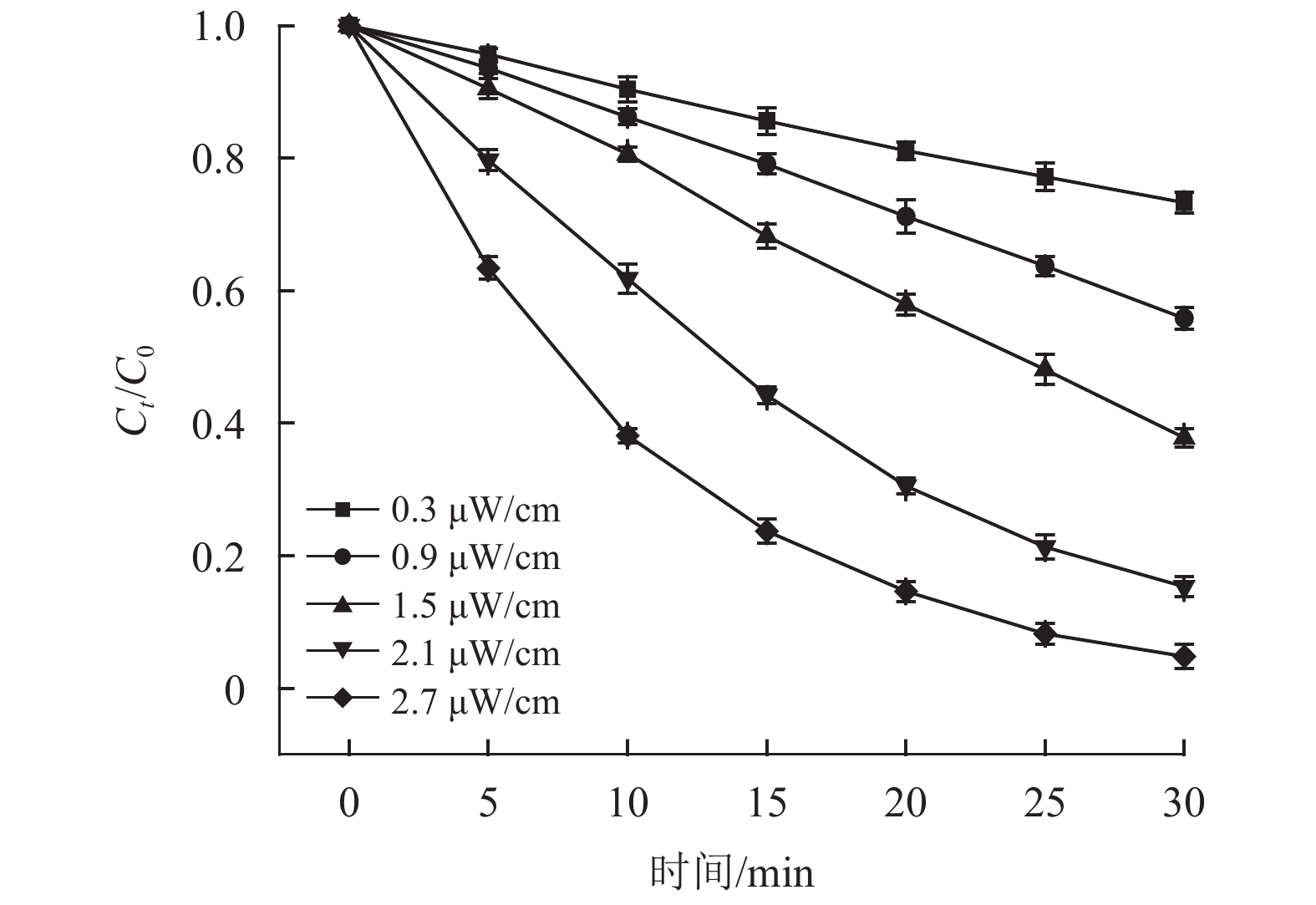
2.2 UV-LED辐照度的影响本实验通过采用铝箔纸包裹不同数量紫外LED灯珠来控制反应体系的辐照度,在MTP初始质量浓度为1.0 mg/L、氯剂量为3.0 mg/L、pH为9.0、温度25 ℃的实验条件下,进行了不同UV-LED辐照度对UV/Cl2降解MTP及其动力学的影响研究,结果如图3所示。
| 表 1 不同工况下降解MTP一级动力学拟合方程及降解速率 Table 1 First-order kinetics equation and degradation rate of the degradation of metoprolol under different degradation methods |
|
图 3 UV-LED辐照度的影响 Figure 3 Effect of UV-LED light intensity on degradation |
当紫外LED辐照度为0.3 µW/cm2时,30 min内MTP的去除率仅为26.7%,随着紫外LED辐照度增至2.7 µW/cm2时,MTP在30 min时去除率可达95.2%。在不同的UV-LED辐照度下,MTP的降解速率由0.0107 min–1(0.3 µW/cm2时)增加至0.1024 min–1(2.7 µW/cm2时),降解速率增加了约92%。拟合方程及降解速率如表2所示。结果表明,不同UV-LED辐照度下UV/Cl2对美托洛尔的降解均符合拟一级动力学,而且降解速率随辐照度的增大而增大。增强紫外LED辐照强度对UV/Cl2降解MTP的效果有着显著的促进作用,同时其降解速率也随辐照度的升高而增大。主要因为辐照度影响自由基的生成,在氯剂量一定的条件下,单位时间内紫外LED辐照度度越大,与MTP反应的自由基就会越多,从而加快MTP的降解反应速率[21]。
| 表 2 不同UV-LED辐照度下UV/Cl2降解MTP一级动力学拟合方程及降解速率 Table 2 First-order kinetics equation and degradation rate of the degradation of metoprolol at different UV-LED irradiance |
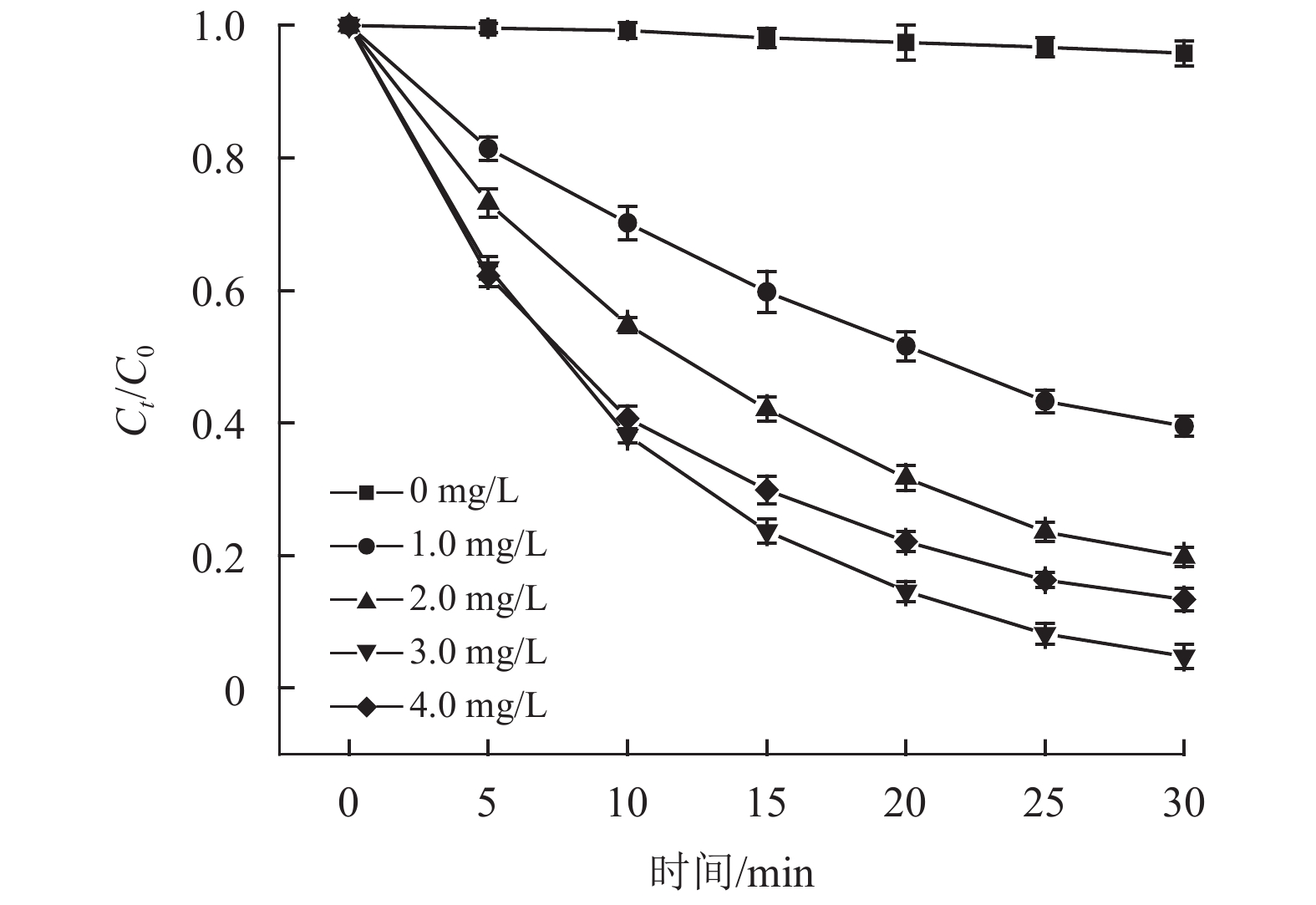
在MTP初始质量浓度为1.0 mg/L、辐照度为2.7 µW/cm2、pH为9.0、温度25 ℃的实验条件下,进行了不同氯剂量对UV/Cl2降解MTP及其动力学的影响研究,结果见图4和表3。
|
图 4 氯剂量的影响 Figure 4 Effect of chlorine dose on degradation |
| 表 3 不同氯剂量下UV/Cl2降解MTP一级动力学拟合方程及降解速率 Table 3 First-order kinetics equation and degradation rate of the degradation of metoprolol at different chlorine dose |
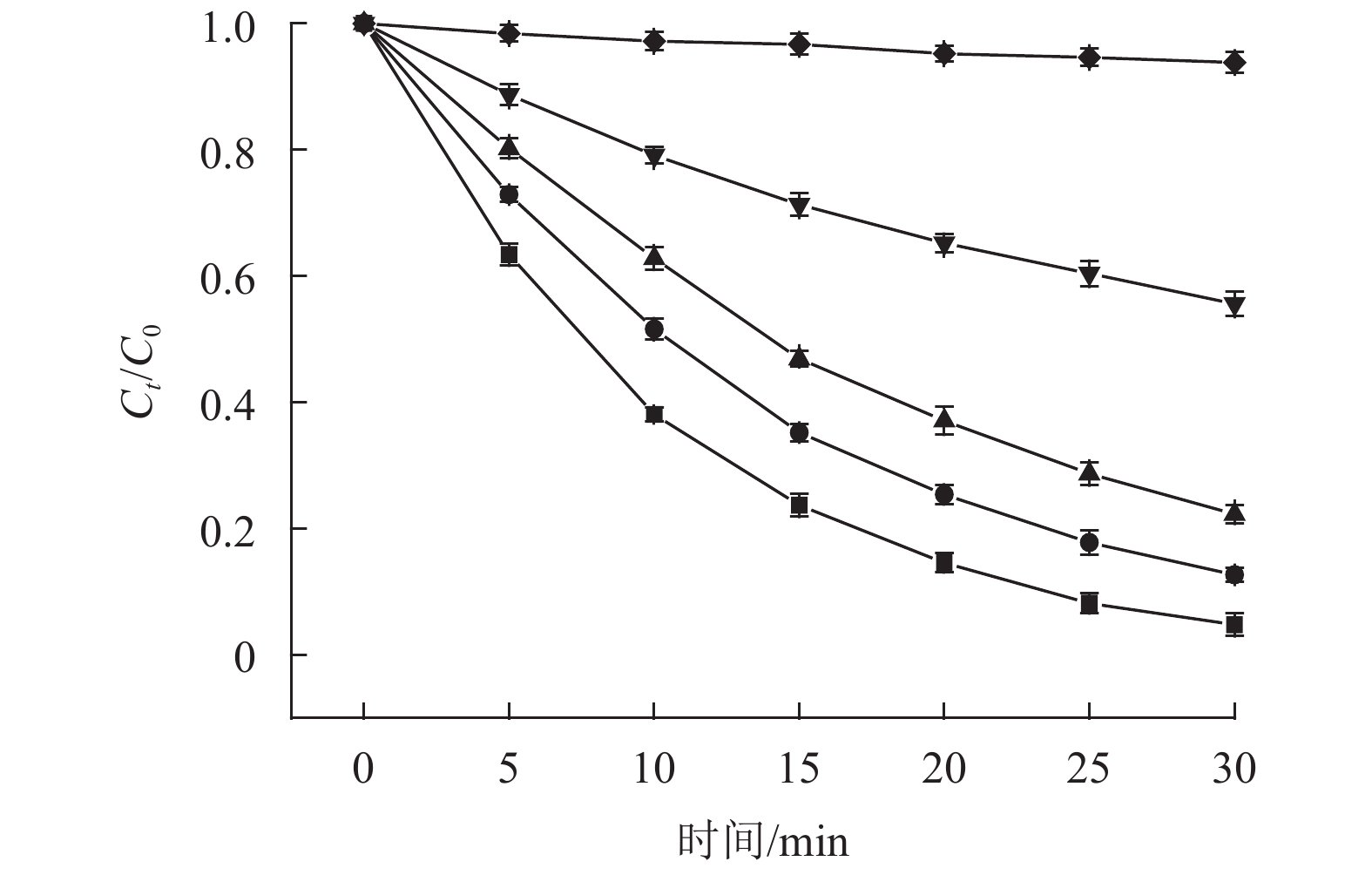
结果表明,不同的氯剂量对于UV/Cl2降解MTP的速率都符合拟一级动力学模型。随着氯剂量从0 mg/L逐渐增加到1.0,2.0,3.0,4.0 mg/L,MTP的去除率从4.2%分别达到60.5%,80.2%,95.2%,86.6%。在一定范围内MTP的降解速率随着氯剂量的增加而加快,这是因为较多的自由氯在紫外辐射的作用下产生了更多的高活性自由基,从而促进了MTP的降解。但当氯气投加量超过4 mg/L,降解率下降。这很可能是因为过量的氯会清除体系中产生的自由基[28, 31-33],该过程与赵刘柱等[20]用紫外-氯降解非那西丁的研究相似。
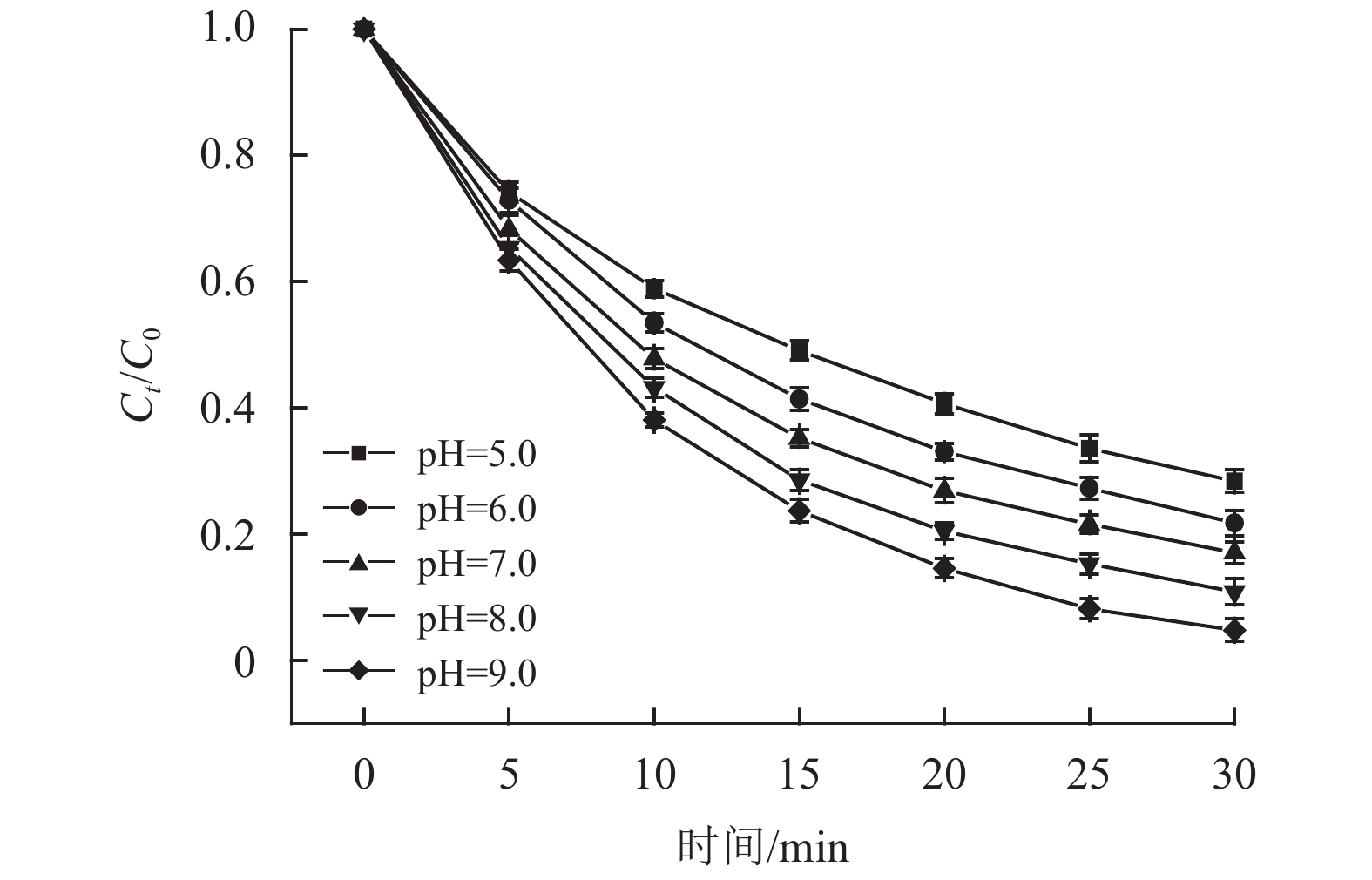
2.4 pH的影响在MTP初始质量浓度为1.0 mg/L、辐照度为2.7 µW/cm2、氯剂量为3.0 mg/L、温度25 ℃的实验条件下,用硫酸和氢氧化钠调节pH 值,考察pH对MTP的去除的影响,结果见图5和表4。
|
图 5 pH的影响 Figure 5 Effect of pH value on degradation |
| 表 4 不同pH下UV/Cl2降解MTP一级动力学拟合方程及降解速率 Table 4 First-order kinetics equation and degradation rate of the degradation of metoprolol by UV/Cl2 atdifferent pH values |
UV/Cl2工艺中,MTP在不同pH值内均有去除效果,而且在碱性环境中的去除效果优于酸性环境。当pH值从5.0增加到9.0时,反应速率常数由0.0416 min–1升高到0.1024 min–1。随着反应体系pH值增大,MTP去除率明显升高,在pH值为9.0时去除效果最好。原因之一是,在酚类亲电取代反应中,反应速率与芳香烃的形态有关。离子态物质的亲电性较强,与自由基的反应速率是分子态的104~105倍[21]。MTP的pKa为9.6,当溶液呈碱性时,MTP以离子态的形式存在,而MTP在酸性溶液中大部分以分子态的形式存在,故碱性溶液中MTP的降解速率高于酸性溶液中[34]。原因二是在碱性条件下UV照射更容易产生•OH,而且氢氧根离子(OH–)是•OH的前驱体[35],表现出较强的氧化性,所以溶液由酸到碱对MTP的去除效率会逐渐变快。
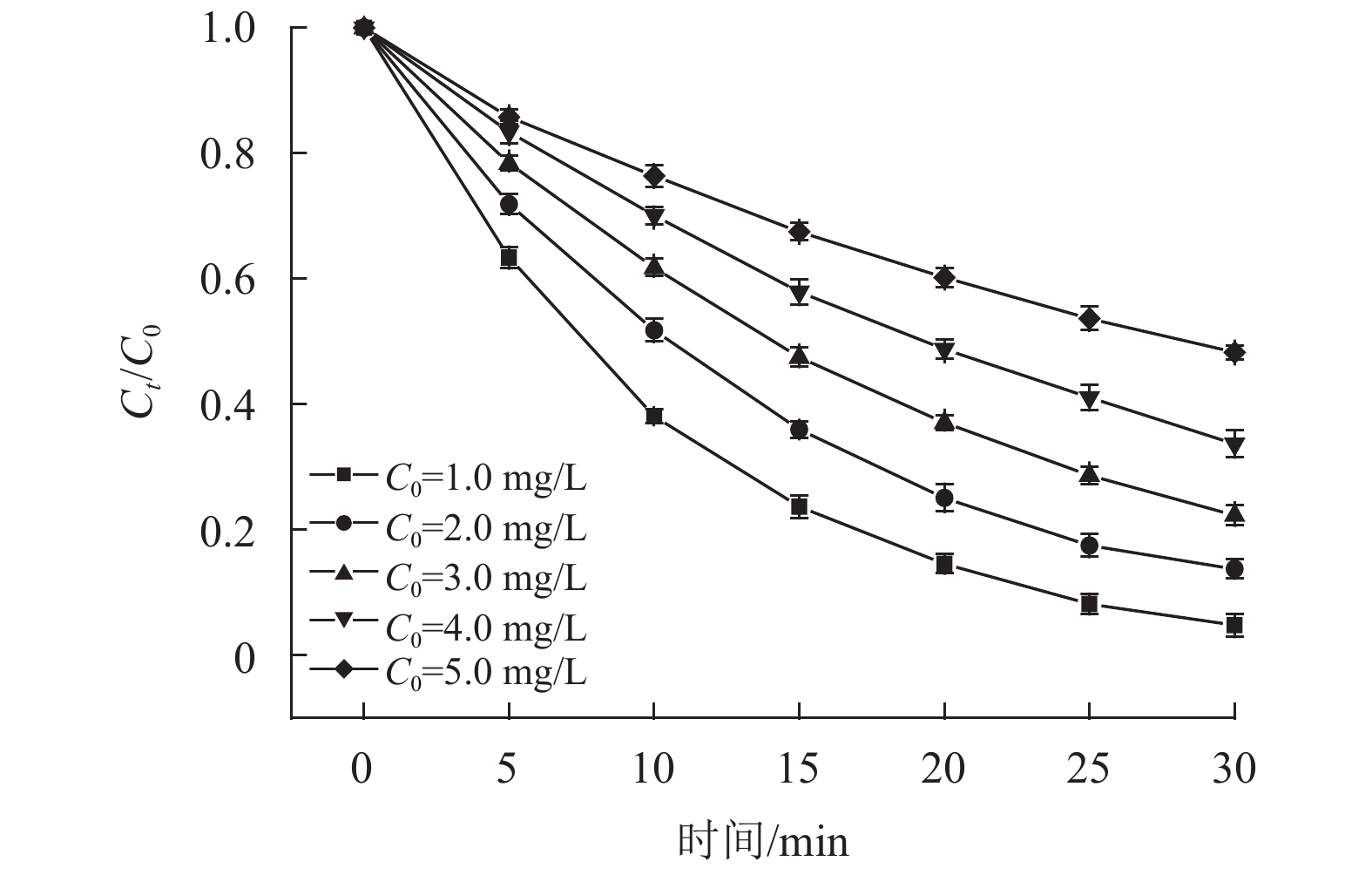
2.5 MTP初始质量浓度的影响在辐照度为2.7 µW/cm2、氯剂量为3.0 mg/L、pH为9.0、温度25 ℃的实验条件下,改变MTP初始质量浓度以考察其对降解速率的影响,结果如图6所示。当MTP初始质量浓度设置为1.0 mg/L时,30 min UV/Cl2反应后MTP的降解率可达95.2%,当MTP初始质量浓度为5.0 mg/L时,30 min反应后降解率仅为51.7%。初始质量浓度的改变对MTP降解率有一定影响,随着MTP初始质量浓度的增加,其降解率随之降低。对不同初始质量浓度下MTP的降解规律进行准一级反应动力学拟合,如表5所示。当MTP初始质量浓度由1.0 mg/L增至5.0 mg/L时,MTP的降解速率降至原速率的22.5%,即从0.1024 min–1降低到0.0230 min–1。
|
图 6 MTP初始质量浓度的影响 Figure 6 Effect of initial mass concentration on degradation |
| 表 5 不同初始质量浓度下UV/Cl2降解MTP一级动力学拟合方程及降解速率 Table 5 First-order kinetics equation and degradation rate of the degradation of metoprolol by UV/Cl2 at different initial mass concentration |
不同初始质量浓度下MTP的降解规律均符合拟一级反应动力学,而且其降解速率随着底物质量浓度增加而减小。初始质量浓度对MTP降解产生的影响是因为在辐照度与氯剂量不变的情况下自由基的产生数量是一定的,MTP初始质量浓度的增加,势必使底物之间竞争加剧,进而减小了降解反应速率。另一个原因是较高质量浓度的MTP会生成较多的中间产物,这些中间产物会消耗一定量的氧化自由基,进而降低了MTP的去除。
2.6 自由基抑制剂的影响为了进一步验证自由基在UV/ Cl2体系中对MTP的降解作用,本文分析了不同浓度的TBA对MTP的去除效果。TBA通常用作•OH和•Cl的抑制剂,而不是•Cl2–,因为它能够与•Cl和•OH快速反应,二级速率常数分别高达6×108,1.9×109 L·(mol·s) –1,而与•Cl2–反应缓慢,速率常数为7×102 L·(mol·s)–1[36]。图7的结果表明,随着初始TBA浓度从0上升到5 mmol/L,MTP的去除率从95.2%下降到87.3%。此外,随着TBA浓度不断增大,MTP的降解速率不断降低,到20 mmol/L,MTP几乎完全抑制了UV/ Cl2体系对MTP的降解。
|
图 7 自由基抑制剂TBA浓度的影响 Figure 7 Effect of the concentration of free-radical scavenger TBA on degradation |
对反应进行准一级动力学拟合后结果如表6所示,可以发现,当TBA浓度为5 mmol/L时,MTP降解速率为0.0699 min–1,仅为空白实验MTP降解速率的61.58%,随着TBA浓度增加,MTP降解速率持续下降。自由基抑制剂的影响实验表明TBA是有效的自由基淬灭剂,MTP的UV/ Cl2体系降解主要是由自由基完成的。
| 表 6 不同TBA浓度下UV/Cl2降解MTP一级动力学拟合方程及降解速率 Table 6 First-order kinetics equation and degradation rate of the degradation of metoprolol by UV/Cl2 at different concentration of TBA |
(1) 与单独水解(无UV无Cl2)、单独UV光解、单独氯化相比,在紫外发光二极管联合次氯酸钠产生的活性自由基共同作用下,UV/ Cl2工艺降解MTP的效果显著,去除率达95.2%,降解反应符合拟一级降解动力学模型。
(2) MTP降解速率常数随UV辐照度的增加而增大,随MTP初始质量浓度增大而减少,随氯剂量增大先增大后减小,碱性条件明显促进MTP在UV/ Cl2反应中的降解,叔丁醇被证实在MTP的降解反应中产生强烈抑制作用。
| [1] |
胡洪营, 王超, 郭美婷. 药品和个人护理用品(PPCPs)对环境的污染现状与研究进展[J].
生态环境学报, 2005, 14(6): 947-952.
HU H Y, WANG C, GUO M T. The present status of environmental pollution by pharmaceuticals and personal care products (PPCPs)[J]. Ecology and Environmen, 2005, 14(6): 947-952. DOI: 10.3969/j.issn.1674-5906.2005.06.032. |
| [2] |
DAUGHTON C G, TERNES T A. Pharmaceuticals and personal care products in the environment: Agents of subtle change?[J].
Environmental Health Perspectives Supplements, 1999, 107(6): 907-938.
|
| [3] |
MAURER M, ESCHER B I, RICHLE P, et al. Elimination of β-blockers in sewage treatment plants[J].
Water Research, 2007, 41(7): 1614-1622.
DOI: 10.1016/j.watres.2007.01.004. |
| [4] |
FILIPE O M S, MOTA N, SANTOS S A O, et al. Identification and characterization of photodegradation products of metoprolol in the presence of natural fulvic acid by HPLC-UV-MSn[J].
Journal of Hazardous Materials, 2016, 323(Part A): 250-263.
|
| [5] |
QUESADA H B, BAPTISTA A T A, CUSIOLI L F, et al. Surface water pollution by Pharmaceuticals and an alternative of removal by low-cost adsorbents: a review[J].
Chemosphere, 2019, 222: 766-780.
DOI: 10.1016/j.chemosphere.2019.02.009. |
| [6] |
YANG Y, YONG S O, KIM K H, et al. Occurrences and removal of pharmaceuticals and personal care products (PPCPs) in drinking water and water/sewage treatment plants: A review[J].
Science of the Total Environment, 2017, 596-597: 303-320.
DOI: 10.1016/j.scitotenv.2017.04.102. |
| [7] |
EBELE A J, ABDALLAH AE M, HARRAD S. Pharmaceuticals and personal care products (PPCPs) in the freshwater aquatic environment[J].
Emerging Contaminants, 2017, 3(1): 1-16.
DOI: 10.1016/j.emcon.2016.12.004. |
| [8] |
SCHEURER M, RAMIL M, METCALFE C D, et al. The challenge of analyzing beta-blocker drugs in sludge and wastewater[J].
Analytical Bioanalytical Chemistry, 2010, 396: 845-856.
DOI: 10.1007/s00216-009-3225-7. |
| [9] |
RUBIROLA A, LLORCA M, RODRIGUEZ-MOZAZ S, et al. Characterization of metoprolol biodegradation and its transformation products generated in activated sludge batch experiments and in full scale WWTPs[J].
Water Research, 2014, 63: 21-32.
DOI: 10.1016/j.watres.2014.05.031. |
| [10] |
LACEY C, BASHA S, MORRISSEY A, et al. Occurrence of pharmaceutical compounds in wastewater process streams in Dublin, Ireland[J].
Environmental Monitoring, 2012, 184: 1049-1062.
DOI: 10.1007/s10661-011-2020-z. |
| [11] |
VIENO N M, HARKKI H, TUHKANEN T, et al. Occurrence of pharmaceuticals in river water and their elimination in a pilot-scale drinking water treatment plant[J].
Environmental Science Technology, 2007, 41(14): 5077-5084.
DOI: 10.1021/es062720x. |
| [12] |
BEHERA S K, KIM H W, OH J E, et al. Occurrence and removal of antibiotics, hormones and several other pharmaceuticals in wastewater treatment plants of the largest industrial city of Korea[J].
Science of the Total Environment, 2011, 409(20): 4351-4360.
DOI: 10.1016/j.scitotenv.2011.07.015. |
| [13] |
金玲. 膜生物反应器去除水中PPCPs的效果及SRT的影响研究[D]. 哈尔滨: 哈尔滨工业大学, 2010.
|
| [14] |
张永吉, 刘文君, 张琳. 氯对紫外线灭活枯草芽孢杆菌的协同作用[J].
环境科学, 2006, 27(2): 329-332.
ZHANG Y J, LIU W J, ZHANG L. Synergistic disinfection of bacillus subtilis spores by UV irradiation and chlorine[J]. Environmental Science, 2006, 27(2): 329-332. DOI: 10.3321/j.issn:1001-0742.2006.02.022. |
| [15] |
陈成, 杨绍贵, 孙成, 等. 阿特拉津在紫外-氯消毒中的转化特性及机理研究[J].
农业环境科学学报, 2009, 28(6): 1302-1306.
CHEN C, YANG S G, SUN C, et al. Conversion characteristics and mechanism of atrazine in a combination of UV and chlorination[J]. Journal of Agro-Environment Science, 2009, 28(6): 1302-1306. DOI: 10.3321/j.issn:1672-2043.2009.06.037. |
| [16] |
FANG J, FU Y, SHANG C J, et al. The roles of reactive species in micropollutant degradation in the UV/free chlorine system[J].
Environmental Science, 2014, 48(3): 1859-1868.
DOI: 10.1021/es4036094. |
| [17] |
刘嘉健, 吴梓昊, 方晶云. UV/氯高级氧化技术对水中嗅味物质的降解动力学研究[C]//2015年中国环境科学学会年会论文集.北京: 中国环境科学出版社, 2015: 44-49.
|
| [18] |
KONG X J, JIANG J, MA J, et al. Degradation of atrazine by UV/chlorine: efficiency, influencing factors, and products[J].
Water Research, 2016, 90: 15-23.
DOI: 10.1016/j.watres.2015.11.068. |
| [19] |
PAN Y H, CHENG S S, YANG X, et al. UV/chlorine treatment of carbamazepine: transformation products and their formation kinetics[J].
Water Research, 2017, 116: 254-265.
DOI: 10.1016/j.watres.2017.03.033. |
| [20] |
赵刘柱, 吴敏, 朱延平, 等. 紫外−氯降解非那西丁影响因素及机理研究[J].
水处理技术, 2019, 45(3): 69-73.
ZHAO L Z, WU M, ZHU Y P, et al. Influencing factors and mechanism of ultraviolet/chorine degradation on phenacetin[J]. Technology of Water Treatment, 2019, 45(3): 69-73. |
| [21] |
周思琪, 李佳琦, 杜尔登, 等. UV/Cl工艺对三氯生的去除与降解机理研究[J].
中国环境科学, 2019, 39(3): 1000-1008.
ZHOU S Q, LI J Q, DU E D, et al. Removal and degradation mechanism of triclosan by the UV/clorine process[J]. China Environmental Science, 2019, 39(3): 1000-1008. DOI: 10.3969/j.issn.1000-6923.2019.03.013. |
| [22] |
冉治霖, 方远航, 唐婧, 等. 紫外LED协同纳米TiO2光催化处理水中PPCPs的研究综述[J].
深圳信息职业技术学院学报, 2018, 16(2): 72-77.
RAN Z L, FANG Y H, TANG J, et al. Overview of the researches on UV LED and nano-TiO2 treatment of PPCPs in water[J]. Journal of Shenzhen Institute of Information Technology, 2018, 16(2): 72-77. DOI: 10.3969/j.issn.1672-6332.2018.02.013. |
| [23] |
RENNECKER J L, DRIEDGER A M, RUBIN S A, et al. Synergy in sequential inactivation of cryptosporidium parvum with ozone/free chlorine and ozone/monochloramine[J].
Water Research, 2000, 34(17): 4121-4130.
DOI: 10.1016/S0043-1354(00)00188-3. |
| [24] |
GUO Z B, LIN Y L, XU B, et al. Degradation of chlortoluron during UV irradiation and UV/chlorine processes and formation of disinfection by-products in sequential chlorination[J].
Chemical Engineering Journal, 2016, 283: 412-419.
DOI: 10.1016/j.cej.2015.07.074. |
| [25] |
陆保松, 马晓雁, 李青松, 等. NaClO、UV及UV/NaClO消毒过程中TCC的去除特性及遗传毒性[J].
中国环境科学, 2018, 38(5): 1752-1759.
LU B S, MA X Y, LI Q S, et al. Study on the removal characteristics and genotoxicity of trichlorocarban during disinfections by NaClO, UV and UV/NaClO[J]. China Environment Scince, 2018, 38(5): 1752-1759. DOI: 10.3969/j.issn.1000-6923.2018.05.018. |
| [26] |
潘继生, 邓家云, 张棋翔, 等. 羟基自由基高级氧化技术应用进展综述[J].
广东工业大学学报, 2019, 36(2): 70-77.
PAN J S, DENG J Y, ZHANG Q X, et al. A review of the application of advanced oxidation technology of hydroxyl radicals[J]. Journal of Guangdong University of Technology, 2019, 36(2): 70-77. DOI: 10.12052/gdutxb.180121. |
| [27] |
韩志涛, 杨少龙, 郑德康, 等. 紫外辐照强化 NaClO溶液湿法脱硝的实验研究[J].
科学技术与工程, 2016, 16(28): 134-138.
HAN Z T, YANG S L, ZHENG D K, et al. No removal from simulated flue gas by UV-irradiated sodium hypochlorite solution[J]. Science Technology and Engineering, 2016, 16(28): 134-138. DOI: 10.3969/j.issn.1671-1815.2016.28.023. |
| [28] |
HIRAKAWA, TSUTOMU, NOSAKA, et al. Properties of O2•– and OH•formed in TiO2 aqueous suspensions by photocatalytic reaction and the influence of H2O2 and some ions
[J].
Langmuir, 2002, 18(8): 3247-3254.
DOI: 10.1021/la015685a. |
| [29] |
BEITZ T, BECHMANN W, MITZNER R. Investigations of reactions of selected azaarenes with radicals in water. 2. chlorine and bromine radicals[J].
The Journal of Physical Chemistry A, 1998, 102(34): 6766-6771.
DOI: 10.1021/jp980655a. |
| [30] |
伊学农, 方佳男, 高玉琼, 等. 紫外线-氯联合高级氧化体系降解水中的萘普生[J].
环境工程学报, 2019, 13(5): 1030-1037.
YI X N, FANG J N, GAO Y Q, et al. Degradation of naproxen in water by UV/chlorine advanced oxidation process[J]. Chinese Journal of Environmental Engineering, 2019, 13(5): 1030-1037. DOI: 10.12030/j.cjee.201811102. |
| [31] |
KONG X, WU Z, REN Z, et al. Degradation of lipid regulators by the UV/chlorine process: Radical mechanisms, chlorine oxideradical(ClO•)-mediated transformation pathways and toxicity changes
[J].
Water Research, 2018, 137: 242-250.
DOI: 10.1016/j.watres.2018.03.004. |
| [32] |
XIANG Y Y, FANG J, Shang C. Kinetics and pathways of ibuprofen degradation by the UV/chlorine advanced oxidation process[J].
Water Research, 2016, 90: 301-308.
DOI: 10.1016/j.watres.2015.11.069. |
| [33] |
YIN K, HE Q, LIU C B, et al. Prednisolone degradation by UV/chlorine process: influence factors, transformation products and mechanism[J].
Chemosphere, 2018, 212: 56-66.
DOI: 10.1016/j.chemosphere.2018.08.032. |
| [34] |
BENITEZ F J, REAL F J, ACERO J L, et al. Removal of selected pharmaceuticals in waters by photochemical processes[J].
Journal of Chemical Technology Biotechnology Biotechnology, 2009, 84(8): 1186-1195.
DOI: 10.1002/jctb.2156. |
| [35] |
ZHAO J H. Research on UV/TiO2 photocatalytic oxidation of organic matter in drinking water and its influencing factors
[J].
Applied Mechanics and Materials, 2012, 12(Part A): 445-452.
|
| [36] |
GILBERT B C, STELL J K, PEET W J, et al. Generation and reactions of the chlorine atom in aqueous solution[J].
Journal of the Chemical Society Faraday Transactions, 1988, 84(10): 3319-3330.
DOI: 10.1039/f19888403319. |
 2021, Vol. 38
2021, Vol. 38

