文章信息
- 梁家浩, 魏智强, 朱学良, 张旭东, 武晓娟, 姜金龙
- LIANG Jia-hao, WEI Zhi-qiang, ZHU Xue-liang, ZHANG Xu-dong, WU Xiao-juan, JIANG Jin-long
- 尖晶石结构Ni掺杂ZnFe2O4纳米颗粒的性能表征
- Property characterization of spinel structure Ni-doped ZnFe2O4 nanoparticles
- 材料工程, 2019, 47(10): 113-119
- Journal of Materials Engineering, 2019, 47(10): 113-119.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2018.000042
-
文章历史
- 收稿日期: 2018-01-11
- 修订日期: 2019-01-15
2. 兰州理工大学 理学院, 兰州 730050
2. School of Science, Lanzhou University of Technology, Lanzhou 730050, China
近年来,尖晶石结构铁氧体纳米晶的独特结构和优良性能引起人们的广泛关注。ZnFe2O4是一种多功能尖晶石结构半导体材料,也是一种重要的软磁铁氧体材料,禁带宽度较窄(约为1.9eV),属于Fd3m空间群[1]。其具有无毒、化学性质稳定、耐光化学腐蚀、制备简便和成本低等特点,对太阳光敏感,可见光吸收范围广,光催化活性较强[2-3],在生物医学、光催化、磁流体、光电转换、抗菌剂和磁性材料等方面具有广阔的应用前景[4-7]。尖晶石结构铁氧体的通式为AB2O4,其中A和B分别表示二价金属离子占据的四面体位置和三价金属离子占据的八面体位置。ZnFe2O4是正尖晶石结构,Zn2+占据四面体的A位置,Fe3+占据八面体的B位置,A位和B位金属离子可以相互替换,导致其性质具有多变性[8-9]。铁氧体纳米晶的微观结构和物理性能主要取决于其合成方法以及工艺条件,可以通过过渡金属离子掺杂来调整半导体的晶体结构和能带结构,以达到有效控制新型半导体的物理性能[10-11]。制备纳米结构ZnFe2O4的技术主要有机械球磨法[12]、水热法[13]、化学共沉淀法[14]、溶胶凝胶法[15]、微乳液法[16]、共沉淀法[17]、喷雾热解法[18]和静电纺丝法[19]等。与传统技术相比,水热法由于在分子水平上进行反应物之间的相互作用,化学计量比便于控制、反应温度低、合成产物的粒度均匀、纯度高、分散性好,同时操作工艺简单、成本低廉、重复性好、产物的组成和结构容易控制等,是一种理想的制备技术[20]。
本工作利用水热法成功合成不同含量Ni掺杂Zn1-xNixFe2O4(x=0,0.1,0.3,0.5)纳米颗粒,并通过X射线衍射(XRD)、高分辨透射电子显微镜(HRTEM)和选区电子衍射(SAED)、X射线能量色散分析(XEDS)、紫外可见吸收光谱(UV-Vis)、傅里叶变换红外光谱(FT-IR)和振动样品磁强计(VSM)等表征技术研究Ni掺杂浓度对Zn1-xNixFe2O4纳米复合材料的形貌、晶体结构、光学性能和磁学性能的影响。
1 实验采用水热法制备Zn1-xNixFe2O4(x=0,0.1,0.3,0.5)样品。使用的试剂主要有硝酸镍(Ni(NO3)2·6H2O)、硝酸铁(Fe(NO3)3·9H2O)、硝酸锌(Zn(NO3)2·6H2O)、十六烷基三甲基溴化铵(CTAB)、氢氧化钠、无水乙醇和去离子水等,均为分析纯。具体制备过程:根据Zn1-xNixFe2O4的化学公式和金属离子的摩尔配比,分别称取Ni(NO3)2·6H2O,Zn(NO3)2·6H2O和Fe(NO3)3·9H2O,溶解于蒸馏水中得到0.02mol/L混合金属盐溶液,并在室温下进行磁力搅拌使之混合均匀。同时称取适量NaOH溶于40mL蒸馏水中,磁力搅拌至完全溶解,用于调控混合金属盐溶液的pH值。称取一定量的表面活性剂CTAB缓慢加入上述混合溶液中,磁力搅拌至充分混合。然后将混合溶液转移到聚四氟乙烯内衬的反应釜中,在160℃电热恒温干燥箱中进行24h水热反应。反应结束后自然冷却至室温,对所得沉淀分别采用去离子水和无水乙醇反复离心洗涤。最后将样品置于真空干燥器中60℃下干燥,即得到Zn1-xNixFe2O4样品。
样品的物相结构采用D/Max-2400X型射线衍射仪(Cu靶Kα辐射,X射线波长为0.154nm,扫描范围为10°~80°,扫描速率为12(°)/min,步长为0.02°)进行分析,并用Scherrer公式计算晶粒粒度;样品的形貌、粒径及其分布采用JEM-2010型高分辨透射电子显微镜(加速电压200kV,点分辨率0.19nm)观察,配以KEVEX型X射线能量色散分析谱仪(EDS)分析确定其化学成分;样品的吸收光谱采用紫外可见近红外光谱仪(TU-1901)进行测定;采用Nicolet Nexus 670FT-IR型傅里叶变换红外光谱仪进行粉体结构分析;室温下的磁滞回线采用振动试样磁强计(VSM, Lakeshore 7304)测定。
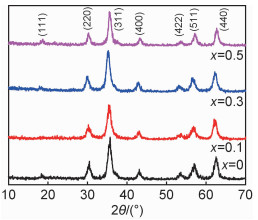
2 结果与讨论 2.1 物相分析不同含量Ni掺杂Zn1-xNixFe2O4(x=0,0.1,0.3,0.5)样品的X射线衍射图如图 1所示。纯ZnFe2O4样品衍射的峰位在2θ=18.32°,30.47°,35.42°,43.09°,53.62°,57.01°和62.53°出现7个明显的特征衍射峰,分别对应与ZnFe2O4的(111),(220),(311),(400),(422),(511)和(440)晶面,与立方尖晶石结构ZnFe2O4的JCPDS卡片(No.022-1012)基本一致。所有Ni掺杂样品的XRD谱图中没有呈现杂质相的衍射峰,各个衍射峰的位置和相对强度与立方相ZnFe2O4尖晶石结构吻合。
|
图 1 Zn1-xNixFe2O4(x=0,0.1,0.3,0.5)样品的XRD谱图 Fig. 1 XRD patterns of Zn1-xNixFe2O4(x=0, 0.1, 0.3, 0.5)samples |
根据X射线衍射理论,采用Scherrer公式D=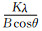
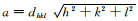
| x | 2θ/(°) | FWHM/ (°) |
dhkl/ nm |
a/nm | D/nm |
| 0 | 35.421 | 0.668 | 0.2532 | 0.839 | 12 |
| 0.1 | 35.719 | 0.619 | 0.2512 | 0.833 | 13 |
| 0.3 | 35.839 | 0.528 | 0.2510 | 0.830 | 16 |
| 0.5 | 35.978 | 0.422 | 0.2494 | 0.827 | 20 |
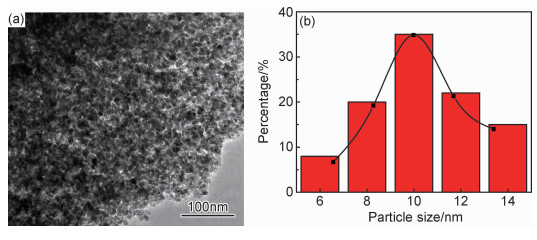
纯ZnFe2O4样品的HRTEM图和相应粒径分布如图 2所示。由图 2(a)可知,纯ZnFe2O4样品的形貌主要为不规则的椭球形,表面比较粗糙,边缘不规整。纳米颗粒之间存在范德华力、库仑力或化学键合作用,呈现不同程度的团聚现象。样品的粒径分布直方图如图 2(b)所示,明显看出颗粒尺寸比较均匀,主要分布在5~15nm范围内,平均粒径约为10nm。图 3为Zn0.7Ni0.3Fe2O4样品的HRTEM图和相应粒径分布图。与纯ZnFe2O4样品相比,掺杂样品的颗粒尺寸变得比较粗大,粒度分布区间变宽,形貌基本是椭球形,表面比较粗糙,粒度主要分布在10~25nm范围内,平均粒度约为20nm。
|
图 2 纯ZnFe2O4样品的HRTEM图(a)和相应粒径分布(b) Fig. 2 HRTEM image(a) and the corresponding histogram of the particle size distribution(b) of pure ZnFe2O4 samples |
|
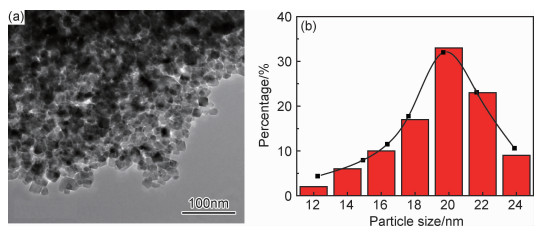
图 3 Zn0.7Ni0.3Fe2O4样品的HRTEM图(a)和相应粒径分布(b) Fig. 3 HRTEM image(a) and the corresponding histogram of the particle size distribution(b)of Zn0.7Ni0.3Fe2O4 samples |
图 4为Zn0.7Ni0.3Fe2O4样品的HRTEM图和对应选区电子衍射图。图 4(a)显示出排列整齐的晶格条纹,说明纳米颗粒结晶化程度良好。计算得到晶面间距约为0.251nm,对应与立方尖晶石结构ZnFe2O4的(311)晶面,说明ZnFe2O4纳米晶沿着(311)晶面择优生长,由于晶格收缩使得晶格间距小于标准块体ZnFe2O4的值,HRTEM分析和XRD分析结果一致。表明Ni2+以替代Zn2+的形式掺杂到ZnFe2O4晶格中,尖晶石型ZnFe2O4纳米晶的晶体结构没有改变,掺杂Ni只是改变了其微观结构,但未引起ZnFe2O4晶体结构的变化。Zn0.7Ni0.3Fe2O4的选区电子衍射图如图 4(b)所示。由于晶粒之间取向随机, 在衍射图样

|
图 4 Zn0.7Ni0.3Fe2O4样品的HRTEM图(a)和对应选区电子衍射图(b) Fig. 4 HRTEM image(a) and SAED pattern(b) of Zn0.7Ni0.3Fe2O4 samples |
中呈现一系列规则的不同半径的同心圆环,表明掺杂样品Zn0.7Ni0.3Fe2O4属于多晶结构。多晶衍射环由里到外分别对应于ZnFe2O4的(111),(220),(311),(400),(422),(511)和(440)晶面。SAED和HRTEM的研究结果进一步表明,所得样品为立方相ZnFe2O4尖晶石结构,与XRD分析结果相一致。
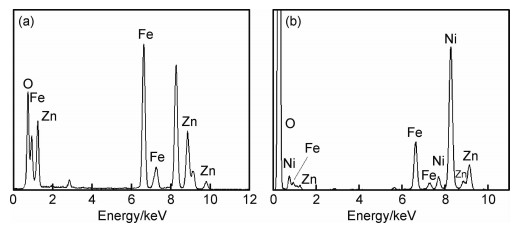
2.3 成分分析为进一步验证所制备样品的化学成分,对ZnFe2O4和Zn0.7Ni0.3Fe2O4样品进行了XEDS谱图分析,如图 5所示。图 5(a)为纯ZnFe2O4样品的XEDS谱图,在0.9,6.7,7.3keV处出现了Fe的特征峰,在1.2,8.9,9.8keV处出现了Zn的特征峰,在0.6keV处出现O的特征峰,可见样品中主要存在Zn,Fe和O元素的特征峰。在图 5(b)的Zn0.7Ni0.3Fe2O4样品的XEDS谱图中,除了Zn,Fe和O元素的特征峰外,还在0.8, 7.7,8.4keV处出现了Ni元素的特征峰,说明掺杂样品中存在Ni元素,而纯ZnFe2O4样品并没有发现Ni元素的存在。XEDS结果进一步表明,采用水热法成功合成Ni掺杂ZnFe2O4纳米晶,Ni2+以替代Zn2+的形式掺杂到ZnFe2O4晶格中。
|
图 5 ZnFe2O4(a)和Zn0.7Ni0.3Fe2O4(b)样品的XEDS谱图 Fig. 5 XEDS spectra of ZnFe2O4(a) and Zn0.7Ni0.3Fe2O4 samples(b) |
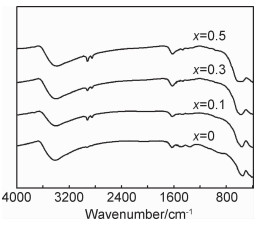
Zn1-xNixFe2O4(x=0,0.1,0.3,0.5)样品的红外光谱图如图 6所示。由于样品表面的化学吸附水引起分子间氢键结合后O—H基团的纵向伸缩振动,因此在3420cm-1附近出现1个明显的强而宽的吸收带。由于N—H键的伸缩振动导致在2923cm-1和2854cm-1附近出现弱吸收,样品中游离水中的H—O—H弯曲振动产生1627cm-1处的吸收峰。由于样品在制备和随后的洗涤过程中可能引入一些有机杂质,在1382cm-1处的吸收峰对应的是C—H键的弯曲振动。对于尖晶石结构ZnFe2O4纳米晶,Zn2+主要占据A位,Fe3+主要占据B位,在563cm-1和410cm-1处出现了2个明显的特征吸收峰,分别对应于四面体位中的Zn—O键的伸缩振动和八面体位中的Fe—O键的振动模式。可以看出,随着Ni掺杂浓度的增加,样品的红外光谱变化不明显,表明Ni2+成功取代Zn2+位置进入ZnFe2O4晶格不改变晶体结构,此结果与XRD实验结果吻合。
|
图 6 Zn1-xNixFe2O4(x=0,0.1,0.3,0.5)样品的红外光谱 Fig. 6 FT-IR spectra of Zn1-xNixFe2O4(x=0, 0.1, 0.3, 0.5)samples |
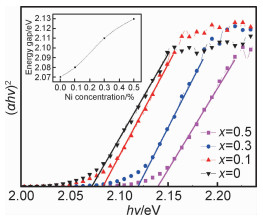
Zn1-xNixFe2O4纳米晶为直接带隙半导体材料,光学吸收系数α与光学带隙Eg满足Tauc法则[21]:(αhν)2=A(hν-Eg),其中hν是入射光子能量,h是普朗克常数,ν是光的频率,A是常数。样品的(αhν)2与hν的关系曲线如图 7所示,将(αhν)2与hν曲线的线性部分延长至α=0时在hν轴上的截距得到Eg。样品的光学带隙随Ni掺杂浓度的变化如图 7中插图所示,ZnFe2O4,Zn0.9Ni0.1Fe2O4,Zn0.7Ni0.3Fe2O4和Zn0.5Ni0.5Fe2O4的光学带隙分别为2.05,2.08,2.11eV和2.13eV。由此可见,掺杂Zn1-xNixFe2O4纳米晶的带隙大于纯ZnFe2O4,随着Ni掺杂浓度的增加,光学带隙呈增大的趋势,块体ZnFe2O4的带隙为1.9eV,掺杂样品发生了蓝移现象。未掺杂和掺杂Ni对Zn1-xNixFe2O4纳米晶带隙的微小变化表明,半导体激发态和Ni2+的3d能级之间能量的直接转移,红移现象是由于纳米晶粒的量子尺寸效应和表面效应,随着Ni掺杂量的增加,能带电子与主晶格Zn位的Ni2+局域d壳层电子之间的sp-d自旋交互作用。这表明主晶格中Zn2+被Ni2+取代,由于Ni2+的半径小于Zn2+的半径,从而导致主晶格收缩,使得导带电位变大,价带电位变小,能带增大。
|
图 7 Zn1-xNixFe2O4(x=0,0.1,0.3,0.5)样品的(αhν)2与hν的关系曲线 Fig. 7 (αhν)2 versus hν of Zn1-xNixFe2O4(x=0, 0.1, 0.3, 0.5)samples |
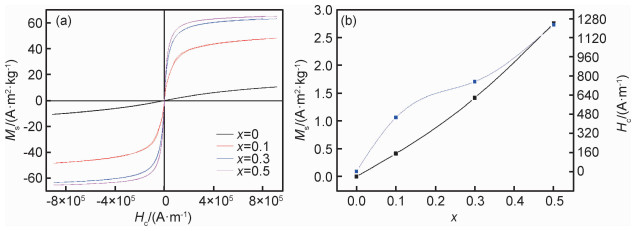
Zn1-xNixFe2O4样品在室温下的磁滞回线及矫顽力Hc和饱和磁化强度Ms随Ni含量的变化关系如图 8所示。由图 8(a)可知,纯ZnFe2O4纳米晶在室温下的磁滞回线通过原点,剩磁和矫顽力是零,说明纯ZnFe2O4纳米晶在室温下表现超顺磁性。Ni掺杂Zn1-xNixFe2O4样品在室温下呈现出明显的滞后环,具有室温铁磁性,磁化强度随磁场增大而达到饱和。由图 8(b)可知,样品矫顽力随着Ni掺杂量的增加而增加。掺杂Zn1-xNixFe2O4纳米晶的镍铁磁性的起源主要是由于Ni2+取代Zn2+位置进入ZnFe2O4晶格引起的,而不是由磁性镍金属团簇或其他化合物引起,通过XRD和HRTEM研究表明,样品中并不存在杂质相。这是由于ZnFe2O4正尖晶石结构中Zn2+占据的四面体位置,由4个氧离子包围形成的四面体空隙,Fe3+占据的八面体位置,由6个氧离子包围形成的八面体空隙。在室温下,纯ZnFe2O4的Fe3+由于B-O-B超交换作用而呈反铁磁有序结构,相互间磁矩反平行排列,结果净磁矩等于零,所以表现为超顺磁性。对于Ni掺杂的Zn1-xNixFe2O4样品,当颗粒尺寸达到纳米尺度时,Zn1-xNixFe2O4纳米晶中阳离子分布发生显著变化,部分Fe3+进入四面体的A位,Zn2+进入八面体的B位,当磁性Ni2+替代ZnFe2O4中的一部分非磁性Zn2+,Ni2+有强烈的B位趋势。随着掺杂比例的增大,B位Ni2+增多导致A-B之间超交换作用的离子对数增多,自旋耦合作用增强。Zn1-xNixFe2O4纳米晶中占据四面体A位的Ni2+和占据八面体B位的Fe3+分布不平衡,A位的总磁矩与B位的总磁矩不相等,使得粒子的净磁矩不为零,表现出较强的铁磁性。
|
图 8 Zn1-xNixFe2O4(x=0,0.1,0.3,0.5)样品的磁滞回线(a)及Ms和Hc随Ni含量x的变化关系(b) Fig. 8 M-Hloops of Zn1-xNixFe2O4(x=0, 0.1, 0.3, 0.5) samples(a), and relationship of M sand Hc with Ni doping concentrations x(b) |
(1) 采用水热法合成了Ni掺杂Zn1-xNixFe2O4纳米颗粒,样品形貌为不规则的椭球形,粒度比较均匀,颗粒有一定的团聚现象,结晶性良好。
(2) Zn1-xNixFe2O4纳米晶中,Ni2+以替代Zn2+的形式掺杂到ZnFe2O4晶格中,生成立方相ZnFe2O4尖晶石结构,随着Ni含量的增加,晶粒尺寸增大,晶格常数发生收缩。
(3) 随着Ni掺杂浓度的增加, 样品的红外光谱吸收峰位置基本没有变化,UV-Vis光谱发生了蓝移现象,光学带隙增大。
(4) 在室温下, 纯ZnFe2O4纳米晶呈现超顺磁性,掺杂样品具有明显的铁磁性,矫顽力随着Ni掺杂量的增加而增大。
| [1] | TANG X Q, HOU X H, YAO L M, et al. Mn-doped ZnFe2O4, nanoparticles with enhanced performances as anode materials for lithium ion batteries[J]. Materials Research Bulletin, 2014, 57 : 127–134. DOI: 10.1016/j.materresbull.2014.05.038 |
| [2] | HOU G Q, ZHANG Y J, GAO S J. Enhanced visible-light phot-ocatalytic activities of flower-like ZnFe2O4 decorated with Ag3PO4 nanoparticles[J]. Materials Letters, 2017, 209 : 598–601. DOI: 10.1016/j.matlet.2017.08.108 |
| [3] | JING L, XU Y, QIN C, et al. Visible-light-driven ZnFe2O4/Ag/Ag3VO4 photocatalysts with enhanced photocatalytic activity under visible light irradiation[J]. Materials Research Bulletin, 2017, 95 : 607. DOI: 10.1016/j.materresbull.2017.06.003 |
| [4] | CUI C X, XU L J, XIE T P, et al. Synthesis and photocatalytic activity of magnetic heterostructure ZnFe2O4-SrFe12O19[J]. Materials Technology, 2016, 31 (8): 454–462. DOI: 10.1080/10667857.2015.1105578 |
| [5] | TONG G X, DU F F, WU W H, et al. Enhanced reactive oxygen species (ROS) yields and antibacterial activity of spongy ZnO/ZnFe2O4 hybrid micro-hexahedra selectively synthesized through a versatile glucose-engineered co-precipitation/annealing process[J]. Journal of Materials Chemistry B, 2013 (20): 2647–2657. |
| [6] | GUO P, CUI L, WANG Y, et al. Facile synthesis of ZnFe2O4 nanoparticles with tunable magnetic and sensing properties[J]. Langmuir, 2013, 29 (28): 8997–9003. DOI: 10.1021/la401627x |
| [7] | THANKACHAN R M, RAHMAN M M, SULTANA I, et al. Enhanced lithium storage in ZnFe2O4-C nanocomposite produced by a low-energy ball milling[J]. Journal of Power Sources, 2015, 282 : 462–470. DOI: 10.1016/j.jpowsour.2015.02.039 |
| [8] | WANG H G, GAO J M, LIU W, et al. Recovery of metal-doped zinc ferrite from zinc-containing electric arc furnace dust:process development and examination of elemental migration[J]. Hydro-metallurgy, 2016, 166 : 1–8. |
| [9] | KHAZAEI A, RANJBARAN A, ABBASI F, et al. ABBASI F, et al. Synthesis, characterization and application of ZnFe2O4 nanoparticles as a heterogeneous ditopic catalyst for the synthesis of pyrano[2, 3-d] pyrimidines[J]. RSC Advances, 2015, 5 (18): 13643–13647. DOI: 10.1039/C4RA16664G |
| [10] | ZHANG L, GUAN H, DONG Q, et al. Synthesis and charac-terization of Ni0.7Zn0.3Fe2O4 and Mn0.7Zn0.3Fe2O4 nanoparti-cles by water-in-oil microemulsion[J]. Integrated Ferroelec-trics, 2014, 154 (1): 103–109. DOI: 10.1080/10584587.2014.904170 |
| [11] | BAYKAL A, ESIR S, DEMIR A, et al. Magnetic and optical properties of Cu1-xZnxFe2O4 nanoparticles dispersed in a silica matrix by a sol-gel auto-combustion method[J]. Ceramics Inter-national, 2015, 41 (1): 231. DOI: 10.1016/j.ceramint.2014.08.063 |
| [12] | CHEN Z H, SUN Y P, KANG Z T, et al. Preparation of ZnxCo1-xFe2O4 nanoparticles by microwave-assisted ball milling[J]. Ceramics International, 2014, 40 (9): 14687–14692. DOI: 10.1016/j.ceramint.2014.06.058 |
| [13] | WANG Y L, ZHANG L X. Synthesis and electrochemical performance of hollow ZnFe2O4 microspheres[J]. Chinese Journal of Process Engineering, 2015, 15 (1): 169–173. |
| [14] | ERFANINIA N, TAYEBEE R, FOLETTO E L, et al. Prepa-ration of magnetically recyclable ZnFe2O4 nanoparticles by easy single-step co-precipitation method and their catalytic perfor-mance in the synthesis of 2-aminothiophenes[J]. Applied Orga-nometallic Chemistry, 2018, 32 (2): 4047. DOI: 10.1002/aoc.4047 |
| [15] | WU Y L, WANG Q H, WANG L, et al. Preparation of ZnFe2O4 nanometer powders by sol-gel method and research about its electrochemical performance[J]. Advanced Materials Research, 2013, 743 : 179–182. DOI: 10.4028/www.scientific.net/AMR.743.179 |
| [16] | GAO D. Synthesis and characterization of NiZnFeO and MnZnFeO nanoparticles by water-in-oil microemulsion[J]. Integrated Ferroelectrics an International Journal, 2014, 154 (1): 103–109. DOI: 10.1080/10584587.2014.904170 |
| [17] | YANG L I, LAI X, QIN D, et al. Preparation of spinel CoxZn1-x-Fe2O4 nanocrystallines by sodium hydroxide co-precipitation met-hod[J]. Journal of Sichuan Normal University, 2013, 36 (4): 610–613. |
| [18] | SUTKA A, ZAVICKIS J, MEZINSKIS G, et al. Ethanol moni-toring by ZnFe2O4 thin film obtained by spray pyrolysis[J]. Sensors & Actuators B Chemical, 2013, 176 (6): 330–334. |
| [19] | WANG C, TAN X, YAN J, et al. Electrospinning direct synth-esis of magnetic ZnFe2O4/ZnO multi-porous nanotubes with enhanced photocatalytic activity[J]. Applied Surface Science, 2017, 396 : 780–790. DOI: 10.1016/j.apsusc.2016.11.029 |
| [20] | DHIMAN M, SHARMA R, KUMAR V, et al. Morphology controlled hydrothermal synthesis and photocatalytic properties of ZnFe2O4 nanostructures[J]. Ceramics International, 2016, 42 (11): 12594–12605. DOI: 10.1016/j.ceramint.2016.04.115 |
| [21] | SHETTY K, RENUKA L, NAGASWARUPA H P, et al. A comparative study on CuFe2O4, ZnFe2O4 and NiFe2O4:morph-ology, impedance and photocatalytic studies[J]. Materials Today Proceedings, 2017, 4 (11): 11806–11815. DOI: 10.1016/j.matpr.2017.09.098 |
 2019, Vol. 47
2019, Vol. 47


