文章信息
- 权月, 尹杰, 王园园, 包斯元, 鲁雄, 冯波, 周杰
- QUAN Yue, YIN Jie, WANG Yuan-yuan, BAO Si-yuan, LU Xiong, FENG Bo, ZHOU Jie
- 暴露高活性晶面的TiO2纳米管的制备及生物活性
- Preparation and bioactivity of TiO2 nanotubes exposed with highly active facets
- 材料工程, 2019, 47(4): 97-104
- Journal of Materials Engineering, 2019, 47(4): 97-104.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2017.000761
-
文章历史
- 收稿日期: 2017-06-15
- 修订日期: 2018-10-22
2. 西南交通大学 材料先进技术教育部重点实验室, 成都 610031
2. Key Laboratory for Advanced Technologies of Materials(Ministry of Education), Southwest Jiaotong University, Chengdu 610031, China
钛及钛合金因具有良好的生物相容性,被广泛应用在人工骨关节、形状记忆合金等医用领域[1-2]。钛本身为生物惰性,且大部分反应都发生在钛表面的TiO2层,其生物学性能主要由其表面结构所决定,为增强其生物活性,常对其进行表面改性以适应不同的生物应用环境。
锐钛矿型TiO2相较于金红石型有较高的生物活性和稳定性,因此受到较多关注[3-5]。而锐钛矿型TiO2不同晶面具有不同的原子密度,从而使得具有不同优势晶面族的TiO2具有不同的表面能和化学活性。其中,锐钛矿TiO2晶面中表面能依次为(101)(0.44J/m2) < (100)(0.53J/m2) < (001)(0.90J/m2)[6-8],表面能越大的晶面具有相对更好的潜在化学活性。一般来说,TiO2中晶面的分布遵从Wulff规则[9-11],锐钛矿中主要以表面能较小热力学稳定的(101)面为主,而较高能量的活性表面(001)晶面较少。由于(001)晶面具有更高的潜在化学活性,近年来,制备具有更高比例(001)晶面的锐钛矿TiO2引起了广大研究者浓厚的兴趣,并取得了一定的进展[12-14]。Yang等[15]以四氟化钛为前驱体,氢氟酸为生长控制剂,180℃水热反应不同时间后,得到规整的四方锥截面状TiO2,其(001)晶面比例达47%。随后,此课题组[6]研究了合成暴露(001)晶面的TiO2,然而制备方法都是采用HF作为生长控制剂以稳固(001)晶面族。探索低氟或无氟的合成方法成了目前TiO2晶面定向合成的一个研究热点。同时,对于TiO2晶面的性能研究目前还主要集中在其光电应用方面[16-17],而关于TiO2中晶面比例对生物学性能的研究较少。
本工作在前期阳极氧化制备TiO2纳米管工作的基础上[18-19],采用多次阳极氧化技术,通过调节电解液中H2O含量制备具有不同晶面族比例的高度有序的TiO2纳米管阵列。通过扫描电子显微镜(SEM)、X射线衍射(XRD)对试样进行表面形貌表征,采用生物矿化和蛋白吸附来考察不同晶面对TiO2纳米管生物活性的影响。
1 实验 1.1 试样制备纯钛片(TA2,ϕ10mm×1.5mm)打磨和预处理后,在HF:HNO3:H2O=1:4:5(体积比)的混酸中进行化学抛光,清洗、干燥备用。40V恒压下反应120min,然后在去离子水中超声震荡,将TiO2纳米管层剥离。样品清洗烘干后进行第二次阳极氧化,恒定电压40V。电解液配比及阳极氧化时间如表 1所示。阳极氧化结束后进行热处理,450℃保温120min。
| Sample | Mass fraction of NH4F/% | Volume fraction/% | Reaction time/min | |||
| H2O | (CH2OH)2 | The first anodic oxidation | The second anodic oxidation | |||
| A | 0.4 | 1 | 99 | 120 | 45 | |
| B | 0.4 | 2 | 98 | 120 | 60 | |
| C | 0.4 | 3 | 97 | 120 | 75 | |
| D | 0.4 | 4 | 96 | 120 | 90 | |
每种样品设置3个平行样,浸入2倍浓度模拟体液(2×SBF),放置于37℃恒温水浴震荡箱中(60r/h)恒温震荡,每24h换一次液,分别在3天和7天取出试样,室温干燥。利用SEM和XRD对试样进行检测,并用称重法计算各个试样矿化前后平均增重。
1.3 蛋白吸附磷酸盐缓冲溶液(PBS)为溶剂,配制牛血清白蛋白(BSA, 1mg/mL)溶液。各试样分别浸入45mL BSA溶液中,37℃水浴恒温震荡,分别吸附0.5,1,2,4,6,12,24h后取出2mL BSA溶液。通过紫外分光光度计(UV,UV-2550)在280nm波长处测量试样BSA溶液的吸光度,计算试样表面蛋白质的吸附量;采用傅里叶变换红外光谱(FT-IR)测量试样表面吸附的BSA结构中的酰胺特征键。
1.4 样品表征采用扫描电镜(FEI,Quanta200)观察试样阳极氧化后的表面形貌;利用(PANalytical X Pert Pro)X射线衍射仪检测晶体学特征,加速电压40kV,电流40mA,Cu靶,扫描范围20°~80°,扫描模式为连续扫描;用衰减全反射傅里叶变换红外光谱仪(ATR-FTIR,Nicolet SXFYIRI 70/Magna 550)研究蛋白吸附后样品表面的成分;利用能量色散光谱(EDS,FEI,Quanta200)分析试样生物矿化后表面元素情况。
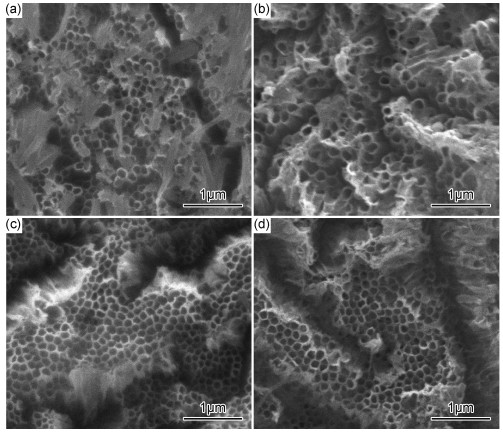
2 结果与讨论图 1是电解液中含H2O为1%,2%,3%和4%的一次阳极氧化后各试样表面的SEM图。可以看出,经过一次阳极氧化后TiO2纳米管呈簇状分布,簇与簇之间存在较大缝隙,且有相互倾轧的趋向,管口有大量的破损。这可能是由于在有机电解液体系中纳米管表面的不均匀腐蚀形成的。电解液中H2O含量的不同会造成纳米管生长速率的不一致,为了得到形貌高度有序且管长近似一致的纳米管阵列,将各试样进行不同时间的二次阳极氧化,表面形貌及断面如图 2所示。各样品表面纳米管阵列呈网状分布,且管状趋近坚固的蜂窝结构,管径大小均匀,约90~110nm,表面光滑,管口无破损及长短不一的情况。由图 2右上的断图面可以看出,经过不同时间的二次阳极氧化后,样品的管长都在4μm左右。说明经过两次阳极氧化后,各样品表面TiO2纳米管阵列形貌规整,管径及管长基本保持一致。
|
图 1 一次阳极氧化后试样的SEM图 (a)1%H2O;(b)2%H2O;(c)3%H2O;(d)4%H2O Fig. 1 SEM images of the samples after the first anodic oxidation (a)1%H2O; (b)2%H2O; (c)3%H2O; (d)4%H2O |

|
图 2 不同时间二次阳极氧化后试样的SEM图 (a)45min;(b)60min;(c)75min;(d)90min Fig. 2 SEM images of the samples after the second anodic oxidation with different time (a)45min; (b)60min; (c)75min; (d)90min |
图 3为经过二次阳极氧化和热处理后各样品的XRD谱图。热处理后纳米管转换成锐钛矿型,但是由于所形成的纳米管层比较薄,有部分X射线穿透照射到钛基底,所以XRD谱图上出现了钛峰。一般而言,锐钛矿TiO2最强衍射峰为(101)晶面,位于2θ=25.28°。然而在2%H2O条件下制备的TiO2纳米管样品,其位于37.8°的(004)晶面的衍射峰强度却明显强于(101)晶面峰强,(004)晶面为优势晶面。说明通过改变电解液中H2O含量,可以让TiO2沿着[001]晶向择优生长,即表现出一定的纹理。虽然这种纳米管的生长行为在以往的文献中也有报道[16, 20-21],但很少有深入研究其结构和性能的。

|
图 3 二次阳极氧化和热处理后试样的XRD谱图 (a)1%H2O; (b)2%H2O; (c)3%H2O; (d)4%H2O Fig. 3 XRD patterns of the samples after the secondary anodic oxidation and heat treatment (a)1%H2O; (b)2%H2O; (c)3%H2O; (d)4%H2O |
当一种材料晶体学取向发生变化时,可以用织构系数Tc(hkl)半定量地衡量指定晶面取向变化的程度,其范围为1(无纹理)到N(单取向晶体)。锐钛矿TiO2(004)晶面的织构系数Tc(004)可以根据Ariosa等报道的方法[22],用式(1)进行计算。
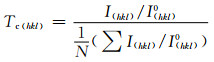
|
(1) |
式中:Ihkl为试样实际测量(hkl)晶面的衍射强度;Ihkl0为(hkl)晶面标定强度,即各项同性随机取向的粉末反射强度;N是布拉格反射级数(本实验中N=6)。对于一个各向同性随机取向微晶,其Tc(hkl)=1,而Tc值大于1则代表有大量微晶在(hkl)方向择优取向。(004)晶面织构系数Tc(004)和强度比值(I(004)/I(101))计算结果如表 2所示。随着电解液体系中H2O含量的逐渐增大,TiO2纳米管中锐钛矿TiO2晶面族强度比值和织构系数都呈现先增加后减小的变化趋势,并在H2O含量为2%的B试样中达到最大值。各样品的晶面织构系数Tc(004)均大于1,说明在本实验条件下,制备得到的TiO2纳米管中的锐钛矿TiO2在[001]晶面方向都能够择优生长。通过控制电解液中H2O含量,可以便捷调控样品中(004)晶面的相对强度,得到具有不同晶面比例的TiO2纳米管。
| Sample | Tc(004) | I(004)/I(101) |
| A | 3.05 | 0.59 |
| B | 4.76 | 6.98 |
| C | 2.56 | 0.66 |
| D | 2.26 | 0.46 |
图 4为生物矿化3天和7天后试样表面的SEM图。可以观测到所有样品表面都被一层沉积物所覆盖,说明试样表面的纳米管结构能够使钙磷盐沉积。

|
图 4 矿化3天(1)和7天(2)后试样表面SEM图 (a)1%H2O;(b)2%H2O;(c)3%H2O;(d)4%H2O Fig. 4 SEM images of the samples surface mineralized 3 days(1) and 7 days(2) (a)1%H2O; (b)2%H2O; (c)3%H2O; (d)4%H2O |
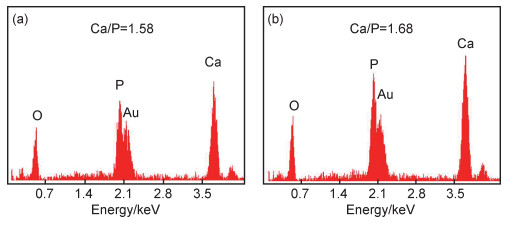
电解液中H2O含量为2%制备得到的TiO2纳米管(B试样)生物矿化3天和7天后EDS能谱结果见图 5。Ca,P和O峰很强,说明样品表面CaP盐的沉积物厚度较大,已经掩盖了基底TiO2的信号。矿化3天和7天后B试样表面通过EDS能谱估算得到的Ca/P比分别为1.58和1.68,接近于羟基磷灰石(HA)中1.67的Ca/P比,推测各样品表面的沉积物主要是以HA为主的CaP盐。
|
图 5 B试样(2%H2O)生物矿化3天(a)和7天后(b)EDS能谱图 Fig. 5 EDS spectra of B sample(2%H2O) mineralized 3 days(a) and 7 days(b) |
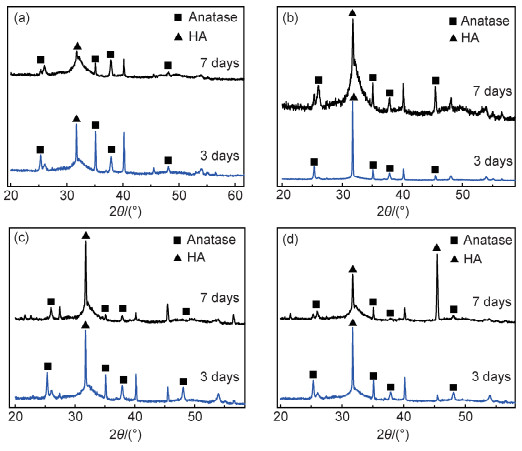
图 6为不同H2O含量下阳极氧化样品生物矿化3天和7天后的XRD谱图。可以看出,每组样品中都检测到锐钛矿TiO2和HA的衍射峰,说明生物矿化后纳米管表面的沉积物主要为HA。
|
图 6 矿化3天和7天后试样表面的XRD谱图 (a)1%H2O;(b)2%H2O;(c)3%H2O;(d)4%H2O Fig. 6 XRD patterns of the samples surface mineralized for 3 days and 7 days (a)1%H2O; (b)2%H2O; (c)3%H2O; (d)4%H2O |
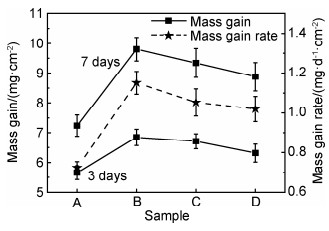
图 7是各试样生物矿化3天和7天后增重及增重速率。由图 7中虚线(增重速率曲线)可以看出,B试样(2%H2O)具有最快的矿化速率,说明具有更高(001)晶面族比例的TiO2纳米管可以促进HA的快速沉积。在矿化液中,溶液OH-能与TiO2中Ti4+结合形成Ti—OH功能团[23-25]。当溶液中pH值为7.4,Ti—OH能够发生去质子化,成为带负电[Ti—OH]-基团,并作为成核位点吸引大量的Ca,P离子吸附在纳米管表面形成CaP微晶体。CaP微晶体作为HA晶核,不断吸附溶液中H2PO4-和OH-等离子,当Ca2+,H2PO4-和OH-达到过饱和状态,CaP盐将会在纳米管表面沉积变厚,直至形成涂层并覆盖表面。因此,Ti—OH基团是诱导HA沉积的诱因。相较锐钛矿TiO2热力学稳定的(101)晶面,(001)晶面族具有更高的不饱和Ti原子密度,可以生成更多的Ti—OH活性基团,为生物矿化CaP盐的沉积提供更多的活性位点,从而在矿化初期明显提高矿化速率,增加材料表面HA沉积量。结合矿化XRD,SEM,EDS以及增重分析来看,在本实验条件下,B试样由于具有更高比例(001)晶面族,显示出更快的矿化速率和更明显的增重,表现出更好的生物学活性。
|
图 7 生物矿化后试样增重及增重速率 Fig. 7 Mass gain and mass gain rate of the samples mineralization |
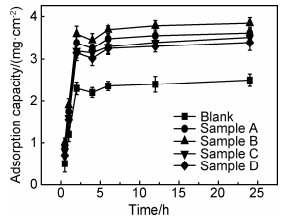
图 8是在波长为280nm条件下利用朗伯比尔定律测得的各试样24h牛血清白蛋白(BSA)吸收曲线,Blank为空白对照组。蛋白吸附是一个动态平衡的过程,即在吸附的同时存在蛋白质的脱附。在初始的2h内,各试样蛋白吸附量几乎与时间呈线性增加,并在2h左右达到吸附初期的最大值。随着时间的增加,脱吸附速率逐渐增加,并在4h左右超过吸附速率,造成试样表面吸附的蛋白量有所下降,最后吸附和脱吸附过程在6h左右达到初步平衡,经过24h的恒温放置,蛋白的吸附与脱落达到最终平衡。蛋白吸附量由多到少依次为:B>A>C>D>Ti,具有(001)晶面最高比例的B组的蛋白吸附量最多。
|
图 8 试样在BSA中24h的吸附曲线 Fig. 8 Adsorption curves of samples after soaking in BSA solution for 24h |
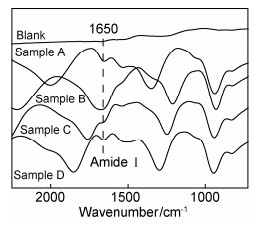
图 9为各试样表面吸附蛋白后的FT-IR图。波数1650cm-1处的吸收峰为BSA中酰胺键的C=O伸缩振动峰(称为酰胺I带)和N—H弯曲振动峰[26]。4组试样在此波数处均有峰值存在,说明蛋白质都吸附到试样上。其中,试样B在特征吸收处具有明显的吸收峰,表明(001)晶面高比例的试样B表面吸附了更多的蛋白质。说明(001)晶面占比与蛋白吸收量呈正相关。
|
图 9 蛋白吸附后的试样表面FT-IR谱图 Fig. 9 FT-IR spectra of the sample surfaces after protein adsorption |
综合各样蛋白吸附曲线和红外光谱结果可以发现,(001)晶面优势取向更为明显的TiO2纳米管样品能够促进更多的蛋白质吸附。因此可以认为,暴露更多高活性的(001)晶面能够对蛋白质的吸附起到积极的促进作用,其相应的样品则具有更好的生物活性。
3 机理讨论相关文献报道已经证实,F-作为保护剂可以优先吸附在TiO2(001)晶面族上,降低的表面能可以稳定(001)晶面族并促进其择优生长[27]。在本实验中,TiO2(001)晶面族除了受到F-的作用,还受到电解液中H2O含量的影响。一方面,H2O作为一种必需成分在阳极被电解并提供氧与金属钛结合,以形成无定形TiO2纳米管,H2O含量的增加可以提高TiO2形成速率。另一方面,电解液中H2O电离出的OH-与TiO2结合,二者的大量接触会使无定形的纳米管在退火过程中被破坏,从而阻碍(001)晶面族的形成。综上所述,F-对(001)晶面的择优生长起促进作用,而水分子具有双重作用,即H2O作为氧源可以促进氧化的进程,但随着H2O含量的增加,使得OH-和TiO2大量接触又抑制TiO2形成特定(001)晶面。在本实验条件下,2%H2O样品中锐钛矿TiO2具有相对较高的(001)晶面比例。
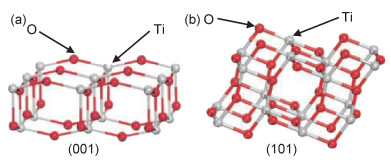
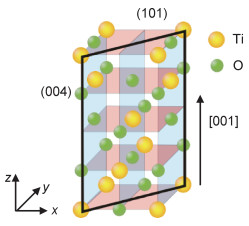
(001) 优势晶面的锐钛矿具有较高的反应活性,主要有两个原因:(1) (001)晶面的Ti—O—Ti键角(约120.5°)比(101)晶面的Ti—O—Ti键角大得多(图 10);(2) (001)晶面比(101)晶面的原子密度大(图 11),可以提供更多的不饱和Ti原子,进而与OH-形成Ti—OH基团,而Ti—OH基团则是TiO2生物活性的关键物种,一般来说样品表面Ti—OH基团密度越大,其生物活性越好。因此(001)优势晶面能够促进HA的矿化沉积,并提高表面蛋白质的吸附量。
|
图 10 锐钛矿TiO2球棍模型示意图 (a)(001)晶面;(b)(101)晶面 Fig. 10 Schematic diagrams of ball stick model for anatase TiO2 (a)(001) facet; (b)(101) facet |
|
图 11 锐钛矿TiO2的晶体结构 Fig. 11 Crystal structure of anatase TiO2 |
(1) 利用二次阳极氧化法,在金属钛表面制备得到高度有序的TiO2纳米管阵列,通过控制电解液中H2O含量可以对TiO2中高活性的(001)晶面族占比进行可控调节。
(2) 2%H2O得到的TiO2纳米管中(001)晶面族择优取向最明显,锐钛矿TiO2(004)晶面的织构系数Tc(004)可达4.76。
(3) 生物矿化和蛋白吸附实验结果表明,得益于(001)晶面族更高的化学活性,具有更高比例(001)晶面族的样品具有更高矿化沉积速率,并有利于生物矿化进程,还可以增加材料表面蛋白吸附量,体现出更为优异的生物学活性。
| [1] | ZHANG Y, CHEN Y, KOU H, et al. Enhanced bone healing in porous Ti implanted rabbit combining bioactive modification and mechanical stimulation[J]. J Mech Behav Biomed Mater, 2018, 86 : 336–344. DOI: 10.1016/j.jmbbm.2018.06.042 |
| [2] | UREÑA J, TSIPAS S, JIMÉNEZ-MORALES A, et al. Cellular behaviour of bone marrow stromal cells on modified Ti-Nb surfaces[J]. Materials & Design, 2018, 140 : 452–459. |
| [3] |
戈军伟, 陈梁锋, 李亚男, 等. 高(001)晶面锐钛矿二氧化钛纳米材料的合成与应用[J].
应用化工, 2015, 44 (4): 739–745.
GE J W, CHEN L F, LI Y N, et al. Synthesis and application of anatase TiO2 with exposed (001) facet[J]. Applied Chemical Industry, 2015, 44 (4): 739–745. |
| [4] | GONG X Q, SELLONI A. Reactivity of anatase TiO2 nanopa-rticles:the role of the minority (001) surface[J]. The Journal of Physical Chemistry B, 2005, 109 (42): 19560–19562. DOI: 10.1021/jp055311g |
| [5] |
李智, 葛少华. 纳米二氧化钛在生物医学中的应用进展[J].
口腔医学, 2017, 37 (1): 85–88.
LI Z, GE S H. Research progress on the application of nano-sized dioxide titanium in biomedicine field[J]. Stomatology, 2017, 37 (1): 85–88. |
| [6] | WEN C Z, JIANG H B, QIAO S Z, et al. Synthesis of highrea-ctive facets dominated anatase TiO2[J]. Journal of Materials Chemistry, 2011, 21 (20): 7052–7061. DOI: 10.1039/c1jm00068c |
| [7] | ZHOU J, YIN L, LI H, et al. Heterojunction of SrTiO3/TiO2 nanotubes with dominant (001) facets:synthesis, formation mech-anism and photoelectrochemical properties[J]. Materials Science in Semiconductor Processing, 2015, 40 : 107–116. DOI: 10.1016/j.mssp.2015.06.023 |
| [8] |
陈昱, 王京钰, 李维尊, 等. 新型二氧化钛基光催化材料的研究进展[J].
材料工程, 2016, 44 (3): 103–113.
CHEN Y, WANG J Y, LI W Z, et al. Research progress in TiO2-based photocatalysis material[J]. Journal of Materials Engin-eering, 2016, 44 (3): 103–113. |
| [9] | GORDON T R, CARGNELLO M, PAIK T, et al. Nonaqueous synthesis of TiO2 nanocrystals using TiF4 to engineer morph-ology, oxygen vacancy concentration, and photocatalytic activity[J]. Journal of the American Chemical Society, 2012, 134 (15): 6751–6761. DOI: 10.1021/ja300823a |
| [10] | HERMAN G, SIEVERS M, GAO Y. Structure determination of the two-domain (1×4) anatase TiO2 (001) surface[J]. Physical Review Letters, 2000, 84 (15): 3354–3357. DOI: 10.1103/PhysRevLett.84.3354 |
| [11] | XU H, REUNCHAN P, OUYANG S, et al. Anatase TiO2 single crystals exposed with high-reactive {111} facets toward efficient H2 evolution[J]. Chemistry of Materials, 2013, 25 (3): 405–411. DOI: 10.1021/cm303502b |
| [12] | ONG W J, TAN L L, CHAI S P, et al. Highly reactive {001} facets of TiO2-based composites:synthesis, formation mechanism and characterization[J]. Nanoscale, 2014, 6 (4): 1946–2008. DOI: 10.1039/c3nr04655a |
| [13] | YANG Z, MA Z, PAN D, et al. Enhancing the performance of front-illuminated dye-sensitized solar cells with highly[J]. Ceramics International, 2014, 40 (1): 173–180. DOI: 10.1016/j.ceramint.2013.05.119 |
| [14] | JUNG M H, KO K C, LEE J Y. Single crystalline-like TiO2 nanotube fabrication with dominant (001) facets using poly(vinylpyrrolidone) for high efficiency solar cells[J]. The Journal of Physical Chemistry C, 2014, 118 (31): 17306–17317. DOI: 10.1021/jp5039078 |
| [15] | YANG H G, SUN C H, QIAO S Z, et al. Anatase TiO2 single crystals with a large percentage of reactive facets[J]. Nature, 2008, 453 (7195): 638–641. DOI: 10.1038/nature06964 |
| [16] | ACEVEDOP P, GONZALEZ F, GONZALEZ G, et al. The effect of anatase crystal orientation on the photoelectrochemical performance of anodic TiO2 nanotubes[J]. Phys Chem Chem Phys, 2014, 16 (47): 26213–26220. DOI: 10.1039/C4CP03930K |
| [17] | MA X, DAI Y, GUO M, et al. Insights into the role of surface distortion in promoting the separation and transfer of photog-enerated carriers in anatase TiO2[J]. The Journal of Physical Chemistry C, 2013, 117 (46): 24496–24502. DOI: 10.1021/jp4092706 |
| [18] | LI H, ZHOU J, ZHANG X, et al. Constructing stable NiO/N-doped TiO2 nanotubes photocatalyst with enhanced visible-light photocatalytic activity[J]. Journal of Materials Science:Materials in Electronics, 2015, 26 (4): 2571–2578. DOI: 10.1007/s10854-015-2724-x |
| [19] | ZHONG J S, WANG Q Y, ZHOU J, et al. Highly efficient photoelectrocatalytic removal of RhB and Cr(Ⅵ) by Cu nanop-articles sensitized TiO2 nanotube arrays[J]. Applied Surface Science, 2016, 367 : 342–346. DOI: 10.1016/j.apsusc.2016.01.189 |
| [20] | YANG Z, MA Z, PAN D, et al. Enhancing the performance of front-illuminated dye-sensitized solar cells with highly[J]. Ceramics International, 2014, 40 (1): 173–180. DOI: 10.1016/j.ceramint.2013.05.119 |
| [21] | LEE S, PARK I J, KIM D H, et al. Crystallographically preferred oriented TiO2 nanotube arrays for efficient photovoltaic energy conversion[J]. Energy & Environmental Science, 2012, 5 (7): 7989–7995. |
| [22] | ARIOSA D, ELHORDOY F, DALCHIELE E A, et al. Texture vs morphology in ZnO nano-rods:on the X-ray diffraction characterization of electrochemically grown samples[J]. Journal of Applied Physics, 2011, 110 (12): 124901–124909. DOI: 10.1063/1.3669026 |
| [23] | MA Q, LI M, HU Z, et al. Enhancement of the bioactivity of titanium oxide nanotubes by precalcification[J]. Materials Letters, 2008, 62 (17/18): 3035–3038. |
| [24] | ROHANIZADEH R, ALSADEQ M, LEGEROS R Z. Prepara-tion of different forms of titanium oxide on titanium surface:effects on apatite deposition[J]. J Biomed Mater Res A, 2004, 71 (2): 343–352. |
| [25] | SVETINA M, COLOMBI C L, SBAIZERO O, et al. Deposition of calcium ions on rutile (110):a first-principles investigation[J]. Acta Materialia, 2001, 49 (12): 2169–2177. DOI: 10.1016/S1359-6454(01)00136-7 |
| [26] | CHANG M C, TANAKA J. FT-IR study for hydroxyapatite/collagen nanocomposite cross-linked by glutaraldehyde[J]. Biomaterials, 2002, 23 (24): 4811–4818. DOI: 10.1016/S0142-9612(02)00232-6 |
| [27] | ZHANG H, LIU X, LI Y, et al. {001} facets dominated anatase TiO2:morphology, formation/etching mechanisms and perfor-mance[J]. Science China Chemistry, 2012, 56 (4): 402–417. |
 2019, Vol. 47
2019, Vol. 47


