文章信息
- 王朴, 杜继涛
- WANG Pu, DU Ji-tao
- 电流密度对水热电化学沉积HA涂层性能的影响
- Effect of Current Density on Properties of HA Coatings Fabricated by Hydrothermal-electrochemical Deposition
- 材料工程, 2018, 46(4): 58-65
- Journal of Materials Engineering, 2018, 46(4): 58-65.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2017.000787
-
文章历史
- 收稿日期: 2017-06-21
- 修订日期: 2018-01-10
2. 上海市高级技工学校, 上海 200437
2. Shanghai Technician School, Shanghai 200437, China
钛及钛合金由于具有较好的生物相容性和力学适应性成为人工骨植入体最为理想的生物医用金属材料[1],但钛合金表面活性不足,其与骨之间只是一种机械嵌连式的骨整合,亟需通过表面改性使之具备诱导骨组织长入并与植入部位实现骨性结合的能力。羟基磷灰石(Ca10(PO4)6(OH)2,hydroxyapatite,HA)作为一种有潜在利用价值的生物活性陶瓷材料,具有优良的骨结合性和骨诱导性,成为目前国际上公认的具有良好生物相容性和生物活性的硬组织替代材料之一[2]。但HA脆性高、抗折强度低,难以满足硬组织植入材料的力学性能要求。因此,将羟基磷灰石涂覆于钛合金表面得到具有两者优点的生物医用复合材料,已成为研究的热点。目前钛基表面HA涂层的制备方法主要有等离子喷涂法[3]、激光熔覆法[4]、仿生溶液生长法[5]、溶胶-凝胶法[6]、电化学法[7]、水热法[8]等。水热电化学法是将水热法和电化学法结合起来极具潜力的一项软溶液工艺[9],是在密闭反应釜中,在高温高压的水溶液中进行的电化学反应,可制备出纯度高、均匀致密且具有较小粒径和较高结晶度的HA涂层。Ban等[10]采用水热电化学技术在钛基体上成功制备HA涂层,研究了水热电化学沉积工艺参数,如温度、电流密度、时间和HA晶体尺寸的关系,并建立了相应的数学公式。Xiao等[11]采用水热电化学法制备了HA/TiO2复合涂层,对涂层的表面形貌、物相组成、复合涂层各组分共沉积量、热稳定性和结合强度进行了研究。然而,涂层与基体之间因较低的结合强度仍无法满足临床应用的要求。
纳米二氧化钛材料,特别是TiO2纳米管近年来在生物材料领域表现出较为广阔的发展前景。有研究表明[12-13],TiO2纳米管结构具有更大的比表面积和较强的吸附能力,不仅能够增强蛋白质和成骨细胞在植入体表面的吸附,促进成骨细胞增殖,而且能够增强材料与骨组织的结合性能。Kodama等[14]表明具有TiO2纳米管结构表面的试样在模拟体液浸泡实验中可加快HA的形成速度。严雅静[15]在含氟溶液中阳极氧化制备TiO2纳米管,然后在其表面采用电化学技术制备HA涂层,发现不仅可促进HA的形核生长,而且能够显著增强涂层与基体的结合强度。
在水热电化学沉积HA涂层的调控参数中,电流密度直接决定氢氧根的生成速度,从而影响电极附近pH值的分布,因此对HA的结晶过程和涂层的性能有较大影响,但该方面的研究鲜有报道。本工作通过阳极氧化对Ti6Al4V合金进行改性处理,用水热电化学技术在预处理的基体表面制备HA涂层,研究了电流密度对涂层物相、微观形貌、结合强度和生物活性的影响。
1 实验材料与方法 1.1 Ti6Al4V合金阳极氧化处理实验用Ti6Al4V合金板材由西北有色金属研究院提供,切割成25mm×25mm×3mm的基片,并经600#,800#,1200#水磨砂纸研磨,然后依次置于丙酮、无水乙醇、去离子水中各超声清洗10min。
阳极氧化实验采用SW171500SL型直流稳压电源,试样为阳极,不锈钢为阴极。将清洗干净的试样放入0.15mol/L HF+2mol/L H3PO4溶液中,在25V的稳定电压下氧化30min,取出经去离子水冲洗后放入60℃恒温干燥箱中备用。
1.2 水热电化学沉积HA涂层将0.02mol/L CaCl2,0.012mol/L K2HPO4·3H2O和0.139mol/L NaCl溶于去离子水配制成电解液,预处理的钛片为阴极,铂片为阳极,置于高压反应釜中,采用恒电流模式,沉积温度120℃,压强0.2MPa,沉积时间2h,电流密度分别为0.75,1.00,1.25,1.50mA/cm2,搅拌速率100r/min。
1.3 模拟体液(SBF)浸泡按照表 1的顺序配制成生物活性实验所需的模拟体液,用6.118g/L(CH2OH)3CNH2和1mol/L HCl(0~5mL)调节溶液的pH值为7.42。将水热电化学沉积的试样置于36.5℃的SBF中恒温浸泡,每天更换1次SBF溶液,6天后取样。
| Component | Value |
| NaCl | 8.035g/L |
| NaHCO3 | 0.355g/L |
| KCl | 0.225g/L |
| K2HPO4·3H2O | 0.231g/L |
| MgCl2·6H2O | 0.311g/L |
| 1mol/L HCl | 39mL |
| CaCl2 | 0.292g/L |
| Na2SO4 | 0.072g/L |
用D/MAX 2550 VB/PC型X射线衍射仪(XRD)分析阳极氧化后的试样和涂层的物相组成,测试条件铜靶(λ=0.15406nm),扫描速率4(°)/min,预处理试样的扫描范围20°~80°,涂层的扫描角度为20°~60°。采用QUANTAN FEG-450场发射扫描电子显微镜(FESEM)观察阳极氧化试样、HA涂层及SBF浸泡试样的表面微观形貌。用AMBIOS XP-1台阶仪测试不同电流密度下涂层的厚度。根据标准ASTMC633-2001(2008)采用粘接拉伸法测试涂层与基体的结合强度,用E7胶(QJ 1992.14-1990)将涂层与基体粘接,放入60℃恒温箱保温3h后随炉冷却至室温,实验设备为Zwick 50KN万能材料试验机,拉伸速率1mm/min。
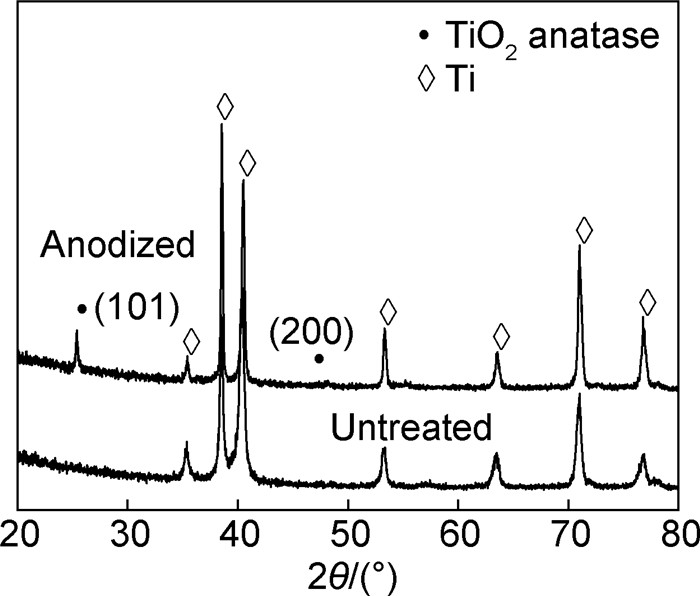
2 结果和讨论 2.1 阳极氧化试样的物相组成和表面形貌图 1为Ti6Al4V基体未经阳极氧化处理和经25V电压阳极氧化30min后的XRD图谱。与标准图谱(JCPDS 44-1295和21-1272)对照可知[16],未经氧化的试样表面只有基体的衍射峰,而预处理的样品在2θ=25°,2θ=47°左右出现(101)和(200)晶面衍射峰,峰形尖锐,物相分析表明为锐钛矿型TiO2的特征衍射峰。有研究发现[17-18],锐钛矿型TiO2晶体结构中的原子排列有利于磷灰石晶体的外延生长,并且可在涂层与基体之间形成化学键连接,提高两者的结合强度。
|
图 1 Ti6Al4V基体阳极氧化处理前后的XRD图谱 Fig. 1 XRD patterns of Ti6Al4V substrate before and after anodic oxidation treatment |
图 2是Ti6Al4V基体阳极氧化处理前后的SEM形貌图。从图中可以看出,经预处理后,基体表面形成一层高度有序、规整排列的TiO2纳米管,纳米管形貌整洁,管径大小均匀。Bjursten等[19]曾报道100nm左右的TiO2纳米管表现出更高的骨整合性。黄平等[20]研究发现当形成晶核所需的临界尺寸大小和接触角一致时,凹面处的晶核由于具有较小的体积容易成核且成核率较高,平面次之,凸面最差。TiO2纳米管的多孔结构使之存在较多的凹面,能够显著增加基体与溶液的接触面积,可为水热电化学沉积羟基磷灰石提供更多有利的形核位置,故有望提高涂层与基体间的结合强度[21]。

|
图 2 Ti6Al4V基体阳极氧化处理前后的SEM微观形貌图 (a)未经阳极氧化处理; (b)经阳极氧化处理 Fig. 2 SEM micrographs of Ti6Al4V substrate before and after anodic oxidation treatment (a)untreated; (b)anodized |
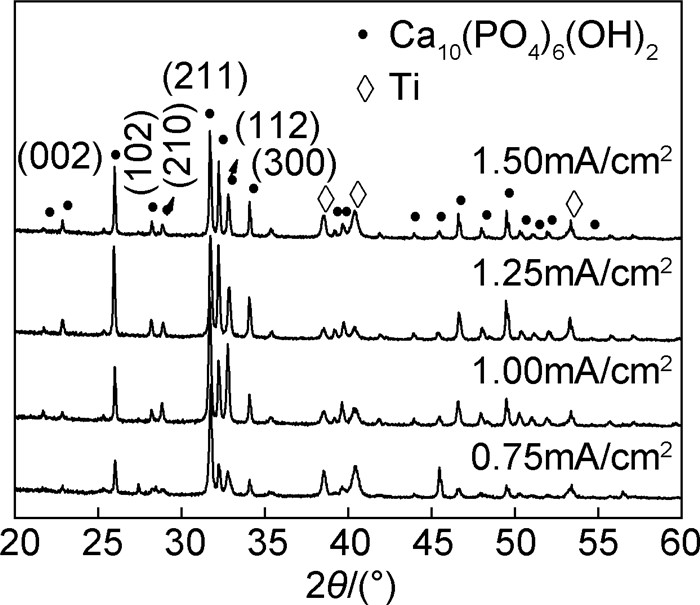
图 3为阳极氧化试样在不同电流密度0.75~1.50mA/cm2下水热电化学沉积HA涂层的XRD图谱。根据标准图谱(JCPDS 09-0432)可知[22],在相当大的电流密度范围内,沉积得到涂层的衍射峰的位置与标准HA的峰位都能很好吻合,这表明电流密度大小对涂层的物相组成几乎没有影响。图中HA的特征峰(211), (112), (300)明显窄化,说明产物晶化程度较好;(002)晶面衍射峰的强度随着电流密度的增加先增大后减小,在1.25mA/cm2时,衍射峰强度较其他峰高,说明得到的HA具有很强的沿c轴择优取向性。
|
图 3 不同电流密度下水热电化学沉积HA涂层的XRD图谱 Fig. 3 XRD patterns of HA coatings deposited by hydrothermal-electrochemical method with different current densities |
通常认为[23],一定范围内,较高的化学势(即单体浓度)有利于生成具有较大长径比的纳米材料。水热电化学沉积过程中,具有各向异性晶体结构的HA (002)晶面的晶面能较高,在特定温度下,当反应体系的化学势高于晶核(002)晶面所含原子的化学势能时,加热过程中将会释放出亚稳态储存的化学能,这在一定程度上促使了HA晶体沿c轴方向生长,即晶体的各向异性结构和具有较高化学势的溶液会对HA晶体沿某一特定晶面方向择优生长起关键作用。
在水热电化学过程中,Shirkhanzadeh[24]认为电解液pH值较低而溶液浓度较高时,H+的活度高,在阴极附近首先发生析氢还原反应,如式(1)所示:
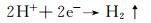
|
(1) |
随着析氢反应的进行,H+很快被消耗掉,导致阴极附近扩散层区域的电解液pH值迅速上升,H+活度降低,此时主要通过阴极电解水生成OH-的反应促使pH值升高,即:
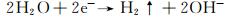
|
(2) |
此外,阴极附近钛合金表面经预处理后形成的TiO2氧化膜会和水中的H+发生反应形成Ti-OH基团,同时Ti4+得到电子被还原成Ti3+,进一步提高了阴极表面的OH-浓度,如式(3):
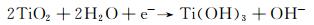
|
(3) |
随着溶液pH值升高,阴极附近生成的OH-会与HPO42-反应,最终将其转变为PO43-,同时在外加电场作用下,Ca2+向阴极附近迁移,使阴极表面Ca2+的浓度大于电解液中的平均浓度[25],此时阴极附近的Ca2+,PO43-浓度升高导致溶液的过饱和度增加,一旦达到HA形核的临界值,就会在阴极钛合金表面形成初步的形核点,并以形成的HA晶核为生长中心,形成羟基磷灰石涂层,反应式如下:
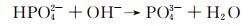
|
(4) |
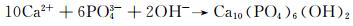
|
(5) |
图 4为不同电流密度下HA涂层的SEM图。可以看出,当电流密度为0.75mA/cm2时,HA的晶粒尺寸较大,呈棒状,涂层杂乱排列;随着电流密度的增加,涂层生成比较容易,出现分层生长,在1.25mA/cm2时底部棒状HA晶粒呈直立状,排列紧凑,涂层也最为致密,顶部絮状HA排列疏松。继续增大电流密度,HA晶体呈花簇状,晶粒间排列松散,分布不均匀,并且涂层表面起伏程度大,黏附力降低,甚至从试样表面脱落,这可能是由于较大的电流密度使得水热电化学沉积过程中阴极析氢反应加剧,氢气泡的逸出破坏了HA紧密排列的结构。

|
图 4 不同电流密度下水热电化学沉积HA涂层的SEM微观形貌图 (a)0.75mA/cm2; (b)1.0mA/cm2; (c)1.25mA/cm2; (d)1.5mA/cm2 Fig. 4 SEM micrographs of HA deposited by hydrothermal-electrochemical method with different current densities (a)0.75mA/cm2; (b)1.0mA/cm2; (c)1.25mA/cm2; (d)1.5mA/cm2 |
在水热电化学过程中,出现第二层晶体的原因可能是在较高的电解液浓度下,第一层棒状HA晶体密度较小没有将钛表面完全覆盖,因而存在一些较大空隙使钛片直接与溶液接触,导致电化学反应强烈,这些位置附近溶液的pH值升高并最终促使在第一层棒状HA晶体之上再生长第二层絮状HA。当电流密度较小为0.75mA/cm2时,溶液中OH-浓度低,棒状HA沉积量少且比较疏松,来不及形成絮状HA晶体;随着电流密度的升高,析氢反应迅速,提供了大量的OH-使得HA沉积速率加快,棒状HA含量增多,而在一些空隙处也促使絮状HA晶粒的形核,在1.25mA/cm2时含量最多。继续增加电流密度,剧烈的析氢反应阻碍了絮状HA的形核,使晶粒不断长大,呈花簇状。这种多层生长下得到的涂层,底部致密的棒状HA晶体可与基体牢固结合,顶部疏松的絮状HA可提供骨组织生长的空间,具有更好的骨诱导能力,故可有效地兼顾涂层的力学与生物学性能[26]。
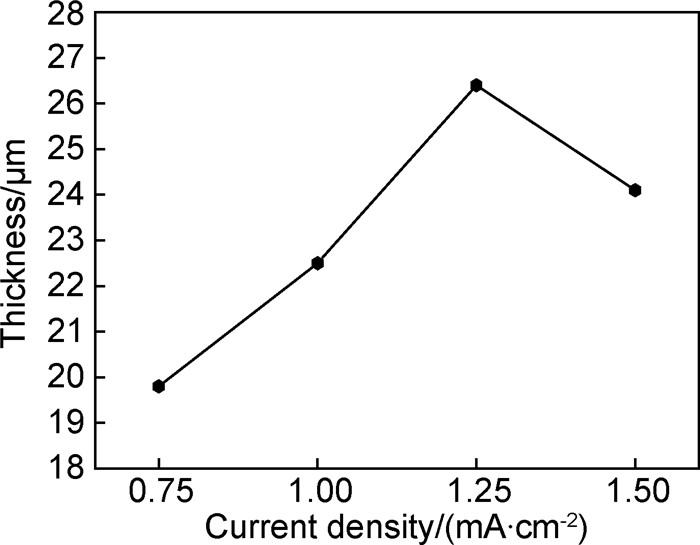
图 5为HA涂层的厚度随电流密度的变化趋势图。可以看出,随着电流密度的增加,涂层的厚度先增加后减小,在1.25mA/cm2时达到最大为26.4μm。出现这种现象的原因是:水热电化学沉积HA过程中,电流密度与沉积量的关系表现在以下两个方面[27],一方面是增加电流密度,将会增大电场强度,降低电解液中离子扩散到基体表面的能量,加快离子的扩散速率,提高HA的沉积速率;另一方面,电流密度的增加,可加快阴极析氢反应,使阴极表面pH值升高,Ca2+,PO43-达到过饱和而促使HA的生成。电流密度刚开始增加时,在电场强度和阴极析氢反应的综合作用下,Ca2+,PO43-向阴极扩散速率加快,涂层厚度增加,在1.25mA/cm2时最大,继续增加电流密度,析氢反应成为主要矛盾,在阴极表面形成强烈的对流搅拌,阻碍了HA的形成,并使涂层易于脱落,导致厚度减小。
|
图 5 不同电流密度下水热电化学沉积HA涂层的厚度 Fig. 5 Thickness of HA coatings deposited by hydrothermal-electrochemical method with different current densities |
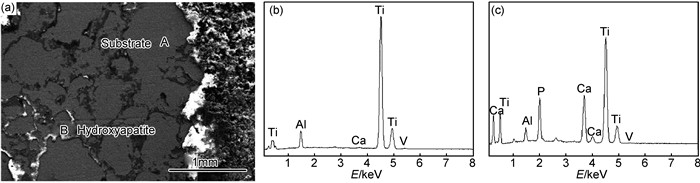
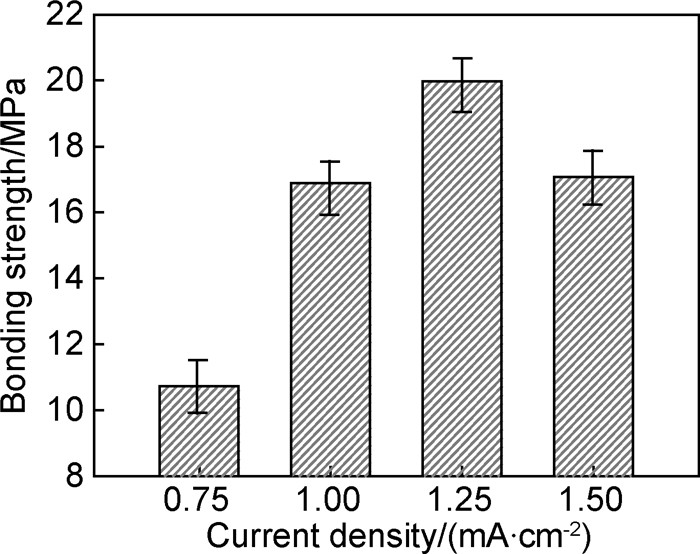
钛合金表面水热电化学沉积HA涂层的最终目的是植入人体,这就要求涂层与基体应具有一定的结合强度, 而影响涂层结合强度的因素主要有两个,即涂层和基体之间的结合强度以及涂层内部的结合强度。从植入材料的长期稳定性来说,HA与基体界面之间的结合情况是衡量涂层制备工艺适用性的一个重要指标。图 6为电流密度1.25mA/cm2沉积得到的涂层经粘接拉伸实验后的断面形貌和EDS能谱图,根据分析结果,试样粘接部分可明显看到钛基体(图 6(b))表面,仅残留有少数的羟基磷灰石(图 6(c)),这表明断裂发生在涂层与基体界面处而非涂层内部,故能较好地反映出涂层的结合性能。图 7给出了涂层与基体间结合强度随电流密度变化的趋势图。可以看出,当电流密度为0.75mA/cm2时,涂层的结合强度较低,这可能是由于得到的涂层较薄所致。随着电流密度的增加,结合强度随之增加,在1.25mA/cm2时达到最大,约20.0MPa左右,根据图 4,5分析可知,此时得到的HA晶粒排列紧密,涂层最为致密,且具有最大的厚度,故结合强度最大。继续增大电流密度,结合强度下降,这是因为电流密度过大导致阴极表面析氢反应加剧,涂层脱落,并且电流密度的升高会增加涂层内部的残余应力[28],致使在较大电流密度下得到的涂层结合强度较低。
|
图 6 电流密度1.25mA/cm2时水热电化学沉积HA涂层与基体之间的SEM断面图及EDS能谱图 (a)SEM断面图;(b)图(a)中位置A的EDS谱图;(c)图(a)中位置B的EDS谱图 Fig. 6 Fracture surface morphology of the sample deposited with 1.25mA/cm2 current density after bonding strength testing and EDS analysis (a)fracture SEM morphology; (b)EDS analysis of position A in fig.(a); (c)EDS analysis of position B in fig.(b) |
|
图 7 不同电流密度水热电化学沉积HA涂层与基体之间的结合强度 Fig. 7 Bonding strength between anodized substrate and HA coatings deposited by hydrothermal-electrochemical method with different current densities |
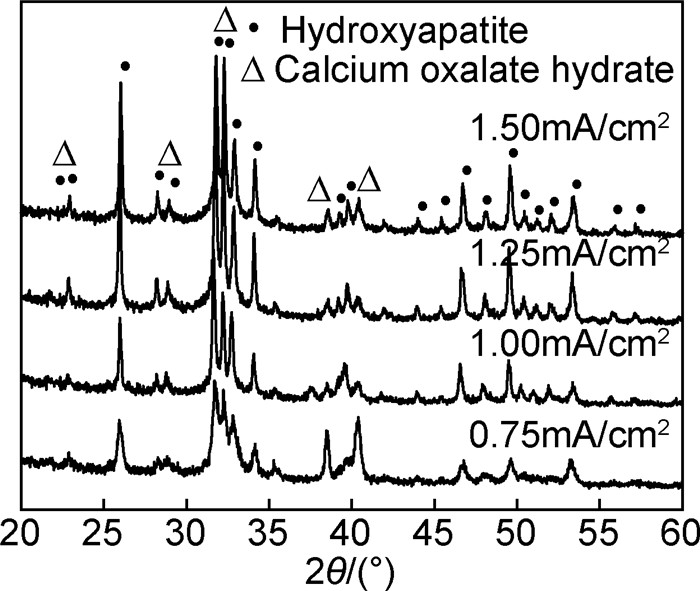
图 8为不同电流密度下的HA涂层在SBF中浸泡6天后的表面形貌图。对比浸泡前HA的表面形貌(图 4),可以看出涂层的上方出现了新的馒头状颗粒。通过后面XRD谱图(图 9)分析可知,这种颗粒状物质为SBF诱导生成的类骨磷灰石(CHA),这是因为溶液中的碳酸根离子对诱导CHA的形成产生了一定的影响,使CO32-取代了磷灰石中PO43-的位置,形成了与人骨成分接近的碳磷灰石,即表明得到的涂层具有很好的生物活性。从图中可以看出,电流密度从0.75mA/cm2增加到1.5mA/cm2的过程中,CHA的晶粒尺寸由直径1μm增大到7~8μm左右,继续增大电流密度,CHA的尺寸下降。研究表明[27, 29],模拟体液中HA的溶解可增加碳磷灰石的过饱和度,而羟基磷灰石涂层表面粗糙程度能够提高涂层的溶解度,并降低界面能,从而促进CHA晶核的形成。在电流密度为1.25mA/cm2时CHA晶粒较大,这可能是由于第二层絮状HA含量较多,结晶度低,粗糙多孔结构使得试样浸入模拟体液中易于溶解,局部过高的过饱和度加快了CHA的形核和长大。

|
图 8 不同电流密度水热电化学沉积HA涂层经过模拟体液浸泡后的SEM微观形貌图 (a)0.75mA/cm2; (b)1.0mA/cm2; (c)1.25mA/cm2; (d)1.5mA/cm2 Fig. 8 SEM micrographs of HA coating after soaking in SBF solution with different depositing current densities (a)0.75mA/cm2; (b)1.0mA/cm2; (c)1.25mA/cm2; (d)1.5mA/cm2 |
|
图 9 水热电化学沉积HA涂层经过SBF浸泡后的XRD图 Fig. 9 XRD patterns of HA coatings after soaking in SBF solution with different depositing current densities |
(1) Ti6Al4V基体经25V电压阳极氧化处理30min后,表面生成了锐钛矿型TiO2,表现为高度有序的纳米管阵列结构。
(2) 改变水热电化学沉积电流密度在预处理的钛基体上均得到了HA涂层。随着电流密度的增加,涂层出现分层生长,部分晶体呈花簇状。HA(002)晶面衍射峰的强度先增大后减小,电流密度为1.25mA/cm2时涂层表现出较强的择优取向性。涂层厚度随电流密度的增加先增大后减小,在1.25mA/cm2时达到最大为26.4μm,同时最为致密。
(3) HA涂层与基体的结合强度随电流密度的增加先升高后降低,在1.25mA/cm2时取到最大值20.0MPa。并且在SBF中可较快诱导CHA生成,最大直径7~8μm,表现出较好的生物活性。
| [1] |
齐美丽, 肖桂勇, 吕宇鹏, 等. 氨基酸对水热合成羟基磷灰石纤维形貌的影响[J].
材料工程, 2017, 45 (5): 46–51.
QI M L, QIAO G Y, LYU Y P, et al. Effect of amino acids on morphology of hydrothermally synthesized hydroxyapatite fibers[J]. Journal of Materials Engineering, 2017, 45 (5): 46–51. DOI: 10.11868/j.issn.1001-4381.2016.000994 |
| [2] | SUCHANEK K, BARTKOWIAK A, GDOWIK A, et al. Crystalline hydroxyapatite coatings synthesized under hydrothermal conditions on modified titanium substrates[J]. Materials Science and Engineering:C, 2015, 51 : 57–63. DOI: 10.1016/j.msec.2015.02.029 |
| [3] | ROY M, BANDYOPADHYAY A, BOSE S. Induction plasma sprayed nano hydroxyapatite coatings on titanium for orthopaedic and dental implants[J]. Surface and Coatings Technology, 2011, 205 (8/9): 2785–2792. |
| [4] |
张晓伟, 刘洪喜, 蒋业华, 等. Ti6Al4V合金表面激光熔覆功能复合涂层研究进展[J].
稀有金属材料与工程, 2012, 41 (1): 178–183.
ZHANG X W, LIU H X, JIANG Y H, et al. Research progress of functional composite coatings on Ti6A14V alloy surface prepared by laser cladding technique[J]. Rare Metal Materials and Engineering, 2012, 41 (1): 178–183. |
| [5] | HUANG Y, HAN S G, PANG X F, et al. Electro deposition of porous hydroxyapatite/calcium silicate composite coating on titanium for biomedical applications[J]. Applied Surface Science, 2013, 271 (6): 299–302. |
| [6] | ZHANG W D, CAO N N, CHAI Y M, et al. Synthesis of nanosize single-crystal strontium hydroxyapatite via a simple sol-gel method[J]. Ceramics International, 2014, 44 (10): 16061–16064. |
| [7] | HE D H, WANG P, LIU P, et al. HA coating fabricated by electrochemical deposition on modified Ti6Al4V alloy[J]. Surface and Coatings Technology, 2015, 277 : 203–209. DOI: 10.1016/j.surfcoat.2015.07.038 |
| [8] |
邓城, 漆小鹏, 李倩, 等. 沉淀法与水热法合成载银羟基磷灰石及其抗菌性能[J].
材料工程, 2017, 45 (4): 113–120.
DENG C, QI X P, LI Q, et al. Synthesis and antibacterial property of silver doped hydroxyapatite by precipitation and hydrothermal method[J]. Journal of Materials Engineering, 2017, 45 (4): 113–120. DOI: 10.11868/j.issn.1001-4381.2016.000319 |
| [9] | YOSHIMURA M. Importance of soft solution processing for advanced inorganic materials[J]. Journal of Materials Research, 1998, 13 (4): 796–802. DOI: 10.1557/JMR.1998.0101 |
| [10] | BAN S, HASEGAWA J. Morphological regulation and crystal growth of hydrothermal-electrochemically deposited apatite[J]. Biomaterials, 2002, 23 (14): 2965–2972. DOI: 10.1016/S0142-9612(02)00025-X |
| [11] | XIAO X F, LIU R F, ZHENG Y Z. Characterization of hydroxyapatite/titania composite coatings codeposited by a hydrothermal-electrochemical method on titanium[J]. Surface and Coatings Technology, 2006, 200 (14/15): 4406–4413. |
| [12] | BENEA L, MARDARE-DANAILA E, MARDARE M, et al. Preparation of titanium oxide and hydroxyapatite on Ti-6Al-4V alloy surface and electrochemical behaviour in bio-simulated fluid solution[J]. Corrosion Science, 2014, 80 : 331–338. DOI: 10.1016/j.corsci.2013.11.059 |
| [13] | YAN Y J, DING Q Q, HUANG Y, et al. Magnesium substituted hydroxyapatite coating on titanium with nanotublar TiO2 intermediate layer via electrochemical deposition[J]. Applied Surface Science, 2014, 305 : 77–85. DOI: 10.1016/j.apsusc.2014.02.163 |
| [14] | KODAMA A, BAUER S, KOMATSU A, et al. Bioactivation of titanium surfaces using coatings of TiO2 nanotubes rapidly pre-loaded with synthetic hydroxyapatite[J]. Acta Biomaterials, 2009, 5 (6): 2322–2330. DOI: 10.1016/j.actbio.2009.02.032 |
| [15] |
严雅静. 金属钛表面TiO2纳米管磷灰石复合涂层的制备与生物活性研究[D]. 成都: 电子科技大学, 2015. YAN Y J. Preparation and bioactivity of calcium phosphate/TiO2 nanotube composite coating on titanium[D]. Chengdu: University of Electronic Science and Technology of China, 2015. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=D665516 |
| [16] | LEE K, JEONG Y H, BRANTLEY W A, et al. Surface characteristics of hydroxyapatite films deposited on anodized titanium by an electrochemical method[J]. Thin Solid Films, 2013, 546 : 185–188. DOI: 10.1016/j.tsf.2013.04.077 |
| [17] | TSUCHIYA H, MACAK J M, MVLLER L, et al. Hydroxyapatite growth on anodic TiO2 nanotubes[J]. Journal of Biomedical Materials Research Part A, 2006, 77 (3): 534–541. |
| [18] | XIAO X F, YU J, TANG H Z, et al. TiO2 nanotube arrays induced deposition of hydroxyapatite coating by hydrothermal treatment[J]. Materials Chemistry and Physics, 2013, 138 (2/3): 695–702. |
| [19] | BJURSTEN L M, RASMUSSON L L, OH S, et al. Titanium dioxide nanotubes enhance bone bonding in vivo[J]. Journal of Biomedical Materials Research Part A, 2010, 92 (3): 1218–1224. |
| [20] |
黄平, 徐可为, 憨勇, 等. 富含钙磷的多孔氧化钛膜及其生物活化机理[J].
硅酸盐学报, 2004, 32 (12): 1449–1454.
HUANG P, XU K W, HAN R, et al. Porous titania layer of containing calcium and phosphate and its mechanism of bioactivity[J]. J Chin Ceram Soc, 2004, 32 (12): 1449–1454. DOI: 10.3321/j.issn:0454-5648.2004.12.001 |
| [21] | DEY T, ROY P, FABRY B, et al. Anodic mesoporous TiO2 layer on Ti for enhanced formation of biomimetic hydroxyapatite[J]. Acta Biomaterials, 2011, 7 (4): 1873–1879. DOI: 10.1016/j.actbio.2010.11.011 |
| [22] | ZHAO L C, CUI C X, WANG X, et al. Corrosion resistance and calcium-phosphorus precipitation of micro-arc oxidized magnesium for biomedical applications[J]. Applied Surface Science, 2015, 330 : 431–438. DOI: 10.1016/j.apsusc.2015.01.041 |
| [23] |
梁琼, 韩冬梅, 顾福博, 等. 水热重结晶法制备羟基磷灰石纳米棒[J].
无机化学学报, 2007, 23 (1): 86–90.
LIANG Q, HAN D M, GU F B, et al. Synthesis of hydroxyapatite nanorods by hydrothermal recrystallization method[J]. Chinese Journal of Inorganic Chemistry, 2007, 23 (1): 86–90. |
| [24] | SHIRKHANZADEH M. Direct formation of nanophase hydroxyapatite on cathodically polarized electrodes[J]. Journal of Materials Science, 1998, 9 (2): 67–72. |
| [25] |
霍明峰. 钛基表面TiO2/HA生物涂层的制备与性能研究[D]. 南京: 南京理工大学, 2008. HUO M F. Preparation and properties of TiO2/HA coating on titanium substrate[D]. Nanjing: Nanjing University of Science and Technology, 2008. http://cdmd.cnki.com.cn/Article/CDMD-10288-2008158119.htm |
| [26] |
付涛, 李浩, 张玉梅, 等. 电流密度对电结晶羟基磷灰石生物涂层性能的影响[J].
稀有金属材料与工程, 2000, 29 (4): 247–250.
FU T, LI H, ZHANG Y M, et al. Effect of current density changes on the properties of hydroxyapatite biocoatings[J]. Rare Metal Materials and Engineering, 2000, 29 (4): 247–250. |
| [27] |
肖秀峰. 水热电化学沉积羟基磷灰石涂层的工艺、结构和性能研究[D]. 秦皇岛: 燕山大学, 2005. XIAO X F. Structure and properties of hydoxyapatite coating prepared by hydrothermal electrochemical technique[D]. Qinhuangdao: Yanshan University, 2005. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y866838 |
| [28] | HAN Y, FU T, LU J, et al. Characterization and stability of hydroxyapatite coatings prepared by an electrodeposition and alkaline-treatment process[J]. Journal of Biomedical Materials Research, 2001, 54 (1): 96–101. DOI: 10.1002/(ISSN)1097-4636 |
| [29] |
郑学斌, 丁传贤, 王毅, 等. 等离子喷涂HA/Ti复合涂层研究[J].
无机材料学报, 2000, 15 (6): 1083–1088.
ZHENG X B, DING C X, WANG Y, et al. Study on plasma sprayed HA/Ti composite coatings[J]. Journal of Inorganic Materials, 2000, 15 (6): 1083–1088. |
 2018, Vol. 46
2018, Vol. 46


