文章信息
- 杨珍, 鲁金涛, 张夏妮, 赵新宝, 袁勇, 党莹樱, 尹宏飞, 谷月峰
- YANG Zhen, LU Jin-tao, ZHANG Xia-ni, ZHAO Xin-bao, YUAN Yong, DANG Ying-ying, YIN Hong-fei, GU Yue-feng
- 水蒸气温度对700℃先进超超临界锅炉候选合金GH2984氧化行为的影响
- Effect of Steam Temperature on Oxidation Behavior of GH2984 Alloy as a Candidate for 700℃ Advanced Ultra-supercritical Boilers
- 材料工程, 2018, 46(1): 74-82
- Journal of Materials Engineering, 2018, 46(1): 74-82.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2015.000305
-
文章历史
- 收稿日期: 2015-03-18
- 修订日期: 2017-08-08
为解决激增的用电需求、日益凸显的能源紧缺及环境污染问题,在现役超临界发电技术基础上发展700℃先进超超临界(Advanced Ultra-supercritical, AUSC)燃煤发电技术(温度700~760℃、压力35~37.5MPa)已成必然的趋势[1-3]。然而,传统的铁素体不锈钢和奥氏体不锈钢受限于其较差的力学性能和氧化性能,已不再适用于700℃先进超超临界电站[4-6]。研发相应服役条件下使用的高温合金管材是发展AUSC电站的一个关键技术难题。这是因为,在高的温度和应力条件下许多高温合金难以同时具有良好的组织稳定性、高强度和优良的耐蚀性。从众多合金中,欧洲和日本筛选出镍基合金Inconel 617及其改进型合金(CCA 617)作为锅炉过/再热器和集箱等的候选材料[7];美国则推荐Inconel 740及其改进型合金(Inconel 740H)作为高温管道的候选材料[8-9]。GH2984是我国自主研制的Fe-Ni-Cr基变形高温合金,依靠加入Mo,Cr等元素产生固溶强化,同时加入Al,Ti,Nb和C等元素产生沉淀强化,其主要性能与美国Special Metal公司研发的Inconel 740合金处于同一水平[10-11]。相较于CCA 617合金和Inconel 740合金,由于不含Co,且Fe含量高,GH2984合金兼具优异的加工性能和较低的成本,已广泛应用于大型舰艇的过热器管(服役温度为650~700℃),并成为我国700℃级AUSC燃煤机组过/再热器的重要候选材料[12]。
作为过/再热器管,其内壁要长期承受高温蒸汽的氧化作用,相应的管材合金通常依赖于其表面形成一层生长缓慢、致密且黏附性好的Cr2O3膜来提供持久的保护。然而,大量的研究认为,含水蒸气的环境抑制富Cr氧化物的形成或使富Cr的氧化物变得不稳定,加速合金的氧化。这是由于在水蒸气和氧气共同存在的情况下,Cr的挥发变得非常重要并可能引发氧化膜的化学失稳。研究指出,在500~900℃的温度范围内,Cr主要以CrO2(OH)2的形式挥发[13-15]。温度升高,Cr的挥发速率升高,则合金内Cr的贫化加剧,从而氧化膜的失效加速。对304不锈钢在500~800℃,分别于O2和O2+40%(体积分数) H2O(g)中的氧化研究表明[16],水蒸气存在时富Cr的M2O3型氧化膜转变为富Fe的M2O3/M3O4型氧化膜的时间随温度升高而缩短,直接证实了上述论断。此外,温度升高,Cr在合金中的扩散速率也将增加。这意味着,Cr由合金内向外扩散供氧化膜生长的速率与由CrO2(OH)2挥发消耗Cr的速率的竞争将决定Cr2O3膜的保护性能。
本课题组针对GH2984合金在模拟蒸汽环境中的高温氧化行为进行了探讨[17]。研究表明,该合金在750℃纯水蒸气中氧化1000h后表面形成单一的Cr2O3膜,其中分布少量的TiO2;在外氧化膜下方的基体中,Ti和Al优先沿晶界发生内氧化,分别形成TiO2和Al2O3。值得提及的是,此时CrO2(OH)2的挥发速率远低于合金的氧化增重速率,从而,由外氧化和内氧化导致的增重动力学并未明显偏离抛物线规律。然而,温度进一步升高时,合金的氧化机制是否改变,仍有待于进一步的研究。基于此,本工作开展了GH2984合金在750℃和850℃纯水蒸气中的氧化实验。通过对比研究不同温度下合金的氧化动力学以及氧化膜的组成结构,探讨了水蒸气温度对GH2984合金氧化行为的影响。
1 实验材料与方法GH2984合金采用真空感应熔炼,浇铸成电极棒后进行电渣重熔。将重熔锭在1150℃加热,使用锻锤进行锻造,锻成管坯后切成一定尺寸的热穿管坯料,并最终经4道热轧制成板材。随后进行标准热处理,即在1100℃固溶1h后空冷至室温,然后在760℃时效8h,炉冷至650℃并在此温度下保温16h,最终空冷至室温。合金的化学成分如表 1所示。采用线切割将板材切成尺寸为10mm×10mm×2mm的片状试样,经1200#SiC砂纸打磨后丙酮清洗,吹干备用。
| Cr | Fe | Mo | Ti | Al | Nb | Si | Mn | C | Ni |
| 18-20 | 32-34 | 1.8-2.2 | 0.9-1.2 | 0.2-0.5 | 0.9-1.2 | ≤0.5 | ≤0.5 | 0.04-0.08 | Bal |
蒸汽氧化实验的温度为750℃和850℃,压力为1.01×105Pa,于水平管式马弗炉中进行,实验装置详见图 1。实验过程中,将电阻率为18.25MΩ·cm的超纯水(氧的溶解量为5~6mg/L)预热至250℃后泵入到反应管内(反应管的材质为石英),蒸汽流速约为100~120mL/s。为保证反应管内的气氛为纯水蒸气,实验前利用高纯N2将反应管内的空气排除,待反应炉加热至目标温度时,关闭N2并通入水蒸气。实验结束后,关闭水蒸气并通入N2,直至反应炉炉温冷却至室温,取出样品并分析。实验采用不连续称重法获得GH2984合金的氧化动力学数据(每个数据为3个试样氧化增重的平均值),即在设定温度氧化一定时间后,取出样品进行称重、观察,随后将样品再放入马弗炉中继续进行氧化。称重使用精度为0.01mg的电子天平。

|
图 1 蒸汽氧化实验装置示意图 Fig. 1 Schematic diagram of the steam oxidation apparatus |
氧化实验结束后,采用SHIMAZDU XRD-7000型X射线衍射仪对氧化产物的物相组成进行定性分析与表征,使用附带能谱分析仪的HITACHI S-4800型扫描电子显微镜对试样表面氧化膜的形貌进行观察,并对其成分进行定量分析;为获得氧化膜中元素的深度分布,将试样化学镀镍后封样处理,对其截面进行观察。
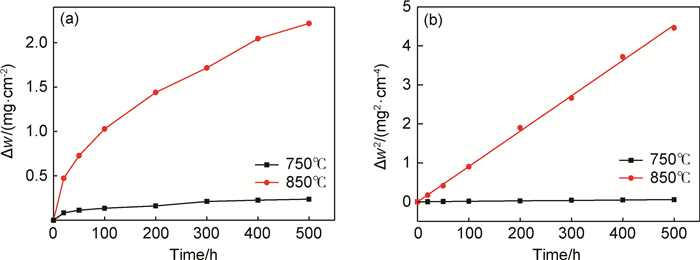
2 结果与分析 2.1 氧化动力学图 2给出了GH2984合金在纯水蒸气中分别于750℃和850℃氧化500h后的增重-时间关系曲线。由图 2可知,温度升高,合金的氧化急剧加速。将增重平方(Δw2)与时间的关系进行拟合(见图 2(b)),结果表明,增重平方与时间之间近似呈直线关系,意味着GH2984合金在所研究温度范围内的增重动力学均近似遵循抛物线规律。计算可得750℃时合金的增重动力学抛物线速率常数kp为1.59×10-4mg2·cm-4·h-1(4.42×10-14g2·cm-4·s-1),温度升高至850℃时kp增至9.97×10-3mg2·cm-4·h-1(2.77×10-12g2·cm-4·s-1)。
|
图 2 GH2984合金分别在750℃和850℃纯水蒸气中的增重动力学曲线(a)以及增重平方与时间关系的拟合曲线(b) Fig. 2 Mass gain vs oxidation time (a) and fitting relationship curves between the square of mass gain andoxidation time (b) for GH2984 alloy oxidized in pure steam at 750℃ and 850℃ |
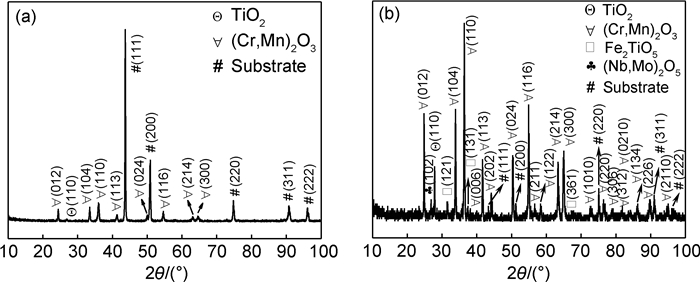
图 3为GH2984合金分别在750℃和850℃纯水蒸气中氧化500h后的XRD图谱。由图 3(a)可知,750℃时合金表面形成的氧化物由TiO2和(Cr, Mn)2O3组成。在这两种氧化物中,(Cr, Mn)2O3的衍射峰强度明显较强。这表明,该温度下合金表面的氧化产物以(Cr, Mn)2O3为主。此外,XRD图谱中还出现来自金属基体的衍射峰,且其峰强远大于TiO2和(Cr, Mn)2O3的峰强,表明750℃时形成的氧化膜很薄。温度升高,TiO2,(Cr, Mn)2O3衍射峰的相对强度增加。同时,在X射线衍射仪的探测深度内(10μm),来自基体的衍射信号减弱,如图 3(b)所示。这意味着氧化膜的厚度随温度升高而增加。与750℃显著不同的是,850℃时XRD图谱中出现强度较高的Fe2TiO5的衍射峰,元素的面分布结果进一步验证了这一结论(见2.3节)。
|
图 3 GH2984合金在不同温度纯水蒸气中氧化500h后的XRD图谱(a)750℃;(b)850℃ Fig. 3 XRD patterns of GH2984 alloy after oxidation for 500h in pure steam at different temperatures(a)750℃; (b)850℃ |
为揭示GH2984合金在纯水蒸气中暴露500h后的氧化膜结构及水蒸气温度对膜组成结构的影响,采用带能谱(EDS)的扫描电子显微镜(SEM)对氧化后的合金进行观察,结果如图 4所示。在750℃纯水蒸气中氧化500h后,GH2984合金表面形成平整的氧化膜,不同区域的颜色衬度有浅灰色和深灰色之分。在较高的放大倍数下可观察到,浅灰色区域为尺寸较大、颗粒状的氧化物所覆盖,而深灰色区域由晶粒尺寸较小、紧密结合的氧化物构成(见图 4(a-1))。能谱(EDS)分析表明,这些尺寸不同的氧化物的成分均富Cr。结合前述XRD表征结果,可知这些氧化物由Cr2O3构成。对氧化膜的生长过程进行研究时发现,这些颗粒状的Cr2O3由刀片状的Cr2O3演化而来。有关刀片状Cr2O3的形成及演化机制已有大量文献报道,即其形成是由Cr沿氧化膜中的短路扩散通道(如位错、孪晶等)向外扩散所致[18-21]。截面形貌图(图 4(a-2))表明,氧化膜的平均厚度为(1.9±0.4)μm,在膜与基体界面处形成尺寸小于0.5μm的空洞。相应的元素面分布结果(图 5)进一步证实,GH2984合金在750℃氧化500h后,形成单一、富Cr的氧化膜,且膜中发生Mn的富集。氧化膜组成因此可表示为(Cr, Mn)2O3。同时,氧化膜中发生少量Ti的富集。结合XRD分析,可知膜中Ti是以TiO2的形式存在。与(Cr, Mn)2O3膜毗邻的基体中,Ti,Al优先于晶界处内氧化,分别形成TiO2和Al2O3,且后者发生在较深的基体中。

|
图 4 GH2984合金在不同温度纯水蒸气中氧化500h后的表面形貌(1)和相应的截面形貌(2) (a)750℃;(b)850℃ Fig. 4 Surface (1) and cross-sectional (2) morphologies of GH2984 alloy oxidized for 500h in puresteam at different temperatures (a)750℃; (b)850℃ |

|
图 5 GH2984合金在750℃纯水蒸气中氧化500h后的截面形貌及相应的元素深度分布图 (a)截面形貌;(b)O; (c)Ni; (d)Fe; (e)Cr; (f)Mn; (g)Ti; (h)Al Fig. 5 Cross-sectional morphology and the corresponding X-ray elemental mapping images of GH2984 alloy after oxidation in puresteam for 500h at 750℃ (a)cross-sectional morphology; (b)O; (c)Ni; (d)Fe; (e)Cr; (f)Mn; (g)Ti; (h)Al |
温度升高至850℃,氧化膜表面的衬度差异消失,氧化物晶粒尺寸增大,氧化膜中尤其是氧化物晶粒的三角晶界处形成数量较多且尺寸不一的空洞,如图 4(b-1)所示。由相应的截面形貌(图 4(b-2))可清楚地观察到,850℃时氧化膜内空洞的尺寸远大于750℃时,而氧化膜的厚度增加至(16±3)μm,与图 2给出的氧化动力学结果相当一致。同样对850℃氧化后合金中的元素分布进行分析,结果如图 6所示。显然,此时合金表面形成外层富集Fe和Ti,次外层富集Cr,Mn和内层富集Nb,Mo的3层氧化膜。结合2.2节中的XRD图谱,可知外层氧化膜为Fe2TiO5,次外层氧化膜由(Cr, Mn)2O3构成,而内层氧化膜为(Nb, Mo)2O5。其中,Fe2TiO5层的平均厚度约为1μm,(Cr, Mn)2O3层的厚度约为15μm,而(Nb, Mo)2O5层的厚度约为1.5μm。与750℃相似,850℃时内氧化产物仍为TiO2和Al2O3,且优先于晶界发生;但内氧化产物的数量和尺寸明显增加,内氧化区的深度增大(由750℃时的5μm左右增至850℃时的40μm左右,如图 6所示)。

|
图 6 GH2984合金在850℃纯水蒸气中氧化500h后的截面形貌及相应的元素深度分布图 (a)截面形貌;(b)O; (c)Ni; (d)Fe; (e)Nb; (f)Cr; (g)Mn; (h)Ti; (i)Al; (j)Mo Fig. 6 Cross-sectional morphology and the corresponding X-ray elemental mapping images of GH2984 alloy after oxidation in pure steamfor 500h at 850℃ (a)cross-sectional morphology; (b)O; (c)Ni; (d)Fe; (e)Nb; (f)Cr; (g)Mn; (h)Ti; (i)Al; (j)Mo |
根据Wagner理论,在干空气中或O2中氧化膜的生长遵循抛物线规律:
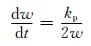
|
(1) |
式中:w为样品的单位面积增重,g·cm-2;kp为氧化增重抛物线速率常数,g2·cm-4·s-1。在湿空气中的瞬时氧化增重速率为[22]:
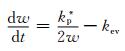
|
(2) |
式中:kp*为湿空气中的氧化增重抛物线速率常数;kev为由CrO2(OH)2挥发导致的失重速率,g·cm-2·s-1。
GH2984合金在750℃静态空气中氧化动力学抛物线速率常数为1.21×10-4mg2·cm-4·h-1(3.36×10-8mg2·cm-4·s-1)[17],这一结果表明氧化膜未发生失稳时含水蒸气环境中GH2984合金的表观增重速率(扣除由CrO2(OH)2挥发导致的失重)与干空气中合金的氧化增重速率近似相等;因此,水蒸气环境中合金的氧化增重速率可表示为:
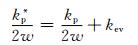
|
(3) |
由式(3)可知kev为水蒸气环境中的氧化增重速率与干空气中的氧化增重速率之差。根据Graham和Davis的推导[23],CrO2(OH)2的挥发速率kev为:
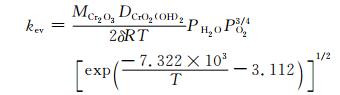
|
(4) |
式中:DCrO2(OH)2表示CrO2(OH)2通过厚度为δ的边界层的扩散速率,cm2·s-1,与T的1.75次方成正比;R为理想气体常数;T为绝对温度;PH2O为水蒸气的分压;PO2为氧分压。显然,CrO2(OH)2的挥发速率随温度的升高而增加,与前言部分的论述一致。
结合文献报道[24],DCrO2(OH)2可表示为:
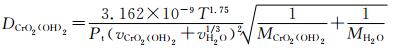
|
(5) |
式中:vi为i的扩散体积分数,m3·mol-1;Pt为总的气体压强。据此,可估算在本工作研究条件下,750℃时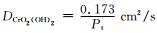
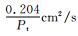
在不考虑溶解氧的影响下,则反应形成CrO2(OH)2(Cr2O3(s)+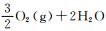
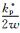
温度升高至850℃,阳离子(或原子)在氧化膜(或合金)中的扩散加速,因而合金的氧化速率增加:
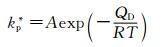
|
(6) |
式中:QD为扩散激活能;R为理想气体常数;T为绝对温度;A为常数项[26]。虽然较750℃时CrO2(OH)2的挥发速率增加了1个数量级,且任意时刻的单位面积增重w亦增加(增加量小于1个数量级),但合金的氧化增重速率仍远大于CrO2(OH)2的挥发速率;因而850℃时CrO2(OH)2的挥发仍较氧化增重所占比例要小,表现在增重动力学上,就是合金的增重动力学未明显偏离抛物线规律。
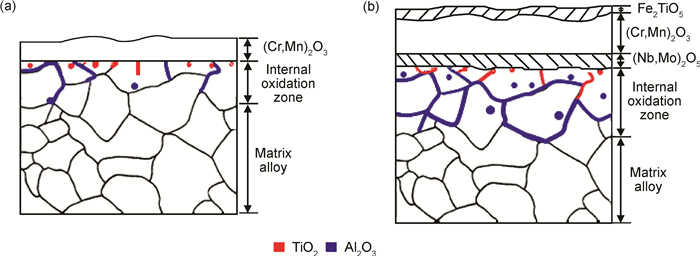
2.4.2 水蒸气温度对氧化区域组织结构的影响由上述可知,在纯水蒸气环境中,GH2984合金表面形成富Cr的氧化膜。Cr的挥发甚微,并未明显改变氧化膜的组成。然而,水蒸气温度升高,外氧化和内氧化均加剧,氧化膜的组成结构也随之发生明显的变化。在750℃时,合金表面形成单层致密的(Cr, Mn)2O3膜,其中分布少量TiO2;温度升高至850℃,氧化膜转变为由薄的外层Fe2TiO5、厚的次外层(Cr, Mn)2O3和薄的内层(Nb, Mo)2O5组成的3层结构。与750℃相比,850℃氧化膜中空洞的数量和尺寸大幅增加。在外氧化产物生长的同时,Al和Ti优先于晶界处发生内氧化,分别形成Al2O3和TiO2。内氧化物的数量、尺寸及内氧化区的深度均随温度升高而增加。不同水蒸气温度下暴露500h后,氧化区域的结构示意图如图 7所示。
|
图 7 不同温度纯水蒸气中暴露500h后GH2984合金表面的氧化区域结构示意图(a)750℃;(b)850℃ Fig. 7 Schematic diagrams of the oxidized zone of GH2984 alloy after exposure to pure steam for 500hat different temperatures (a)750℃; (b)850℃ |
经典氧化理论认为,氧化初期金属元素在合金表面同时氧化形核。然而在实际的氧化环境中,成膜过程不仅与热力学因素有关,更加受到动力学因素影响。换言之,成熟氧化膜的组成取决于合金组元的浓度、化学活性及其在基体中的扩散速率[27]。对于GH2984合金,其中高的Cr含量及缺陷密度(轧制变形带来的位错等缺陷),促使合金表面在短期热暴露阶段即形成一层连续的Cr2O3膜,从而使氧化膜与基体界面处的氧分压大幅降低(降至Cr2O3的平衡氧分压(PO2Cr2O3))。初期形核的Fe等化学活性较低的合金元素的氧化物将被Cr还原;相反地,化学活性较高的Ti,Al的氧化物TiO2和Al2O3继续形核、生长。由于合金中Ti,Al的浓度低,TiO2和Al2O3均不能形成连续的氧化层(见图 7)。事实上,TiO2因其生长速率较快,部分被包裹并溶解进入快速生长的Cr2O3膜中,部分以内氧化产物的形式存在于与Cr2O3膜相邻的基体中;而生长速率较慢的Al2O3仅作为内氧化产物存在。此外,在合金中扩散速率较快的Mn源源不断地扩散至Cr2O3膜并溶解于其中,从而使Cr2O3膜富集少量的Mn[28-29]。上述氧化过程受Cr3+,Ti4+通过(Cr, Mn)2O3膜的向外扩散控制,因而合金的氧化动力学遵循抛物线规律。在阳离子向外扩散的同时,其相应的空位流反向扩散,并优先在氧化膜与基体的界面处沉积,形成空洞。750℃时,空位的沉积、形核并长大成为空洞的速率较低,因此(Cr, Mn)2O3膜与基体界面处空洞的尺寸较小且数量较少(见图 4(a-2))。
温度升高至850℃,一方面,阳离子(或原子)在氧化膜(或合金)中的向外扩散加速(见2.4.1节)。相应地,反向扩散的阳离子空位流增加且其扩散速率增大,则空位的沉积、空洞形核和生长均加速,从而氧化膜中空洞的数量和尺寸均增大。另一方面,由水蒸气分解产生的阴离子如OH-或/和O2-的向内扩散也变得重要[14, 30]。关于这一点,可通过内氧化程度的加剧来间接佐证(对比图 4(a-2),(b-2))。阴离子向内快速扩散,使得氧化膜的生长加速,由阳离子空位沉积形成的空洞被不断生长的(Cr, Mn)2O3膜包裹进去,从而形成多孔的氧化膜结构(图 4(b-2)),明显不同于750℃时空洞仅在(Cr, Mn)2O3膜与基体界面沉积的情形。氧化膜中的空洞又为Cr3+, Mn3+和O2-或/和OH-提供了表面快速扩散通道,进一步加快(Cr, Mn)2O3膜的生长、空位的沉积及空洞的形成和长大[14]。
(Cr, Mn)2O3膜中大量空洞的形成,为化学活性和扩散速率均较低的Fe提供了快速扩散通道,使之可通过空洞的表面扩散至(Cr, Mn)2O3膜表面,并可能与Ti和O通过反应(7)或/和(8)生成Fe2TiO5。
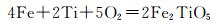
|
(7) |
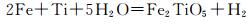
|
(8) |
这就是在(Cr, Mn)2O3膜上方可观察到Fe2TiO5形成的原因。
空洞的存在,也使O2或/和H2O(g)向(Cr, Mn)2O3膜内扩散成为可能,从而(Cr, Mn)2O3膜相邻的基体中氧的浓度升高,促使Nb,Mo的氧化物形核。Nb,Mo的氧化物不断生长,最终成为连续的(Nb, Mo)2O5层。从热力学上讲,(Nb, Mo)2O5的平衡氧分压低于Cr2O3,前者在750℃时形成成为可能。然而,如前所述,(Nb, Mo)2O5连续膜的形成还受到动力学因素的影响,形成(Nb, Mo)2O5连续膜所需Nb(或Mo)的临界浓度NNb(Mo)(0):

|
(9) |
式中:g*为(Nb, Mo)2O5的体积分数;b为分子式中氧与金属的原子个数比;NO(S)为氧化膜/基体界面处氧的浓度;DO,DNb(Mo)分别为氧,Nb(或Mo)在合金中的扩散系数;Vm,V(Nb, Mo)2O5分别为金属基体和(Nb, Mo)2O5的摩尔体积。由式(9)可知,氧的扩散系数越大,(Cr, Mn)2O3膜与基体界面氧的浓度愈高;溶质Nb(或Mo)的扩散系数越小,发生外氧化时所需溶质Nb(或Mo)在合金中的含量愈高。显然,水蒸气温度升高,NO(S)和DO均增大,则850℃时形成连续(Nb, Mo)2O5膜所需的Nb(或Mo)的临界浓度应高于750℃,更难于形成(Nb, Mo)2O5连续膜。然而,实验结果是750℃未形成(Nb, Mo)2O5而850℃时形成了连续的(Nb, Mo)2O5层。其原因可能在于:温度升高,在NO(S)和DO均增大的同时,溶质Nb(或Mo)在合金中的扩散速率也增大,且增加幅度更大;因此,较高温度下所需的临界Nb(或Mo)浓度更小,反而形成连续的(Nb, Mo)2O5层。
水蒸气温度升高,不仅加速外氧化膜生长,改变外氧化膜的组织结构,也使得合金的内氧化加剧。根据Wagner理论[31-32],温度升高,氧通过氧化膜向合金内的扩散速率明显增加,内氧化区的深度ξ也随之增大:
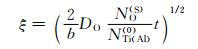
|
(10) |
由式(10)还可以看出,内氧化区的深度与氧化膜/基体界面的氧浓度的平方根成正比。结合本研究工作,NO(S)随温度升高而增加,则内氧化区深度ξ也因此而增大。温度对内氧化产物的颗粒数量和尺寸的影响比较复杂。根据绝对反应速率理论[33],内氧化产物的形核速率J为:
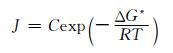
|
(11) |
式中:C为常数;ΔG*为形核激活能垒。从式(11)可以看出,温度越高,内氧化产物的形核速率越大,那么形成的内氧化物颗粒尺寸越小。但是,一般情况下,温度对内氧化产物颗粒长大速度的影响要比对其形核速率的影响更显著。这是由于温度升高时,溶质Ti(和/或Al)与氧的反应速率升高,内氧化产物颗粒的长大速度快,最后形成的颗粒尺寸也大。
3 结论(1) 暴露于750℃和850℃纯水蒸气中时,由外氧化和内氧化导致的GH2984合金的增重动力学均遵循抛物线规律。蒸汽温度升高,Cr的挥发速率增大,但与氧化增重速率的增加程度相比还较小,Cr挥发导致的失重与氧化增重相比占比例甚小。
(2) 750℃时,GH2984合金表面形成连续致密的(Cr, Mn)2O3膜,其中固溶少量TiO2。温度升高至850℃,阴离子O2-或OH-的扩散变得重要,氧化膜生长加速,并将由阳离子空位沉积形成的空洞不断地包裹进氧化膜中,使氧化膜由致密转变为多孔。大量空洞的形成加快Fe向外扩散,使(Cr, Mn)2O3膜的上方形成薄薄的一层Fe2TiO5。此外,在(Cr, Mn)2O3的下方,形成连续的(Nb, Mo)2O5层。
(3) Ti,Al优先于晶界发生内氧化,分别形成TiO2和Al2O3。温度升高,TiO2和Al2O3颗粒的数量和尺寸均增加。
| [1] | VISWANATHAN R, HENRY J F, TANZOSH J, et al. US program on materials technology for ultra-supercritical coal power plants[J]. Journal of Materials Engineering and Performance, 2005, 14 (3): 281–292. DOI: 10.1361/10599490524039 |
| [2] |
徐炯, 周一工. 700℃高效超超临界火力发电技术发展的概述[J].
上海电气技术, 2012, 5 (2): 50–54.
XU J, ZHOU Y G. Overreview of the development of 700℃ USC technique[J]. Journal of Shanghai Electric Technology, 2012, 5 (2): 50–54. |
| [3] |
曾莉, 王岩, 李莎, 等. 700℃超超临界锅炉材料GH4700镍基合金组织演变研究[J].
材料工程, 2013 (9): 44–47.
ZENG L, WANG Y, LI S, et al. Microstructure evolution of GH4700 superalloy for 700℃ ultra-supercritical boilers[J]. Journal of Materials Engineering, 2013 (9): 44–47. |
| [4] | CHI C Y, YU H Y, XIE X S. Advanced austenitic heat-resistant steels for ultra-super-critical (USC) fossil power plants[M]. Rijeka, Croatia: INTECH Open Access Publisher, 2011: 171-200. |
| [5] | GIBBONS T B. Recent advances in steels for coal fired power plant:a review[J]. Transactions of the Indian Institute of Metals, 2013, 66 (5/6): 631–640. |
| [6] |
方旭东, 王岩, 范光伟, 等. 超超临界锅炉材料TP310HCbN(HR3C)持久及析出行为[J].
材料工程, 2017, 45 (6): 112–117.
FANG X D, WANG Y, FAN G W, et al. Stress rupture and precipitation behavior of TP310HCbN (HR3C) for supercritical boilers[J]. Journal of Materials Engineering, 2017, 45 (6): 112–117. DOI: 10.11868/j.issn.1001-4381.2015.001068 |
| [7] | TERRY C T, REN W J. Procurement and initial characterization of alloy 230 and CMS alloy 617[R]. Idaho, US: Idaho National Laboratory, 2006: 1-8. |
| [8] | COWEN C J, DANIELSON P E, JABLONSKI P D. The microstructural evolution of Inconel alloy 740 during solution treatment, aging, and exposure at 760℃[J]. Journal of Materials Engineering and Performance, 2011, 20 (6): 1078–1083. DOI: 10.1007/s11665-010-9731-0 |
| [9] | ZHANG S D, TAKAHASHI Y. Advances in materials technology for fossil power plants[C]. Hawaii, US: ASM International, 2013: 242-253. |
| [10] |
王淑荷, 杜秀魁, 郭建亭. GH984合金中碳化物在长期时效过程中的变化[J].
金属热处理学报, 1998, 19 (3): 36–41.
WANG S H, DU X K, GUO J T. Changes of carbides during long term aging in GH984 alloy[J]. Transactions of Metal Heat Treatment, 1998, 19 (3): 36–41. |
| [11] |
郭建亭, 杜秀魁. 一种性能优异的过热器管材用高温合金GH2984[J].
金属学报, 2005, 41 (11): 1221–1227.
GUO J T, DU X K. A superheater tube superalloy GH2984 with excellent properties[J]. Acta Metallurgica Sinica, 2005, 41 (11): 1221–1227. DOI: 10.3321/j.issn:0412-1961.2005.11.017 |
| [12] |
郭建亭. 高温合金在能源工业领域中的应用现状及发展[J].
金属学报, 2010, 46 (5): 513–527.
GUO J T. The current situation of application and development of superalloys in the fields of energy industry[J]. Acta Metallurgica Sinica, 2010, 46 (5): 513–527. |
| [13] | PENG X, YAN J, ZHOU Y, et al. Effect of grain refinement on the resistance of 304 stainless steel to breakaway oxidation in wet air[J]. Acta Materialia, 2005, 53 (19): 5079–5088. DOI: 10.1016/j.actamat.2005.07.019 |
| [14] | YOUNG D J. Effects of water vapour on the oxidation of chromia formers[J]. Materials Science Forum, 2008, 595/598 : 1189–1197. DOI: 10.4028/www.scientific.net/MSF.595-598 |
| [15] | OTHMAN N K, OTHMAN N, ZHANG J, et al. Effects of water vapour on isothermal oxidation of chromia-forming alloys in Ar/O2 and Ar/H2 atmospheres[J]. Corrosion Science, 2009, 51 (12): 3039–3049. DOI: 10.1016/j.corsci.2009.08.032 |
| [16] | ASTEMAN H, SVENSSON J E, JOHANSSON L G. Evidence for chromium evaporation influencing the oxidation of 304L:the effect of temperature and flow rate[J]. Oxidation of Metals, 2002, 57 (3/4): 193–216. DOI: 10.1023/A:1014877600235 |
| [17] |
杨珍, 鲁金涛, 谷月峰. 高温合金GH2984在750℃水蒸气中的氧化行为研究[J].
稀有金属材料与工程, 2017, 46 (4): 1013–1019.
YANG Z, LU J T, GU Y F. Oxidation mechanism of GH2984 alloy in pure steam at 750℃[J]. Rare Metal Materials and Engineering, 2017, 46 (4): 1013–1019. |
| [18] | TALLMAN R L, GULBRANSEN E A. Dislocation and grain boundary diffusion in the growth of α-Fe2O3 whiskers and twinned platelets peculiar to gaseous oxidation[J]. Nature, 1968, 218 (5146): 1046–1047. DOI: 10.1038/2181046a0 |
| [19] | VOSS D A, BULTER E P, MITCHELL T E. The growth of hematite blades during the high temperature oxidation of iron[J]. Metallurgical Transactions A, 1982, 13 (5): 929–935. DOI: 10.1007/BF02642408 |
| [20] | HANSEL M, QUADAKKERS W, YOUNG D. Role of water vapor in chromia-scale growth at low oxygen partial pressure[J]. Oxidation of Metals, 2003, 59 (3/4): 285–301. DOI: 10.1023/A:1023040010859 |
| [21] | PUJILAKSONO B, JONSSON T, HALVARSSON M, et al. Paralinear oxidation of chromium in O2+H2O environment at 600-700℃[J]. Oxidation of Metals, 2008, 70 (3/4): 163–188. |
| [22] | TEDMON C. The effect of oxide volatilization on the oxidation kinetics of Cr and Fe-Cr alloys[J]. Journal of the Electrochemical Society, 1966, 113 (8): 766–768. DOI: 10.1149/1.2424115 |
| [23] | GRAHAM H C, DAVIS H. Oxidation/vaporization kinetics of Cr2O3[J]. Journal of the American Ceramic Society, 1971, 54 (2): 89–93. DOI: 10.1111/jace.1971.54.issue-2 |
| [24] | HOLCOMB G R. Calculation of reactive-evaporation rates of chromia[J]. Oxidation of Metals, 2008, 69 (3/4): 163–180. |
| [25] | BARIN I. Thermochemical data of pure substances[M]. Weinheim, Germany: VCH Verlagsgesellschaft mbH, 2003. |
| [26] |
李美栓.
金属的高温腐蚀[M]. 北京: 冶金工业出版社, 2001.
LI M S. High temperature corrosion of metals[M]. Beijing: Metallurgical Industry Press, 2001. |
| [27] | KOFSTAD P. High temperature corrosion[M]. London/New York: Elsevier Applied Science, 1988. |
| [28] | SPEIDEL D, MUAN A. The system manganese oxide-Cr2O3 in air[J]. Journal of the American Ceramic Society, 1963, 46 (12): 577–578. DOI: 10.1111/jace.1963.46.issue-12 |
| [29] | KJELLQVIST L, SELLEBY M. Thermodynamic assessment of the Cr-Mn-O system[J]. Journal of Alloys and Compounds, 2010, 507 (1): 84–92. DOI: 10.1016/j.jallcom.2010.04.252 |
| [30] | HENRY S, MOUGIN J, WOUTERS Y, et al. Characterization of chromia scales grown on pure chromium in different oxidizing atmospheres[J]. Materials at High Temperatures, 2000, 17 (2): 231–234. DOI: 10.3184/096034000783640866 |
| [31] | WAGNER C. Reaktionstypen bei der oxydation von legierungen[J]. Zeitschrift für Elektrochemie, 1959, 63 (7): 772–782. |
| [32] | DOUGLASS D L. A critique of internal oxidation in alloys during the post-wagner era[J]. Oxidation of Metals, 1995, 44 (1/2): 81–111. |
| [33] | AUER S, FRENKEL D. Prediction of absolute crystal-nucleation rate in hard-sphere colloids[J]. Nature, 2001, 409 (6823): 1020–1023. DOI: 10.1038/35059035 |
 2018, Vol. 46
2018, Vol. 46


