文章信息
- 梁嘉香, 何吉宇, 齐祉, 范海波, 杨荣杰
- LIANG Jia-xiang, HE Ji-yu, QI Zhi, FAN Hai-bo, YANG Rong-jie
- 环梯形聚苯基硅倍半氧烷的硝化研究
- Nitration Study of Cyclic Ladder Polyphenylsilsesquioxane
- 材料工程, 2017, 45(5): 64-70
- Journal of Materials Engineering, 2017, 45(5): 64-70.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2015.000335
-
文章历史
- 收稿日期: 2015-03-25
- 修订日期: 2017-02-12
聚有机硅倍半氧烷(Polysilsesquioxane,PSQ)指分子式为(RSiO1.5)n的聚硅氧烷,其中侧基R是与硅原子直接相连的各种基团。PSQ分子结构上既含有无机硅氧烷的“骨架”结构,又通过侧基引进了有机基团,密度较大的无机内核能抑制它的链运动而赋予其良好的耐热性能,相应的有机侧基则赋予其良好的韧性和可加工性,使材料同时具备有机聚合物和无机陶瓷的基本特征。因此,与一般的含硅树脂相比,PSQ具有更优异的耐热性、电绝缘性、耐候性、耐辐照性、耐化学药品性及阻燃性等[1, 2]。
聚苯基硅倍半氧烷(Polyphenylsilsesquioxane,PPSQ)作为近年来发展迅速的一种PSQ,除具有PSQ的优异性能外,还具有优良的成膜性及在有机溶剂中良好的溶解性,已被用于阻燃材料、超疏水材料、耐烧蚀材料、低介电材料、光敏材料等[3, 4]。制备PPSQ的衍生物是进一步提高PPSQ与有机聚合物相容性的方法,但由于其较高的化学稳定性,使其衍生物的制备并非容易。PPSQ最重要的一个衍生化学反应是对苯环进行的硝化反应,Kim等通过缩聚制备得到了分子量高达2.5×104的PPSQ,并使用浓度为90%(质量分数,下同)的发烟硝酸对其进行了硝化实验,发现产物分子量急剧下降到1800,多分散性系数(PDI)从2.49降到1.34[5]。
本实验室在PPSQ的合成研究基础上,深入系统地对PPSQ的合成方法和结构进行了研究,制备出环梯形结构的聚苯基硅倍半氧烷(Cyclic Ladder Polyphenylsilsesquioxane,CL-PPSQ)[6, 7],是两种规整的化学结构的混合物。本工作使用不同种类的硝化试剂,对CL-PPSQ的硝化反应进行了研究,制备了含硝基基团的NO2-PPSQ,并对硝化机理进行了分析。
1 实验材料与方法 1.1 试剂与仪器红外分析(FTIR):Nicolet 6700 FTIR傅里叶变换红外仪;元素分析:Vario EL Ⅲ元素分析仪;凝胶渗透色谱(GPC)分析:Waters凝胶渗透色谱系统;核磁共振谱分析:Bruker DMX600核磁共振谱仪;热失重分析(TGA):Netzsch 209 F1热重分析仪;TG-FTIR联用测试:Netzsch 209 F1热重分析仪和Nicolet 6700 FTIR傅里叶变换红外仪相连用。
环梯形聚苯基硅倍半氧烷(CL-PPSQ):自制[7];(CH3CO)2O:西亚试剂,中国四川;发烟HNO3(96%)、浓HNO3(65%)、浓H2SO4(98%)、KNO3、CH3COOH、Na2CO3、乙醇均为市售分析纯。
1.2 多硝基聚苯基硅倍半氧烷(NO2-PPSQ)的制备参考作者前期工作[8, 9]中八硝基苯基硅倍半氧烷(ONPS)的制备方法[10]。在一定温度下,向装有磁力搅拌和温度计的100mL三口烧瓶中加入一定量的硝化试剂(见表 1,9种方法制得的硝化产物分别记为NO2-PPSQ-1, 2, …, 8, 9),磁力搅拌至均匀。称量1g PPSQ,溶于2.5mL CH2Cl2,滴入到硝化试剂中。加料结束后,持续搅拌一定时间。反应结束后,将反应混合物倾入100mL离子水冰中,50℃旋蒸除去CH2Cl2,立刻出现淡黄色沉淀。抽滤,用质量分数为5%的Na2CO3水溶液洗涤沉淀至中性,再用乙醇洗涤3次。50℃真空干燥,得淡黄色样品,记为NO2-PPSQ,产率90%以上。
| Method | Reaction temperature/℃ | Nitration reagent (amount)/mLa or gb | Reaction time/h | Mng | PDIh | Mass fraction of N/% | Reference |
| 1 | 20 | 90% HNO3(6) | 20 | 1634 | 1.067 | 7.96 | [5, 8-12] |
| 2 | 20 | 86% HNO3(6) | 20 | 1849 | 1.115 | 7.42 | |
| 3 | 20 | 84.5% HNO3(6) | 20 | 1864 | 1.119 | 6.83 | |
| 4 | 0 | HNO3(6)c+H2SO4(6)d | 1 | 1866 | 1.116 | 7.93 | [11, 12, 14-17] |
| 5 | 0 | KNO3(2.5)+H2SO4(10)d | 1 | 1649 | 1.057 | 7.21 | [11, 12] |
| 6 | 75 | HNO3(6)c+KNO3(6) | 15 | 3172 | 1.511 | < 0.3 | [13] |
| 7 | 75 | CH3COOH(10)e+KNO3(2.5) | 20 | 3022 | 1.436 | < 0.3 | [11, 12] |
| 8 | 25 | HNO3(3)c+(CH3CO)2O(10)f | 1.5 | 3102 | 1.375 | 4.21 | [11, 12, 16, 17] |
| 9 | 25 | HNO3(3)c+(CH3CO)2O(10)f | 3 | 3278 | 1.655 | 4.81 | |
| mLa: HNO3, H2SO4, CH3COOH, (CH3CO)2O; gb: KNO3; HNO3c: 65%;H2SO4d: 98%; CH3COOHe: 99%; (CH3CO)2Of: 99%;Mng (CL-PPSQ)=3053; PDIh (CL-PPSQ)=1.362 | |||||||
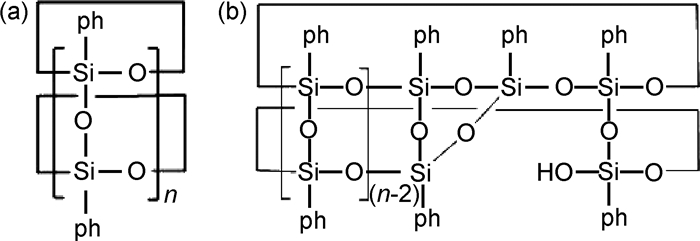
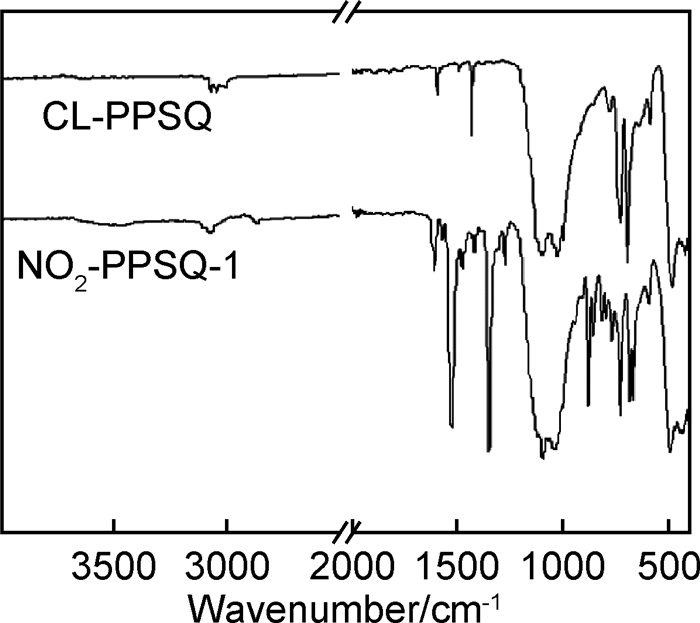
相比Kim等[5]合成的PPSQ,本工作合成的PPSQ产物结构更规整(化学结构式见图 1),分子量也较低。鉴于发烟硝酸是最常用的硝化试剂[5, 8-12],本工作首先使用浓度为90%的发烟硝酸对CL-PPSQ进行硝化实验,制得硝化产物NO2-PPSQ-1。NO2-PPSQ-1的红外谱图如图 2所示,与CL-PPSQ相比,在1524cm-1和1346cm-1处吸收谱带分别为—NO2的不对称伸缩振动和对称伸缩振动吸收峰,同时在600~800cm-1范围内,因取代基团位置不同苯环出现相应吸收振动峰的变化,这表明在所得产物中,确实在苯环上连着一定数量的—NO2。随后对产物做了元素分析测试,结果如表 1所示,硝化后产物氮元素的质量分数为7.96%,而每个苯环上连接有一个硝基的产物的理论含氮量为8.04%,二者相差甚小。然而这还不足以说明已经制备得到每个苯环上含有一个硝基的环梯形聚硝基苯基硅倍半氧烷。
|
图 1 CL-PPSQ的化学结构式 (a)全环状;(b)一个—SiOH基环状 Fig. 1 Chemical structures of CL-PPSQ (a)all cyclic; (b)cyclic including one—SiOH group |
|
图 2 NO2-PPSQ-1和CL-PPSQ红外谱图 Fig. 2 FTIR spectra of NO2-PPSQ-1 and CL-PPSQ |
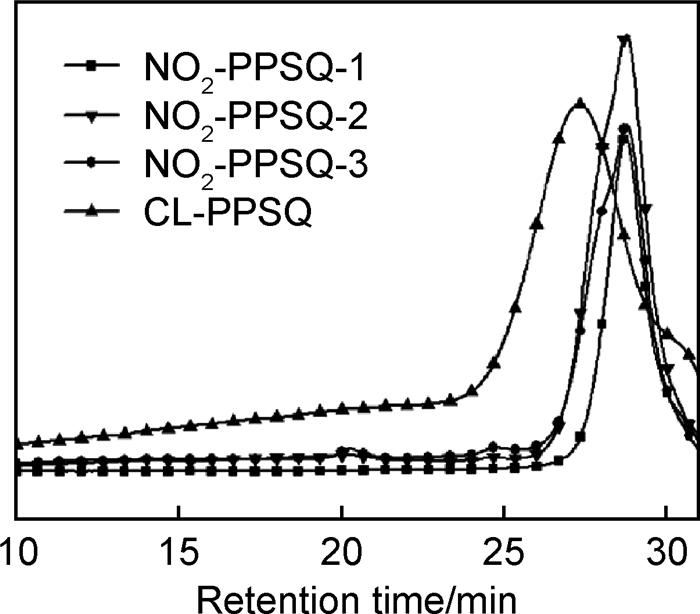
从图 3NO2-PPSQ-1与CL-PPSQ的GPC对比图中可以看到,使用质量分数为90%的发烟硝酸对CL-PPSQ硝化后,产物的Mn有了很明显的降低,多分散性系数(PDI)也有了很明显的下降(表 1),表明所得产物发生了分子链的断链,即高分子量的CL-PPSQ在90%发烟硝酸的作用下,分子链发生断裂,可能生成硅羟基。同时,由于硅羟基更容易与发烟硝酸反应生成硝酸酯基,因此,所得产物中可能存在一定量的硝酸酯基。
|
图 3 NO2-PPSQ-1, 2, 3和CL-PPSQ的GPC谱图 Fig. 3 GPC spectra for NO2-PPSQ-1, 2, 3 and CL-PPSQ |
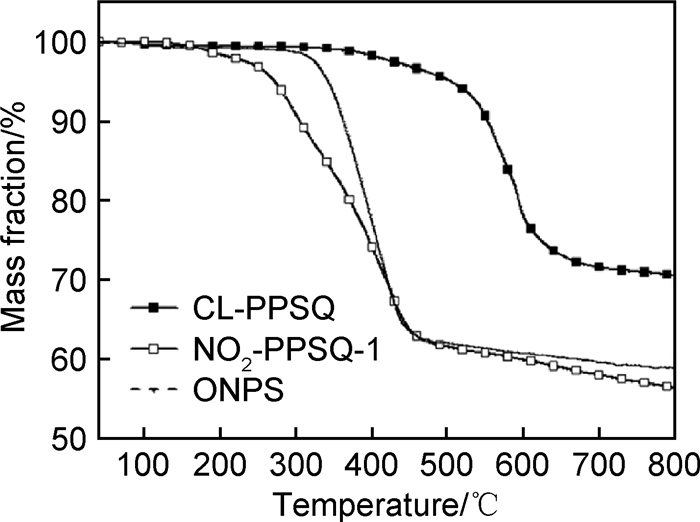
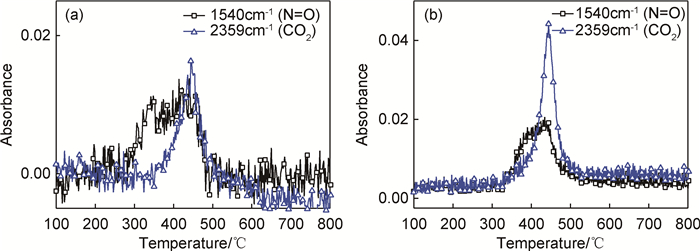
图 4是NO2-PPSQ-1、CL-PPSQ和笼型八硝基苯基硅倍半氧烷(ONPS)[8]的TGA对比图。可以看到,CL-PPSQ在400℃之前没有发生分解,而没有硝酸酯基存在的ONPS的初始分解温度远高于NO2-PPSQ-1。因此,最合理的解释是CL-PPSQ在条件1的硝化过程中可能生成了部分硝酸酯基。众所周知,硝酸酯基的分解温度较低,故造成NO2-PPSQ-1的初始分解温度低于ONPS。对此,使用TGA-FTIR联用测试对NO2-PPSQ-1和ONPS作了进一步测试分析。图 5为气相N=O和CO2吸收峰在热分解过程中随温度变化曲线。NO2-PPSQ-1和ONPS的CO2吸收峰几乎在相同的时间出现。对于NO2-PPSQ-1,N=O的吸收峰的出现提前于CO2;而相比于ONPS,二者的吸收峰却同时出现。表明NO2-PPSQ-1在350℃前的分解产物为含有N=O的物质,而此时的N=O最有可能是硝酸酯基团所提供。此结果更加证明了上述的推断:CL-PPSQ在硝化过程中出现分子链的水解断裂,并生成一定量的硝酸酯基团。
|
图 4 NO2-PPSQ-1, ONPS和CL-PPSQ的TGA曲线 Fig. 4 TGA curves of NO2-PPSQ-1, ONPS and CL-PPSQ |
|
图 5 NO2-PPSQ-1 (a)和ONPS (b)在2359cm-1和1540cm-1处的二维TGA-FTIR谱图 Fig. 5 2D TGA-FTIR spectra of NO2-PPSQ-1 (a) and ONPS (b) at 2359cm-1 and 1540cm-1 |
为了获得分子链不断裂的PPSQ硝化产物,首先对发烟硝酸作进一步稀释,使用了更低溶度的发烟硝酸(86%和84.5%)对CL-PPSQ进行硝化实验。结果如图 3和表 1所示,硝化产物仍然发生分子链的断裂。而当使用浓HNO3(65%)对CL-PPSQ进行硝化后,在硝化产物中并没有出现—NO2,即浓HNO3对CL-PPSQ没有硝化能力。
2.2 其他体系下PPSQ硝化研究除使用发烟硝酸硝化外,文献中还报道了多种硝化方法,常用的硝化方法还有:HNO3-H2SO4体系[11, 12, 14-16]、KNO3-H2SO4体系[11, 12]、HNO3-KNO3体系[13]、CH3COOH-KNO3体系[11, 12]、乙酸酐((CH3CO)2O)-HNO3体系[11, 12, 15, 16]。同时,在实验中使用FTIR和元素分析测试手段判断硝化反应是否发生及其硝化程度,使用GPC观察CL-PPSQ的分子量,用以判断其分子链是否发生断裂。
2.2.1 HNO3-H2SO4和KNO3-H2SO4硝化体系发烟硝酸和硝硫混酸是最常用的硝化试剂,除常用的硝硫混酸体系外,也常使用KNO3代替HNO3,和H2SO4一起使用[11, 12, 14-16]。在实验过程中,尝试了此两种体系在不同温度和不同时间条件下的反应。而所有结果无一例外地均发生了硝化反应,且均引起分子链的断裂。
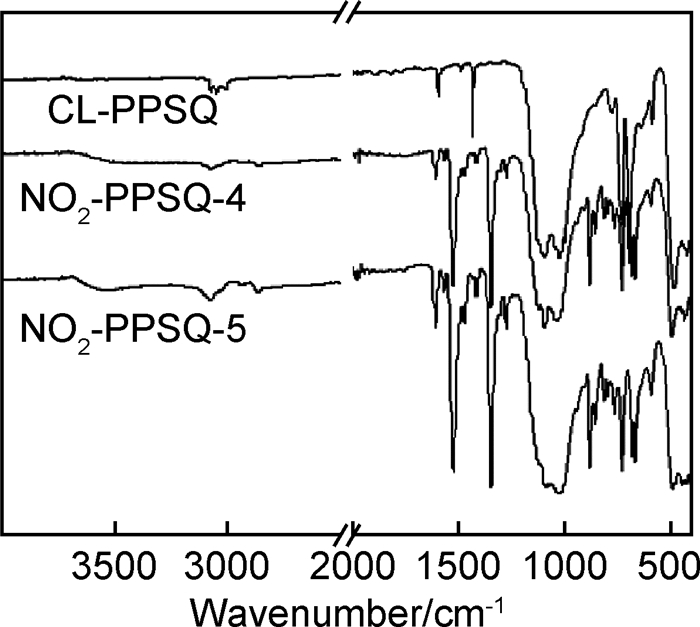
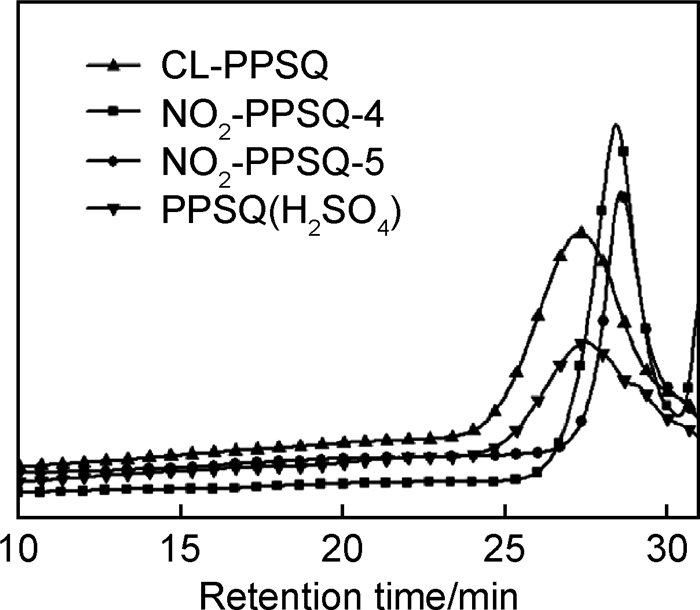
图 6是NO2-PPSQ-4(HNO3-H2SO4体系在0℃下反应1h的产物)和NO2-PPSQ-5(KNO3-H2SO4体系在0℃下反应1h的产物)的FTIR谱图。在两产物的FTIR图中,均可发现在1524cm-1和1346cm-1处有很强的硝基的吸收峰出现,表明在0℃下仍发生了硝化反应。元素分析结果表明,产物中—NO2数目也较多。同时,对此两种产物进行了GPC分析,结果如图 7所示。NO2-PPSQ-4,5与NO2-PPSQ-1相似,二者的Mn和PDI与PPSQ相比,均出现很大程度的降低,表明两者都发生了分子链的断裂。
|
图 6 NO2-PPSQ-4, 5和CL-PPSQ红外谱图 Fig. 6 FTIR spectra of NO2-PPSQ-4, 5 and CL-PPSQ |
|
图 7 NO2-PPSQ-4, 5,CL-PPSQ和PPSQ(H2SO4)的GPC谱图 Fig. 7 GPC spectra for NO2-PPSQ-4, 5, CL-PPSQ and PPSQ(H2SO4) |
由于浓H2SO4也具有很强的酸性,为了证明在HNO3-H2SO4和KNO3-H2SO4体系下,硝化产物分子链的断裂不是仅由于浓H2SO4的作用所导致,将体系中的HNO3或KNO3去掉,仅在浓H2SO4的存在下对PPSQ进行了相同反应条件下的测试,产物记为PPSQ(H2SO4)。GPC结果如图 7所示,PPSQ(H2SO4)分子链并没有发生断裂。因此,在HNO3-H2SO4和KNO3-H2SO4的硝化体系下,CL-PPSQ分子链的断裂是由HNO3或KNO3和H2SO4二者共同作用的结果。
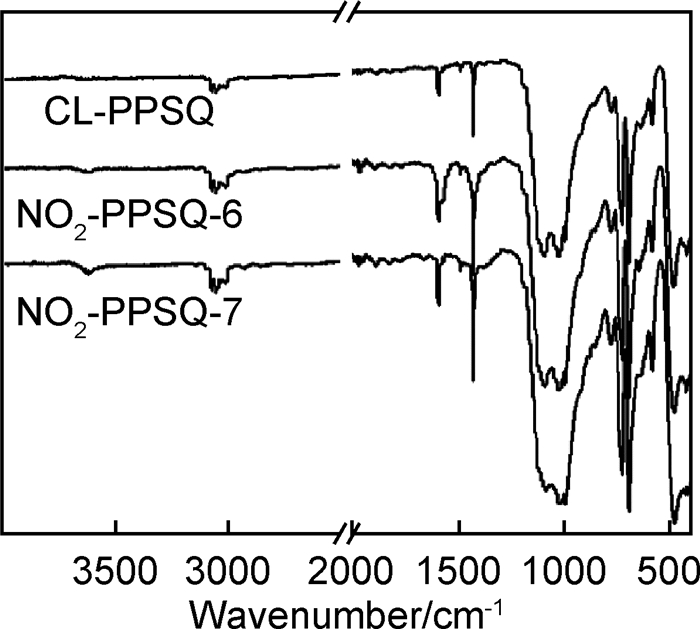
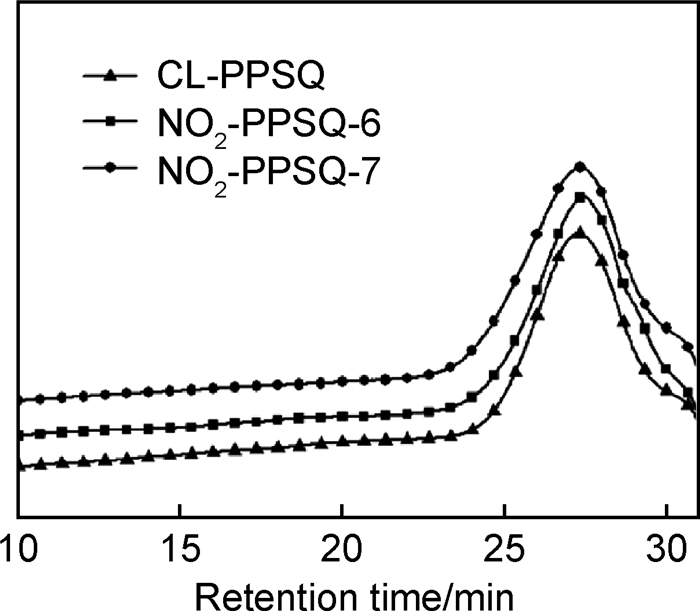
2.2.2 HNO3-KNO3和CH3COOH-KNO3硝化体系与发烟硝酸和加有H2SO4的硝化体系相比,使用HNO3-KNO3和CH3COOH-KNO3两种方法进行硝化反应后,硝化产物中均没有出现—NO2,并且也不存在分子链断裂的问题。如图 8所示,NO2-PPSQ-6(HNO3-KNO3体系下75℃下反应15h的产物)和NO2-PPSQ-7(CH3COOH-KNO3体系在75℃下反应20h的产物)的FTIR谱图,与CL-PPSQ的红外谱图相比,此两体系下的产物没有变化,尽管在这两种体系下的反应条件与体系4和5相比更加苛刻,反应温度为75℃,反应时间为15~20h。GPC结果表明(图 9),在此两种体系下,产物均没有发生分子链的断裂。另外,尝试CH3COOH-HNO3体系下的硝化实验,结果和CH3COOH-KNO3体系一样,没有发生硝化反应。
|
图 8 NO2-PPSQ-6, 7和CL-PPSQ的红外谱图 Fig. 8 FTIR spectra of NO2-PPSQ-6, 7 and CL-PPSQ |
|
图 9 NO2-PPSQ-6, 7和CL-PPSQ的GPC谱图 Fig. 9 GPC spectra for NO2-PPSQ-6, 7 and CL-PPSQ |
与发烟硝酸和加有浓H2SO4的硝化体系相比,(CH3CO)2O-HNO3硝化体系更加温和,也常用于硝化实验。控制反应温度为25℃,反应1.5h和3h,得到了硝化产物NO2-PPSQ-8和NO2-PPSQ-9。
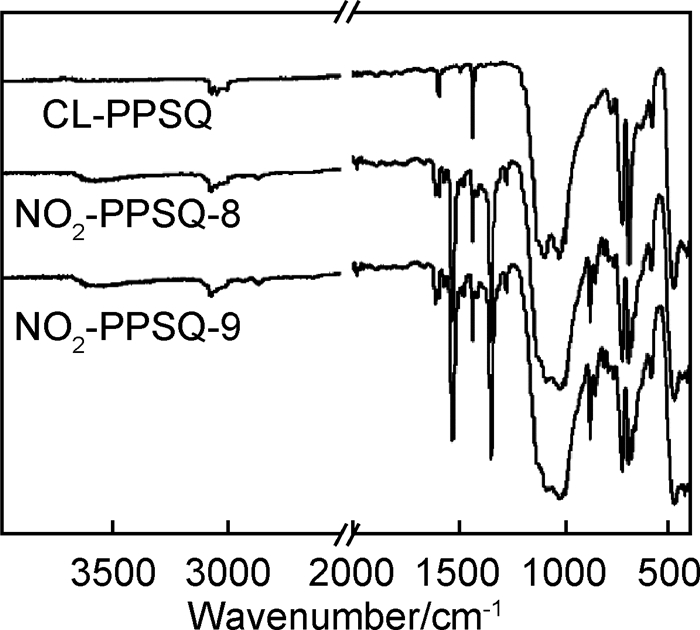
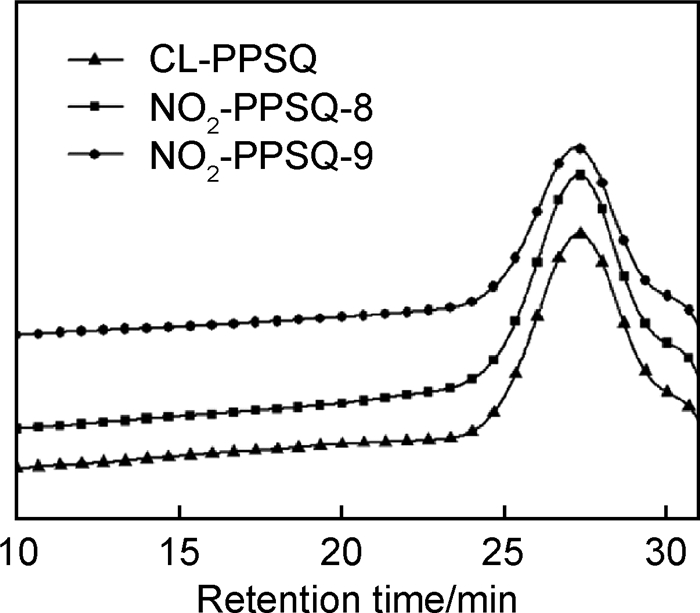
图 10是两种产物的FTIR谱图,从图中可以看到,与CL-PPSQ和NO2-PPSQ-1,4,5的红外谱图相比,可发现在1524cm-1和1346cm-1处有中等强度的—NO2的吸收峰出现,表明在此反应条件下CL-PPSQ可被硝化,但硝化程度较弱。同时,图 11和表 1中的GPC结果表明,NO2-PPSQ-8,9的Mn与CL-PPSQ相比,均稍有增高,PDI变化不大;而与方法1~5的硝化产物相比,NO2-PPSQ-8,9的Mn和PDI都要高出很多,表明使用(CH3CO)2O-HNO3体系对CL-PPSQ进行硝化反应可以得到分子链不发生断裂的硝化产物。虽然从表 1中可以看到,NO2-PPSQ-8,9中N的质量分数比方法1~5的硝化产物要低一些,即NO2-PPSQ-8,9中硝基数目较少,但它们可以保持CL-PPSQ的环梯形结构不被破坏。
|
图 10 NO2-PPSQ-8, 9和CL-PPSQ红外谱图 Fig. 10 FTIR spectra of NO2-PPSQ-8, 9 and CL-PPSQ |
|
图 11 NO2-PPSQ-8, 9和CL-PPSQ的GPC谱图 Fig. 11 GPC spectra for NO2-PPSQ-8, 9 and CL-PPSQ |
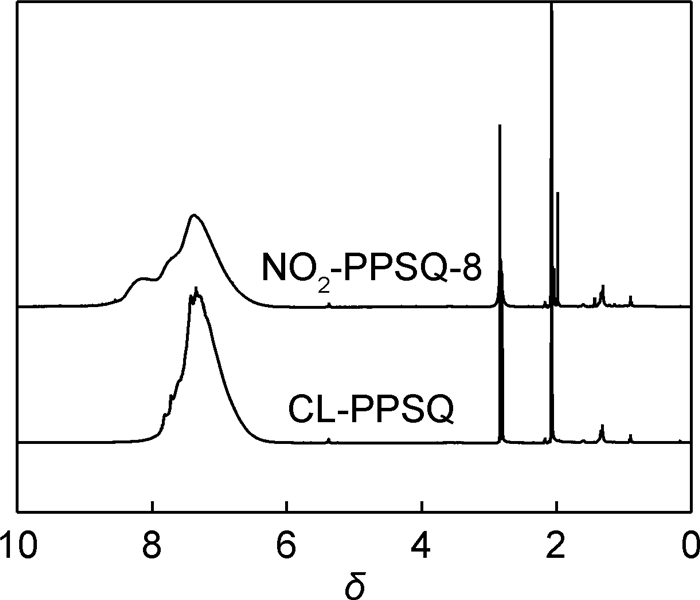
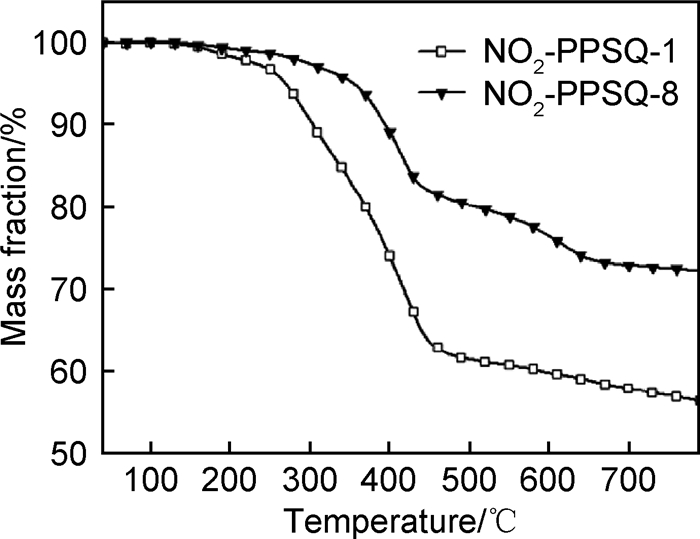
图 12是NO2-PPSQ-8与CL-PPSQ的1H NMR对比图,由于—NO2基团的强吸电子诱导效应对苯环氢产生的去屏蔽作用, 使其化学位移向低场,即高位移处移动。因此,NO2-PPSQ-8与CL-PPSQ相比,在高位移处出现更多的苯环上氢质子的共振峰。对NO2-PPSQ-8进行了热失重分析,图 13是NO2-PPSQ-8的TG曲线,与NO2-PPSQ-1相比,NO2-PPSQ-8的初始分解温度(失重5%的温度)提高了将近100℃,初始分解温度提高最重要的原因是NO2-PPSQ-8没发生分子链的断裂,因为未出现和NO2-PPSQ-1一样多的硝酸酯基。从图 13中还可看到NO2-PPSQ-8的残炭率与NO2-PPSQ-1相比有了很明显的提高,原因有二:一是NO2-PPSQ-8的环梯形结构得以保持,结构更规整,更容易形成残炭;二是NO2-PPSQ-8中的—NO2数目小于NO2-PPSQ-1,因此,分解失重减少。
|
图 12 NO2-PPSQ-8和CL-PPSQ的1H NMR图 Fig. 12 1H NMR spectra of NO2-PPSQ-8和CL-PPSQ |
|
图 13 NO2-PPSQ-1, 8的TGA曲线 Fig. 13 TGA curves of NO2-PPSQ-1, 8 |
HNO3是最主要的硝化剂,由于被硝化物性质和活性的不同,硝化剂常常不是单独的HNO3,而是HNO3和各种质子酸(如H2SO4、发烟H2SO4、氢氟酸等)、有机酸及其酸酐以及各种刘易斯酸的混合物。通常,硝化反应过程中是不加溶剂的,有时为了防止被硝化物和硝化产物与硝化混合剂发生反应或水解,硝化反应可以采取在有机溶剂中进行。因此,在我们的实验过程中,全部加入了适量的CH2Cl2溶剂。
苯的硝化反应是亲电取代反应,普遍认为主要活泼质点是NO2+。具有NO2-X通式的化合物,都可以产生NO2+。其硝化能力或活性决定于NO2-X中X基对电子的亲和力的大小,一般常见的硝化剂的硝化能力大小排列为[11]:
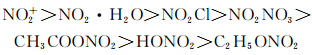
|
(1) |
对于不同的硝化试剂,其硝化作用的过程也不同。在发烟HNO3中,起作用的是NO2+,且NO2+浓度与HNO3浓度密切相关,发烟HNO3的硝化能力随HNO3浓度的降低而减弱。当使用HNO3和其他酸共同作为硝化试剂时,硝酸体现出其两性特性,它既是酸,又是碱。HNO3对强质子酸如硫酸起碱的作用,而HNO3对水、CH3COOH等则起到酸的作用。当HNO3起碱的作用时,硝化能力就增大,反之,如果起酸的作用时,硝化能力就降低。HNO3和(CH3CO)2O混合硝化剂的特点是反应较缓和,适用于易被氧化和易为硝硫混酸所分解的被硝化物的硝化反应。对于HNO3和(CH3CO)2O混合硝化剂的硝化活化剂,如果HNO3加入量低于42%,系统中主要形成乙酰硝酸酯(CH3COONO2)。
根据上述分析,不难分析出在实验过程中所使用的数种硝化体系硝化能力的强弱。对于发烟HNO3(90%)和H2SO4-HNO3(KNO3)体系,能电离出一定数量的NO2+,具有很强的硝化能力;随着发烟HNO3浓度的降低(86%,84.5%),NO2+数量减少,硝化能力减弱;对于(CH3CO)2O-HNO3体系,由于HNO3质量分数小于42%,因此主要电离出CH3COONO2,根据式(1) 判断,硝化能力适中;对于浓HNO3(65%),其浓度已降低到很难电离出NO2+,因此其硝化能力较弱;而对于CH3COOH-HNO3(KNO3)体系,HNO3起到酸的作用,进一步降低了其硝化能力,故其硝化能力最弱,最终导致在不同体系下,CL-PPSQ被硝化为不同的硝化产物。
3 结论(1) 使用发烟硝酸对CL-PPSQ进行硝化后,产物中发现有大量硝基的出现,然而,产物分子量与PPSQ相比有较大下降,表明硅氧烷链段断裂,出现热稳定性较差的硝酸酯基团,影响产物的热稳定性。
(2) HNO3-H2SO4和KNO3-H2SO4体系硝化能力强,同发烟硝酸一样,硝化产物分子链都发生了断裂;而HNO3-KNO3和CH3COOH-KNO3体系对CL-PPSQ没有硝化能力,也未使其分子链发生断裂。
(3) 使用(CH3CO)2O-HNO3体系,硝化过程温和,虽然硝化产物中的硝基个数较少,但可制备得到分子链不断裂的硝化产物,使其结构更加规整,同时,硝化产物的热稳定性也更加优异。
| [1] | CHANG S, MATSUMOTO T, MATSUMOTO H. Synthesis and characterization of heptacyclic laddersiloxanes and ladder polysilsesquioxane[J]. Appl Organomet Chem, 2010, 24 (3): 241–246. DOI: 10.1002/aoc.v24:3 |
| [2] | HANDKE M, HANDKE B, KOWALEWSKA A, et al. New polysilsesquioxane materials of ladder-like structure[J]. Journal of Molecular Strucuture, 2009, 924 : 254–263. |
| [3] | ZHANG Z X, HAO J K, XIE P. A well-defined ladder polyphenylsilsesquioxane (Ph-LPSQ) synthesized via a new three-step approach: monomer self-organization-lyophilization-surface-confined polycondensation[J]. Chem Mater, 2008, 20 (4): 1322–1330. DOI: 10.1021/cm071602l |
| [4] | ZHANG L L, TIAN G F, WANG X D, et al. Polyimide/ladder-like polysilsesquioxane hybrid films: mechanical performance, microstructure and phase separation behaviors[J]. Composites: Part B, 2014, 56 (1): 808–814. |
| [5] | KIM S G, TAMAKI C R, LAINE R M. Synthesis of amino-containing oligophenylsilsesquioxanes[J]. Polymer, 2005, 46 (12): 4514–4524. DOI: 10.1016/j.polymer.2005.02.036 |
| [6] | 蒋云芸. 梯形聚苯基硅倍半氧烷的合成及应用研究[D]. 北京: 北京理工大学, 2012. JIANG Y Y. Synthesis and application of ladder polyphenylsilsesquioxane[D]. Beijing: Beijing Institute of Technology, 2012. |
| [7] | 梁嘉香. 环梯形聚苯基硅倍半氧烷的合成及表征[D]. 北京: 北京理工大学, 2014. LIANG J X. Synthesis and characterization of cyclic ladder polyphenylsilsesquioxane[D]. Beijing: Beijing Institute of Technology, 2014. |
| [8] | 范海波, 杨荣杰, 李向梅. 多面体低聚八硝基苯基硅倍半氧烷纯度分析[J]. 化学学报, 2012, 70 (16): 1737–1742. FAN H B, YANG R J, LI X M. Purity analysis of polyhedral oligomeric octa(nitrophenyl)silsesquioxane[J]. Acta Chim Sinica, 2012, 70 (16): 1737–1742. |
| [9] | 范海波, 杨荣杰, 李定华. 多面体低聚八氨基苯基硅倍半氧烷合成方法改进及其表征[J]. 化学学报, 2012, 70 (4): 429–435. FAN H B, YANG R J, LI D H. Synthesis improvement and characterization of polyhedral oligomeric octa(aminophenyl)silsesquioxane[J]. Acta Chim Sinica, 2012, 70 (4): 429–435. |
| [10] | TAMAKI R, TANAKA Y, ASUNCION M. Octa(aminophenyl)silsesquioxane as a nanoconstruction site[J]. J Am Chem Soc, 2001, 123 : 12416–12417. DOI: 10.1021/ja011781m |
| [11] | 周发岐. 炸药合成化学[M]. 北京: 国防工业出版社, 1984: 230-317. ZHOU F Q. Explosive Synthesis Chemistry[M]. Beijing: National Defence Industry Press, 1984: 230-317. |
| [12] | 樊能廷. 有机合成事典[M]. 北京: 北京理工大学出版社, 1995: 129-181. FAN N T. Organic Synthesis[M]. Beijing: Beijing Institute of Technology Press, 1995: 129-181. |
| [13] | 陈树森, 邱文革, 于永忠. 六苯甲酰基六氮杂异伍兹烷的硝解[J]. 兵工学报, 2000, 21 (2): 116–118. CHEN S S, QIU W G, YU Y Z. Nitrolysis of hexabenzoylhexaazaisowurzitane[J]. Acta Armamentarii, 2000, 21 (2): 116–118. |
| [14] | 李玉川, 祁才, 孙成辉, 等. 2, 6, 8, 12-四硝基-2, 4, 6, 8, 10, 12-六氮杂异伍兹烷的合成及量子化学研究含能材料[J]. 含能材料, 2010, 18 (2): 121–127. LI Y C, QI C, SUN C H, et al. Synthesis and quantum chemical study on 2, 6, 8, 12-tetranitro-2, 4, 6, 8, 10, 12-hexaazaisowurtzitane[J]. Chinese J Energ Mater, 2010, 18 (2): 121–127. |
| [15] | 魏运洋, 金铁柱. 十二烷基苯的硝化选择性[J]. 应用化学, 1995, 12 (1): 43–47. WEI Y Y, JIN T Z. Orientation of nitration on dodeeylbenzene[J]. Chinese J Appl Chem, 1995, 12 (1): 43–47. |
| [16] | 孙成辉, 方涛, 杨宗云. 硝-硫混酸硝化四乙酰基六氮杂异伍兹烷制备CL-20反应机理[J]. 含能材料, 2009, 17 (2): 161–165. SUN C H, FANG T, YANG Z Y. Reaction mechanism of preparation CL-20 from tetraacetylhexaazaisowurtzitane nitrated by mixture of nitric acid and sulfuric acid[J]. Chinese J Energ Mater, 2009, 17 (2): 161–165. |
 2017, Vol. 45
2017, Vol. 45


