文章信息
- 王丹军, 申会东, 郭莉, 张洁, 付峰
- WANG Dan-jun, SHEN Hui-dong, GUO Li, ZHANG Jie, FU Feng
- 三维介孔Bi2WO6光催化剂的制备及无机离子对其光催化活性的影响
- Synthesis of Three-dimensional Mesoporous Bi2WO6 Photocatalyst and Effect of Inorganic Ion on Its Photocatalytic Activity
- 材料工程, 2016, 44(2): 8-16
- Journal of Materials Engineering, 2016, 44(2): 8-16.
- http://dx.doi.org/10.11868/j.issn.1001-4381.2016.02.002
-
文章历史
- 收稿日期: 2014-11-15
- 修订日期: 2015-07-15
染料废水由于其色度深、有机污染物含量高、成分复杂、稳定性强,严重威胁着大自然的生态平衡和人类的生命与健康,在排放前需要进行降解或脱色处理[1],而传统的物理方法和生化处理方法效率不高,因此染料废水的处理一直是水污染控制领域的技术难题。近年来,半导体多相光催化技术引起了国内外的广泛关注,利用太阳光催化氧化有机污染物作为一种有效的污染物处理方法,面对能源枯竭和污染加剧,开启了污染物处理的新时代[2, 3]。
钨酸盐纳米材料是一类重要的功能材料,其在光致发光、传感器、磁性器件等领域具有广阔的应用前景,已成为研究热点之一[4]。近年来,金属钨酸盐作为一类新型光催化剂,以其优异的光催化性能逐渐引起国内外学者的关注[5, 6, 7, 8]。Bi2WO6是一种结构最为简单的Aurivillius型层状化合物,钙钛矿层(WO6)2n-n沿c轴方向插入两个(Bi2O2)2n+n层中间,形成典型的二维结构(图 1)。Bi2WO6特殊的结构赋予其特殊的介电、发光、离子导体、催化等性能。Bi2WO6的Bi6s轨道和O2p轨道杂化形成价带,W5d轨道形成导带,所以其禁带宽度较窄(约为2.7eV),可以被420nm以上的可见光激发,具有可见光催化活性,是一种新型的光催化材料[7]。
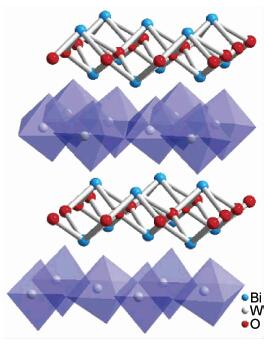 | 图1 Bi2WO6的结构示意图 Fig.1 Structure diagram of Bi2WO6 | |
近年来,人们对Bi2WO6光催化材料的制备技术进行了系统研究[10],除固相法外,探索使用一些软化学法合成Bi2WO6基光催化材料,如溶胶-凝胶法[11]、沉淀法[12] 、超声法[13]、水热/溶剂法[14, 15, 16]等,其中水热法在控制晶粒尺寸和形貌上有其自身的优势,成为普遍采用的合成方法。朱永法课题组[14]以Na2WO4 和Bi(NO3)3 为原料采用水热法制备片状纳米Bi2WO6,由于其较大的比表面积,表现出较强的可见光催化活性。王文中课题组[15, 16]通过加入PVP作为模板剂成功制备了由片状堆积的微球和八面体结构Bi2WO6。近期本课题组采用水热法制备了多孔结构Bi2WO6材料[17],并对其进行了改性研究[18, 19, 20]。研究表明,Bi2WO6的能带结构、形貌、结构、尺寸和比表面积等因素决定其光催化活性。然而,在实际应用中水体的pH值和自然水体中富含的无机离子对Bi2WO6光催化性能的影响文献报道却较少。此外,一维和二维结构的Bi2WO6催化材料在实际应用中不易回收重复使用。所以,人们通过添加表面活性剂和形貌控制剂获得了三维结构的Bi2WO6,如花状[21]和轮胎状[22]。
在前期研究工作的基础上,采用水热合成技术,在不添加任何形貌控制剂的条件下,合成了三维球状介孔结构Bi2WO6,以亚甲基蓝模拟印染废水中的模型偶氮类污染物,探讨了溶液的pH值以及水体中常见的无机离子等对亚甲基蓝光催化降解的影响,以期为光催化技术的实际应用提供借鉴。
1 实验方法 1.1 试剂硝酸铋(Bi(NO3)3·5H2O),钨酸铵((NH4)2WO4·5H2O),无水乙醇(CH3CH2OH),硝酸(HNO3),氢氧化钠(NaOH),氯化铵(NH4Cl),硝酸铜(Cu(NO3)2·3H2O),硫酸亚铁(FeSO4·7H2O),硝酸铁(Fe (NO3)3·9H2O),碘化钾(KI),溴化钾(KBr),氯化钾(KCl),亚硝酸钠(NaNO2),亚甲基蓝(C16H18ClN3S·3H2O,简写MB)均为分析纯,实验用水为实验室自制I级蒸馏水。
1.2 样品的制备称取0.98g Bi(NO3)3·5H2O固体,将其溶于20mL 0.4mol·L-1的HNO3溶液,40℃下搅拌至固体溶解,加入10mL 0.02mol·L-1 (NH4)2WO4·5H2O溶液,磁力搅拌2h。停止搅拌后将此混合溶液转入水热反应釜,密封后置于电热恒温鼓风干燥箱中于190℃下恒温分别0.5,1.0,2.0h,反应结束后自然冷却至室温,离心,所得沉淀经过洗涤(水洗和醇洗),干燥,得到样品分别记做Bi2WO6-0.5h,Bi2WO6-1.0h和Bi2WO6-2.0h。
1.3 样品的表征样品的物相结构采用XRD-7000型全自动X射线粉末衍射仪(XRD)鉴定,CuKα (Ni滤玻片滤波,λ=0.15418nm),管电压40kV,管电流30mA,步长0.02°,扫描范围2θ:20°~80°,扫描速率1(°)/min;样品的形貌在JEOL-6701型场发射扫描电子显微镜(FE-SEM)上观察;样品的固体UV-Vis吸收光谱采用UV-2550型紫外-可见分光光度计测定,扫描范围200~600nm;比表面积V-Sorb2008P型比表面积及孔径分析仪测定,双气路H2-N2载气,78K低温氮气吸附。
1.4 样品的光催化活性评价图 2为光催化评价装置,用400W金卤灯模拟可见光(用滤光片滤去420nm以下的光)。将200mL浓度为 20mg·L-1的亚甲基蓝溶液加入石英试管中,再加入0.2000g 粉末状Bi2WO6加入反应器中,用硝酸和氢氧化钠调节其pH值,并将其置于黑暗中搅拌120min达到吸附平衡后,开启光源进行光化学反应。每隔10min取样离心分离催化剂,取上清液测定紫外-可见吸收光谱和最大吸收波长处的吸光度,以此来评价催化剂的光催化活性。在研究无机离子对亚甲基蓝光催化降解的影响时,向石英夹套反应器中加入0.2000g 粉末状Bi2WO6和10mL 200mg·L-1的亚甲基蓝溶液,然后分别加入200mL 10mmol·L-1的NH4Cl,Cu(NO3)2,FeSO4,Fe(NO3)3,KI,KBr,KCl,NaNO2水溶液和200mL蒸馏水(对照),将其置于光化学反应仪中进行光照,30min后离心分离催化剂,取上清液测定UV-Vis吸收光谱和最大吸收波长处的吸光度,并以此来评价溶液中的阴、阳离子对亚甲基蓝光催化降解的影响。
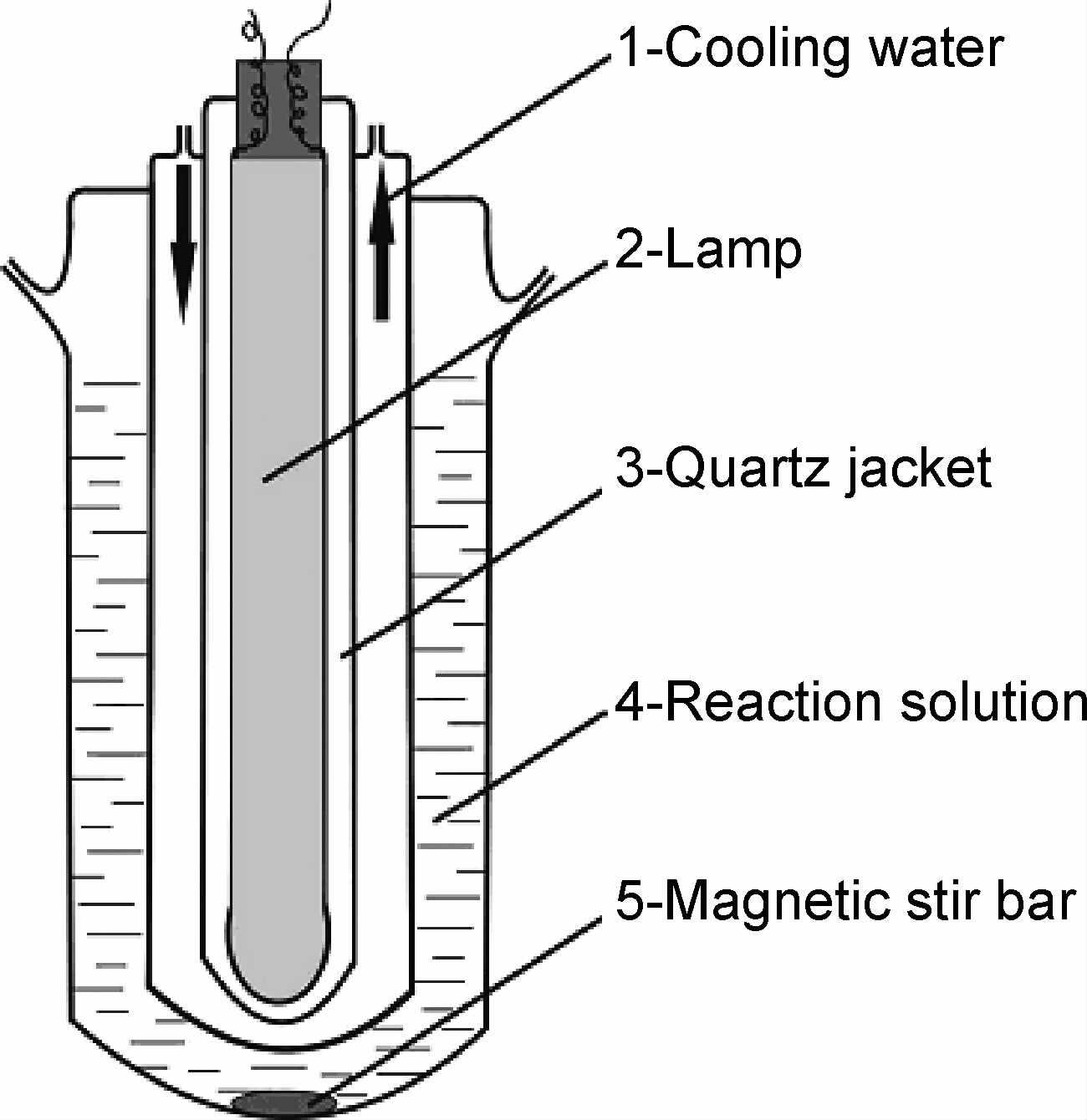 | 图2 光催化实验装置 Fig.2 The photocatalysis experimental apparatus | |
图 3(a)是190℃水热反应2h所得Bi2WO6的XRD图谱,可以看出,衍射峰(2θ为28.3°,32.8°,32.9°,47.0°,47.1°,55.8°,58.5°,68.7°,75.9°和78.5°)位置均与正交晶系的Bi2WO6吻合,与准卡片(PDF卡号:39-0256)一致,对应于正交晶系Bi2WO6的 (131),(200),(002),(260),(202),(331),(262),(400),(103) 和(204)晶面,可确认样品为正交晶系Bi2WO6,另外,在XRD图谱中没有杂峰出现,表明样品的纯度较高[17];为了考察样品的多孔结构,对样品进行N2吸附-脱附测试(图 3(b))。从样品Bi2WO6-2.0h的N2吸附-脱附等温线可以看出,脱附曲线具有明显的滞后,属于典型的IV型特征,表明样品属于介孔结构材料[23, 24, 25]。图 3(b)中插入小图为样品Bi2WO6-2.0h的孔径分布图,表明样品表面有大量的尺寸约10nm的孔;此外,在30~70nm范围内也有孔的分布,这些大孔可能来自于纳米片的定向自组装过程。样品的比表面积(SBET)通过N2吸附等温线(-196.68℃)计算,大约为47.72m2·g-1,样品具有大的比表面积是由其特殊形貌决定的。
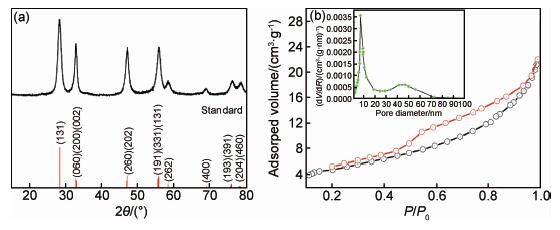 | 图3 Bi2WO6-2.0h的XRD图谱(a)和N2吸附-脱附曲线(b) Fig.3 XRD patterns (a) and N2 gas adsorption-desorption isotherm (b) of the as-synthesized Bi2WO6 | |
图 4是样品的FE-SEM,TEM和HR-TEM照片及EDS能谱图,由图 4可以看出,所得Bi2WO6样品形貌规整,呈三维球形结构,分散性好,大小均匀,粒径在3μm左右;由图 4(c),(d)可以看出,Bi2WO6微球是由厚度20~40nm的纳米片按照一定方向组装而成,纳米片交错联结形成大小不同的孔。由图 4(e)可以清晰看出样品的轮廓为球形;此外,由图 4(e)插入的选区电子衍射图可以看出明亮的衍射斑点和多个同心光环,表明组成Bi2WO6微球的纳米片是多晶结构。图 4(f)为样品高分辨透射电镜照片(HR-TEM),可见Bi2WO6微球的片层结构的晶格间距为0.315nm,对应于(131)晶面的面间距,表明组成Bi2WO6微球的纳米片沿(131)晶面定向生长[14, 16]。图 4(g)是样品的EDS能谱,可以看出,Bi2WO6由Bi,W,O 3种元素组成,不含其他杂质元素,进一步表明所得样品的纯度较高。根据前期工作,高结晶度和高的纯度表明催化剂表面的光生电子-空穴对的捕获陷阱较少,有利于催化活性的提高;此外,多孔结构有利于增加催化剂的比表面积,对催化剂的活性有利[17]。
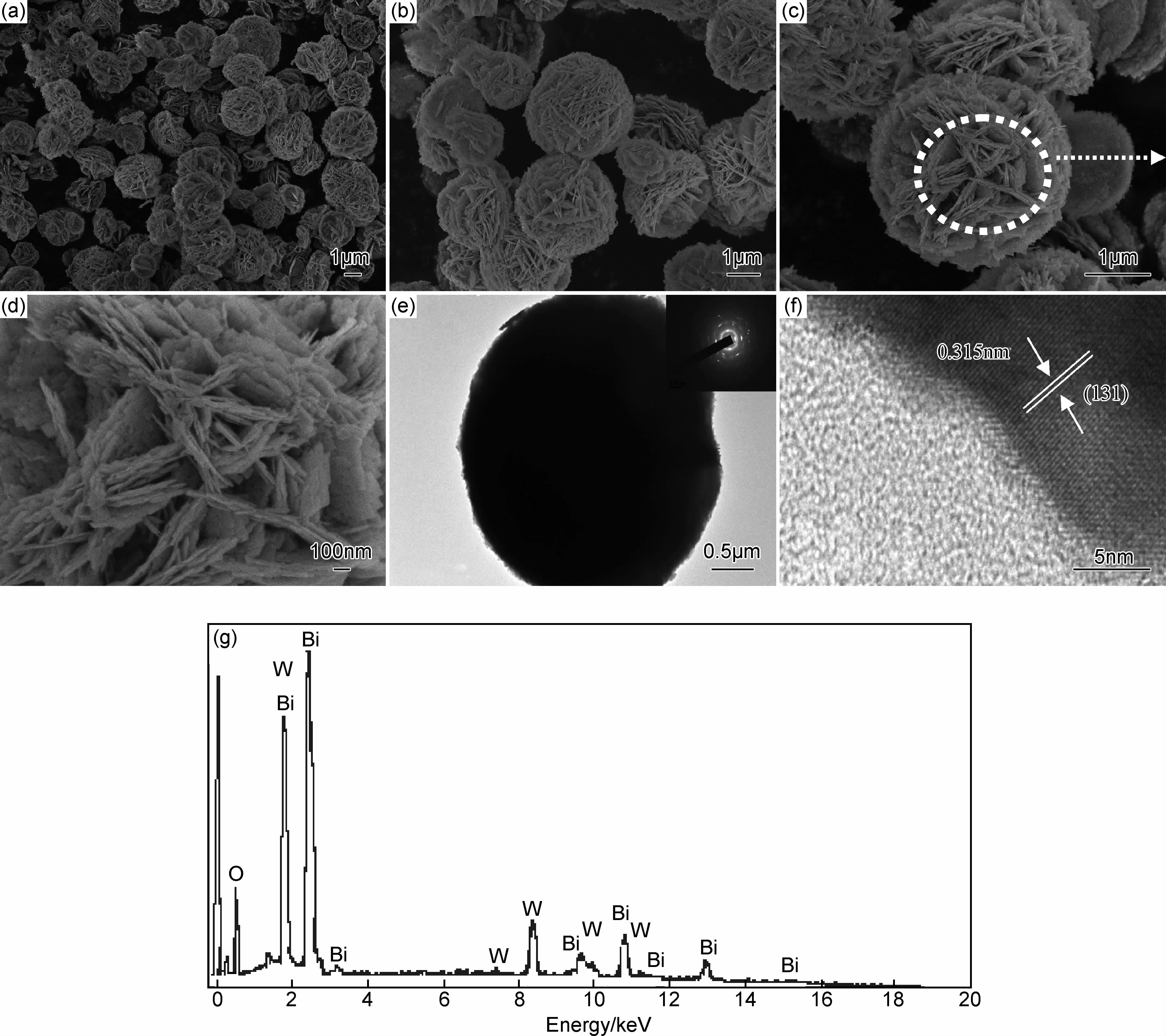 | 图4 样品Bi2WO6-2.0h的FE-SEM,TEM和HR-TEM照片及EDS能谱图 (a)~(d)扫描电镜照片;(e)透射电镜照片和选区电子衍射图;(f)高分辨透射电镜照片;(g)EDS能谱图 Fig.4 FE-SEM, TEM, HR-TEM pictures and EDS spectrum of the Bi2WO6-2.0h sample (a)-(d)low-magnification and high-magnification FE-SEM images of the sample;(e)TEM image and its corresponding SAED of an individual Bi2WO6;(f)HR-TEM image of the simple;(g)EDS spectrum of the Bi2WO6-2.0h sample | |
为了考察三维Bi2WO6微球的形成过程,固定其他反应条件不变,改变水热反应时间,所得样品FE-SEM照片和XRD图如图 5所示,各样品比表面积如表 1所示。由图 5(a)可以看出,水热反应0.5h时,样品为球形纳米粒子,尺寸约20~50nm,样品的比表面积为25.6m2/g;反应时间延长至1h时,开始出现片状结构,比表面积增加至32.6m 2/g;继续延长反应时间至2h,则形成形貌规整的多级三维球形结构(图 5(c)),样品的比表面积上升至47.72m 2/g;由图 5(d)可以看出,190℃水热反应30min,样品为非晶态结构,衍射峰为宽化的弥散峰;当反应时间延长至60min时,开始出现(131),(200),(202)和(331)晶面的特征衍射峰,表明Bi2WO6纳米粒子开始定向生长;当水热时间延长至2h时,样品主要特征衍射峰全部出现,强度增大。样品的FE-SEM照片和XRD图谱完全吻合,证明了三维Bi2WO6微球是由定向生长的纳米片组装而形成的。
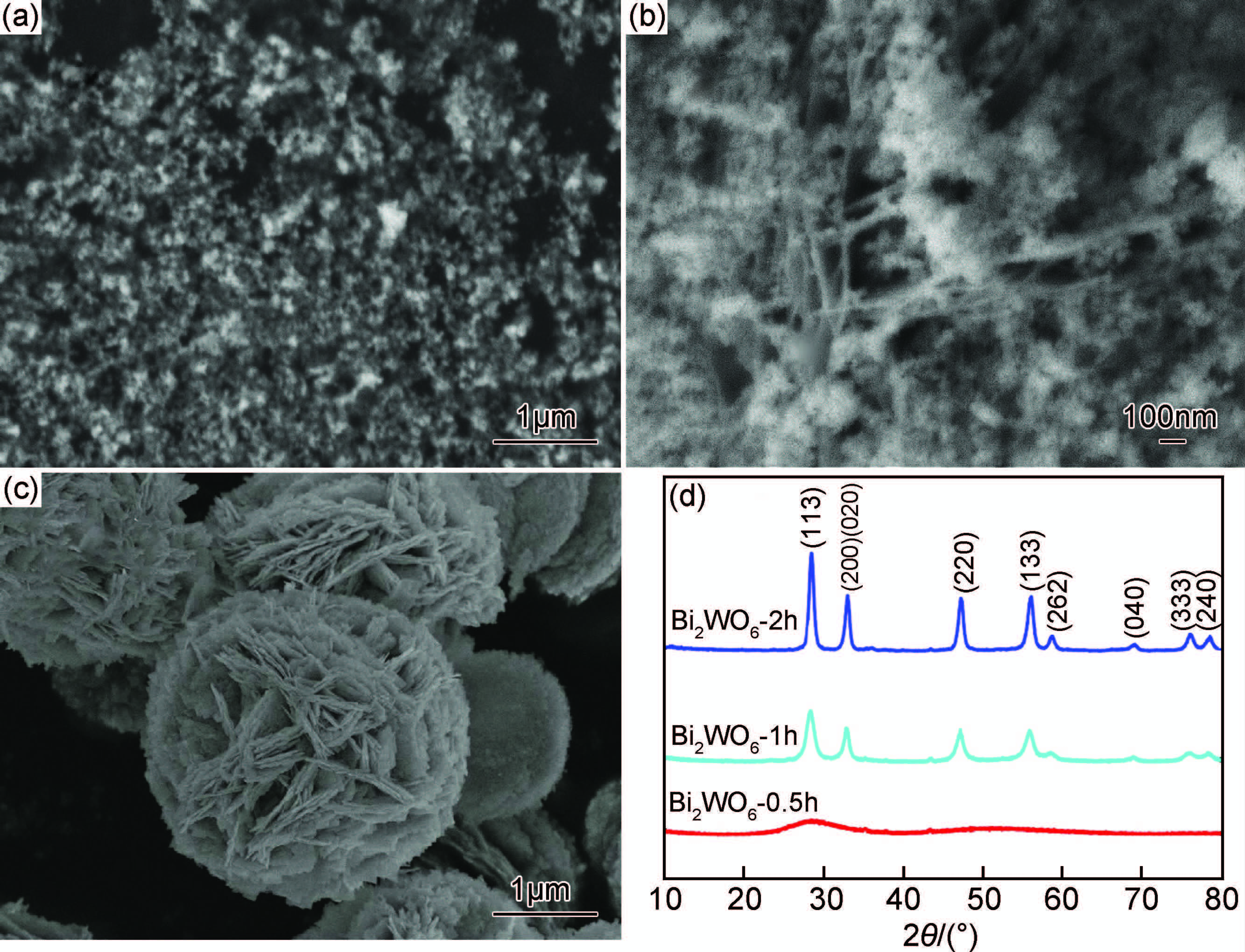 | 图5 不同水热反应时间所得Bi2WO6的扫描电镜照片和XRD图谱 (a)Bi2WO6-0.5h;(b)Bi2WO6-1h;(c)Bi2WO6-2h;(d)XRD图谱 Fig.5 FE-SEM images and XRD patterns of the Bi2WO6 samples (a)Bi2WO6-0.5h;(b)Bi2WO6-1h;(c)Bi2WO6-2h;(d)XRD patterns | |
| Sample | BET surface area/(m2·g-1) |
| Bi2WO6-0.5h | 25.60 |
| Bi2WO6-1.0h | 32.60 |
| Bi2WO6-2.0h | 47.72 |
图 6是不同水热反应时间所得样品的FT-IR图谱。从图中可以看出,在3425cm-1和1632cm-1处出现OH基伸缩振动吸收和变形振动吸收[26],且随着水热反应时间的延长,吸收峰逐渐变弱;在700~1000cm-1和400~600cm-1两个范围内出现系列吸收带,分别归属于Bi2WO6中的W—O键的伸缩振动(900cm-1处的吸收峰归属于不同组WO6八面体W—O端氧键的伸缩振动,而750cm-1处的吸收峰归属于共顶点的W—O键的伸缩振动)和Bi—O键的伸缩振动以及弯曲振动[27, 28],随着水热反应时间的延长,该处的吸收峰强度降低;此外,从图 6可以看出,当反应时间为30min时,样品在两个范围的吸收峰均发生宽化,且吸收峰出现了“红移”和“蓝移”并存的现象,这是由于此时所得产物为纳米粒子(粒径约为 20nm),粒子尺寸较小而导致各类影响因素更为显著所致[29]。
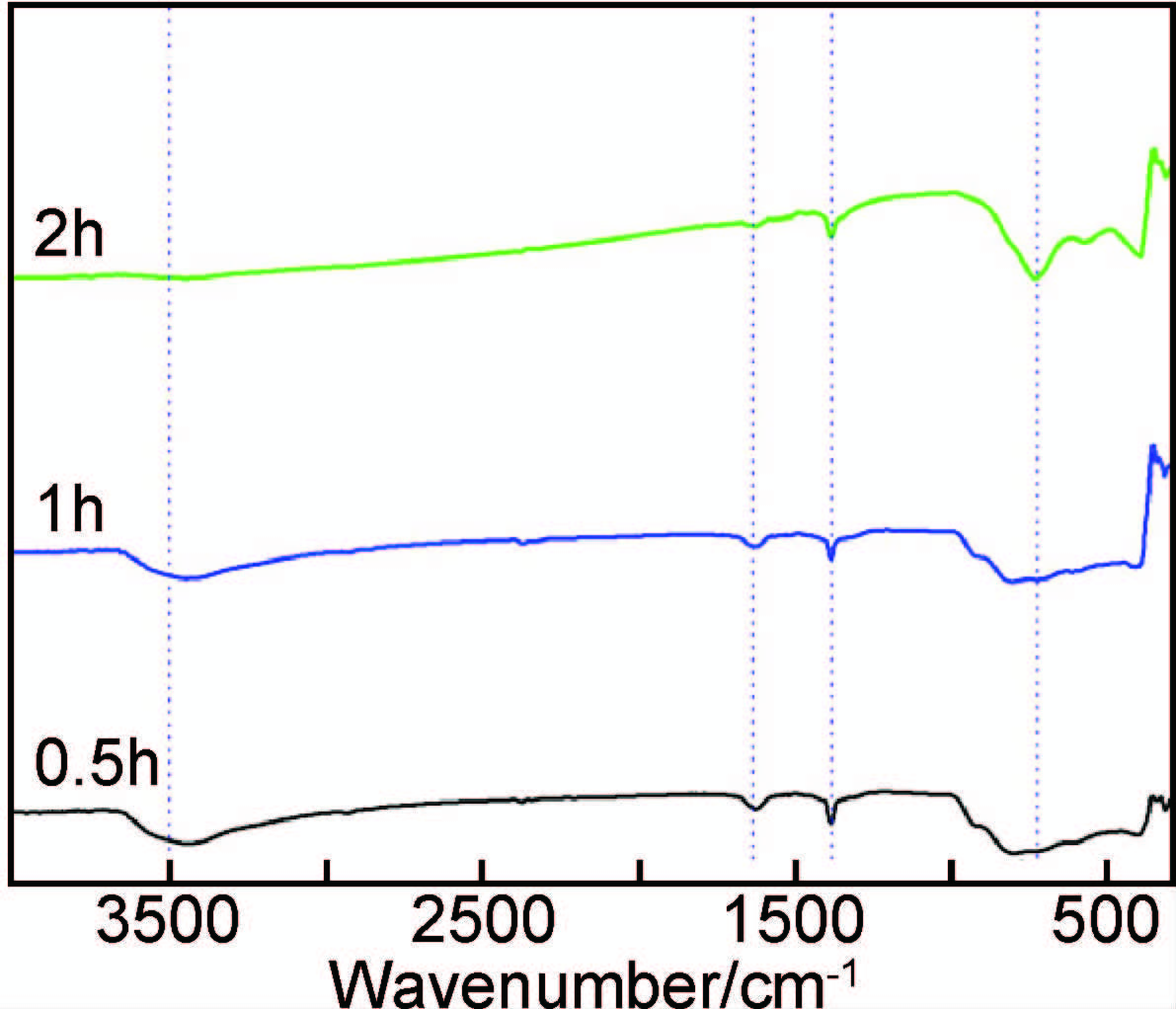 | 图6 不同水热时间所得Bi2WO6的红外光谱 Fig.6 FT-IR spectra of as-prepared Bi2WO6 under different hydrothermal time | |
Bi2WO6是一种典型的层状结构,[Bi2O2]2+平面层和八面体结构的[WO6]2-层交替出现(见图 1),[WO6]2-八面体之间有较大的排斥力,同样[Bi2O2]2+层之间也存在一定的斥力,Bi2WO6的这一结构特点决定了其在反应过程中容易形成片层状结构。根据XRD,FE-SEM和IR分析结果,推测Bi2WO6三维球形结构的形成机理如下:在水热反应初期,体系内形成大量Bi2WO6晶粒;随着反应时间的延长,Bi2WO6晶粒在溶液中发生溶解-结晶的过程。在强酸性条件下,H+抑制Bi3+的水解过程,导致Bi2WO6的成核速率远大于晶粒的成长速率,这样体系中存在的大量Bi2WO6就会相互聚集形成热力学稳定的球形粒子;在“奥斯特瓦尔德熟化(Ostwald ripening)”过程中,小晶粒消失同时形成大的晶粒。同时,大晶粒各向异性生长成纳米片;由于正交晶系的Bi2WO6是由(Bi2O2+2)n层和(WO2-6)n层交替堆积而成,导致Bi2WO6纳米片具有两个极性面,纳米片表面的静电作用导致其自发的相互靠拢、相互作用、定向组装(oriented attachment)形成形貌规整的三维球状纳米结构体系(见图 7)。
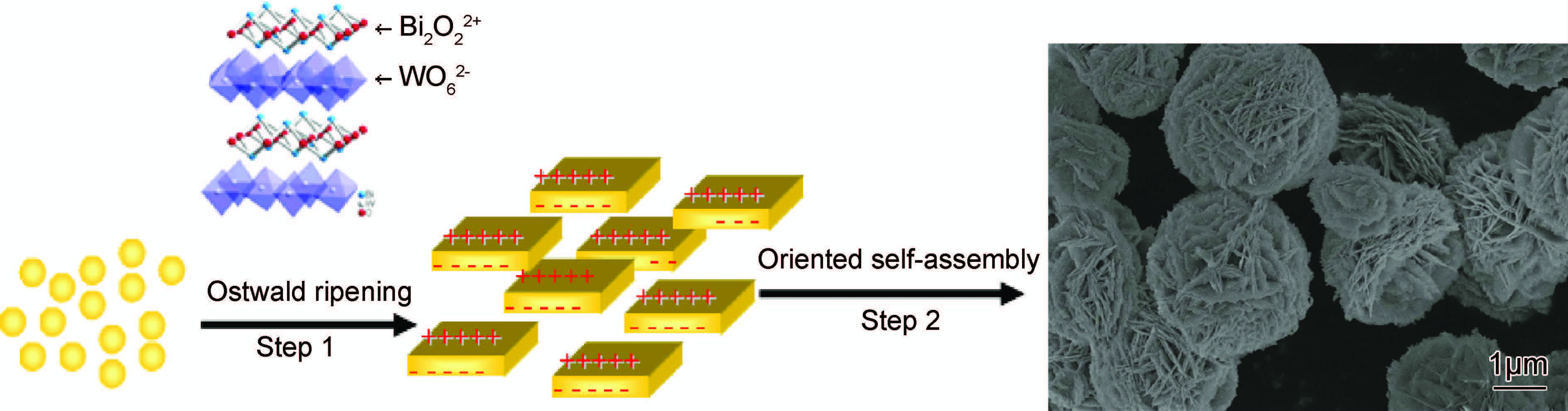 | 图7 三维介孔Bi2WO6纳米结构体系的形成机理 Fig.7 Formation mechanism of three-dimensional mesoporous Bi2WO6 nanoarchitectures | |
半导体材料的光吸收性质与其电子结构密切相关,也是决定其光催化活性的关键因素。图 8是190℃水热反应2h所得样品的UV-Vis吸收光谱,根据公式ahν=A(hν-Eg)n/2可估算样品的带隙[16, 17, 18, 19, 20, 30],其中,a,ν,A和Eg分别是样品的吸收系数,光子频率,常数和带隙,h为普朗克场常数,Bi2WO6的n值为1,作图(图 8中插入小图)可得,样品Bi2WO6-2h的带隙约为2.72eV,吸收边为456nm。
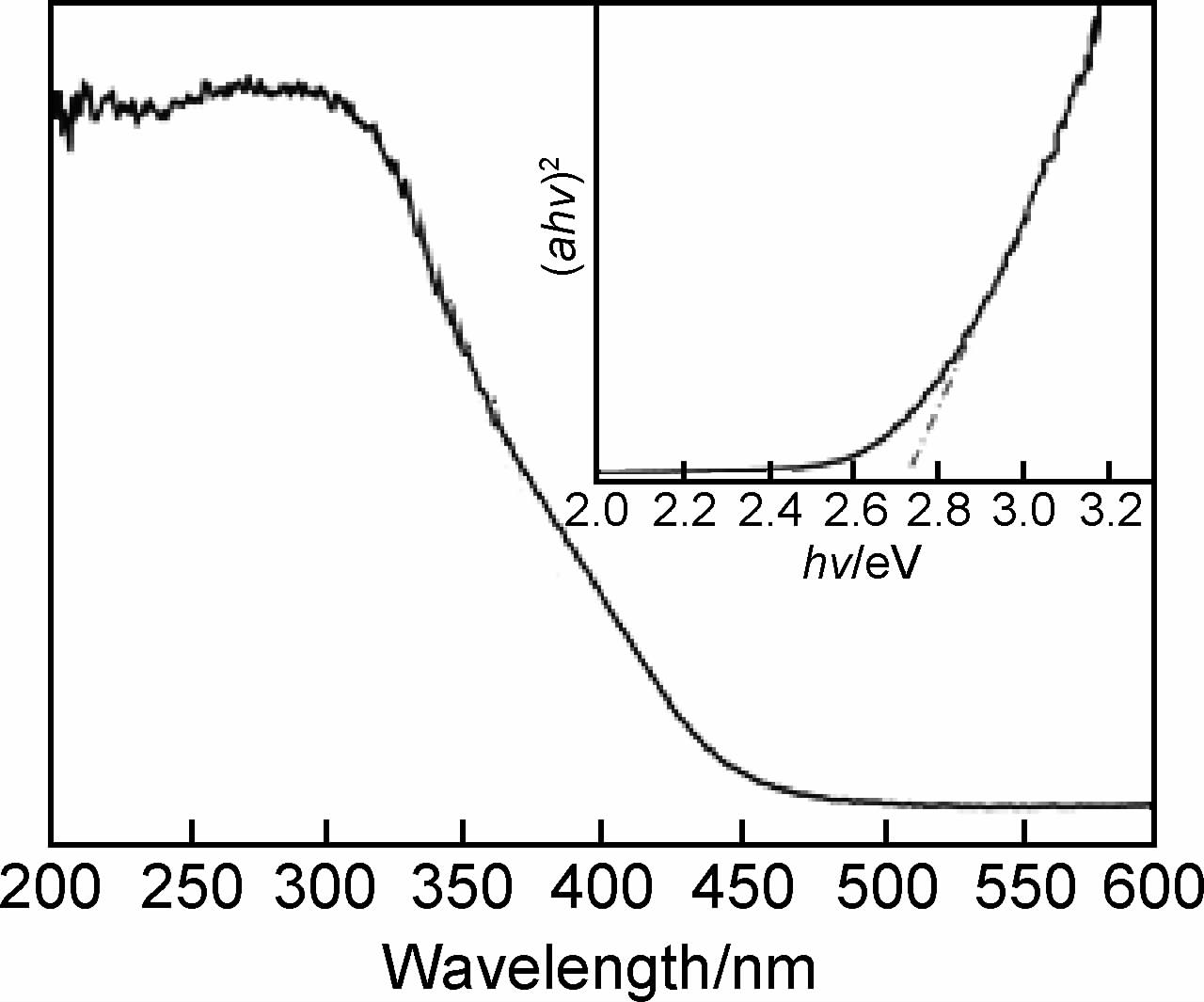 | 图8 三维介孔结构Bi2WO6光催化剂的 UV-Vis吸收光谱 Fig.8 UV-Vis absorption spectrum of 3D mesoporous Bi2WO6 photocatalysts | |
图 9是溶液pH值对亚甲基蓝光催化降解的影响,由图 9可见,亚甲基蓝的降解率随着溶液pH值的增加而明显下降,表明相比弱酸和碱性环境,在强酸性环境中,Bi2WO6催化剂对亚甲基蓝降解有更好的光催化活性,这是由于三维介孔结构Bi2WO6是在强酸性条件下获得,其表面呈现强酸性,在酸性环境中有利于催化剂的稳定,且酸性环境中Bi2WO6 表面更易吸附亚甲基蓝分子,有利于光催化反应的进行。
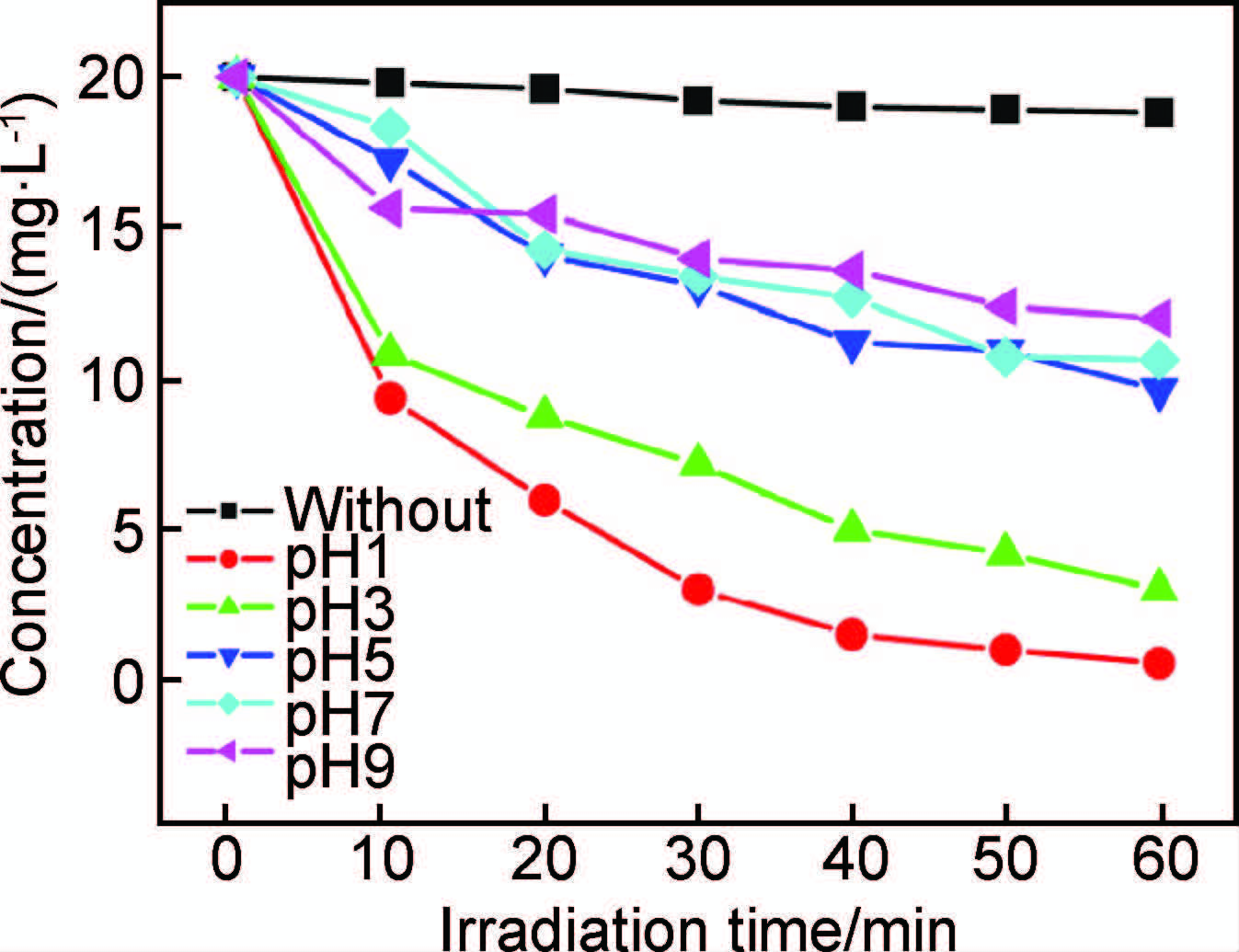 | 图9 pH值对亚甲基蓝光催化降解的影响 Fig.9 The effect of pH value on the photocatalytic degradation of methyl-blue | |
图 10是阳离子对亚甲基蓝光催化降解的影响,可以看出,NH4+和Fe3+对亚甲基蓝光催化降解有促进作用,相比之下Fe3+影响最大,可见光照射0.5h Fe3+存在的亚甲基蓝溶液,其光催化降解率是98.8%,对照组亚甲基蓝光催化降解率是84.2%;此外,实验结果表明 Cu2+的影响很小,而Fe2+对亚甲基蓝光催化降解有明显抑制作用,加有Fe2+的体系中亚甲基蓝光催化降解率是71.7%,比对照组亚甲基蓝光催化降解率降低了14.8%。
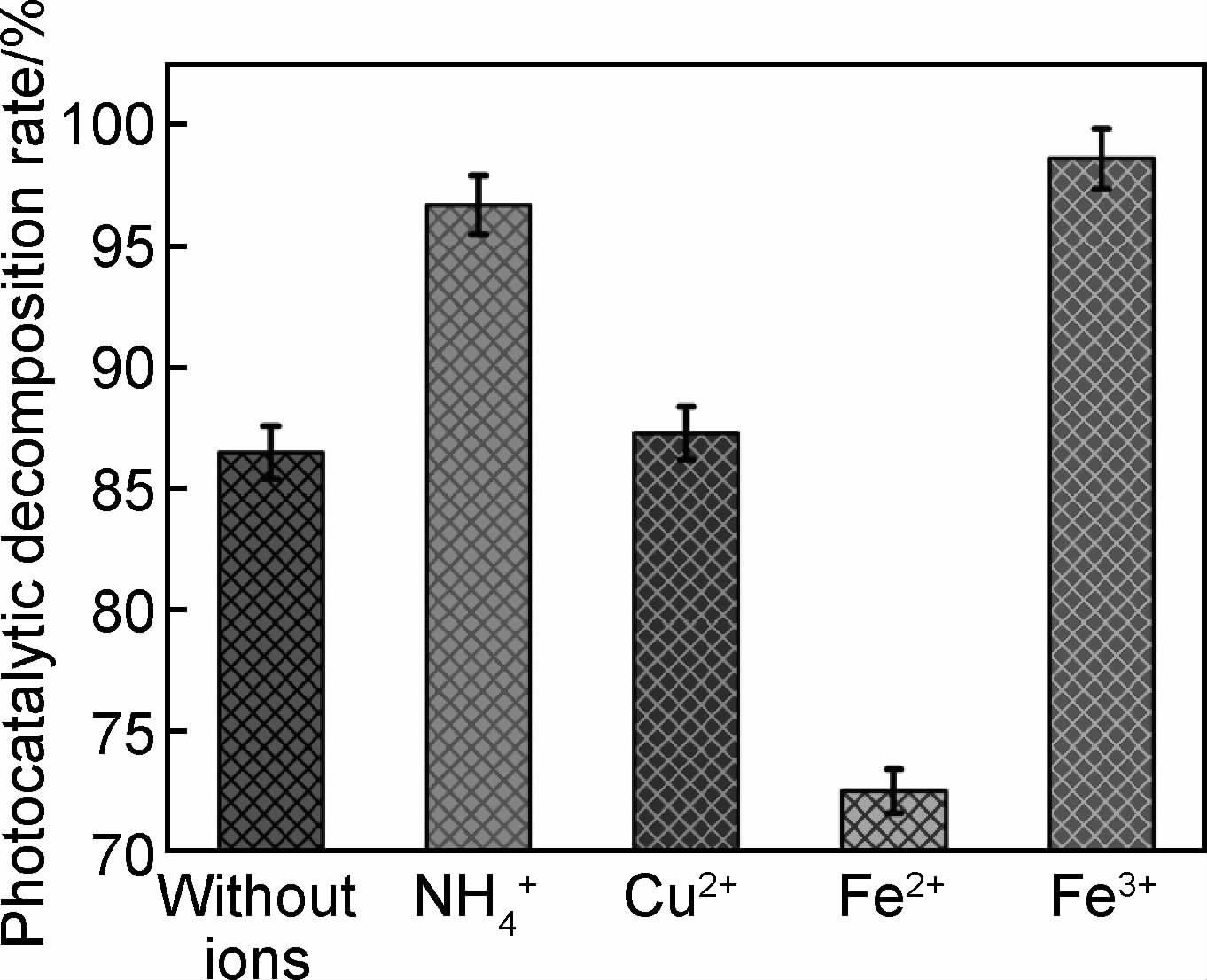 | 图10 阳离子对亚甲基蓝光催化降解的影响 Fig.10 The effect of cation on the photocatalytic degradation of methyl-blue | |
图 11是阴离子对亚甲基蓝光催化降解的影响,结果表明卤素离子X-离子(Br-,Cl-,I- )对亚甲基蓝光催化降解有促进作用,其中Br-,Cl-对亚甲基蓝光催化降解促进作用较显著,加有Br-,Cl-的体系中亚甲基蓝中光催化降解率是96.9%,是对照组的1.15倍,其次是I-,加有I-的体系中亚甲基蓝光催化降解率是对照组的1.12倍,而NO2-对亚甲基蓝光催化降解影响不明显。
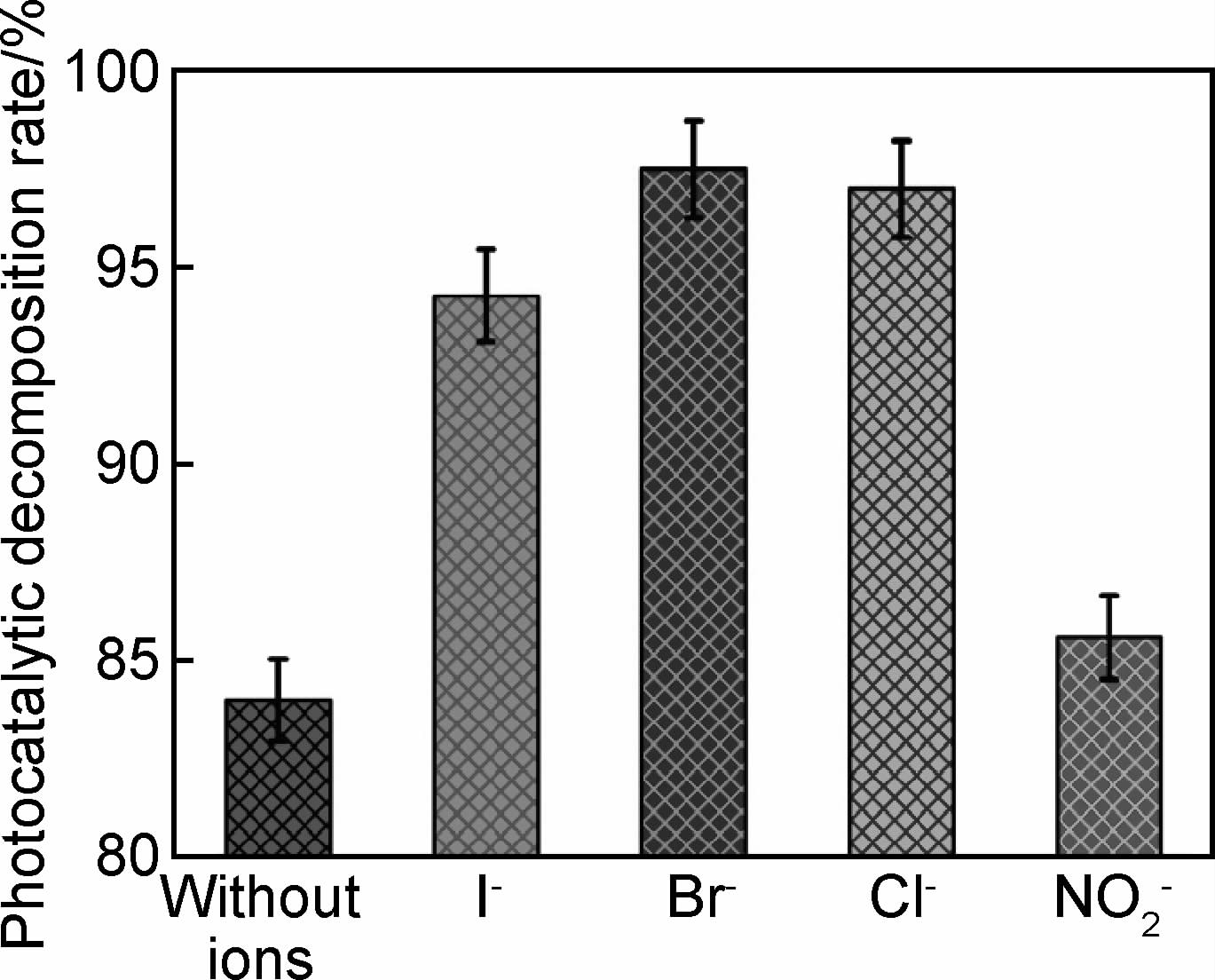 | 图11 阴离子对亚甲基蓝光催化降解的影响 Fig.11 The effect of anion on the photocatalytic degradation of methyl-blue | |
催化剂的稳定性对催化剂的实际应用具有重要意义。考察了三维介孔结构Bi2WO6催化剂其稳定性,结果见图 12和图 13。由图 12可以看出,重复使用5次,催化剂的对次甲基蓝的降解活性没有明显下降。图 13是重复使用5次后Bi2WO6的XRD图谱与新制Bi2WO6的XRD图谱的对比,可以看出,使用5次催化剂的物相组成没有明显变化,进一步表明三维介孔结构Bi2WO6催化剂性能稳定。
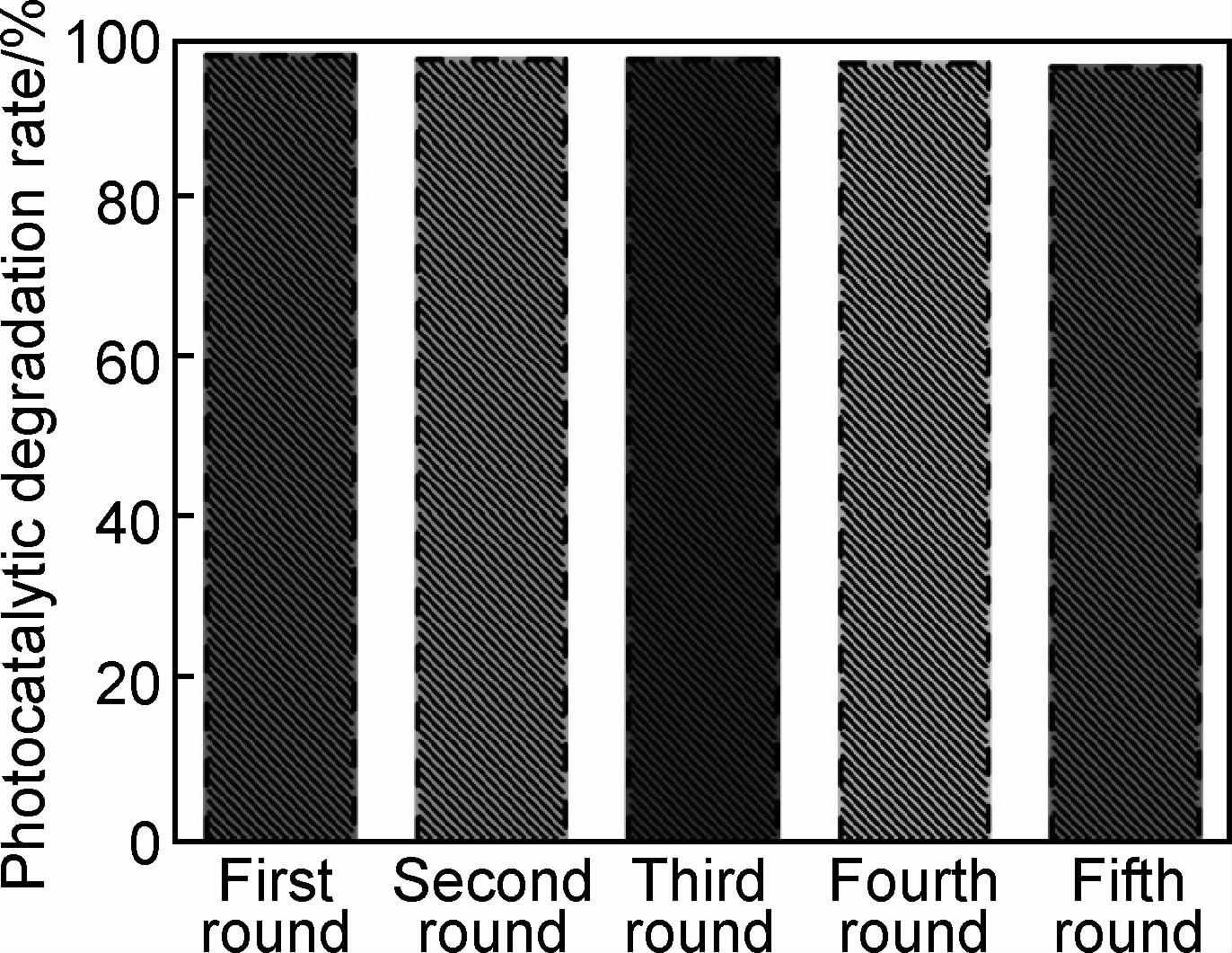 | 图12 Bi2WO6催化剂的稳定性和重复使用性能 Fig.12 The stability and repeated use of Bi2WO6 photocatalyst (initial concentration methyl-blue, 20mg·L-1; pH=-1) | |
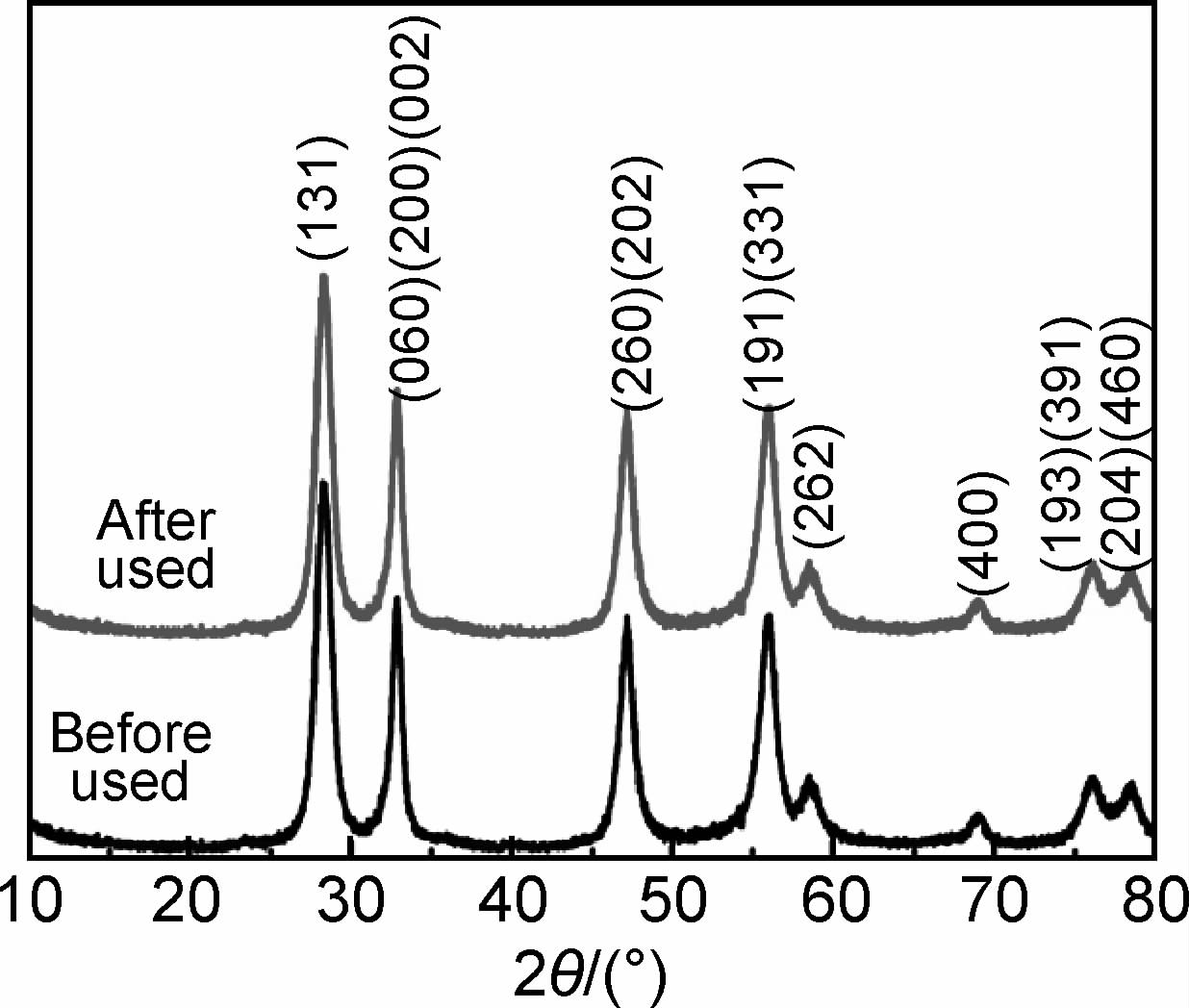 | 图13 Bi2WO6催化剂使用前后的物相组成对比 Fig.13 Comparison of phase composition of Bi2WO6 photocatalyst before and after used | |
无机离子对于偶氮染料光催化降解的影响比较复杂,一方面,无机离子与染料可能存在竞争性吸附,另一方面无机离子和染料可能存在化学反应;再者,无机离子还可能俘获光催化反应的活性物种,同时又与催化剂、染料以及无机离子的种类和浓度有关,不同体系中研究者得出了不同的结论[31, 32, 33, 34]。结合文献报道和光催化实验结果,推测可能的机理如下:首先,实验所制备的Bi2WO6是由大量具有极性面的纳米片组装而成,其带负电荷的Bi2WO6-(WO4)2n-n面易于吸附NH4+和Fe3+等阳离子,相反带正电荷的Bi2WO6 -(Bi2O2)2n+n面则易于吸附卤素离子等阴离子;其次,在光照条件下,Bi2WO6的导带电子可转移给吸附的NH4+和Fe3+等阳离子,其可作为电子受体接收激发至导带的电子,从而能抑制光生电子-空穴对的复合过程,有利于提高催化剂的活性,这与缺电子元素掺杂Bi2WO6活性提高的机制类似[20]。Fe2+与活性物种羟自由基反应,从而抑制了羟自由基氧化分解亚甲基蓝[31]。关于Cu2+对于偶氮染料光催化降解的影响,文献报道[32],Cu2+对偶氮染料维多利亚紫的降解没有影响,而对酸性铬深蓝和酸性铬蓝K的降解有抑制作用,主要是由于Cu2+和“-N=N-”发生相互作用而生成了更稳定的化合物,结合本论文实验结果,可以认为Cu2+对染料降解的影响与染料分子种类直接相关。
亚甲基蓝(MB)的光催化降解实验表明[19],O2·-和光生空穴(h+VB)是MB光催化分解的主要的活性物种。在光催化反应过程中,O2·-的产生可能通过两种途径,一方面染料可能吸收可见光被激发至激发态(MB*),激发态的染料分子将电子注入Bi2WO6的导带,注入导带的电子被吸附于Bi2WO6表面的O2捕获产生O2·-,即活性O2·-由染料敏化作用产生,然而,MB的还原电位(0.532 eV)比O2·-(-0.28eV)正,因此,激发态(MB*)不可能将电子转移至Bi2WO6的导带。 另一方面,光照下Bi2WO6的价带电子激发至导带,导带电子直接被O2捕获产生O2·-。活性物质继而去氧化分解MB,光催化反应过程如下所示[19]:
Bi2WO6 +hγ→Bi2WO6 (eCB-+ hVB+)
Bi2WO6 (eCB-)+ O2→Bi2WO6+ O2·-
MB + hVB+[Bi2WO6]→中间产物
O2·- + MB→中间产物
体系中同时发生的反应:
O2·- + MB→中间产物
中间产物+ h+VB[Bi2WO6] 或 O2·- →
CO2+H2O+…
在MB的光催化降解过程中,反应体系中的卤素离子作为电子给体吸附在Bi2WO6-(Bi2O2)2n+n面上,吸附态的卤素X-(Br-,Cl-,I- ),可能将电子转移至的Bi2WO6导带,从而促进O2·-活性自由基的产生(反应(2)),有利于MB的光催化降解。而NO2-对有机物的光催化降解影响比较复杂[34],一方面,NO2-本身是一种含氮污染物,可以与光催化反应活性物种羟自由基反应而降解,另一方面,其在降解过程中又可以产生羟自由基。然而,Bi2WO6作为光催化剂时,主要活性物种是O2·-而非·OH自由基[19],故在本实验中NO2-对MB降解的影响不显著。
3 结论(1)水热法所得Bi2WO6属于正交晶系Bi2WO6,呈三维球状结构,粒径在3μm左右,是由纳米片定向组装而成的;氮气吸附-脱附结果表明,所得Bi2WO6具有介孔结构,比表面积为47.72m2·g-1。
(2)光催化降解体系的pH对Bi2WO6光催化降解亚MB影响显著,相比之下,在强酸性条件下降解率较高;NH4+,Cu2+,Fe3+对Bi2WO6光催化降解亚甲基蓝有促进作用,其中Fe3+影响最大,其次是NH4+,影响最小的是Cu2+,Fe2+对Bi2WO6光催化降解MB有抑制作用;卤素离子(Br -,Cl-,I-)对MB光催化降解有较为明显的促进作用,而NO2-对MB光催化降解几乎无影响。
(3)无机离子对MB光催化降解的影响机理比较复杂,与Bi2WO6结构和离子的种类有关,带负电荷的(WO4)2n-n面易于吸附NH4+和Fe3+等阳离子,而带正电荷的(Bi2O2)2n+n面则易于吸附卤素离子(X-),而吸附于催化剂表面的无机离子分别作为电子受体、电子给体或自由基捕获剂对MB的光催化降解产生影响。
| [1] | 吴祖望, 杨威. 21世纪20年代我国的染料工业与染料学科展望[J].染料与染色, 2007,44(1):1-4. WU Zu-wang, YANG Wei. A prospect for dyestuff industry and dyestuff science in China in 2020'[J].Dyestuff and Coloration, 2007,44(1):1-4. |
| [2] | 赵荣祥, 李秀萍, 徐铸德. 离子液体辅助水热合成数值状硫化镉及光催化性能[J]. 材料工程, 2014,(2):7-12. ZHAO Rong-xiang, LI Xiu-ping, XU Zhu-de. Synthesis and photocatalytic performance of dendritic CdS nanostructures by and ionic liquid-assisted hydrothermal route[J]. Journal of Materials Engineering, 2014,(2):7-12. |
| [3] | 杨丽丽, 都玲, 于杨, 等. 磷酸处理HZSM-5负载TiO2光催化降解活性艳红X-3B[J]. 材料工程, 2014,(9):94-99. YANG Li-li, DU Ling, YU Yang, et al. Photocatalytic degradation of reactive Brilliant red X-3B on TiO2supported on HZSM-5 with phosphoric acid[J]. Journal of Materials Engineering, 2014,(9):94-99. |
| [4] | NAGIRNYI V, KIRM M, KOTLOV A, et al. Separation of excitonic and electron-hole process in metal tungstates[J]. Journal of Luminescence, 2003, 102(3):597-603. |
| [5] | KATO H, MATSUDO N, KUDO A. Photophysical and photocatalytic properties of molybdates and tungstates with a scheelite structure[J]. Chemistry Letters, 2004, 33(9):1216-1217. |
| [6] | ZHAO X, YAO W Q, ZHU Y F, et al. Fabrication and photoelectrochemical properties of porous ZnWO4 film[J]. Journal of Solid State Chemistry, 2006, 179(11):2562-2570. |
| [7] | WU Y, ZHANG S C, ZHU Y F, et al. Photocatalytic activity of nanosized ZnWO4 prepared by the sol-gel method[J].Chemical Research in Chinese Universities, 2007, 23(4):465-468. |
| [8] | TANG J W, ZOU Z G, YE J H. Photocatalytic decomposition of organic contaminants by Bi2WO6 under visible light irradiation[J].Catalysis Letters, 2004, 92(2):53-56. |
| [9] | XU C X, WEI X, GUO Y M, et al. Surfactant-free synthesis of Bi2WO6 multilayered disks with visible-light-induced photocatalytic activity[J]. Materials Research Bulletin, 2009, 44(8):1635-1641. |
| [10] | TIAN Y, HUA G M, XU W, et al. Bismuth tungstate nano/microstructures:controllable morphologies, growth mechanism and photocatalytic properties[J]. Journal of Alloys Compounds, 2011, 509(3):724-730. |
| [11] | ZHANG G K, LU F, LI M, et al. Synthesis of nanometer Bi2WO6 synthesized by sol-gel method and its visible-light photocatalytic acitvity for degradation of 4BS[J]. Journal of Physical and Chemical of Solids, 2010, 71(4):579-582. |
| [12] | ALFARO O, MARTINEZ-DE C A. Synthesis, characterization and visible-light photocatalytic properties of Bi2WO6 and Bi2W2O9 obtained by Co-precipitation method[J]. Applied Catalysis A:General, 2010, 383(1):128-133. |
| [13] | HUANG Y, AI Z H, HO W K, et al. Ultrasonic spray pyrolysis synthesis of porous Bi2WO6 microspheres and their visible-light-induced photocatalytic removal of NO[J]. The Journal of Physical Chemistry C, 2010, 114(14):6342-6349. |
| [14] | ZHANG C, ZHU Y F. Synthesis of square Bi2WO6 nanoplates as high activity visible-light-driven photocatalysts[J].Chemistry of Materials, 2005, 17(13):3537-3545. |
| [15] | SHANG M, WANG W Z, SUN S M, et al. Bi2WO6 nanocrystals with high photocatlaytic activities under visible light[J]. The Journal of Physical Chemistry C, 2008, 112(28):10407-10411. |
| [16] | ZHANG L S, WANG W Z, ZHOU L, et al. Bi2WO6 nano-and microstructures:shape control and associated visible-light driven photocatalytic activities[J]. Small, 2007, 3(9):1618-1625. |
| [17] | WANG D J, ZHEN Y Z, XUE G L, et al. Synthesis of mesoporous Bi2WO6 architectures and their gas sensitivity to ethanol[J]. Journal of Materials Chemistry C, 2013, 1(26):4153-4162. |
| [18] | WANG D J, XUE G L, ZHEN Y Z, et al. Monodispersed Ag nanoparticles loaded on the surface of spherical Bi2WO6 nanoarchitectures with enhanced photocatalytic activities[J]. Journal of Materials Chemistry, 2012, 22(11):4751-4758. |
| [19] | WANG D J, GUO L, ZHEN Y Z, et al. AgBr quantum dots decorated mesoporous Bi2WO6 architectures with enhanced photocatalytic activities for methylene blue[J]. Journal of Materials Chemistry A, 2014, 2(30):11716-11727. |
| [20] | WANG D J, YUE L L, GUO L, et al. Synthesis and enhanced photocatalytic mechanism of Fe3+ doped three-dimensional Bi2WO6hierarchical nanoarchitectures[J]. Chinese Journal of Inorganic Chemistry, 2014, 30(4):961-968. |
| [21] | ZHANG L S, WANG W Z, CHEN Z G, et al. Fabrication of flower-like Bi2WO6 superstructures as high performance visible-light driven photocatalysts[J]. Journal of Materials Chemistry, 2007,17(24):2526-2532. |
| [22] | MA D K, HUANG S M, CHEN W X, et al. Self-assembled three-dimensional hierarchical umbilicate Bi2WO6 microspheres from nanoplates:controlled synthesis, photocatalytic activities, and wettability[J]. The Journal of Physical Chemistry C, 2009, 113(11):4369-4374. |
| [23] | LI Y Y, LIU J P, HUANG X T, et al. Hydrothermal synthesis of Bi2WO6 uniform hierarchical microspheres[J].Crystal Growth & Design, 2007, 7(7):1350-1355. |
| [24] | WANG C Y, ZHANG H, LI F, et al. Degradation and mineralization of Bisphenol A by mesoporous Bi2WO6 under simulated solar light irradiation[J]. Environmental Science and Technology, 2010, 44(17):6843-6848. |
| [25] | SING K S W, EVERETT D H, HAUL R A W, et al. Reporting physisorption data for gas/solid system with special reference to the determination of surface area and porosity[J]. Pure and Applied Chemistry, 1985, 57(4):603-619. |
| [26] | HONG S S, LEE M S, PARK S S, et al. Synthesis of nanosized TiO2/SiO2 particles in the microemulsion and their photocatalytic activity on the decomposition of p-nitrophenol[J]. Catalysis Today, 2003, 87(1-4):99-105. |
| [27] | TRIFIRO F, HOSER H, SCARLE R D. Relationship between structure and activity of mixed oxides as oxidation catalysts[J]. Journal of Catalysis, 1972, 25(1):12-24. |
| [28] | CARRAZAN S R G, MARTIN C, RIVES V, et al. An FT-IR spectroscopy study of the adsorption and oxidation of propene on multiphase Bi, Mo and Co catalysts[J]. Spectrochimica Acta Part A:Molecular and Biomelcular Spectroscopy, 1996, 52(9):1107-1118. |
| [29] | 王丹军, 李东升, 郭莉, 等. 球形α-Fe2O3纳米粉体的超声水解法合成与表征[J].无机化学学报, 2006, 22(7):1317-1319. WANG Dan-jun, LI Dong-sheng, GUO Li, et al. Synthesis and characterization of spherical hematite(α-Fe2O3) nanopowder by sonochemical hydrolysis method[J].Chinese Journal of Inorganic Chemistry, 2006, 22(7):1317-1319. |
| [30] | REN J, WANG W Z, SUN S M, et al. Enhance photocatalytic activity of Bi2WO6 loaded with Ag nanoparticles under visible light irradiation[J]. Applied Catalysis B:Environmental, 2009, 92(1-2):50-55. |
| [31] | 吕学军, 许宜铭,王智,等. Fe(Ш)参与TiO2光催化降解X3B的反应机理研究[J].化学学报, 2004, 62(16):1455-1459. LU Xue-jun, XU Yi-ming, WANG Zhi, et al. Reaction mechanism of Fe(Ⅲ) participated photocatalytic degradation of X3B over TiO2[J]. Acta Chmica Sinca, 2004, 62(16):1455-1459. |
| [32] | 刘祥虎. 金属离子与染料分子相互作用对染料分子催化降解的影响[D].上海:同济大学, 2008. LIU Xiang-hu. Metal ions interact with dye molecules and its effect on the catalytic degradation of dye molecules[D]. Shanghai:Tongji University, 2008. |
| [33] | 白图雅. 无机阴离子对光催化降解有机染料的影响研究[D].呼和浩特:内蒙古大学, 2007. BAI Tu-ya. Investigation of the influence of inorganic anion on photocatalytic degradation of organic dye[D]. Hohhot:Inner Mongolia University, 2007. |
| [34] | 王新颖. 亚硝酸根对水中4-氯酚光降解的影响[D]. 大连:大连理工大学, 2011. WANG Xin-ying. Effect of on photo-degradation of 4-chlorophenol[D]. Dalian:Dalian University of Technology, 2011. |
 2016, Vol. 44
2016, Vol. 44


