2. 北京化工大学 膜分离过程与技术北京市重点实验室, 北京 100029
2. Beijing Key Laboratory of Membrane Science and Technology, Beijing University of Chemical Technology, Beijing 100029, China
环氧环己烷是合成农药克螨特的主要原料,近年来随着我国农药市场的发展,环氧环己烷的市场需求量呈增长趋势[1]。然而传统的环氧环己烷生产方法存在反应时间长、成本高、环保达标难度大等缺点[2]。
以环己烯为原料生产环氧环己烷是近几年出现的一种新方法。该方法根据氧源的不同分为有机过氧化物环氧化法、次氯酸法、电化学法、分子氧氧化法和双氧水氧化法。其中,有机过氧化物环氧化法因过氧化物存在不稳定、容易分解、不易储存、污染严重等缺点限制了其工业化应用[3];次氯酸法对设备腐蚀严重、环境污染较大[4];电化学法符合当今的环保需求,但成本较高,且对电流密度要求较为严格[5];分子氧氧化法副反应较多,产物分离成本高。章彬等[6]用负载型Co3O4/SiO2催化分子氧氧化环己烯制环氧环己烷,然而反应时间长,生成副产物多。双氧水氧化法是一种不会对环境造成污染的绿色环保新技术,对其进行深入研究并实现工业化具有重要意义[7]。针对环己烯氧化制环氧环己烷为连串反应的特点,韩瑞峥[8]在微分反应器中进行了催化氧化环己烯合成环氧环己烷的研究。袁年武等[9]采用分走水相再反应的方法提高了环己烯催化氧化生成环氧环己烷的选择性。李坤兰等[10]、王振兴[11]、刘颖等[12]围绕如何提高催化剂的选择性进行了研究,其中王振兴[11]制备了聚苯乙烯接枝季铵盐磷钨杂多酸催化剂催化H2O2氧化环己烯,但存在反应时间长的不足;刘颖等[12]制备了杂多酸盐相转移催化剂,设计了以H2O2为氧化剂催化环己烯合成环氧环己烷的绿色催化反应体系。但有关用平推流反应器控制反应时间,抑制副产物的生成,并提高收率的文章鲜见报道。本文以环己烯为原料,双氧水为氧源,自制十六烷基吡啶过氧磷钨酸为催化剂,首先在釜式反应器内制备环氧环己烷,确定了管式反应器管长,在此基础上使用管式平推流反应器探讨反应温度、环己烯与H2O2物质的量比、反应溶液的pH、催化剂用量等因素对环氧环己烷收率的影响。
1 实验部分 1.1 实验原料和仪器环己烯,分析纯,唐山中浩化工有限公司;30%双氧水,分析纯,石家庄柏坡正元化肥有限公司;钨酸、磷酸、氯仿、磷酸二氢钾,均为分析纯,天津市永大化学试剂有限公司;乙酸乙酯、氯代十六烷基吡啶,分析纯,石家庄试剂厂。
FA1004电子天平,上海精科仪器有限公司;SHZ-Ⅲ循环水真空泵,上海亚荣生化仪器厂;XMTD电热鼓风干燥箱,余姚长江温度仪表厂;GC789 Ⅱ型气相色谱仪,上海良平仪器仪表有限公司。微型混合器、釜式反应器和管式反应器,均为自制。
1.2 催化剂的制备文献[12]采用乙醇和二氯甲烷作为溶剂,制得的催化剂在体系中高度分散,需通过抽滤、洗涤得到最终产物,收率较低。本文使用乙酸乙酯作为溶剂,所得催化剂可团成小球从油水两相析出,收率可达82%,且乙酸乙酯可回收利用。
将2.89 g钨酸置于100 mL烧杯中,再加入10 g双氧水,待钨酸全部溶解后,加入磷酸0.3 g,再加入10 mL蒸馏水,于室温下搅拌20 min,加热至60 ℃,搅拌5 min,得到无色透明溶液。将3 g氯代十六烷基吡啶与70 mL乙酸乙酯混合后滴加至上述溶液,2 min内滴完,随即出现少量淡黄色沉淀。继续搅拌约40 min,淡黄色催化剂在油水两相界面发生聚合并析出,经抽滤、洗涤、烘干后得到固体催化剂。
1.3 环氧环己烷的合成釜式反应器装置:称量一定量的催化剂于三口烧瓶中,加入一定量双氧水、磷酸二氢钾和环己烯,升温至设定温度,反应一定时间后取上层产物进行分析,并计算环氧环己烷的收率。
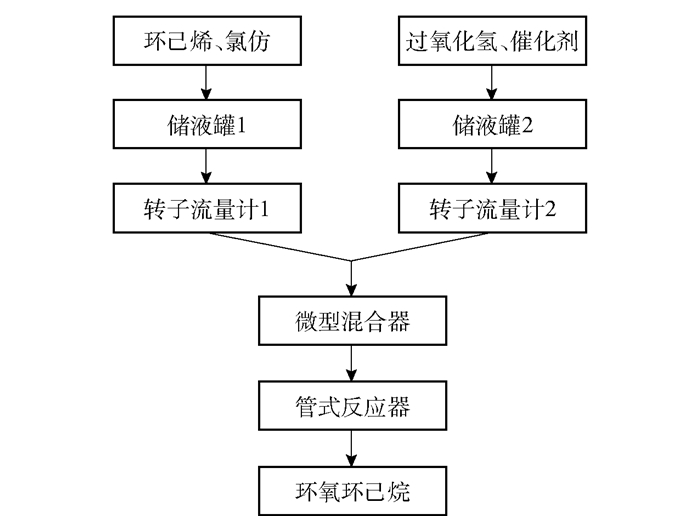
管式反应器装置由储液罐、转子流量计、微型混合器、恒温水浴锅、管式反应器组成,合成实验流程图如图 1所示。将一定量的催化剂溶于过氧化氢,再将该溶液和环己烯、氯仿分别加入储罐中。水浴锅升温至设定温度,调节转子流量计使过氧化氢和环己烯以设定的物质的量比进入管式反应器反应。收集产物进行分析并计算环氧环己烷的收率。
|
图 1 双氧水氧化法制环氧环己烷实验流程简图 Fig.1 Brief introduction of the experimental process for the preparation of epoxycyclohexane by hydrogen peroxide oxidation |
以环己烷为内标物,利用气相色谱仪采用内标法对原料和产物进行定量分析。
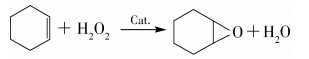
H2O2氧化环己烯合成环氧环己烷反应如下。
|
(1) |
式(1)表明,反应掉1 mol H2O2就应消耗掉1 mol环己烯,理论上就有1 mol目的产物环氧环己烷生成。本文所用未转化环己烯物料不易回收,故以H2O2为关键组分,并以此进行环氧环己烷收率的定义及计算。
| $ Y=\frac{n_{1}}{n_{2}} \times 100 \% $ | (2) |
式中,Y为环氧环己烷的收率;n1为生成环氧环己烷的物质的量;n2为初始加入的过氧化氢的物质的量。
2 结果与讨论 2.1 釜式反应器下最佳反应时间的确定在实验过程中,要合理控制反应时间,以有效降低反应物水解和副产物的生成,提高产品的收率。设置实验条件为:反应温度60 ℃(温度太高,过氧化氢易分解,温度低时,反应速率小),投料物质的量比n(环己烯):n(H2O2):n(催化剂):n(氯仿)=1:1:0.000 25:2,十六烷基吡啶过氧磷钨酸0.5 g,磷酸二氢钾0.5 g。在此条件下考察反应时间对环氧环己烷收率的影响。分别在15、30、45、60、75 min取样,通过气相色谱对产品进行成分分析,并计算环氧环己烷收率。结果如图 2所示。
|
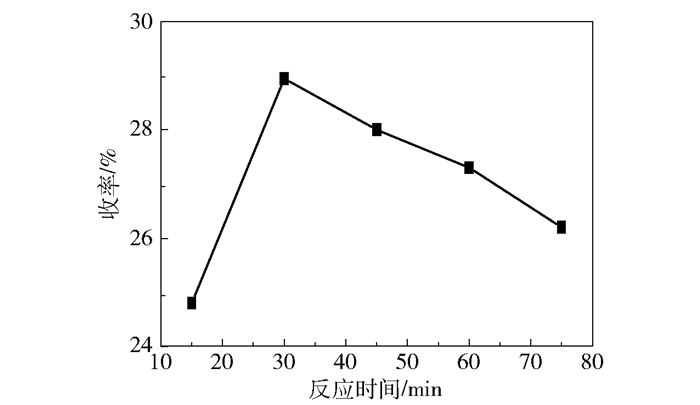
图 2 反应时间对环氧环己烷收率的影响 Fig.2 Effect of varying reaction time on the yield of epoxycyclohexane |
由图 2可知,当反应时间为30 min时,环氧环己烷收率为28.95%。反应时间小于30 min,环氧环己烷收率随着反应时间的增加而增大,继续增加反应时间,环氧环己烷收率略微降低。出现这种现象的可能原因是:反应初期反应物浓度大、催化剂活性高,环氧环己烷收率随反应时间的增加而增大;当反应物的停留时间增加时,反应生成的环氧环己烷会发生水解,生成1, 2-环己二醇副产物,继续延长反应时间,生成的环氧环己烷有可能氧化为环己烯醇等副产物。因此可以判定在30 min后继续增加反应时间,反应的水解速率将会大于生成速率,所以最佳的反应时间为30 min。
2.2 管式反应器下的实验条件优化在釜式反应器得到的最佳反应时间基础上确定管式反应器的管长,再进一步通过单因素实验探究管式反应器下反应温度、环己烯与H2O2物质的量比、反应溶液的pH和催化剂用量等因素对环氧环己烷收率的影响。
2.2.1 管长的确定本文实验选用直径为3 mm的不锈钢管作为管式反应器。依据反应时间为30 min的优化条件,利用转子流量计控制过氧化氢和环己烯的流量分别为3 mL/min和4 mL/min,则在管式反应器中过氧化氢和环己烯所形成的混合液的流量为7 mL/min。反应所需混合液最少为210 mL,管式反应器的横截面积为7.065×10-2 cm2,因此所需管式反应器的管长为30 m。
2.2.2 反应温度在n(环己烯):n(H2O2):n(催化剂):n(氯仿)=1:1:0.000 25:2、反应时间30 min、十六烷基吡啶过氧磷钨酸0.5 g、磷酸二氢钾0.5 g的实验条件下,反应温度分别控制在30、40、50、60、70 ℃,然后在相应的温度下取样并用气相色谱进行成分分析,计算环氧环己烷的收率,结果如图 3所示。
|
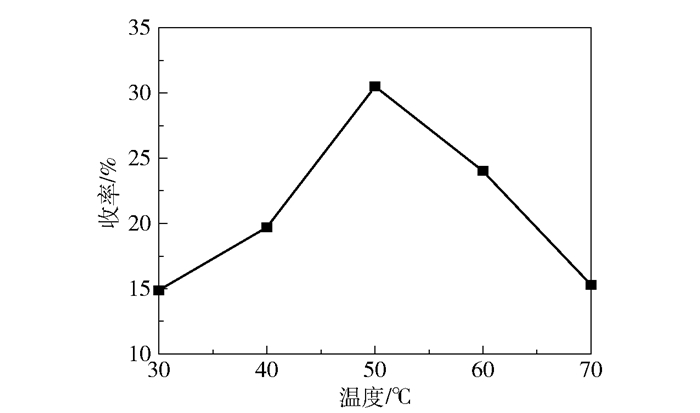
图 3 反应温度对环氧环己烷收率的影响 Fig.3 Effect of varying reaction temperature on the yield of epoxycyclohexane |
由图 3可知,反应温度为50 ℃时环氧环己烷收率最高可达30.5%。当反应温度低于50 ℃时,其收率随着温度的升高而升高,然而当反应温度高于50 ℃时,收率则随着反应温度的升高而降低。催化剂十六烷基吡啶过氧磷钨杂多酸为中强酸,在酸性条件下,温度升高有利于环氧环己烷水解生成副产物1, 2-环己二醇。当反应温度低于50 ℃时,环氧环己烷的生成速率大于水解速率;反应温度高于50 ℃时,环氧环己烷的水解速率大于生成速率。因此,50 ℃时的环氧环己烷收率最高。考虑反应能耗情况和综合因素确定实验最佳的反应温度为50 ℃。
2.2.3 环己烯与H2O2物质的量比固定反应温度50 ℃和反应时间30 min,n(环己烯):n(催化剂):n(氯仿)=1:0.000 25:2,十六烷基吡啶过氧磷钨酸0.5 g,磷酸二氢钾0.5 g,改变H2O2的用量,控制n(H2O2)/n(环己烯)值分别为0.5、0.75、1.0、1.5、2.0,反应结束后取样分析环氧环己烷的收率,结果如图 4所示。
|
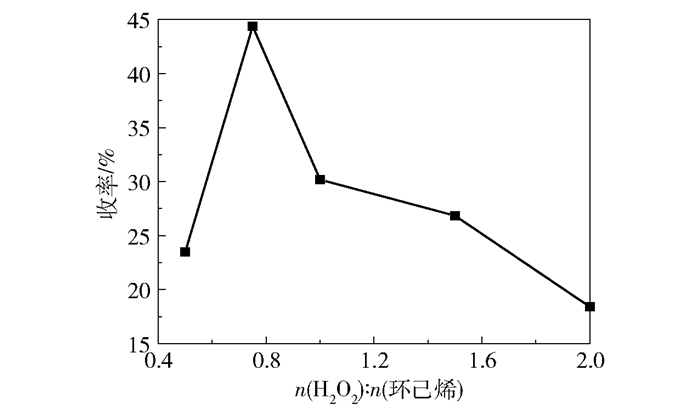
图 4 原料配比对环氧环己烷收率的影响 Fig.4 Effect of varying raw material ratio on the yield of epoxycyclohexane |
由图 4可知,当投料比n(H2O2):n(环己烯)=0.75时,环氧环己烷的收率最高,之后随着投料比的继续增加,环氧环己烷的收率降低。当投料比小于0.75时,过氧化氢浓度偏低,导致环己烯不能完全反应;当投料比大于0.75时,过氧化氢浓度增加,导致反应体系内的酸性增强,使得环氧环己烷的水解速率加大,环氧环己烷的收率降低。
2.2.4 反应体系pH值环氧环己烷在酸性条件下极易水解,体系的酸性强弱对产品收率至关重要。在反应时间30 min,反应温度50 ℃,十六烷基吡啶过氧磷钨酸0.5 g,n(环己烯):n(H2O2):n(催化剂):n(氯仿)= 1:0.75:0.000 25:2条件下,改变磷酸二氢钾用量以考察pH值对环氧环己烷收率的影响,结果如图 5所示。
|
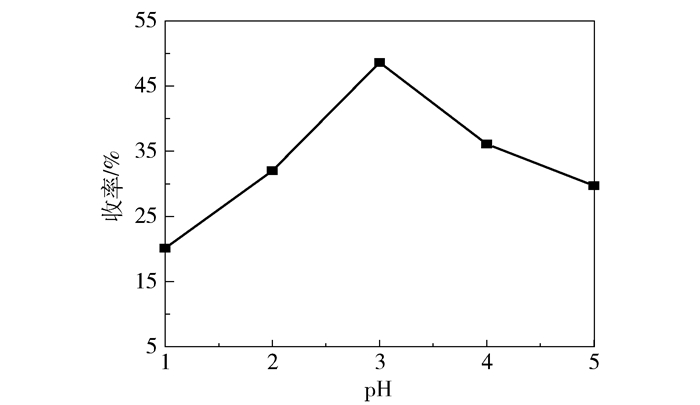
图 5 pH值对环氧环己烷收率的影响 Fig.5 Effect of varying pH on the yield of epoxycyclohexane |
由图 5可知,随着反应体系酸性减弱,环氧环己烷的收率增大,当反应体系pH值为3时,环氧环己烷收率最高为48.61%,反应体系的酸性继续减弱,环氧环己烷的收率逐渐降低。环氧环己烷在强酸反应体系中极易水解成1, 2-环己二醇,所以当pH值较小时,环氧环己烷收率较低。反应体系的酸性减弱,环己烯的反应速率变小,导致环氧环己烷收率变低。因此需要调节合适的pH值,最大化环氧环己烷的收率。实验中采用的催化剂与过氧化氢均显酸性,所以加入助催化剂磷酸二氢钾调节体系的pH值。
2.2.5 催化剂用量在反应温度50 ℃,反应时间30 min,pH=3,n(环己烯):n(H2O2):n(氯仿)=1:0.75:2的条件下,改变催化剂的用量考察其对环氧环己烷收率的影响,结果如图 6所示。
|
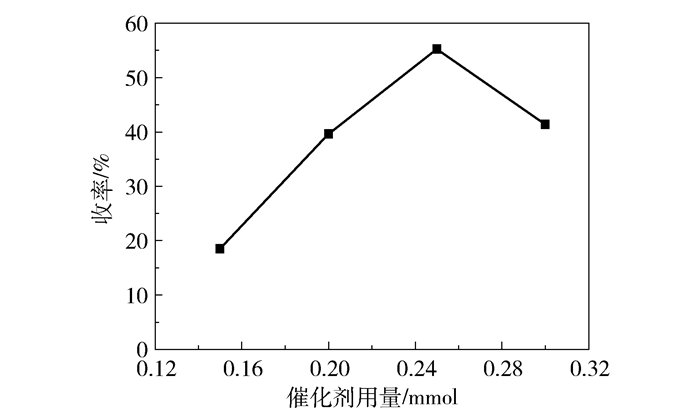
图 6 催化剂用量对环氧环己烷收率的影响 Fig.6 Effect of varying catalyst amount on the yield of epoxycyclohexane |
由图 6可得出,当催化剂用量很少时,环氧环己烷的收率很低几乎为零。随着催化剂用量的增加,环氧环己烷的收率升高,当催化剂用量为0.25 mmol时,环氧环己烷的收率最高达55.24%。继续增加催化剂用量,环氧环己烷的收率呈现出降低的趋势。其原因是催化剂用量增加到一定程度会使催化剂粘连并团聚,导致具有催化活性的表面减少,环己烯不能充分反应,从而使环氧环己烷的收率降低。除此之外,催化剂用量增加,反应体系的酸性增强,环氧环己烷的水解速率增大,使得反应生成的环氧环己烷进一步水解为1,2-环己二醇,也会导致环氧环己烷的收率降低。同时,随着催化剂用量的增加,可能会导致副反应速率增加,从而使得环氧环己烷收率进一步降低。
2.3 最优反应条件通过单因素实验得到了环己烯氧化制环氧环己烷在管式反应器中的最佳反应条件,即反应温度50 ℃,反应时间30 min,n(环己烯):n(H2O2):n(催化剂):n(氯仿)=1:0.75:0.000 25:2,pH=3,经过对产物的检测分析可得该条件下环氧环己烷的收率为55.24%。同样的反应条件下,釜式反应器中环氧环己烷的收率为44.42%。显而易见,在管式反应器中环氧化的效果更好,其原因可能为管式反应器的使用有效地控制并缩短了反应时间,抑制了副产物的生成;同时,环己烯和双氧水分子得到了微观混合,接触面积更大,反应更加充分。
3 结论(1) 选用直径为3 mm的不锈钢管作为管式反应器,根据釜式反应器反应的最佳时间确定了管式反应器的管长为30 m。
(2) 通过在管式反应器内进行单因素实验,得到了合成环氧环己烷的最佳反应条件:按n(环己烯):n(H2O2):n(催化剂):n(氯仿)=1:0.75:0.000 25:2的比例进料,在反应温度50 ℃、pH=3条件下反应30 min,环氧环己烷的收率最高达55.24%。
| [1] |
郭加振, 孟保勋. 环氧环己烷的市场应用分析及生产技术简介[J]. 中国化工贸易, 2012(5): 300-301. GUO J Z, MENG B X. Market application analysis and production technology introduction of epoxycyclohexane[J]. China Chemical Trade, 2012(5): 300-301. (in Chinese) |
| [2] |
盛卫坚, 贾建洪, 韩非, 等. 环氧环己烷的合成新工艺研究[J]. 浙江工业大学学报, 2006, 34(4): 386-388. SHENG W J, JIA J H, HAN F, et al. Novel environment benign process for preparation of cyclohexylene oxide[J]. Journal of Zhejiang University of Technology, 2006, 34(4): 386-388. (in Chinese) |
| [3] |
哈丽丹·买买提, 吾满江·艾力. 过乙酸氧化法制备环氧环己烷的工艺研究[J]. 化学试剂, 2007, 29(5): 315-317. H L D · MAI MAI TI, W M J·AI LI. Study on the preparation of epoxy cyclohexane by peracetic acid oxidation[J]. Chemical Reagent, 2007, 29(5): 315-317. (in Chinese) |
| [4] |
张进, 崔尚平, 韩珺, 等. 1, 2-环氧环己烷的制备与应用进展[J]. 化学推进剂与高分子材料, 2014, 12(6): 50-57. ZHANG J, CUI S P, HAN J, et al. Progress in preparation and application of 1, 2-cyclohexene oxide[J]. Chemical Propellants & Polymeric Materials, 2014, 12(6): 50-57. (in Chinese) |
| [5] |
徐敏强.环氧环己烷的电化学合成研究[D].郑州: 郑州大学, 2003. XU M Q. Studies on the synthesis of epoxycyclohexane using electrochemical method[D]. Zhengzhou: Zhengzhou University, 2003. (in Chinese) |
| [6] |
章彬, 刘欢, 张学龙, 等. SiO2负载钴系催化剂的环己烯环氧化性能[J]. 化工进展, 2019, 38(10): 4582-4587. ZHANG B, LIU H, ZHANG X L, et al. Epoxidation of cyclohexene over SiO2 supported cobalt catalyst[J]. Chemical Industry and Engineering Progress, 2019, 38(10): 4582-4587. (in Chinese) |
| [7] |
WELCH A, SHIJU N R, WATTS I D, et al. Epoxidation of cyclohexene over crystalline and amorphous titanosilicate catalysts[J]. Catalysis Letters, 2005, 105(3/4): 179-182. |
| [8] |
韩瑞峥.环氧环己烷合成新工艺的研究[D].郑州: 郑州大学, 2012. HAN R Z. A new technical research on synthesis of cyclohexane oxide[D]. Zhengzhou: Zhengzhou University, 2012. (in Chinese) |
| [9] |
袁年武, 何嘉勇, 屈铠甲, 等.一种制备环氧环己烷的方法: CN101343261A[P]. 2009-01-14. YUAN N W, HE J Y, QU K J, et al. Method for preparing epoxy cyclohexane: CN101343261A[P]. 2009-01-14. (in Chinese) |
| [10] |
李坤兰, 周宁, 奚祖威. 溶剂和杂多酸盐中季铵盐阳离子对环己烯环氧化反应控制相转移催化的影响[J]. 催化学报, 2002, 23(2): 125-126. LI K L, ZHOU N, XI Z W. Effects of solvents and quaternary ammonium ions in heteropolyoxotungstates on reaction-controlled phase-transfer catalysis for cyclohexene epoxidation[J]. Chinese Journal of Catalysis, 2002, 23(2): 125-126. (in Chinese) |
| [11] |
王振兴.双氧水环氧化环己烯合成环氧环己烷的关键技术研究[D].郑州: 郑州大学, 2006. WANG Z X. Key techniques on synthesis of cyclohexene oxide with hydrogen peroxide as oxidant[D]. Zhengzhou: Zhengzhou University, 2006. (in Chinese) |
| [12] |
刘颖, 刘甲, 杨国强, 等. 相转移催化H2O2氧化环己烯合成环氧环己烷的工艺研究[J]. 南京大学学报(自然科学版), 2019, 55(5): 850-858. LIU Y, LIU J, YANG G Q, et al. Study on phase transfer catalytic synthesis of epoxycyclohexane by H2O2 oxidation of cyclohexene[J]. Journal of Nanjing University(Natural Science), 2019, 55(5): 850-858. (in Chinese) |








