文章信息
- 褚衍茹, 陈奕, 雷松, 张言武, 易波, 马建明, 闫克栋, 王赟, 李保军, 吕梦倩, 许国章, 张栋梁.
- Chu Yanru, Chen Yi, Lei Song, Zhang Yanwu, Yi Bo, Ma Jianming, Yan Kedong, Wang Yun, Li Baojun, Lyu Mengqian, Xu Guozhang, Zhang Dongliang
- 宁波市新型冠状病毒再感染的流行病学特征及其影响因素
- Epidemiological characteristics of reinfection of 2019-nCoV and influencing factors in Ningbo
- 中华流行病学杂志, 2023, 44(9): 1402-1407
- Chinese Journal of Epidemiology, 2023, 44(9): 1402-1407
- http://dx.doi.org/10.3760/cma.j.cn112338-20230301-00114
-
文章历史
收稿日期: 2023-03-01
2. 宁波市卫生健康委员会, 宁波 315010;
3. 宁波市慈溪市疾病预防控制中心, 宁波 315300;
4. 宁波市镇海区疾病预防控制中心, 宁波 315200;
5. 宁波市北仑区疾病预防控制中心, 宁波 315800;
6. 宁波市海曙区疾病预防控制中心, 宁波 315010;
7. 宁波大学医学部, 宁波 315211
2. Ningbo Prefectural Health Commission, Ningbo 315010, China;
3. Cixi County of Ningbo Municipal Center for Disease Control and Prevention, Ningbo 315300, China;
4. Zhenhai District of Ningbo Municipal Center for Disease Control and Prevention, Ningbo 315200, China;
5. Beilun District of Ningbo Municipal Center for Disease Control and Prevention, Ningbo 315800, China;
6. Haishu District of Ningbo Municipal Center for Disease Control and Prevention, Ningbo 315010, China;
7. Medical Department of Ningbo University, Ningbo 315211, China
新型冠状病毒(新冠病毒)Omicron变异株持续突变演化,新亚型免疫逃逸能力不断增强,再感染的发生率也相应增加[1]。爱尔兰的一项研究表明,Omicron变异株的再感染率约为Alpha变异株的30倍,为Delta变异株的10倍[2]。意大利的研究也表明,与Delta变异株相比,Omicron变异株的再感染风险增加了近18倍[3]。当前,我国流行的优势毒株为Omicron变异株BA.5.2和BF.7亚型[4],自2022年12月起我国调整了疫情防控措施[5],对新冠病毒既往感染者开展再感染研究对于科学制定公共卫生决策至关重要。因此,本研究拟通过收集宁波市既往感染者自2022年12月1日起再感染的相关信息,分析年龄、距初次感染时间间隔、新冠病毒疫苗接种、基础疾病史、初次感染疾病严重程度与再感染的关系,以了解新冠病毒再感染者的流行病学特征及其影响因素,为进一步制定预防控制措施提供科学依据。
资料与方法1. 资料来源:在中国疾病预防控制信息系统的传染病监测系统获取2020年1月1日至2022年11月30日宁波市新冠病毒既往感染者的资料,采用横断面调查方法,于2023年1月9-12日,对宁波市新冠病毒再感染状况进行问卷调查,收集研究对象性别、年龄、基础疾病史、新冠病毒疫苗接种情况、再感染状况等信息,了解新冠病毒再感染者的流行病学特征及其影响因素。本研究通过宁波市CDC伦理审查委员会审查(批准文号:202021)。
2. 再感染定义:美国CDC对再感染者的检索标准:无论有无临床症状,新冠病毒核酸初次检测阳性后间隔≥90 d再次核酸检测阳性或初次检测阳性后间隔≥45 d再次核酸检测阳性并伴有症状和流行病学暴露[6]。WHO在《新型冠状病毒感染公共卫生监测》临时指导文件中将再感染者分为疑似再感染病例、可能再感染病例和确诊再感染病例,同时认为再感染应在初次感染后≥90 d,或 < 90 d但确认感染了不同变异株或进化分支[7]。本研究定义再感染:确诊再感染者,初次新冠病毒核酸检测阳性90 d及以后,核酸/抗原再次检测呈阳性者;可能再感染者,初次新冠病毒核酸检测阳性90 d及以后,无核酸/抗原阳性检测结果,但表现出新冠病毒感染症状且有明确暴露史者。
3. 变量分组:距初次感染时间间隔:本研究将既往感染者初次核酸阳性时间至2022年11月30日的时间间隔分为 < 6、6~、≥12个月。不同变异株类型:包括166例原始株病例(初次感染时间:2020年1月19日至2月20日)、89例Delta变异株病例(初次感染时间:2021年8月11日至2022年1月8日)和642例Omicron变异株病例(初次感染时间:2022年3月14日至11月30日)。基础疾病史:主要包括呼吸系统疾病(哮喘、慢性阻塞性肺疾病、慢性支气管炎、肺气肿)、心血管系统疾病(高血压、冠心病、心肌梗死、缺血性脑病)、神经精神系统疾病、糖尿病、恶性肿瘤。
4. 统计学分析:使用Excel 2010软件建立新冠病毒再感染情况个案数据库。使用SPSS 21.0软件进行统计学分析。定性资料采用率或构成比(%)描述,组间比较采用χ2检验。将年龄、距初次感染时间间隔、新冠病毒疫苗接种剂次和初次感染疾病严重程度分别与是否为再感染者进行χ2趋势性检验。将年龄、距初次感染时间间隔、新冠病毒疫苗接种剂次、基础疾病史进行再感染相关风险的单因素分析,对差异有统计学意义的变量进行多因素logistic回归分析。双侧检验,检验水准α=0.05。
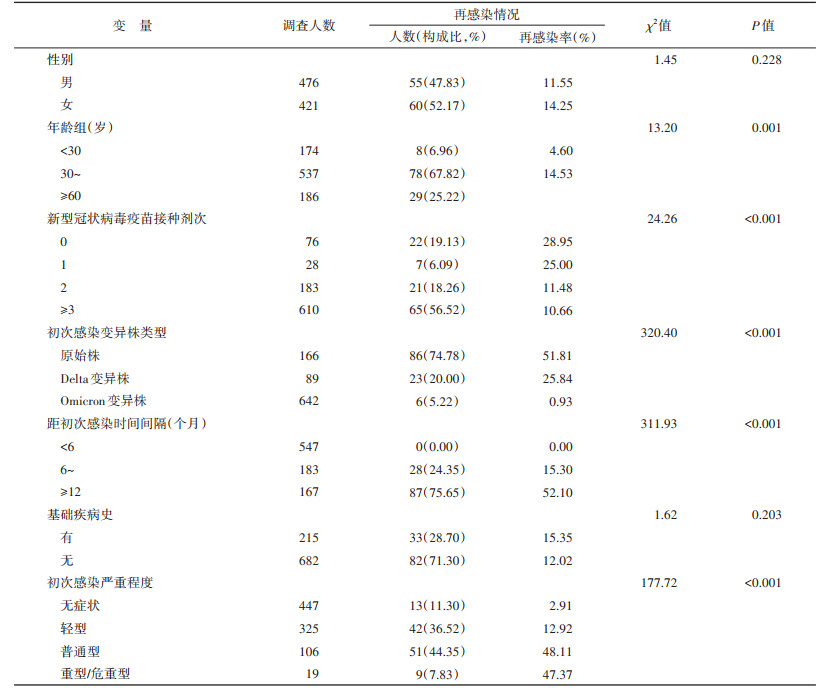
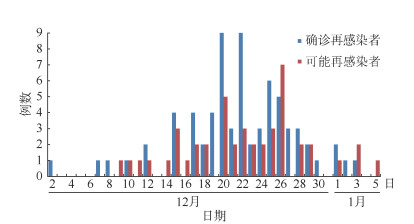
结果1. 基本情况:自2020年1月19日宁波市报告首例新冠病毒感染者以来,截至2022年11月30日,宁波市累计报告1 004例本土新冠病毒感染者(均为初次感染),其中5例死亡,失访102例。共收到897份有效问卷,有效率为89.34%。897例既往感染者中,男性476例,女性421例。年龄最小3岁,最大95岁,M(Q1,Q3)为47(34,59)岁。Omicron变异株感染者占71.57%(642/897),且82.87%(532/642)的Omicron变异株感染者初次核酸检测阳性时间集中在2022年10-11月。截至调查结束,确诊再感染者70例,可能再感染者45例,合计再感染率为12.82%(115/897)。115例再感染者再感染时间范围为2022年12月2日至2023年1月5日,其中72.17%(83/115)再感染时间为2022年12月15- 26日。见图 1。
|
| 图 1 2022-2023年宁波市新型冠状病毒再感染时间分布 |
2. 新冠病毒再感染情况:再感染者距初次感染间隔时间M(Q1,Q3)为1 052(504,1 056)d。新冠病毒再感染率在性别、基础疾病史差异无统计学意义(均P > 0.05)。原始株、Delta和Omicron变异株的再感染率分别为51.81%(86/166)、25.84%(23/89)和0.93%(6/642)。距初次感染 < 6个月组无再感染发生,6~和≥12个月组的再感染率分别为15.30%(28/183)、52.10%(87/167)。距初次感染时间间隔、年龄、新冠病毒疫苗接种剂次、初次感染变异株类型、初次感染严重程度与再感染率差异有统计学意义(均P < 0.05)。见表 1。趋势性χ2检验结果显示,年龄、新冠病毒疫苗接种剂次、距初次感染时间间隔、初次感染严重程度与再感染率有明显的线性趋势关系(均P < 0.05)。随年龄增大、新冠病毒疫苗接种剂次不足、距初次感染时间间隔越久、初次感染严重程度越重,新冠病毒再感染率均有升高趋势。
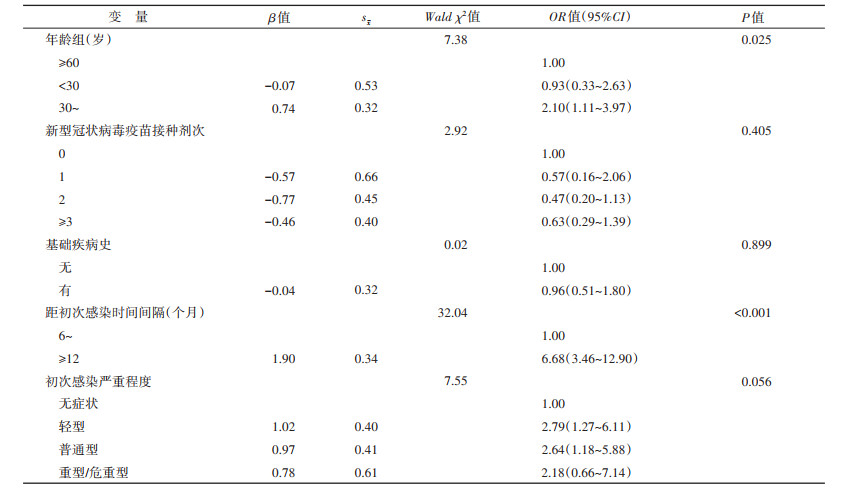
3. 再感染危险因素分析:多因素logistic回归分析结果显示,30~岁组再感染发生风险高于≥60岁组(OR=2.10,95%CI:1.11~3.97);距初次感染 < 6个月组无再感染发生,≥12个月组再感染发生风险高于6~个月组(OR=6.68,95%CI:3.46~12.90);初次感染严重程度为普通型和轻型者再感染发生风险高于无症状感染者(OR=2.64,95%CI:1.18~5.88;OR=2.79,95%CI:1.27~6.11)。见表 2。
机体对新冠病毒的免疫记忆可以通过自然感染、疫苗接种或混合免疫(感染诱导免疫和疫苗诱导免疫的组合)产生,并且可以通过T细胞、B细胞记忆和持久的抗体反应提供持续的疾病保护[8]。然而,新冠病毒诱导的免疫保护作用持续时间和程度尚未得到充分研究。本研究通过对宁波市新冠病毒再感染状况及其影响因素的研究,为科学分析新冠病毒再感染风险和进一步优化疫情防控措施提供理论依据。
本研究显示,我国宁波市新冠病毒再感染率为12.82%,低于英国(18.00%)、意大利(18.09%)和以色列(20.00%)Omicron变异株的再感染率[3, 9]。有研究表明,新冠病毒再感染的风险与年龄、免疫状态和基础疾病等因素有一定联系[10-11]。本研究单因素分析结果显示,年龄、新冠病毒疫苗接种剂次、距初次感染时间间隔、初次感染严重程度均与再感染率有关,未发现性别、基础疾病史与再感染率的关联。虽然多因素logistic回归分析未发现新冠病毒疫苗接种剂次与再感染风险的关联,但国外研究表明,接种新冠病毒疫苗能够降低再感染风险[12],这可能与我国新冠病毒疫苗接种率较高有关。截至2022年11月上旬,我国完成新冠病毒疫苗全程接种人数已超过总人口的90%[5],我国宁波市再感染率与新冠病毒疫苗全程接种率达70%的巴西(再感染率为13%)相近,明显低于全程接种率为28.95%的南非(再感染率为40%)[13]。此外,本研究发现原始株既往感染者的再感染率最高,达51.81%,可能因距初次感染时间已超2年,免疫保护作用减弱所导致[14],而Omicron变异株既往感染者再次感染Omicron变异株的风险需要进一步探讨。
国内外有关年龄与再感染率关系的研究结果存在差异,有研究表明,既往感染对≥65岁人群的再感染保护作用较年轻人低[15],但意大利的研究发现≥60岁人群发生再感染的风险较低[3],英国的研究在70~80岁人群中也观察到较低的再感染率[9]。本研究多因素logistic回归分析显示,30~岁组再感染发生风险高于≥60岁组,这可能与我国老年人新冠病毒疫苗接种率高有关,且与30~岁相比,≥60岁人群在疫情高峰期更倾向于减少社交活动,暴露机会少。
距初次感染时间间隔是再感染的重要影响因素。土耳其对520例Omicron变异株再感染患者的研究发现,16.5%发生在首次感染后的3~6个月内,首次感染后6~12个月内、12个月后发生的再感染率分别为36.7%、46.8%[2]。本研究发现距初次感染 < 6个月者再感染率为0,这可能与2022年上半年我国宁波市Omicron变异株病例数较少,而82.87%的Omicron变异株既往感染者集中在2022年10-11月有关。距初次感染≥12个月者再感染发生风险高于6~11个月者。由于不同国家和地区疫情防控策略和措施,以及群体免疫水平的差异,再感染间隔时间也存在较大的差异。美国和意大利的相关研究显示,再感染平均时间间隔介于149~349 d[16-17],均较本研究时间间隔短,这与我国在2022年12月初疫情防控措施调整[5],使再感染时间延后有关。目前有关初次感染者疾病严重程度与再感染关系尚不明确。本研究发现,初次感染严重程度为普通型和轻型者的再感染风险均高于无症状感染者,但未观察到重型/危重型者再感染的风险增加。已有研究表明,既往感染者临床症状越严重,其中和抗体滴度更高,但防止再感染的能力不一定增加[18]。这可能与既往感染者康复后抗体水平下降较快有关。我国重庆市的一项研究表明,约90%的新冠病毒感染者在出院后2个月总抗体水平会降低70%以上[19]。
综上所述,本研究表明距初次感染时间间隔是再感染风险的重要影响因素,感染新冠病毒6个月内再感染率较低。已有研究表明再感染不会加重疾病严重程度[20],或再感染的严重程度可能明显低于既往感染[21-22]。由于疫情防控措施的调整,以及横断面研究方法的局限性,本研究未能评价再感染者疾病严重程度;此外,由于宁波市既往感染者数量有限,在一些因素的分层上样本量相对较少,有可能对研究结果有一定影响。
利益冲突 所有作者声明无利益冲突
作者贡献声明 褚衍茹:酝酿和设计实验、实施研究、采集/分析解释数据、统计分析、起草文章;陈奕、雷松、张言武、易波、马建明、闫克栋、王赟、李保军、吕梦倩:采集/分析解释数据、内容审阅、统计分析;许国章、张栋梁:酝酿和设计实验、采集/分析解释数据、内容审阅
| [1] |
廖春晓, 王波, 吕筠, 等. 新型冠状病毒重复感染流行病学研究进展[J]. 中华流行病学杂志, 2023, 44(3): 360-366. DOI:10.3760/cma.j.cn112338-20230110-00022 Liao CX, Wang B, Lyu J, et al. Progress in research of epidemiology of 2019-nCoV reinfection[J]. Chin J Epidemiol, 2023, 44(3): 360-366. DOI:10.3760/cma.j.cn112338-20230110-00022 |
| [2] |
Özüdoğru O, Bahçe YG, Acer Ö. SARS CoV-2 reinfection rate is higher in the Omicron variant than in the Alpha and Delta variants[J]. Irish J Med Sci, 2023, 192(2): 751-756. DOI:10.1007/S11845-022-03060-4 |
| [3] |
Sacco C, Petrone D, del Manso M, et al. Risk and protective factors for SARS-CoV-2 reinfections, surveillance data, Italy, August 2021 to March 2022[J/OL]. Euro Surveill, 2022, 27(20): 2200372. DOI: 10.2807/1560-7917.ES.2022.27.20.2200372.
|
| [4] |
国务院联防联控机制2023年1月30日新闻发布会文字实录[EB/OL]. (2023-01-30)[2023-02-03]. http://www.nhc.gov.cn/xcs/s3574/202301/8eb4b4eb6e8b469a8f92a789f94055b8.shtml.
|
| [5] |
新华社: 中国战"疫"进入新阶段——我国因时因势优化疫情防控措施纪实[EB/OL]. (2023-01-08)[2023-02-03]. http://www.nhc.gov.cn/wjw/mtbd/202301/53e4bdbadd0f4a3384c0af7e38f16427.shtml.
|
| [6] |
Centers for Disease Control and Prevention. Investigative criteria for suspected cases of SARS-CoV-2 reinfection (ICR)[EB/OL]. (2020-10-27)[2023-02-03]. https://stacks.cdc.gov/view/cdc/96072.
|
| [7] |
Public health surveillance for COVID-19[EB/OL]. (2022-02-14)[2023-02-03]. https://apps.who.int/iris/bitstream/handle/10665/351761/WHO-2019-nCoV-Surveillance- Guidance-2022.1-eng.pdf?sequence=1&isAllowed=y.
|
| [8] |
Sette A, Crotty S. Immunological memory to SARS-CoV-2 infection and COVID-19 vaccines[J]. Immunol Rev, 2022, 310(1): 27-46. DOI:10.1111/IMR.13089 |
| [9] |
Keeling MJ. Patterns of reported infection and reinfection of SARS-CoV-2 in England[J/OL]. J Theoret Biol, 2023, 556: 111299. DOI: 10.1016/j.jtbi.2022.111299.
|
| [10] |
Piazza MF, Amicizia D, Marchini F, et al. Who is at higher risk of SARS-CoV-2 reinfection? Results from a northern region of Italy[J/OL]. Vaccines (Basel), 2022, 10(11): 1885. DOI: 10.3390/VACCINES10111885.
|
| [11] |
Pilz S, Theiler-Schwetz V, Trummer C, et al. SARS-CoV-2 reinfections: Overview of efficacy and duration of natural and hybrid immunity[J/OL]. Environ Res, 2022, 209: 112911. DOI: 10.1016/j.envres.2022.112911.
|
| [12] |
Flacco ME, Martellucci CA, Baccolini V, et al. Risk of reinfection and disease after SARS-CoV-2 primary infection: Meta-analysis[J/OL]. Eur J Clin Invest, 2022, 52(10): e13845. DOI: 10.1111/ECI.13845.
|
| [13] |
Xavier CR, Oliveira RS, Da Fonseca Vieira V, et al. Characterisation of omicron variant during COVID-19 pandemic and the impact of vaccination, transmission rate, mortality, and reinfection in South Africa, Germany, and Brazil[J/OL]. BioTech (Basel), 2022, 11(2): 12. DOI: 10.3390/BIOTECH11020012.
|
| [14] |
Altarawneh HN, Chemaitelly H, Ayoub HH, et al. Protective effect of previous SARS-CoV-2 infection against omicron BA. 4 and BA. 5 subvariants[J]. N Engl J Med, 2022, 387(17): 1620-1622. DOI:10.1056/NEJMc2209306 |
| [15] |
Hansen CH, Michlmayr D, Gubbels SM, et al. Assessment of protection against reinfection with SARS-CoV-2 among 4 million PCR-tested individuals in Denmark in 2020: a population-level observational study[J]. Lancet, 2021, 397(10280): 1204-1212. DOI:10.1016/S0140-6736(21)00575-4 |
| [16] |
Centers for Disease Control and Prevention. SARS-CoV-2 infection-induced and vaccine-induced immunity[EB/OL]. (2021-10-29)[2023-02-03]. https://www.cdc.gov/coronavirus/2019-ncov/science/science-briefs/vaccine-induced-immunity.html.
|
| [17] |
Flacco ME, Soldato G, Martellucci CA, et al. Risk of SARS-CoV-2 reinfection 18 months after primary infection: population-level observational study[J/OL]. Front Public Health, 2022, 10: 884121. DOI: 10.3389/fpubh.2022.884121.
|
| [18] |
Chen XY, Pan ZW, Yue S, et al. Disease severity dictates SARS-CoV-2-specific neutralizing antibody responses in COVID-19[J/OL]. Signal Transduct Target Ther, 2020, 5(1): 180. DOI: 10.1038/s41392-020-00301-9.
|
| [19] |
Long QX, Tang XJ, Shi QL, et al. Clinical and immunological assessment of asymptomatic SARS-CoV-2 infections[J]. Nat Med, 2020, 26(8): 1200-1204. DOI:10.1038/s41591-020-0965-6 |
| [20] |
Nguyen NN, Houhamdi L, Hoang VT, et al. SARS-CoV-2 reinfection and COVID-19 severity[J]. Emerg Microbes Infect, 2022, 11(1): 894-901. DOI:10.1080/22221751.2022.2052358 |
| [21] |
Abu-Raddad LJ, Chemaitelly H, Bertollini R. Severity of SARS-CoV-2 reinfections as compared with primary infections[J]. N Engl J Med, 2021, 385(26): 2487-2489. DOI:10.1056/NEJMc2108120 |
| [22] |
Qureshi AI, Baskett WI, Huang W, et al. Reinfection with severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) in patients undergoing serial laboratory testing[J]. Clin Infect Dis, 2022, 74(2): 294-300. DOI:10.1093/cid/ciab345 |
 2023, Vol. 44
2023, Vol. 44