文章信息
- 徐韵韶, 姜明月, 曹琰琳, 孙艳侠, 黄蔷如, 杨维中, 冯录召.
- Xu Yunshao, Jiang Mingyue, Cao Yanlin, Sun Yanxia, Huang Qiangru, Yang Weizhong, Feng Luzhao
- 接种天花疫苗对猴痘病毒感染的保护作用研究进展
- Research progress on the effectiveness of smallpox vaccination against mpox virus infection
- 中华流行病学杂志, 2023, 44(4): 673-676
- Chinese Journal of Epidemiology, 2023, 44(4): 673-676
- http://dx.doi.org/10.3760/cma.j.cn112338-20221102-00934
-
文章历史
收稿日期: 2022-11-02
猴痘是由猴痘病毒感染引起的人畜共患病。猴痘病毒属于痘病毒科正痘病毒属的一种DNA病毒。该病毒的传播方式包括呼吸道飞沫传播、皮肤损伤接触传播,或性接触传播[1]。猴痘病毒感染后的症状首先是发热,随后在面部和体表出现多个脓疱、溃疡性病变和淋巴结突出,并发症可能包括肺炎、脑炎、角膜炎和继发性细菌感染[2]。在2022疫情暴发之前,猴痘病例主要局限于流行地区。2003年,在美国发现了37例确诊,这是在非洲地区以外首次报告猴痘病例[3]。之后在以色列[4](2018年1例)、英国[5-6](2018-2021年7例)和新加坡[7](2019年1例)陆续发现猴痘病例。2021年美国又发现2例猴痘病例[8]。自2022年5月以来全球猴痘病例数量呈急剧增加趋势;7月23日,WHO宣布猴痘疫情构成国际关注的突发公共卫生事件;11月28日,为避免歧视和污名化,WHO宣布将猴痘英文名改为“mpox”。据美国CDC报告,截至2022年12月15日,猴痘疫情已蔓延至全球110个国家,累计感染82 553例[9]。本文通过综述目前国内外猴痘疫情中天花疫苗的保护作用以及各类疫苗在临床及动物模型中诱导的免疫应答,阐述天花疫苗对猴痘病毒感染的保护能力,为猴痘疫情的防控策略提供科学证据。
1. 暴发疫情中天花疫苗对猴痘的保护作用:猴痘病毒与天花病毒同属于正痘病毒属,由于正痘病毒之间的基因序列具有高度相似性且正痘病毒可诱发交叉反应型抗体,接种天花疫苗可能会影响猴痘病毒感染者的免疫应答水平及其健康结局。然而在1980年根除天花之后,各国逐渐对新生儿停止接种天花疫苗,我国也于1981年停止接种天花疫苗。在停止天花疫苗大规模接种30年后,刚果民主共和国农村地区的猴痘发病率增加了20倍,其中未接种天花病毒疫苗的人相较于接种天花病毒疫苗的人感染猴痘病毒的风险高5.2倍[10],这意味着1981年以后出生的群体暴露于猴痘病毒时无法得到天花疫苗的交叉保护。
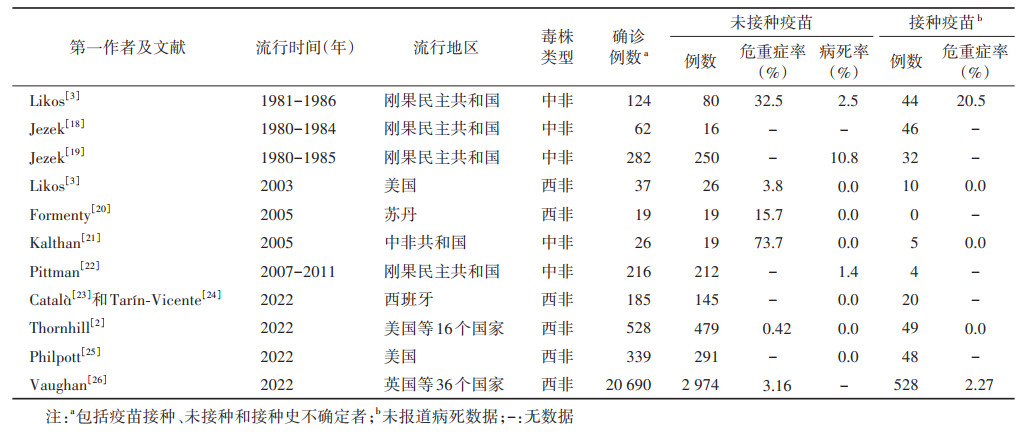
本文汇总1981-2022年发生的猴痘病毒感染中天花疫苗接种和发病情况,根据其来源不同,猴痘病毒被分为中非和西非2个分支(表 1)。1981-1985年2 278例猴痘病例的密切接触者的研究显示,接种过天花疫苗的密切接触者续发感染率为0.9%,而未接种疫苗者为7.5%[11]。2006- 2007年刚果民主共和国的监测表明,全国天花疫苗接种率为26.4%,而同时期猴痘病例中天花疫苗接种者的比例为3.8%,疫苗效力估计为80.7%[12]。2003年,对美国暴发的猴痘病例分析发现,曾在儿童时期接种天花疫苗的6例猴痘病例的发热和皮疹等临床表现较轻[13]。有研究发现,接种过天花疫苗者比未接种者的皮疹范围和皮肤病变范围较小、疾病严重程度较轻[13-15]。值得关注的是,2022年12月Allan-Blitz等[16]对性行为和猴痘感染的相关性分析结果显示,性行为与病变发生的时间和部位存在相关性,性行为的频次与感染率存在相关性,可从阴道分泌物或精液中分离出猴痘病毒,建议将猴痘定义为性传播疾病。同时,Hazra和Cherabie[17]认为既往猴痘病毒感染多为局部暴发且与性行为无关,将猴痘定义为性传播疾病容易导致公众忽视呼吸道及飞沫传播、皮肤损伤接触传播等传播途径,并使感染者被污名化。目前WHO对猴痘的相关指南并未将猴痘纳入性传播疾病。
2. 天花疫苗对预防猴痘病毒感染的作用机制:正痘病毒之间的基因序列具有高度相似性,编码免疫相关蛋白质的基因接近导致正痘病毒间存在大量共享的免疫表位、免疫标志物,因此接种天花疫苗极有可能影响猴痘病毒感染后的免疫应答水平。
适应性免疫反应是初始识别和早期反应后病毒清除的关键,CD14+外周血单核细胞是丰富的造血抗原提呈细胞,能够将猴痘病毒抗原呈递给CD4+ T淋巴细胞(CD4)和CD8+ T淋巴细胞(CD8),这些细胞随后协调产生细胞因子、裂解被感染细胞并诱导宿主的血清学反应等,这在病毒清除过程中具有重要意义[27]。其中,CD4优先识别病毒结构蛋白,而CD8则针对病毒生命期早期产生的蛋白发生免疫应答[17]。有研究发现,天花疫苗具有很强的诱导记忆性细胞产生的能力,记忆性CD4可持续50年或更长时间,半衰期估算为8~15年[28]。然而,一项猴痘二次感染的研究发现,天花疫苗诱导的交叉保护并不由这种持久性的细胞免疫引起,因为在该研究中接种疫苗和未接种疫苗的病例体内检测到正痘病毒特异性CD4反应水平相当,甚至有5例接种过天花疫苗的病例在整个疾病恢复期均未检测到正痘病毒特异性CD4和CD8[13]。
在体液免疫层面,对猴痘病毒感染起免疫作用的抗体主要为IgM和IgG。2007年3月至2011年8月,刚果民主共和国一项纳入200例猴痘患者的前瞻性观察研究显示,猴痘患者在住院期间IgG均呈阳性,但4名接种疫苗的患者均未出现IgM反应;其中同时有IgM和IgG反应的患者,发生严重疾病的可能性是仅有IgG反应患者的5.09倍(OR=5.09,95%CI:2.91~8.93)[22],表明接种天花疫苗可通过体液免疫有效预防感染者病情加重。2003年美国一项临床研究表明,猴痘病毒感染者中,中度或重度临床表现的感染者IgM的滴度(A/COV值)普遍高于轻度患者,且75%的疫苗接种者的A/COV < 0.2,69%的未接种疫苗者的A/COV > 0.2;密切接触者中,接种过天花疫苗者易检测到IgG,疫苗接种者和未接种者的IgG检出率分别为92%和7%[13]。这些结果提示IgM抗体在初次免疫反应占主导地位,可作为疾病严重程度的一个生物标志物,IgG抗体主导再次免疫反应,反映了疫苗的交叉保护作用水平。
3. 新型天花疫苗对猴痘病毒感染的交叉保护作用:第一代天花疫苗为通过动物组织培养获得、具有复制能力的活病毒,代表性产品为天坛株天花疫苗。第二代天花疫苗为通过病毒克隆技术获得、具有复制能力的活病毒,代表性产品为ACAM2000。第三代天花疫苗通过多次传代培养排除了活病毒疫苗潜在的安全隐患,免疫原性高但需两剂接种,代表性产品为MVA和MYVAC。第四代天花疫苗为基因设计改造获得的亚单位疫苗,代表性产品为4pox-VRP,其主要特点为使用少量病毒抗原诱导免疫应答,但安全性和有效性均需进一步研究。
研究显示,接种第一代天花疫苗对猴痘病毒感染的保护作用约为85%,且接种天花疫苗可潜在降低猴痘病毒毒性,临床表现为皮疹范围小、皮肤病变范围少,症状也较轻[10]。新型疫苗在人体中对猴痘病毒感染的保护效果未见报道,但相关动物实验从侧面印证了第二代和第三代天花疫苗对猴痘感染的效力。2004年以来,不同研究通过猴痘感染的啮齿动物模型来测试疫苗的保护效力[6, 29-33]。一项研究对小鼠通过划痕或肌内注射接种天花疫苗,接种组在病毒感染后体重降低程度和疾病严重程度均低于未接种组[34]。另一项针对第二、三代天花疫苗与猴痘感染的动物实验研究显示,这两类疫苗对猴痘病毒感染的保护效力约为85%[35]。第二代天花疫苗的动物实验结果还提示,在感染猴痘病毒后的3 d内接种天花疫苗将对临床表现和健康结局产生影响,感染后第1天和第3天接种ACAM2000的草原犬鼠存活率分别为88%和62%,而未接种疫苗组的存活率为25%,且接种疫苗组的疾病严重程度均有所降低[36]。目前,第二代和第三代疫苗均被美国食品药品监督管理局批准用于预防猴痘,且未接种疫苗者的猴痘发病率是接种疫苗者的7~9倍[37]。
4. 总结:动物实验、疫苗临床试验和真实世界研究证据均支持天花疫苗对猴痘病毒感染具有交叉保护作用。应进一步加强猴痘病毒的免疫学研究,关注其细胞免疫和体液免疫反应情况。对猴痘病毒感染者,可分别观察有无天花疫苗接种史的情况下IgG和IgM抗体水平变化,以及与疾病严重性的关系。猴痘疫情仍在全球蔓延,美国已将天花疫苗纳入国家战略物资储备,并为海关、医疗等具有潜在接触风险的从业者和病例的密切接触者提供天花疫苗接种服务;英国已购买2万剂天花疫苗并计划为医务人员接种[38];此外仍有多国已授权使用第二代天花疫苗来预防猴痘病毒感染[39]。我国针对疫情可能的输入及扩散情况,应提前对已有天花疫苗进行实物或技术储备,并同时研发新一代猴痘疫苗,作为应对猴痘疫情的方法。鉴于普通人群的感染风险低,猴痘疫苗的未来可选策略不是大规模免疫,而是优先考虑高风险人群的疫苗接种。我国需要对猴痘疫情进行实时风险评估,建立监测预警体系,提升应对准备能力,尽早发现和控制输入疫情,避免疫情大范围扩散,保障国家的公共卫生安全。
利益冲突 所有作者声明无利益冲突
| [1] |
Mbala PK, Huggins JW, Riu-Rovira T, et al. Maternal and fetal outcomes among pregnant women with human monkeypox infection in the democratic republic of Congo[J]. J Infect Dis, 2017, 216(7): 824-828. DOI:10.1093/infdis/jix260 |
| [2] |
Thornhill JP, Barkati S, Walmsley S, et al. Monkeypox virus infection in humans across 16 countries — April–June 2022[J]. N Engl J Med, 2022, 387(8): 679-691. DOI:10.1056/NEJMoa2207323 |
| [3] |
Likos AM, Sammons SA, Olson VA, et al. A tale of two clades: monkeypox viruses[J]. J Gen Virol, 2005, 86(Pt 10): 2661-2672. DOI:10.1099/vir.0.81215-0 |
| [4] |
Erez N, Achdout H, Milrot E, et al. Diagnosis of imported monkeypox, Israel, 2018[J]. Emerg Infect Dis, 2019, 25(5): 980-983. DOI:10.3201/eid2505.190076 |
| [5] |
Vaughan A, Aarons E, Astbury J, et al. Two cases of monkeypox imported to the United Kingdom, September 2018[J]. Euro Surveill, 2018, 23(38): 1800509. DOI:10.2807/1560-7917.ES.2018.23.38.1800509 |
| [6] |
Vaughan A, Aarons E, Astbury J, et al. Human-to-human transmission of monkeypox virus, United Kingdom, October 2018[J]. Emerg Infect Dis, 2020, 26(4): 782-785. DOI:10.3201/eid2604.191164 |
| [7] |
Yong SEF, Ng OT, Ho ZJM, et al. Imported monkeypox, Singapore[J]. Emerg Infect Dis, 2020, 26(8): 1826-1830. DOI:10.3201/eid2608.191387 |
| [8] |
Rao AK, Schulte J, Chen TH, et al. Monkeypox in a traveler returning from Nigeria-Dallas, Texas, July 2021[J]. MMWR Morb Mortal Wkly Rep, 2022, 71(14): 509-516. DOI:10.15585/mmwr.mm7114a1 |
| [9] |
Centers for Disease Control and Prevention. 2022 Mpox Outbreak Global Map[EB/OL]. (2022-12-15) [2022-12-16]. https://www.cdc.gov/poxvirus/monkeypox/response/2022/world-map.html.
|
| [10] |
Moschese D, Farinacci D, Pozza G, et al. Is smallpox vaccination protective against human monkeypox?[J]. J Med Virol, 2023, 95(1): e28077. DOI:10.1002/jmv.28077 |
| [11] |
Fleischauer AT, Kile JC, Davidson M, et al. Evaluation of human-to-human transmission of monkeypox from infected patients to health care workers[J]. Clin Infect Dis, 2005, 40(5): 689-694. DOI:10.1086/427805 |
| [12] |
Rimoin AW, Mulembakani PM, Johnston SC, et al. Major increase in human monkeypox incidence 30 years after smallpox vaccination campaigns cease in the Democratic Republic of Congo[J]. Proc Natl Acad Sci USA, 2010, 107(37): 16262-16267. DOI:10.1073/pnas.1005769107 |
| [13] |
Karem KL, Reynolds M, Hughes C, et al. Monkeypox-induced immunity and failure of childhood smallpox vaccination to provide complete protection[J]. Clin Vaccine Immunol, 2007, 14(10): 1318-1327. DOI:10.1128/CVI.00148-07 |
| [14] |
Damon IK. Status of human monkeypox: clinical disease, epidemiology and research[J]. Vaccine, 2011, 29(4): D54-59. DOI:10.1016/j.vaccine.2011.04.014 |
| [15] |
di Giulio DB, Eckburg PB. Human monkeypox: an emerging zoonosis[J]. Lancet Infect Dis, 2004, 4(1): 15-25. DOI:10.1016/S1473-3099(03)00856-9 |
| [16] |
Allan-Blitz LT, Gandhi M, Adamson P, et al. A position statement on mpox as a sexually transmitted disease[J/OL]. Clin Infect Dis, 2022, ciac960. DOI: 10.1093/cid/ciac960.
|
| [17] |
Hazra A, Cherabie JN. Is mpox a sexually transmitted infection? Why narrowing the scope of this disease may be harmful [J/OL]. Clin Infect Dis, 2022, ciac962. DOI: 10.1093/cid/ciac962.
|
| [18] |
Jezek Z, Marennikova SS, Mutumbo M, et al. Human monkeypox: a study of 2, 510 contacts of 214 patients[J]. J Infect Dis, 1986, 154(4): 551-555. DOI:10.1093/infdis/154.4.551 |
| [19] |
Jezek Z, Szczeniowski M, Paluku KM, et al. Human monkeypox: clinical features of 282 patients[J]. J Infect Dis, 1987, 156(2): 293-298. DOI:10.1093/infdis/156.2.293 |
| [20] |
Formenty P, Muntasir MO, Damon I, et al. Human monkeypox outbreak caused by novel virus belonging to Congo basin clade, Sudan, 2005[J]. Emerg Infect Dis, 2010, 16(10): 1539-1545. DOI:10.3201/eid1610.100713 |
| [21] |
Kalthan E, Tenguere J, Ndjapou SG, et al. Investigation of an outbreak of monkeypox in an area occupied by armed groups, Central African Republic[J]. Med Mal Infect, 2018, 48(4): 263-268. DOI:10.1016/j.medmal.2018.02.010 |
| [22] |
Pittman PR, Martin JW, Kingebeni PM, et al. Clinical characterization of human monkeypox infections in the Democratic Republic of the Congo[J/OL]. MedRxiv, 2022 May 29. DOI: 10.1101/2022.05.26.22273379.
|
| [23] |
Català A, Clavo-Escribano P, Riera-Monroig J, et al. Monkeypox outbreak in Spain: clinical and epidemiological findings in a prospective cross‐sectional study of 185 cases[J]. Br J Dermatol, 2022, 187(5): 765-772. DOI:10.1111/bjd.21790 |
| [24] |
Tarín-Vicente EJ, Alemany A, Agud-Dios M, et al. Clinical presentation and virological assessment of confirmed human monkeypox virus cases in Spain: a prospective observational cohort study[J]. Lancet, 2022, 400(10353): 661-669. DOI:10.1016/S0140-6736(22)01436-2 |
| [25] |
Philpott D. Epidemiologic and clinical characteristics of monkeypox cases—United States, May 17-July 22, 2022[J]. MMWR Morb Mortal Wkly Rep, 2022, 71(32): 1018-1022. DOI:10.15585/mmwr.mm7132e3 |
| [26] |
Vaughan AM, Cenciarelli O, Colombe S, et al. A large multi- country outbreak of monkeypox across 41 countries in the WHO European Region, 7 March to 23 August 2022[J]. Euro Surveill, 2022, 27(36): 2200620. DOI:10.2807/1560-7917.ES.2022.27.36.2200620 |
| [27] |
Hammarlund E, Dasgupta A, Pinilla C, et al. Monkeypox virus evades antiviral CD4+ and CD8+ T cell responses by suppressing cognate T cell activation[J]. Proc Natl Acad Sci USA, 2008, 105(38): 14567-14572. DOI:10.1073/pnas.0800589105 |
| [28] |
Hammarlund E, Lewis MW, Hansen SG, et al. Duration of antiviral immunity after smallpox vaccination[J]. Nat Med, 2003, 9(9): 1131-1137. DOI:10.1038/nm917 |
| [29] |
Hutson CL, Damon IK. Monkeypox virus infections in small animal models for evaluation of anti-poxvirus agents[J]. Viruses, 2010, 2(12): 2763-2776. DOI:10.3390/v2122763 |
| [30] |
Americo JL, Moss B, Earl PL. Identification of wild-derived inbred mouse strains highly susceptible to monkeypox virus infection for use as small animal models[J]. J Virol, 2010, 84(16): 8172-8180. DOI:10.1128/JVI.00621-10 |
| [31] |
Carroll DS, Olson VA, Smith SK, et al. Orthopoxvirus variola infection of Cynomys ludovicianus (North American Black tailed prairie dog)[J]. Virology, 2013, 443(2): 358-362. DOI:10.1016/j.virol.2013.05.029 |
| [32] |
Stabenow J, Buller RM, Schriewer J, et al. A mouse model of lethal infection for evaluating prophylactics and therapeutics against monkeypox virus[J]. J Virol, 2010, 84(8): 3909-3920. DOI:10.1128/JVI.02012-09 |
| [33] |
Xiao SY, Sbrana E, Watts DM, et al. Experimental infection of prairie dogs with monkeypox virus[J]. Emerg Infect Dis, 2005, 11(4): 539-545. DOI:10.3201/eid1104.040907 |
| [34] |
Phelps A, Gates AJ, Eastaugh L, et al. Comparative efficacy of intramuscular and scarification routes of administration of live smallpox vaccine in a murine challenge model[J]. Vaccine, 2017, 35(31): 3889-3896. DOI:10.1016/j.vaccine.2017.05.058 |
| [35] |
Kimball S. U. S. has more than 36, 000 Jynneos monkeypox vaccine doses immediately available in national stockpile [EB/OL]. (2022-06-06) [2022-11-01]. https://www.cnbc.com/2022/06/06/us-has-36000-doses-of-jynneos-monkeypox-vaccine-immediately-available-in-national-stockpile.html?&qsearchterm=U.S.%20has%20more%20than%2036,000%20Jynneos%20monkeypox%20vaccine%20doses%20immediately%20available%20in%20national%20stockpile.
|
| [36] |
Keckler MS, Salzer JS, Patel N, et al. IMVAMUNE® and ACAM2000® provide different protection against disease when administered postexposure in an intranasal monkeypox challenge prairie dog model[J]. Vaccines, 2020, 8(3): 396. DOI:10.3390/vaccines8030396 |
| [37] |
Payne AB, Ray LC, Cole MM, et al. Reduced risk for mpox after receipt of 1 or 2 doses of JYNNEOS vaccine compared with risk among unvaccinated persons - 43 U. S. jurisdictions, July 31-October 1, 2022[J]. MMWR Morb Mortal Wkly Rep, 2022, 71(49): 1560-1564. DOI:10.15585/mmwr.mm7149a5 |
| [38] |
Mahase E. Monkeypox: healthcare workers will be offered smallpox vaccine as UK buys 20 000 doses[J]. BMJ, 2022, 377: o1379. DOI:10.1136/bmj.o1379 |
| [39] |
Islam R, Hossain J, Roy A, et al. Repositioning potentials of smallpox vaccines and antiviral agents in monkeypox outbreak: a rapid review on comparative benefits and risks[J]. Health Sci Rep, 2022, 5(5): e798. DOI:10.1002/hsr2.798 |
 2023, Vol. 44
2023, Vol. 44