文章信息
- 张琳, 曹雷, 李燕, 胡莹雪, 唐林, 李克莉, 尹遵栋, 安志杰.
- Zhang Lin, Cao Lei, Li Yan, Hu Yingxue, Tang Lin, Li Keli, Yin Zundong, An Zhijie
- 2017-2021年中国肠道病毒71型灭活疫苗接种现状分析
- Analysis of the vaccination status of enterovirus type 71 inactivated vaccine in China from 2017 to 2021
- 中华流行病学杂志, 2023, 44(4): 561-567
- Chinese Journal of Epidemiology, 2023, 44(4): 561-567
- http://dx.doi.org/10.3760/cma.j.cn112338-20220811-00704
-
文章历史
收稿日期: 2022-08-11
手足口病是一种由肠道病毒引起的儿童常见传染病,主要感染≤5岁儿童,多数患者病情轻微并具有自限性,少数严重病例可导致神经系统疾病等并发症,甚至死亡[1],目前已知有20多种血清型的肠道病毒可引起手足口病。2008年我国将手足口病纳入国家法定报告丙类传染病。2008-2017年报告的手足口病中,约70.03%的严重病例和92.23%的死亡病例由肠道病毒71型(EV71)感染所致[2]。EV71感染可引起多种疾病,其中以手足口病常见,目前尚无有效的治疗方法[3]。2016-2017年,中国医学科学院医学生物学研究所、北京科兴生物制品有限公司和武汉生物制品研究所有限责任公司自主研发的EV71灭活疫苗陆续获批上市[4-5]。目前,EV71灭活疫苗作为非免疫规划疫苗在全国范围使用,近年来部分地区开展了EV71灭活疫苗接种率的相关研究[6-7],但在全国层面分析该疫苗的接种现状尚未见报道,本研究对EV71灭活疫苗上市应用以来在我国的接种现状进行分析,为制定手足口病防控和免疫策略提供参考。
资料与方法 (1) 资料来源(1) 疫苗批签发数据:中国食品药品检定研究院网站公布的2016-2020年EV71灭活疫苗批签发数据[8]。中国医学科学院医学生物学研究所、北京科兴生物制品有限公司和武汉生物制品研究所有限责任公司生产EV71灭活疫苗首次批签发时间分别是2016年3月、2016年5月和2017年4月。2021年3月及以后批签发数据未公布疫苗数量,因此2021年批签发数据未纳入本次分析。
(2) 疫苗接种数据:中国免疫规划信息管理系统基于乡级接种单位按月上报逐级汇总的2017-2021年全国、省级、地市级EV71灭活疫苗报告接种剂次数。2016年EV71灭活疫苗开始批签发,但当年中国免疫规划信息管理系统尚未收集该疫苗接种数据,2016年接种数据未纳入分析。
(3) 疫苗免疫程序:基于疫苗产品说明书,北京科兴生物制品有限公司和武汉生物制品研究所有限责任公司的EV71灭活疫苗接种对象为6月龄至3岁儿童,中国医学科学院医学生物学研究所EV71灭活疫苗接种对象为6月龄至5岁儿童。3种疫苗均接种2剂次,间隔1个月。2021年6月北京科兴生物制品有限公司EV71灭活疫苗接种年龄扩大至71月龄。
(4) 手足口病发病数据:源自国家卫生健康委员会官方网站公布的2017-2021年全国每月手足口病报告发病数。
(5) 其他数据:①全国人口数据来自《2021中国统计年鉴》[9]和2021年全国国民经济和社会发展统计公报[10],省级和地市级人口数据来自中国免疫规划管理信息系统2020年数据;②东/中/西部地区分类、各地人均可支配收入和医疗卫生机构数来自《2019中国城市统计年鉴》数据[11];③各地接种单位数量(2020年)[12]和2008-2017年手足口病平均发病率来自文献[13]。
(2) 接种率估算(1) 不同年份出生队列人数估计:全国各年份出生队列人数用当年总人口×当年出生率估算。省级和地市级各年份出生队列基于中国免疫规划信息管理系统2020年的年龄别人口数据,0岁组人数作为2020年出生队列人数,依次类推至8岁组作为2012年出生队列人数,因中国免疫规划信息管理系统尚未更新2021年人口信息,用2020年0岁组人口数估算2021年出生队列人数。
(2) 累计疫苗接种目标儿童数估算:从2017年开始收集接种数据,按照3种EV71灭活疫苗接种程序的最大年龄为5岁推算,可覆盖的最早出生队列为2012年出生儿童。2017-2021年分别基于上所述方法估算各年度2012年以来出生队列总人数,作为截至该年度的疫苗接种累计目标儿童数,考虑到接种起始月龄为6月龄,当年目标人口数按该年出生队列人数的50%计算。如2017年采用2012-2016年各年度出生人口数总和与2017年50%出生人口数累加,作为2017年度EV71灭活疫苗的累计目标儿童数,其他年度类推,直至2021年。
(3) 累计接种率估算:基于报告的各级每年度EV71灭活疫苗接种汇总剂次数,按照EV71灭活疫苗2剂次全程基础免疫接种程序,估算疫苗接种儿童数=报告接种剂次数÷2。某年度EV71灭活疫苗估算累计接种率=该年度估算累计接种儿童数÷该年度累计目标儿童数×100%,该方法用于估算全国、省级和地市级接种率,以及分析接种率影响因素。此外,对2021年全国累计接种率按照10%全程接种脱漏率[14-15](接种对象只完成1剂次接种)推测,估算该年度全国累计2剂次全程接种率和至少1剂次接种率。
(3) 统计学分析采用SPSS 25.0软件进行统计学分析描述。①不同地区接种率:分别以全国、省、地市为单位估算累计接种率,以省为单位分析各地市级接种率的M(Q1,Q3)。北京市、天津市、上海市、重庆市和新疆生产建设兵团未做地市级分析。②接种率影响因素:将省级的接种单位数量、医疗卫生机构数、人均可支配收入、既往手足口病发病率等变量纳入与省级2021年估算累计接种率做多因素相关性分析。双侧检验,检验水准α=0.05。
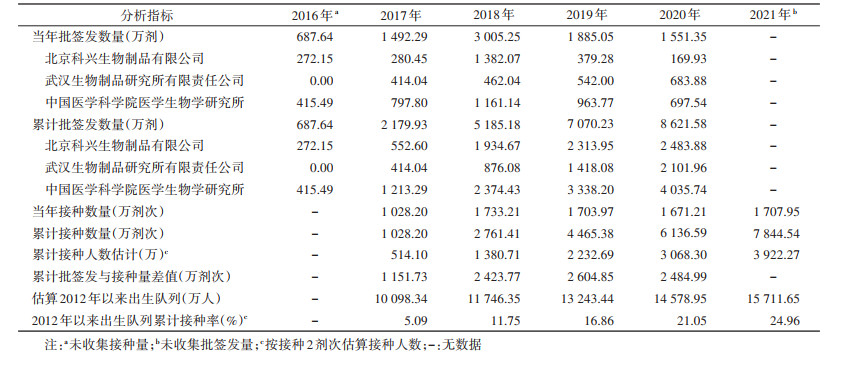
结果1. EV71灭活疫苗批签发数量及接种剂次:2016-2020年EV71灭活疫苗批签发总量为8 621.58万剂,各年度批签发总量分别是687.64万、1 492.29万、3 005.25万、1 885.05万和1 551.35万剂;2017-2021年全国报告EV71灭活疫苗累计接种总量为7 844.54万剂次,各年度接种总量分别是1 028.20万、1 733.21万、1 703.97万、1 671.21万和1 707.95万剂次。2017-2020年各年度累计批签发和累计接种量的差值分别为1 151.73万、2 423.77万、2 604.85万和2 484.99万剂次。见表 1。
2017-2021年EV71灭活疫苗接种总量位居前5位的省份包括广东省、河南省、山东省、四川省和安徽省,接种总剂次数分别为1 169.32万、587.93万、558.39万、509.58万和463.27万剂次;EV71灭活疫苗接种量位居后5位的省份是宁夏回族自治区、新疆维吾尔自治区、青海省、新疆生产建设兵团和西藏自治区,接种总剂次数分别为28.21万、22.90万、13.10万、5.64万和5.27万剂次。
(2) 疫苗接种情况(1) 全国接种率估算:截至2021年底全国累计接种的7 844.54万剂次,按所有接种对象均完成全程2剂次接种估算,全国2012年以来出生目标儿童在2017-2021年累计接种EV71灭活疫苗3 922.27万人,累计接种率从2017年的5.09%上升到2021年的24.96%(表 1)。如按照约10%全程接种脱漏率估算,至2021年底累计接种4 128.71万人(至少接种1剂次),其中3 715.84万人完成2剂次,2012年以来出生目标儿童至少1剂次累计接种率为26.28%,完成2剂次累计接种率为23.65%。
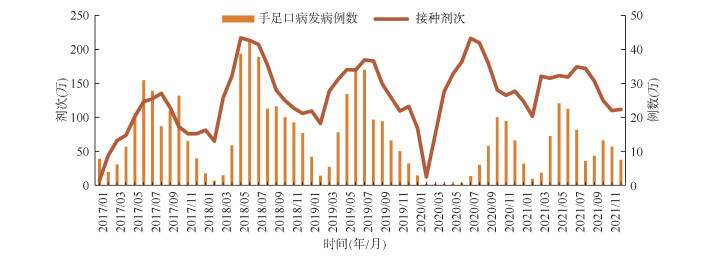
(2) 手足口病发病和EV71灭活疫苗接种时间:EV71灭活疫苗接种和手足口病发病均呈现一定的季节性和周期性。2017-2021年,除2020年受新型冠状病毒感染疫情影响外,其他年份报告病例高峰季节均在5-7月。与之对应,EV71灭活疫苗接种数高峰在每年6-8月。见图 1。
|
| 图 1 2017-2021年手足口病报告病例数和肠道病毒71型灭活疫苗接种剂次数月份分布 |
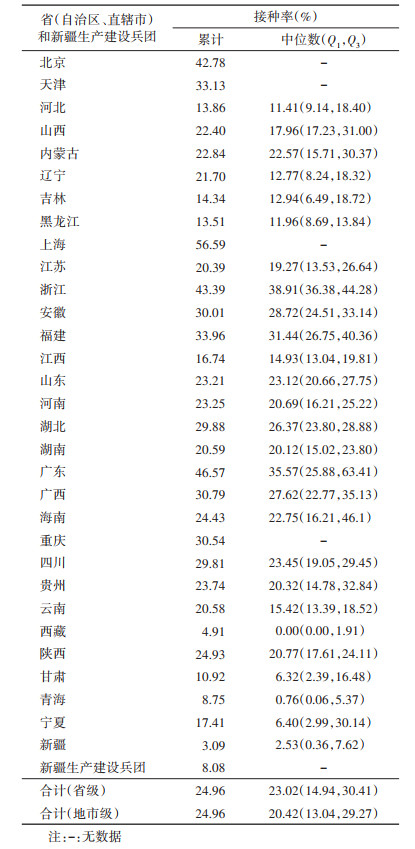
(3) 省级接种率估算:2012年以来,各省出生队列在2021年底EV71灭活疫苗估算累计接种率在3.09%~56.59%之间。估算累计接种率前5位包括上海市(56.59%)、广东省(46.57%)、浙江省(43.39%)、北京市(42.78%)和福建省(33.96%);估算累计接种率后5位包括新疆维吾尔自治区(3.09%)、西藏自治区(4.91%)、新疆生产建设兵团(8.08%)、青海省(8.75%)和甘肃省(10.92%)。见表 2。
(4) 地市级接种率估算:以地市为单位估算2012年以来出生队列在2021年底的累计接种率,位居前5位的地市均在广东省,分别为深圳市(88.17%)、中山市(83.46%)、东莞市(70.47%)、广州市(67.45%)和佛山市(67.06%)。省内各地市的累计接种率差值最大的省份为广东省(74.16%),差值最小的省份为江西省(11.99%)。不同省份的地市级累计接种率最高在14.59%~88.17%之间,最低在0~31.99%之间。
(3) 接种率相关因素分析以省为单位分析各地既往手足口病平均发病率水平、东/中/西部地区分类属性、人均可支配收入、接种单位数、医疗卫生机构数等因素,与2012年以来出生队列估算累计接种率之间的关系进行单因素分析,排除医疗卫生机构数(P > 0.05),将其他因素纳入多因素相关性分析结果发现,人均可支配收入和既往发病率与EV71灭活疫苗累计接种率相关性有统计学意义(P < 0.05)。见表 3。
2016年以来我国自主研发的EV71灭活疫苗陆续上市使用[16]。为了解当前全国EV71灭活疫苗接种现状,本研究利用监测报告数据在全国水平上对EV71灭活疫苗接种现状进行描述性分析,估算不同地区疫苗接种覆盖情况,分析可能的影响因素。结果显示,EV71灭活疫苗作为非免疫规划疫苗已经在全国范围内广泛使用。截至2021年累计接种在7 800万剂次以上,按照2剂次免疫程序估算,全国2012年以后出生儿童EV71灭活疫苗的累计接种率约为25%,但接种率水平在不同地区之间存在较大差异。
本研究根据3种EV71灭活疫苗不同的上市时间、免疫程序规定的适龄儿童年龄范围、2017年以来收集的接种数据进行估算,可反映中国医学科学院医学生物学研究所疫苗覆盖的2012年以来出生儿童、北京科兴生物制品有限公司和武汉生物制品研究所有限责任公司疫苗覆盖的2014年以来出生儿童的接种情况。由于国家层面收集的非免疫规划疫苗接种数据,是接种单位以报表形式每月报告的各疫苗接种汇总剂次数,未收集疫苗种类、接种人数、年龄等明细信息,因此本研究以报告接种数据所能覆盖的全部出生队列人群作为分母,以报告接种剂次数按照2剂次接种程序推算接种人数作为分子,估算了不同行政级别区域的累计接种率。
本研究估算结果与其他地区利用预防接种信息系统收集的接种个案信息分析结果基本一致,但可能略有低估。2012-2018年宁波市出生儿童EV71灭活疫苗接种率为21.97%[7],而本研究估算宁波市2012-2018年出生队列疫苗接种率为20.37%;江苏省基于接种个案信息分析发现,2013-2020年出生队列儿童EV71灭活疫苗接种率为25.91%[17],而本研究估算江苏省2014-2020年出生队列累计接种率为23.57%。表明本研究估算结果基本符合各地实际接种情况。
本研究按照6月龄至5岁免疫程序覆盖的最大年龄范围,估算2012年以来出生队列的累计接种情况,尚不能体现不同年份出生队列的接种情况。EV71灭活疫苗上市早期的一项研究表明,该疫苗实际接种人群主要为1~3岁儿童,占总接种数的84.33%[18]。中国CDC建议EV71灭活疫苗接种对象为≥6月龄易感儿童,越早接种越好,鼓励在12月龄前完成接种程序,以便尽早发挥保护作用[3]。本研究发现,自2018年以后每年EV71灭活疫苗报告接种数稳定在1 700万剂次左右,已超过当年的出生人口数,提示近年来新出生队列的实际接种率,可能会远高于基于2012年以来较为宽泛出生队列估算的平均接种率。
EV71灭活疫苗作为非免疫规划疫苗,受种者自愿自费接种。既往研究表明EV71灭活疫苗的接种与经济、当地疾病流行情况、人口流动情况、接种服务和预防保健资源分配、父母认知、相关宣传工作和当地的政策等多种因素有关[7]。本研究多因素分析结果也显示,既往手足口病发病率水平和人均可支配收入可能是不同地区接种率水平的影响因素,与既往其他非免疫规划疫苗接种率影响因素的研究结果类似[19-20]。疫苗接种水平与地区经济水平密切相关,对于价格较高的非免疫规划疫苗,家庭收入等经济条件可能对疫苗的接受度产生较大影响;既往手足口病发病率较高的地区,EV71灭活疫苗接种率也相对较高,可能是这些地区的专业人员和公众对于疾病的认知较高,更易于接受该疫苗接种。
本研究发现,不仅EV71灭活疫苗接种率地区间存在较大差异,省份、城市间接种率最大差距分别为53.50%、88.17%,而且EV71灭活疫苗每月接种数量呈现明显的季节性波动特点,每年春季接种量逐渐增加,在6-8月接种剂次数达到高峰,之后逐步下降。2020年疫苗接种时间曲线与其他年份差异较大,可能是新型冠状病毒感染疫情防控、各地采取非药物干预措施所致,对当年上半年EV71灭活疫苗接种产生一定影响[21]。EV71灭活疫苗接种量和手足口病发病高峰时间整体呈现基本一致的季节周期性[22],但疫苗接种高峰与手足口病病例报告高峰相比推迟约1~2个月,两者时间上关系不足以证明是疫苗保护作用对疾病季节性流行之间的相互影响,而可能是在手足口病流行高峰季节,相关方对疫苗接种意识均会有所提高,导致了接种服务和行为发生改变,推动了疫苗接种跟随疾病流行呈现了同步的季节性波动。对于季节性流行特征明显的传染性疾病,计划通过疫苗接种对易感者进行有效保护,最佳接种时机应是在传染病流行高峰来临之前完成接种[23]。针对EV71灭活疫苗而言,考虑到EV71母传抗体水平出生后逐渐衰减,在婴儿5~11月龄时最低,而发病最高的年龄组在1~2岁;因此,满6月龄开始及时接种可尽早为易感儿童提供保护,合理把握疫苗接种的最佳时机,在疾病流行季节来临前完成接种。建议进一步开展相关培训和宣传教育,以便有针对性地引导进一步合理使用EV71灭活疫苗。
EV71灭活疫苗上市后真实世界保护效果研究显示,其在个体水平上可有效预防EV71感染导致的手足口病、疱疹性咽峡炎等疾病[4-5, 24]。近年来全国手足口病发病率以及EV71在手足口病例中的占比均有所下降[25-26],但目前我国尚未建立包括EV71的肠道病毒感染所致疾病监测系统,且EV71流行存在周期性,人群易感性也在发生变化,疾病流行减弱是否与EV71灭活疫苗接种相关,有待开展专题研究在群体水平上评估EV71灭活疫苗接种效果。
本研究存在局限性。一是未收集2016年接种数据,疫苗接种的总剂次数略有低估。2016年下半年,中国医学科学院医学生物学研究所和北京科兴生物制品有限公司共有687.64万剂批签发量,假设在2016年全部使用,其对累计接种率低估的相对影响在2个百分点左右。但由于疫苗生产、供应到接种实施均需要时间,参考2018年以来当年累计批签发数与累计接种剂次数的差值,均为2 400万~2 600万,推测2016年批签发量实际不可能在当年均完成接种,该因素导致低估的累计接种率预计不超过2%。二是接种数据由基层接种单位按照预防接种工作规范要求逐级汇总报告,可能存在漏报或错报,但本研究结果与部分地区既往研究结果的一致性较好,表明该因素对本研究结果影响有限。三是接种剂次数为机构汇总信息而非接种个案信息,无法深入分析接种对象特征和全程接种等情况。
综上所述,尽管EV71灭活疫苗已经在全国范围广泛使用,但疫苗接种覆盖情况存在地区间不平衡,地区经济水平可能是影响疫苗接种率的重要因素,疾病流行强度可能对疫苗的接受程度和接种服务模式产生一定影响。EV71灭活疫苗接种对手足口病流行的影响仍需要进一步开展更多的专题研究。
利益冲突 所有作者声明无利益冲突
作者贡献声明 张琳:查阅文献、数据分析、论文撰写/修改;曹雷:数据收集、论文指导/修改;李燕、唐林、李克莉、尹遵栋:论文指导/修改;胡莹雪:查阅文献、数据分析;安志杰:研究设计、论文指导/修改
| [1] |
Lei DL, Griffiths E, Martin J. WHO working group meeting to develop WHO Recommendations to assure the quality, safety and efficacy of enterovirus 71 vaccines[J]. Vaccine, 2020, 38(32): 4917-4923. DOI:10.1016/j.vaccine.2020.05.001 |
| [2] |
Xiao J, Zhu Q, Yang F, et al. The impact of enterovirus A71 vaccination program on hand, foot, and mouth disease in Guangdong, China: a longitudinal surveillance study[J]. J Infect, 2022, 85(4): 428-435. DOI:10.1016/j.jinf.2022.06.020 |
| [3] |
中国疾病预防控制中心. 肠道病毒71型灭活疫苗使用技术指南[J]. 中国疫苗和免疫, 2016, 22(4): 458-464. Chinese Center for Disease Control and Prevention. Guidelines for use of inactivated enterovirus type 71 vaccine[J]. Chin J Vaccines Immun, 2016, 22(4): 458-464. DOI:10.19914/j.cjvi.2016.04.020 |
| [4] |
Li Y, Zhou YH, Cheng YB, et al. Effectiveness of EV-A71 vaccination in prevention of paediatric hand, foot, and mouth disease associated with EV-A71 virus infection requiring hospitalisation in Henan, China, 2017-18: a test-negative case-control study[J]. Lancet Child Adolesc Health, 2019, 3(10): 697-704. DOI:10.1016/S2352-4642(19)30185-3 |
| [5] |
Jiang LN, Wang J, Zhang C, et al. Effectiveness of enterovirus A71 vaccine in severe hand, foot, and mouth disease cases in Guangxi, China[J]. Vaccine, 2020, 38(7): 1804-1809. DOI:10.1016/j.vaccine.2019.12.025 |
| [6] |
Li ZQ, Qin ZQ, Tan HF, et al. Analysis of the coverage of inactivated enterovirus 71 (EV71) vaccine and adverse events following immunization with the EV71 vaccine among children from 2016 to 2019 in Guangzhou[J]. Expert Rev Vaccines, 2021, 20(7): 907-918. DOI:10.1080/14760584.2021.1933451 |
| [7] |
Ye LX, Chen JP, Fang T, et al. Vaccination coverage estimates and utilization patterns of inactivated enterovirus 71 vaccine post vaccine introduction in Ningbo, China[J]. BMC Public Health, 2021, 21(1): 1118. DOI:10.1186/s12889-021-11198-6 |
| [8] |
中国食品药品检定研究院. 中检院生物制品批签发信息公示表[EB/OL]. [2022-03-21]. https://www.nifdc.org.cn/nifdc/.
|
| [9] |
付凌晖, 刘爱华. 2人口: 2-5分地区年末人口数[M]//国家统计局. 2021中国统计年鉴. 北京: 中国统计出版社, 2021: 34. Fu LH, Liu AH. 2 Population: 2-5 Population at year-end by region[M]//National Bureau of Statistics. 2021 China statistical yearbook. Beijing: China Statistics Press, 2021: 34. |
| [10] |
国家统计局. 国民经济和社会发展统计公报[EB/OL]. (2022-02-28)[2022-04-21]. http://www.stats.gov.cn/tjsj/zxfb/202202/t20220227_1827960.html.
|
| [11] |
陈小龙. (三)经济发展: 2-9地区生产总值[M]//国家统计局城市社会经济调查司. 2019中国城市统计年鉴. 北京: 中国统计出版社, 2020: 69-75.
|
| [12] |
孙辉峰. 中国基层预防接种服务现状及趋势研究[D]. 北京: 中国疾病预防控制中心, 2020. DOI: 10.27511/d.cnki.gzyyy.2020.000077. Sun HF. The study on the current status and trend of primary vaccination services in China[D]. Beijing: Chinese Center for Disease Control and Prevention, 2020. DOI: 10.27511/d.cnki.gzyyy.2020.000077. |
| [13] |
李嘉铃, 韦俞伽, 董柏青, 等. 2008-2017年我国手足口病发病和死亡变化趋势研究[J]. 疾病监测, 2022, 37(2): 233-240. Li JL, Wei YJ, Dong BQ, et al. Trends of morbidity and mortality of hand foot and mouth disease in China, 2008-2017[J]. Dis Surveill, 2022, 37(2): 233-240. DOI:10.3784/jbjc.202107090395 |
| [14] |
World Health Organization. Immunization in practice: a practical guide for health staff[EB/OL]. (2015-05-31)[2022-05-13]. https://www.who.int/publications/i/item/immunization-in-practice-a-practical-guide-for-health-staff.
|
| [15] |
吴琳琳, 刘捷宸, 邵慧勇, 等. 上海市儿童肠道病毒71型灭活疫苗接种率和疑似预防接种异常反应监测[J]. 中国疫苗和免疫, 2020, 26(1): 62-66, 81. Wu LL, Liu JC, Shao HY, et al. Surveillance for coverage of inactivated enterovirus 71 (EV71) vaccine and adverse events following immunization with EV71 vaccine among children in Shanghai[J]. Chin J Vaccines Immun, 2020, 26(1): 62-66, 81. DOI:10.19914/j.cjvi.2020.01.014 |
| [16] |
于静, 汤奋扬, 汪志国, 等. 江苏省2013-2020年出生队列儿童肠道病毒71型疫苗接种率[J]. 中国疫苗和免疫, 2021, 27(5): 566-569. Yu J, Tang FY, Wang ZG, et al. Coverage levels of enterovirus 71 vaccine among the 2013-2020 birth cohorts in Jiangsu province[J]. Chin J Vaccines Immun, 2021, 27(5): 566-569. DOI:10.19914/j.CJVI.2021100 |
| [17] |
龙遗芳, 李胜峰, 谢莘, 等. 广东省2017年肠道病毒71型灭活疫苗接种现况分析[J]. 华南预防医学, 2018, 44(4): 349-351. Long YF, Li SF, Xie X, et al. Current status of inoculating inactivated enterovirus 71 vaccine in Guangdong Province, 2017[J]. South China J Prev Med, 2018, 44(4): 349-351. DOI:10.13217/j.scjpm.2018.0349 |
| [18] |
刘艳, 岳晨妍, 李燕, 等. 中国六省份儿童LLR株轮状病毒口服减毒活疫苗接种现状分析[J]. 中华预防医学杂志, 2018, 52(3): 282-286. Liu Y, Yue CY, Li Y, et al. Analysis of vaccination situation of orial live attenuated rotavirus vaccine (LLR strain) among children in 6 provinces of China[J]. Chin J Prev Med, 2018, 52(3): 282-286. DOI:10.3760/cma.j.issn.0253-9624.2018.03.012 |
| [19] |
Li Y, Yue CY, Wang YM, et al. Utilization pattern of Haemophilus influenza type b vaccine in eight provinces of China[J]. Hum Vaccines Immunother, 2018, 14(4): 894-899. DOI:10.1080/21645515.2017.1420447 |
| [20] |
杨芬, 梁文佳, 孙立梅, 等. 广东省EV71疫苗接种水平与手足口病流行分析[J]. 中国公共卫生, 2020, 36(3): 351-354. Yang F, Liang WJ, Sun LM, et al. Innoculation of enterorirus 71 vaccine and incidence of hand-foot-mouth disease in Guangdong province[J]. Chin J Public Health, 2020, 36(3): 351-354. DOI:10.11847/zgggws1119741 |
| [21] |
Goyal D, Hunt X, Kuper H, et al. Impact of the COVID-19 pandemic on people with disabilities and implications for health services research [J/OL]. J Health Serv Res Policy, 2023: 13558196231160047. DOI: 10.1177/13558196231160047.
|
| [22] |
Wang XL, An ZJ, Huo D, et al. Enterovirus A71 vaccine effectiveness in preventing enterovirus A71 infection among medically-attended hand, foot, and mouth disease cases, Beijing, China[J]. Hum Vaccines Immunother, 2019, 15(5): 1183-1190. DOI:10.1080/21645515.2019.1581539 |
| [23] |
国家免疫规划技术工作组流感疫苗工作组. 中国流感疫苗预防接种技术指南(2020-2021)[J]. 中华流行病学杂志, 2020, 41(10): 1555-1576. National Immunization Advisory Committee (NIAC) Technical Working Group (TWG), Influenza Vaccination TWG. Technical guidelines for seasonal influenza vaccination in China (2020-2021)[J]. Chin J Epidemiol, 2020, 41(10): 1555-1576. DOI:10.3760/cma.j.cn112338-20200904-01126 |
| [24] |
王小莉. 北京市手足口病疾病负担及其EV-A71疫苗接种效果的评价研究[D]. 北京: 中国疾病预防控制中心, 2019. Wang XL. Study on the burden of hand, foot, and mouth disease and the effectiveness evaluation of the EV-A71 vaccination program in Beijing[D]. Beijing: Chinese Center for Disease Control and Prevention, 2019. |
| [25] |
潘伟毅, 赵志远, 陈俊磊. 2017~2018年福建省0~5岁儿童出生队列肠道病毒71型疫苗接种率分析[J]. 中国生物制品学杂志, 2020, 33(3): 293-296. Pan WY, Zhao ZY, Chen JL. Birth cohort analysis on inoculation rate of enterovirus 71 vaccine among children at ages of 0-5 years in Fujian Province, China from 2017 to 2018[J]. Chin J Biol, 2020, 33(3): 293-296. DOI:10.13200/j.cnki.cjb.003009 |
| [26] |
曹玲生, 郑景山, 曹雷, 等. 中国2009年儿童预防接种信息管理系统实施进展[J]. 中国疫苗和免疫, 2010, 16(4): 346-348, 365. Cao LS, Zheng JS, Cao L, et al. Progress of childhood immunization information management system in China in 2009[J]. Chin J Vaccines Immun, 2010, 16(4): 346-348, 365. DOI:10.19914/j.cjvi.2010.04.017 |
 2023, Vol. 44
2023, Vol. 44