文章信息
- 赵峥, 洪洁, 苏晴, 黄家祺, 陈希, 乐佳徐, 胡艺, 常昭瑞, 张志杰.
- Zhao Zheng, Hong Jie, Su Qing, Huang Jiaqi, Chen Xi, Le Jiaxu, Hu Yi, Chang Zhaorui, Zhang Zhijie
- 基于真实世界数据研究肠道病毒A71型疫苗对手足口病发病影响的研究进展
- A review on using real-world data to study the impact of Enterovirus A71 vaccine on the incidence of hand, foot and mouth disease
- 中华流行病学杂志, 2023, 44(2): 310-316
- Chinese Journal of Epidemiology, 2023, 44(2): 310-316
- http://dx.doi.org/10.3760/cma.j.cn112338-20220417-00310
-
文章历史
收稿日期: 2022-04-17
2. 中国疾病预防控制中心传染病管理处, 北京 100032
2. Division of Infectious Disease Management, Chinese Center for Disease Control and Prevention, Beijing 100032, China
手足口病(HFMD)是由多种肠道病毒(EVs)引起的儿童常见传染性疾病,通过接触传播,传染性强,易引起暴发或流行,起病急,典型症状为发热,手、足、口等部位斑丘疹或疱疹,破溃后形成溃疡。少数患儿可引起脑炎、心肌炎、肺水肿等并发症,甚至死亡[1]。近20年来,HFMD在多个国家暴发和流行,造成重大疾病负担。2008年5月,我国将HFMD纳入《中华人民共和国传染病防治法》中丙类法定报告传染病管理。在所有39种法定传染病中,HFMD是导致≤5岁儿童死亡的主要原因[2]。我国引起HFMD常见的病毒血清型是肠道病毒A71型(EV-A71)和柯萨奇病毒A16型(CV-A16)[3],其中EV-A71是导致HFMD重症和死亡的主要原因,感染EV-A71与70%的重症病例和92%的死亡病例有关[4-5]。
目前,全球有5家机构均已研发EV-A71灭活疫苗(新加坡Inviragen公司、中国台湾地区国立健康研究所、中国北京微谷生物医药有限公司、北京科兴生物制品有限公司和中国医学科学院医学生物学研究所)[6]。2015年12月,中国医学科学院医学生物学研究所研制的EV-A71单价灭活全病毒疫苗在我国获得许可;北京科兴生物制品有限公司和北京微谷生物医药有限公司研发的EV-A71疫苗也分别在2016年1月和2017年3月获批[7]。2016年,该疫苗逐步在我国各省(市)医疗中心上市,接种目标人群为6~59月龄儿童。为达到最佳效果,鼓励从≥6月龄儿童完成2剂疫苗接种,时间间隔1个月。
在对30 000余名6~35月龄健康儿童进行的Ⅲ期临床试验中发现,接种已获批准的3种疫苗对EV-A71感染所致HFMD保护效力均 > 90%,对EV-A71感染所致的HFMD重症病例保护效力达到100%[8-10]。免疫后2年延续性随访的结果显示,3种疫苗在接种人群2次接种后2年血清转化率保持≥95%,保护持久性良好;且接种后不良反应发生率均在可耐受的范围内,具有良好的安全性[11-13]。尽管多项临床随机对照试验确定了EV-A71疫苗在研究对象中的有效性,但现实环境的接种者不再是经严格标准选入的受试对象,EV-A71疫苗在真实应用中对HFMD的影响仍然未知,而研究真实世界中EV-A71疫苗对HFMD发病的影响对EV-A71疫苗接种计划和HFMD防控策略的实施具有重要科学意义。本研究进行文献检索,对EV-A71疫苗在真实应用中对HFMD影响的相关研究进展进行较全面地回顾与分析,为EV-A71疫苗免疫接种对预防儿童HFMD的有效性提供来自真实世界的有力依据,为今后评估EV-A71疫苗及其他疫苗的短期效果、长期影响等相关研究提供指导和参考。
二、文献检索策略与筛选以“[Title:(hand AND foot AND mouth)OR HFMD OR‘enterovirus 71’ OR ‘EV-A71’ OR ‘EV*71’* Title/Abstract:(vaccine OR vaccination OR immunization strategy)AND(effectiveness OR efficacy OR impact)]”为检索式在PubMed、Web of Science和Elsevier Science Direct数据库中检索英文文献;以“题名:(手足口病+HFMD+肠*病毒+‘EV’)* 摘要:[(疫苗+免疫)*(效果+作用+影响)]”为检索式在中国知网(CNKI)和万方数据知识服务平台中检索中文文献。检索日期截至2022年3月30日,共检索1 456篇文献,经过文献查重和筛选,最终纳入18篇文献。见图 1。
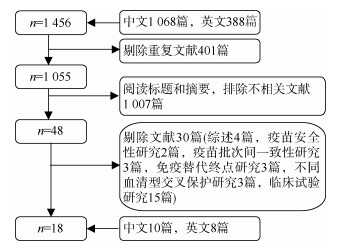
|
| 图 1 基于真实世界数据研究肠道病毒A71型疫苗对手足口病发病影响的文献筛选流程 |
目前基于真实世界数据评估EV-A71疫苗对HFMD影响的研究主要分为3大类:检测阴性设计(test-negative design,TND)病例对照研究、生态学研究和数学流行病学分析。
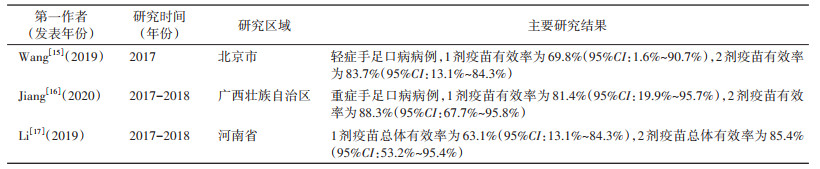
1. TND病例对照研究:基于医疗服务机构的就诊人群,将符合某种或某些临床症状或特征的疑似病例均纳入研究,通过特异性的实验室检测进行确诊,将符合目标疾病的病原体检测阳性的患者归为病例组,而检测阴性的患者归为对照组,同时收集其早期的免疫接种史。然后比较两组间的疫苗接种比例,从而评价疫苗的保护效果[14]。近10年来,TND被广泛用于疫苗上市后的效果评价。通过文献回顾,EV-A71疫苗在真实应用中对HFMD发病影响的研究中有3项针对6~71月龄住院患儿进行TND研究,分别估计HFMD病例(轻、重症)的接种1剂和(或)2剂EV-A71疫苗的有效率,结果显示,接种1剂疫苗的有效率均 > 60%,2剂疫苗有效率均 > 70%,虽然均低于临床试验结果,但接种EV-A71疫苗仍可有效预防EV-A71感染所致HFMD[15-17]。见表 1。
2. 生态学研究:
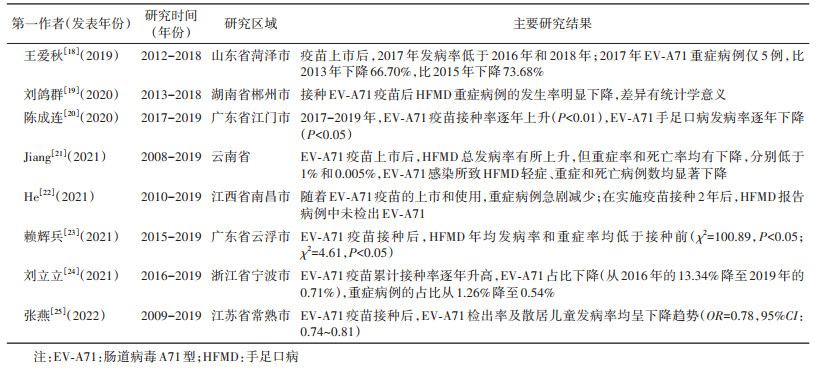
(1)描述性分析:8项研究通过直观地对比、分析在EV-A71疫苗上市前后两阶段HFMD总病例数、重症病例数或死亡病例数的变化,或EV-A71、CV-A16和其他亚型阳性检出率在两阶段的变化,采用χ2检验、秩和检验等比较差异的显著性,发现接种EV-A71疫苗后HFMD发病率所有降低、HFMD重症率及死亡率显著降低,或EV-A71的阳性率明显下降[18-25]。见表 2。
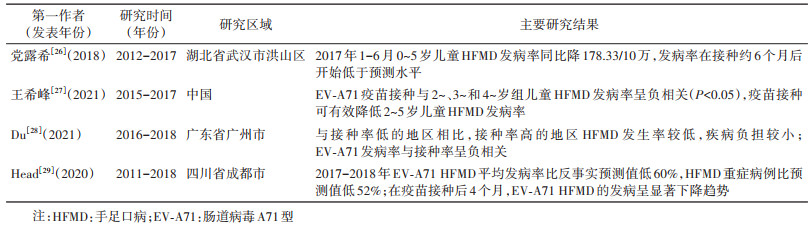
(2)单因素分析:3项研究分析EV-A71疫苗接种率、是否进行疫苗接种等与HFMD发病率的关系,评估EV-A71疫苗对HFMD发病的影响。党露希等[26]通过拟合时间序列模型,反事实预测武汉市洪山区在EV-A71疫苗上市后(2016年8月至2017年12月)HFMD发病率,结果显示,自2017年1月起HFMD实际发病率低于预测值,同年发病高峰期4-6月发病率较往年均值同比下降178.33/10万。王希峰等[27]基于2015-2017年我国≤5岁儿童HFMD发病率的月度数据,以大部分地区正式引进EV-A71疫苗的时间(2016年8月)为干预点,将研究时间分为干预前阶段(2015年1月至2016年7月)和干预后阶段(2016年8月至2017年12月),构建中断时间序列分析发现,接种EV-A71疫苗可有效降低2~5岁儿童的HFMD发病率。Du等[28]根据2016-2018年广州市各区月度EV-A71疫苗接种率,将11个区划分为高和低接种率地区分析发现,高接种率地区的HFMD发病率较低。见表 3。
(3)多因素分析:Du等[28]除考虑疫苗接种外,同时纳入温度和相对湿度等因素,拟合时间序列回归模型,结果显示疫苗接种率的回归系数为负值(P < 0.001),表明接种率越高,EV-A71 HFMD病例数越少。Head等[29]基于疫苗上市前(2011-2015年)HFMD发病率,综合考虑EV-A71疫苗接种率、不同年龄组人口数、发病月份以及群体免疫等因素,拟合广义线性模型和随机森林模型,对疫苗上市后(2017-2018年)HFMD发病率进行反事实预测,结果显示,EV-A71平均HFMD发病率比预测值低60%,重症病例比预测值低52%。见表 3。
3. 数学流行病学分析:传播动力学模型是传染病研究领域中的一个重要工具,它着眼于传染病的传播机制,根据人群在疾病传播过程中所处的不同状态或环节形成对应的仓室,人群随着自身感染状态的变化在仓室间移动,并通过增删、细分仓室来模拟真实情景,开展疾病的流行规律研究,目前已被广泛应用于HFMD的研究中。不同于“理想环境”下的临床试验研究,研究者可借助数学流行病学分析,根据真实世界中不同地区的人口学特征、社会经济水平、卫生资源和生活方式等影响HFMD在人群内传播及流行的相关重要因素,获取研究区域内HFMD传播动力学参数,建立传播动力学模型,模拟HFMD的传播过程,从而分析、量化系列防控措施如疫苗接种、隔离、健康教育等对HFMD的影响。在文献回顾中,发现有3项研究基于传播动力学模型,通过模拟不同场景(如不同疫苗接种率等)来评价其对HFMD的影响,研究结果都表明EV-A71疫苗接种对于HFMD的控制具有积极作用,且随着疫苗接种率的提高,EV-A71 HFMD的发病数将逐渐减少[30-33]。见表 4。
EV-A71疫苗上市前的临床试验研究是在“理想环境”下对疫苗的保护效力进行评价,疫苗上市后,由于接种人群(包括接种人群特征、免疫前抗体水平等)、疾病流行模式(包括流行强度、流行株等)以及接种实施(包括接种针次、接种方法、冷链状况等)的影响,临床试验结果并不完全适用于真实世界中EV-A71疫苗对HFMD的影响。同时,在临床试验中,EV-A71疫苗的有效性是基于100%接种率估计的,这并不能反映实际接种环境中的疫苗覆盖率。因此,了解EV-A71疫苗在真实应用中对HFMD发病的影响是十分必要的,这对EV-A71疫苗接种计划和HFMD防控策略的实施具有重要意义。
通过全面的文献检索与系统回顾,发现我国目前基于真实世界数据评估EV-A71疫苗对HFMD影响的研究较少,研究范围均局限于一个省或市;大部分研究采用TND病例对照研究设计或仅进行较为简单的生态学描述性分析,并未校正其他影响HFMD发病因素(如温度、相对湿度等气象因素、人口年龄结构、国内生产总值等社会人口因素)的作用;其余通过构建时间序列模型、传播动力学模型等估计EV-A71疫苗在真实应用中对HFMD影响的研究,也未对除疫苗接种外的其他HFMD发病相关影响因素进行综合全面地考虑,且动力学模型相关研究在建立模型时做了一些假定,这些假定可能与实际存在偏差,对研究结果有一定的影响。
以往研究证明,EV-A71免疫血清对CV-A16和CV-A6等病原亚型没有交叉保护作用[9-10]。有文献报道,虽然EV-A71疫苗对CV-A16和其他肠道病毒感染所致的HFMD没有预防作用,但对EV-A71的不同基因型均具有良好的交叉保护作用[34-36]。由此可见,接种EV-A71疫苗最大意义在于预防由EV-A71感染引起的HFMD,尤其是减少重症和死亡病例的发生[37]。在2012年以前,EV-A71和CV-A16是引起HFMD的主要血清型;2013年后,以CV-A6为主的其他肠道病毒成为引起我国HFMD的优势病原。2019年和2020年实验室确诊病例中,EV-A71的构成比仅为10%~13%,处于较低水平。未对HFMD的病原亚型加以分型,直接评估EV-A71疫苗接种对全因HFMD的影响,可能会掩盖EV-A71疫苗接种的积极作用。
因此,在真实世界中,接种EV-A71疫苗对我国儿童HFMD的发病和传播的影响及其程度,目前尚不清楚,还需进一步研究与量化分析,以提供较强的科学证据,如基于覆盖我国较大范围的数据,选取病原学监测系统较完善、监测数据较完整的地区,结合有明确来源的疫苗接种率数据,综合考虑气象因素、社会经济和自然环境等相关因素对HFMD的作用,在此基础上精细分析与评估接种EV-A71疫苗对EV-A71和非EV-A71 HFMD的影响,以阐明EV-A71疫苗在真实应用中对我国儿童HFMD发病的影响,明确其短期和长期效果,从而为EV-A71疫苗接种计划和HFMD防控策略的科学制定提供重要参考依据。
近年来,我国HFMD流行规律保持不变,HFMD总体呈现隔年高发、偶数年份流行增强。春季和初夏为发病主要高峰,秋季在南方地区有1个小高峰。根据2008-2020年全国HFMD发病数据,春、夏季(4-7月)和秋季(9-10月)2个发病高峰的HFMD总发病数在2008-2020年占比 > 75%。因此相对于HFMD高发年份、每年发病高峰期,在HFMD低发年份、每年低发月份,由于HFMD发病数本身较少,接种EV-A71疫苗的作用可能无法得以显著体现。由于目前EV-A71疫苗属于自愿和自费接种的二类疫苗,尚未纳入到国家免疫规划中。自2016年EV-A71疫苗上市后,截至2019年年底,我国EV-A71疫苗的累计接种率仅为22%,各省(市)免疫接种率相差较大(1%~50%)。EV-A71疫苗两剂次均价400元的接种费用是我国经济发达地区与经济欠发达地区的接种率存在明显差异的重要因素之一。目前EV-A71疫苗的目标人群为6月龄至5岁,我国HFMD发病和死亡主要为12~23月龄儿童[38]。因此,今后研究可细分为6~11月龄、12~23月龄和2~5岁年龄组,在奇数年和偶数年流行周期的发病率、死亡率和疫苗接种率等,精细研究不同年龄组儿童接种EV-A71疫苗对HFMD的作用,为EV-A71疫苗接种计划及其优化进一步提供有效依据。
利益冲突 所有作者声明无利益冲突
作者贡献声明 赵峥、洪洁:研究设计、论文撰写、数据分析、论文修改;苏晴、陈希、乐侍徐:数据收集与整理;黄家祺:英文校对、审阅文章;胡艺:审阅文章;常昭瑞:研究指导、审阅文章;张志杰:审阅文章、经费支持
| [1] |
邓强, 王子晨, 吴沁, 等. 新型冠状病毒疫苗的研究进展[J]. 暨南大学学报: 自然科学与医学版, 2020, 41(6): 511-519. Deng Q, Wang ZC, Wu Q, et al. Research progress of COVID-19 vaccines[J]. J Jinan Univ: Nat Sci Med Ed, 2020, 41(6): 511-519. DOI:10.11778/j.jdxb.2020.06.006 |
| [2] |
Li Y, Wang LW, Pang LY, et al. The data fitting and optimal control of a hand, foot and mouth disease (HFMD) model with stage structure[J]. Appl Math Comput, 2016, 276: 61-74. DOI:10.1016/j.amc.2015.11.090 |
| [3] |
Xing WJ, Liao QH, Viboud C, et al. Hand, foot, and mouth disease in China, 2008-12: an epidemiological study[J]. Lancet Infect Dis, 2014, 14(4): 308-318. DOI:10.1016/S1473-3099(13)70342-6 |
| [4] |
Bian LL, Wang YP, Yao X, et al. Coxsackievirus A6: a new emerging pathogen causing hand, foot and mouth disease outbreaks worldwide[J]. Exp Rev Anti Infect Ther, 2015, 13(9): 1061-1071. DOI:10.1586/14787210.2015.1058156 |
| [5] |
Ji H, Fan H, Lu PX, et al. Surveillance for severe hand, foot, and mouth disease from 2009 to 2015 in Jiangsu province: epidemiology, etiology, and disease burden[J]. BMC Infect Dis, 2019, 19(1): 79. DOI:10.1186/s12879-018-3659-7 |
| [6] |
包丽娟, 许富民, 梁兴业. 国内手足口病流行病学特征及疫苗研究进展[J]. 微生物学免疫学进展, 2020, 48(6): 82-86. Bao LJ, Xu FM, Liang XY. Epidemiology and progress on vaccine research for hand-foot-mouth disease in China[J]. Prog Microbiol Immunol, 2020, 48(6): 82-86. DOI:10.13309/j.cnki.pmi.2020.06.015 |
| [7] |
童叶青, 胡兴周, 李航, 等. 手足口病疫苗研究进展[J]. 中国药师, 2018, 21(9): 1655-1658. Tong YQ, Hu XZ, Li H, et al. Research progress in HFMD vaccine[J]. Chin Pharm, 2018, 21(9): 1655-1658. DOI:10.3969/j.issn.1008-049X.2018.09.039 |
| [8] |
Zhu FC, Xu WB, Xia JL, et al. Efficacy, safety, and immunogenicity of an enterovirus 71 vaccine in China[J]. N Engl J Med, 2014, 370(9): 818-828. DOI:10.1056/NEJMoa1304923 |
| [9] |
Zhu FC, Meng FY, Li JX, et al. Efficacy, safety, and immunology of an inactivated alum-adjuvant enterovirus 71 vaccine in children in China: a multicentre, randomised, double-blind, placebo-controlled, phase 3 trial[J]. Lancet, 2013, 381(9882): 2024-2032. DOI:10.1016/S0140-6736(13)61049-1 |
| [10] |
Li RC, Liu LD, Mo ZJ, et al. An inactivated enterovirus 71 vaccine in healthy children[J]. N Engl J Med, 2014, 370(9): 829-837. DOI:10.1056/NEJMoa1303224 |
| [11] |
Wei MW, Meng FY, Wang SY, et al. 2-year efficacy, immunogenicity, and safety of vigoo enterovirus 71 vaccine in healthy Chinese children: a randomized open-label study[J]. J Infect Dis, 2017, 215(1): 56-63. DOI:10.1093/infdis/jiw502 |
| [12] |
Li JX, Song YF, Wang L, et al. Two-year efficacy and immunogenicity of Sinovac Enterovirus 71 vaccine against hand, foot and mouth disease in children[J]. Expert Rev Vaccines, 2016, 15(1): 129-137. DOI:10.1586/14760584.2016.1096782 |
| [13] |
Liu LD, Mo ZJ, Liang ZL, et al. Immunity and clinical efficacy of an inactivated enterovirus 71 vaccine in healthy Chinese children: a report of further observations[J]. BMC Med, 2015, 13: 226. DOI:10.1186/s12916-015-0448-7 |
| [14] |
张力, 金鹏飞, 李靖欣, 等. 检测阴性设计在疫苗效果评价中的应用[J]. 中华流行病学杂志, 2020, 41(2): 280-283. Zhang L, Jin PF, Li JX, et al. Application of test-negative design in vaccine efficacy evaluation[J]. Chin J Epidemiol, 2020, 41(2): 280-283. DOI:10.3760/cma.j.issn.0254-6450.2020.02.024 |
| [15] |
Wang XL, An ZJ, Huo D, et al. Enterovirus A71 vaccine effectiveness in preventing enterovirus A71 infection among medically-attended hand, foot, and mouth disease cases, Beijing, China[J]. Hum Vaccin Immunother, 2019, 15(5): 1183-1190. DOI:10.1080/21645515.2019.1581539 |
| [16] |
Jiang LN, Wang J, Zhang C, et al. Effectiveness of enterovirus A71 vaccine in severe hand, foot, and mouth disease cases in Guangxi, China[J]. Vaccine, 2020, 38(7): 1804-1809. DOI:10.1016/j.vaccine.2019.12.025 |
| [17] |
Li Y, Zhou YH, Cheng YB, et al. Effectiveness of EV-A71 vaccination in prevention of paediatric hand, foot, and mouth disease associated with EV-A71 virus infection requiring hospitalisation in Henan, China, 2017-18: a test-negative case-control study[J]. Lancet Child Adolesc Health, 2019, 3(10): 697-704. DOI:10.1016/S2352-4642(19)30185-3 |
| [18] |
王爱秋, 刘海云. EV71型手足口病疫苗的效果评价[J]. 中国现代医生, 2019, 57(16): 143-147. Wang AQ, Liu HY. Evaluation of the effect of type EV71 vaccine for hand, foot and mouth disease[J]. China Mod Doctor, 2019, 57(16): 143-147. |
| [19] |
刘鸽群, 谭徽, 李成华, 等. 2013-2018年郴州市手足口病流行病学特征及EV71疫苗接种效果分析[J]. 中国公共卫生, 2020, 36(3): 385-388. Liu GQ, Tan H, Li CH, et al. Incidence of hand, foot and mouth disease and effect of EV71 vaccine vaccination in Chenzhou city of Hunan province, 2013-2018[J]. Chin J Pub Health, 2020, 36(3): 385-388. DOI:10.11847/zgggws1127276 |
| [20] |
陈成连, 陈阿群, 李昕韵, 等. 2017-2019年江门市肠道病毒71型灭活疫苗接种水平与手足口病流行病学分析[J]. 华南预防医学, 2020, 46(4): 424-426. Chen CL, Chen AQ, Li XY, et al. Epidemiological analysis of hand, foot, and mouth disease and vaccination level of inactivated enterovirus 71 vaccine in Jiangmen, 2017-2019[J]. South Chin J Prev Med, 2020, 46(4): 424-426. DOI:10.12183/j.scjpm.2020.0424 |
| [21] |
Jiang L, Jiang HC, Tian X, et al. Epidemiological characteristics of hand, foot, and mouth disease in Yunnan Province, China, 2008-2019[J]. BMC Infect Dis, 2021, 21(1): 751. DOI:10.1186/s12879-021-06462-4 |
| [22] |
He FL, Rui J, Deng ZQ, et al. Surveillance, epidemiology and impact of EV-A71 vaccination on hand, foot, and mouth disease in Nanchang, China, 2010-2019[J]. Front Microbiol, 2021, 12: 811553. DOI:10.3389/fmicb.2021.811553 |
| [23] |
赖辉兵, 王娟, 陈秋玲, 等. 2015-2019年云浮市手足口病流行病学与EV71灭活疫苗接种效果分析[J]. 现代预防医学, 2021, 48(12): 2268-2271, 2285. Lai HB, Wang J, Chen QL, et al. Incidence of hand, foot and mouth disease and effect of enterovirus 71 vaccine vaccination in Yunfu city of Guangdong province, 2015-2019[J]. Mod Prev Med, 2021, 48(12): 2268-2271, 2285. |
| [24] |
刘立立, 刘志科, 张良, 等. 2016-2019年宁波市5岁及以下儿童手足口病流行病学特征[J]. 北京大学学报: 医学版, 2021, 53(3): 491-497. Liu LL, Liu ZK, Zhang L, et al. Epidemiological and etiological characteristics of hand, foot and mouth disease among children aged 5 years and younger in Ningbo (2016 to 2019)[J]. J Peking Univ: Health Sci, 2021, 53(3): 491-497. DOI:10.19723/j.issn.1671-167X.2021.03.009 |
| [25] |
张燕, 龚利强, 任宇花, 等. 2009-2019年常熟市手足口病流行特征及EV 71疫苗接种效果分析[J]. 医学动物防制, 2022, 38(2): 117-122. Zhang Y, Gong LQ, Ren YH, et al. Analysis on prevalence characteristics of HFMD and EV 71 vaccination effect in Changshu from 2009 to 2019[J]. J Med Pest Control, 2022, 38(2): 117-122. DOI:10.7629/yxdwfz202202004 |
| [26] |
党露希, 王灿, 鲍武波, 等. 武汉市洪山区EV71疫苗防控效果初探[J]. 现代预防医学, 2018, 45(3): 446-448, 461. DOI:CNKI:SUN:XDYF.0.2018-03-017. Dang LX, Wang C, Bao WB, et al. Prevention and control effect of enterovirus 71 vaccine inoculation on HFMD in Hongshan District, Wuhan[J]. Mod Prev Med, 2018, 45(3): 446-448, 461. DOI:CNKI:SUN:XDYF.0.2018-03-017. |
| [27] |
王希峰, 朱大伟, 袁莎莎. EV71疫苗对中国大陆地区儿童手足口病发病率影响间断时间序列分析[J]. 中国公共卫生, 2021, 37(9): 1418-1420. Wang XF, Zhu DW, Yuan SS. Impact of enterovirus 71 vaccine vaccination on incidence of hand, foot and mouth disease among children in China mainland: an interrupted time series analysis[J]. Chin J Public Health, 2021, 37(9): 1418-1420. DOI:10.11847/zgggws1129426 |
| [28] |
Du ZC, Huang Y, Bloom MS, et al. Assessing the vaccine effectiveness for hand, foot, and mouth disease in Guangzhou, China: a time-series analysis[J]. Hum Vaccin Immunother, 2021, 17(1): 217-223. DOI:10.1080/21645515.2020.1763076 |
| [29] |
Head JR, Collender PA, Lewnard JA, et al. Early evidence of inactivated enterovirus 71 vaccine impact against hand, foot, and mouth disease in a major center of ongoing transmission in China, 2011-2018: a longitudinal surveillance study[J]. Clin Infect Dis, 2020, 71(12): 3088-3095. DOI:10.1093/cid/ciz1188 |
| [30] |
李斌. 基于人群的EV71疫苗上市后保护效果评估——以广东省EV71所致手足口病为例[D]. 桂林: 桂林电子科技大学, 2021. DOI: Li B. Protective effectiveness of the enterovirus 71 vaccine on enterovirus 71 associated hand, foot and mouth disease-a population-based study in Guangdong Province[D]. Guilin: Guilin University of Electronic Technology, 2021. DOI: |
| [31] |
Shi L, Zhao HY, Wu DY. Modelling and analysis of HFMD with the effects of vaccination, contaminated environments and quarantine in mainland China[J]. Math Biosci Eng, 2018, 16(1): 474-500. DOI:10.3934/mbe.2019022 |
| [32] |
贾斯月, 李靖欣, 朱凤才. 基于EV71疫苗接种的江苏省手足口病动力学模型研究[J]. 中华疾病控制杂志, 2019, 23(3): 253-258. Jia SY, Li JX, Zhu FC. A dynamic model of hand foot and mouth disease in Jiangsu Province based on EV71 vaccination[J]. Chin J Dis Control Prev, 2019, 23(3): 253-258. DOI:10.16462/j.cnki.zhjbkz.2019.03.002 |
| [33] |
李艺璇, 王岳, 王伟炳, 等. 不同疫苗覆盖场景下上海市和浙江省手足口病发病负担预测的动力学模型[J]. 复旦学报: 医学版, 2020, 47(4): 513-520. Li YX, Wang Y, Wang WB, et al. A dynamic model of hand, foot and mouth disease under different vaccine coverage conditions in Shanghai and Zhejiang province[J]. Fudan Univ: J Med Sci, 2020, 47(4): 513-520. DOI:10.3969/j.issn.1672-8467.2020.04.008 |
| [34] |
Hu YM, Zeng G, Chu K, et al. Five-year immunity persistence following immunization with inactivated enterovirus 71 type (EV71) vaccine in healthy children: A further observation[J]. Hum Vaccin Immunother, 2018, 14(6): 1517-1523. DOI:10.1080/21645515.2018.1442997 |
| [35] |
Mao QY, Cheng T, Zhu FC, et al. The cross-neutralizing activity of enterovirus 71 subgenotype C4 vaccines in healthy Chinese infants and children[J]. PLoS One, 2013, 8(11): e79599. DOI:10.1371/journal.pone.0079599 |
| [36] |
Zhang HF, An D, Liu W, et al. Analysis of cross-reactive neutralizing antibodies in human HFMD serum with an EV71 pseudovirus-based assay[J]. PLoS One, 2014, 9(6): e100545. DOI:10.1371/journal.pone.0100545 |
| [37] |
谭烈明, 沈平. 我国手足口病病原体变迁及EV71疫苗上市的潜在影响研究进展[J]. 中国热带医学, 2022, 22(3): 279-283. Tan LM, Shen P. Research progress in pathogen spectrum of hand, foot, and mouth disease and the potential impact of licensed EV71 vaccines in China[J]. China Trop Med, 2022, 22(3): 279-283. DOI:10.13604/j.cnki.46-1064/r.2022.03.17 |
| [38] |
毛群颖, 姚昕, 卞莲莲, 等. 我国EV-A71疫苗研发特点和挑战[J]. 中国病毒病杂志, 2016, 6(1): 1-5. Mao QY, Yao X, Bian LL, et al. Features and challenges on the research and development of EV-A71 vaccine in China[J]. Chin J Viral Dis, 2016, 6(1): 1-5. DOI:10.16505/j.2095-0136.2016.01.001 |
 2023, Vol. 44
2023, Vol. 44