文章信息
- 袁丹, 李一平, 杨淑娟, 刘芳, 黄晓玲, 姚亮, 李玲, 周玚, 叶黎, 曾亚莉, 梁姝.
- Yuan Dan, Li Yiping, Yang Shujuan, Liu Fang, Huang Xiaoling, Yao Liang, Li Ling, Zhou Chang, Ye Li, Zeng Yali, Liang Shu
- 四川省部分地区HIV-1感染者二线方案抗病毒治疗效果及耐药突变分析
- The antiretroviral treatment effect and drug resistance mutation of antiretroviral treatment for HIV-1 infected patients using second-line regimen in some areas of Sichuan Province
- 中华流行病学杂志, 2023, 44(2): 276-284
- Chinese Journal of Epidemiology, 2023, 44(2): 276-284
- http://dx.doi.org/10.3760/cma.j.cn112338-20220728-00668
-
文章历史
收稿日期: 2022-07-28
2. 四川大学华西公共卫生学院, 成都 610044;
3. 成都市疾病预防控制中心, 成都 610041;
4. 宜宾市疾病预防控制中心, 宜宾 644002;
5. 布拖县人民医院, 布拖 616350
2. West China School of Public Health and West China Fourth Hospital, Sichuan University, Chengdu 610044, China;
3. Chengdu Center for Disease Control and Prevention, Chengdu 610041, China;
4. Yibin Center for Disease Control and Prevention, Yibin 644002, China;
5. Butuo County People's Hospital, Butuo 616350, China
抗病毒治疗(ART)提高了HIV-1感染者的治疗效果和生活质量[1-3],但由于无法完全清除HIV-1感染者体内病毒,在药物选择压力下,HIV-1容易发生耐药突变导致ART失败[4]。目前国内主要ART方案为一线方案[2种核苷类反转录酶抑制剂(NRTIs)和1种非核苷类反转录酶抑制剂(NNRTIs)]。但耐药导致部分HIV-1感染者一线方案ART失败并更换二线方案,即2种NRTIs和1种蛋白酶抑制剂(PIs)。有研究发现,更换二线方案HIV-1感染者的病死率明显低于维持失败一线方案的HIV-1感染者,且病死率随着维持ART失败时间的缩短而减少[5],有必要及时更换二线方案。目前四川省已逐步掌握使用一线方案HIV-1感染者ART效果及耐药突变情况[6-8],但对于更换二线方案后ART效果及耐药突变尚未研究。本研究分析四川省部分地区HIV-1感染者二线方案ART效果及耐药突变,为指导HIV-1感染者正确使用二线方案提供参考依据。
对象与方法1. 研究对象:选择2019年1-12月接受一线方案ART≥6个月、病毒载量(VL) > 1 000拷贝数/ml、HIV-1基因型低度及以上程度耐药的HIV-1感染者,分为暴露组和非暴露组,暴露组为检出耐药后更换二线方案,对照组为检出耐药后继续使用一线方案(或更换其他一线方案)。为进一步研究HIV-1感染者二线方案ART效果,筛选出依从性保持较好(连续2年随访结果至少1个月内未发生漏服)的HIV-1感染者。本研究通过四川省CDC伦理委员会审批(批准文号:SCCDCIRB第2021-25号)。
2. 研究现场:根据四川省存活HIV-1感染者比例较高和ART发生耐药差异的情况,选取凉山彝族自治州布拖县、宜宾市和成都市作为研究现场。
3. 研究内容:2019年1月1日至2021年12月31日,收集研究对象基线、随访12个月和24个月的社会人口学、ART信息、依从性问卷资料和实验室检测数据。通过艾滋病综合防治信息系统收集研究对象社会人口学、ART随访信息、实验室检测结果。当地CDC负责依从性问卷调查、CD4+T淋巴细胞(CD4)计数和VL检测[9-10]。随访期间病毒抑制失败的HIV-1感染者血样送四川省CDC进行HIV-1基因型耐药检测[11]。根据美国斯坦福大学HIV-1耐药数据库,敏感、潜在低度耐药、低度耐药、中度耐药和高度耐药分值分别为0、10、15、30和60分,研究对象的耐药程度由各药物分值累加计分。分别记录HIV-1感染者基线、随访12个月和24个月的HIV-1感染者CD4计数和VL结果、随访24个月病毒抑制失败(VL≥200拷贝数/ml)的耐药突变位点情况[12]。
4. 相关定义:①持续CD4计数 > 200个/μl:随访12个月和24个月均CD4计数 > 200个/μl;②持续病毒抑制:2次VL均 < 200拷贝数/ml;③未持续病毒抑制:至少1次VL≥200拷贝数/ml;④及时更换二线方案:基线1年内更换为二线方案;⑤未及时更换二线方案:更换二线方案时间 > 1年[13]。
5. 统计学分析:采用SPSS 17.0软件进行统计学分析。分析暴露组和非暴露组HIV-1感染者观察终点病毒抑制失败并发生耐药突变的检出情况。采用χ2检验比较持续CD4计数 > 200个/μl及持续病毒抑制的差异。使用logistic回归模型分析HIV-1感染者二线方案ART效果的影响因素,单因素分析结果P < 0.05的自变量纳入多因素分析,逐步回归法筛选自变量的进入标准为0.05,剔除标准为0.10。双侧检验,检验水准α=0.05。
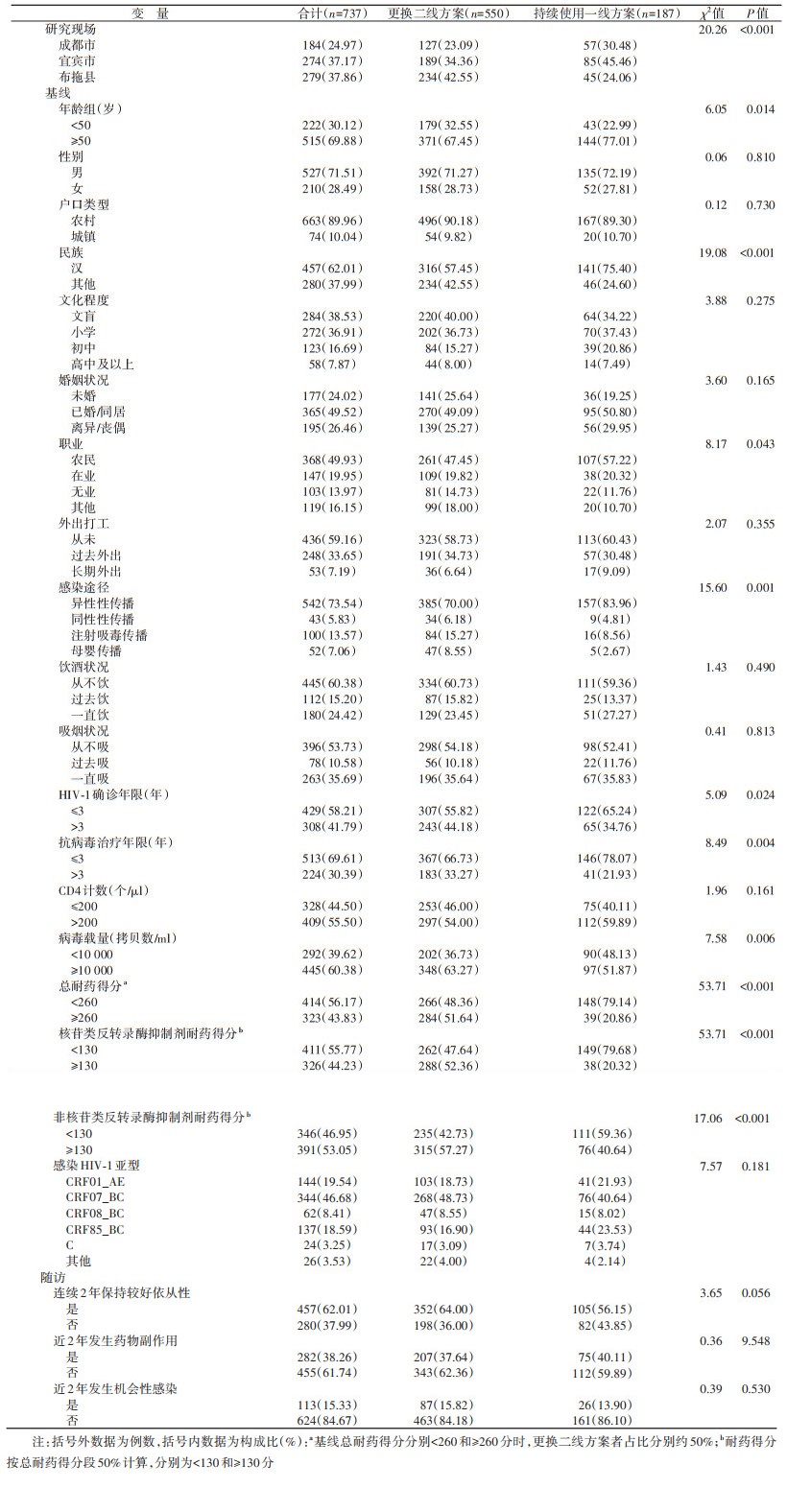
结果1. 基本情况:共招募737例研究对象,其中,成都市、宜宾市和布拖县分别为184例(24.97%)、274例(37.17%)和279例(37.86%)。在基线时,≥50岁占69.88%、男性占71.51%、农村户口占89.96%、汉族占62.01%、文盲占38.53%、已婚/同居占49.52%、农民占49.93%、从未外出打工占59.16%、异性性传播占73.54%、HIV-1确诊年限≤3年占58.21%、ART年限≤3年占69.61%,CD4计数 > 200个/μl和VL≥10 000拷贝数/ml分别占55.50% 和60.38%,总耐药得分 < 260分、NRTIs耐药得分 < 130分和NNRTIs耐药得分≥130分分别占56.17%、55.77%和53.05%,CRF07_BC亚型占46.68%。在随访时,连续2年保持较好依从性占62.01%,随访期间未出现药物副作用和未发生机会性感染分别占61.74%和84.67%。见表 1。
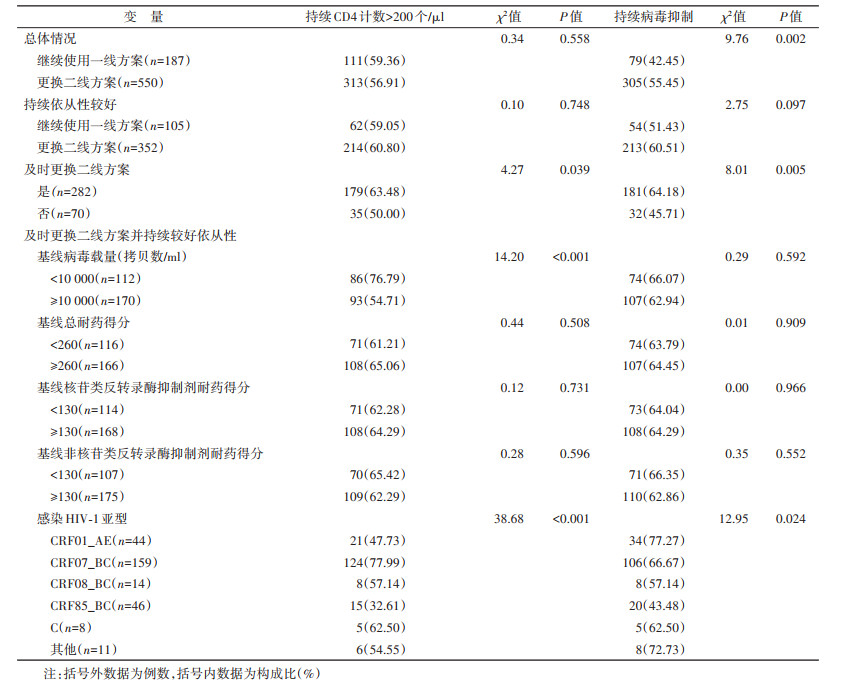
2. 更换二线方案的ART效果:总体来看,更换二线方案者持续病毒抑制的比例高于继续使用一线方案者(P=0.002);持续保持较好依从性的情况下,及时更换二线方案者持续CD4计数 > 200个/μl和持续病毒抑制比例高于未及时更换二线方案者(P=0.039和P=0.005)。在及时更换二线方案并持续保持较好依从性的HIV-1感染者中,基线VL < 10 000拷贝数/ml者持续CD4计数 > 200个/μl的比例高于基线VL≥10 000拷贝数/ml HIV-1感染者的比例(P < 0.001);感染CRF85_BC亚型的HIV-1感染者持续CD4计数 > 200个/μl和持续病毒抑制的比例低于感染其他亚型者(P < 0.001和P=0.024);基线总耐药、NRTIs耐药和NNRTIs耐药得分均对持续CD4计数 > 200个/μl和持续病毒抑制的比例差异无统计学意义。见表 2。
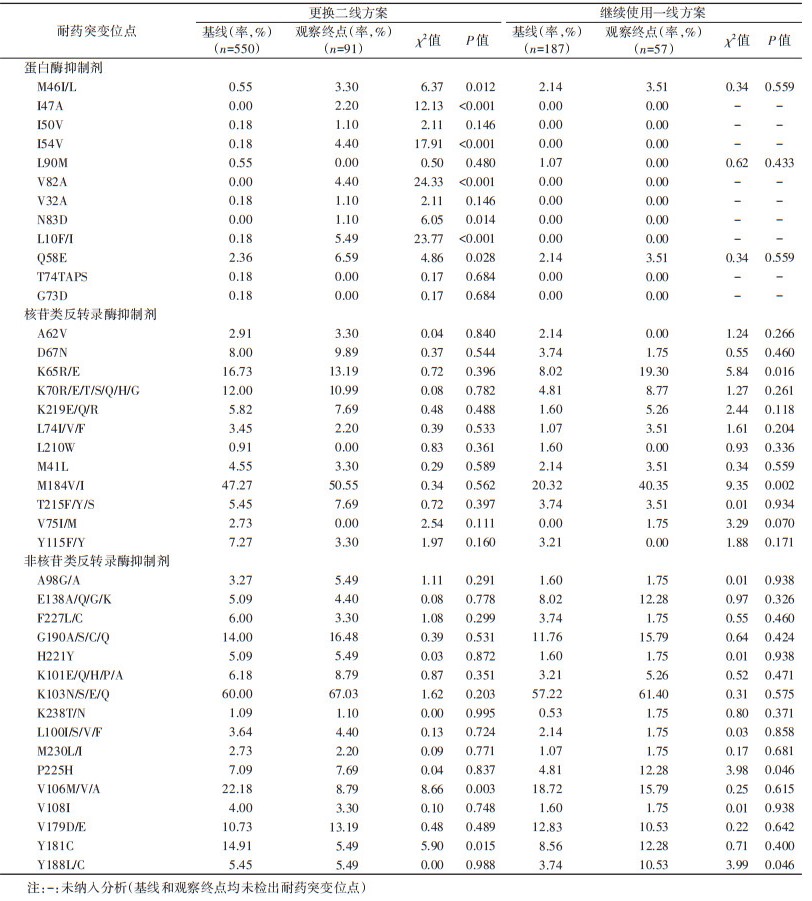
3. 耐药突变分析:更换二线方案和继续使用一线方案的HIV-1感染者在随访第24个月时,病毒抑制失败并检出耐药分别有91例(16.55%)和57例(30.48%)。更换二线方案HIV-1感染者在随访24个月时,病毒抑制失败124例,PIs高度耐药5例(4.03%)。更换二线方案者部分耐药突变位点检出率在随访24个月与基线的差异有统计学意义。PIs耐药突变位点M46I/L、I47A、I54V、V82A、N83D、L10F/I、Q58E检出率差异有统计学意义,呈上升趋势;NNRTIs耐药突变位点V106M/V/A和Y181C检出率的差异有统计学意义,且呈下降趋势。在继续使用一线方案者中,也有部分耐药突变位点在随访24个月与基线的差异有统计学意义。PIs未见耐药突变位点的差异有统计学意义;NRTIs耐药突变位点K65R/E和M184V/I检出率的差异有统计学意义,NNRTIs耐药突变位点P225H和Y188L/C检出率的差异有统计学意义,呈上升趋势。见表 3。
4. 二线方案ART效果的影响因素:多因素logistic回归分析结果显示,在更换二线方案且依从性较好的HIV-1感染者中,未持续病毒抑制的影响因素包括母婴传播是异性性传播感染的3.01 (95%CI:1.29~7.00)倍、未及时更换二线方案是及时更换二线方案的2.55(95%CI:1.41~4.62)倍、CRF85_BC亚型是CRF01_AE亚型的3.32(95%CI:1.49~7.42)倍,同性性传播是异性性传播的0.28(95%CI:0.09~0.93)倍。见表 4。
本研究发现,在已发生一线方案耐药的HIV-1感染者中,更换和及时更换二线方案者的VL得到了持续抑制,而继续使用一线方案者,即使保持良好依从性的条件下,VL仍不能持续抑制,主要原因是前期一线方案失败后导致NRTIs和NNRTIs各自内部交叉耐药影响了后续NRTIs和NNRTIs药物的使用[14]。及时更换二线方案者在2年ART期间持续CD4计数 > 200个/μl的比例明显上升,说明及时更换二线方案者体内病毒得到有效抑制,免疫水平开始恢复。研究还发现,在及时更换二线方案并保持良好依从性的HIV-1感染者中,基线VL越高,免疫水平恢复的负担越重,感染不同亚型也影响ART效果[15-16]。而基线总耐药、NRTIs耐药和NNRTIs耐药差异均不影响HIV-1感染者更换二线方案后的ART效果。目前四川省的二线方案为2种NRTIs和1种PIs,在使用一线方案发生病毒抑制失败HIV-1感染者中,耐药突变以NNRTIs为主,对二线方案ART效果无影响。发生NRTIs耐药突变的HIV-1感染者在更换二线方案时,临床医生会根据其耐药情况考虑调整二线方案中的NRTIs[9],可能是NRTIs耐药不影响二线方案治疗效果的另一原因。PIs是二线方案中重要的药物,该药物可与病毒的蛋白酶催化基因结合抑制酶活性,导致前体蛋白不能裂解和形成成熟的病毒,从而抑制病毒复制。另外,研究对象基线均未出现明显PIs耐药,这是更换二线方案HIV-1感染者VL得到持续抑制的主要原因。
耐药检测方面,更换二线方案HIV-1感染者发生病毒抑制失败时,部分NNRTIs耐药突变检出率明显下降,主要原因是二线方案中的洛匹那韦/利托那韦(LPV/r)取代了NNRTIs,导致HIV-1感染者体内NNRTIs药物压力降低,野生株复制能力超过NNRTIs耐药株成为优势株[17]。但是,PIs主要耐药突变位点M46I/L、I47A、I54V、V82A检出率明显上升,造成PIs严重交叉耐药,并针对LPV/r高度耐药。以上突变位点中,除了M46I/L可能是治疗前获得的耐药突变外[18-20],本研究出现的其余3个耐药突变位点是在LPV/r的药物选择压力下产生,其中I47A可造成LPV/r和福沙那韦(FPV/r)高度耐药、奈非那韦(NFV)和替拉那韦(TPV/r)中度耐药,I54V可造成除茚地那韦(IDV/r)和FPV/r处的其他PIs低度耐药。有研究报道,HIV-1感染者使用PIs治疗失败后,产生至少1种PIs耐药的占28%,对所有PIs药物产生耐药的占11%[21]。本研究发现,在更换二线方案的HIV-1感染者中,对多数PIs耐药的仅5例(4.03%),原因可能与现行检测方法有关,也有可能与观察时间较短有关。继续使用和更换其他一线方案HIV-1感染者,耐药突变检出率无明显改善,部分NRTIs和NNRTIs耐药突变进一步加重[22-24]。
更换二线方案并保持良好依从性的条件下,传播途径为母婴传播、未及时更换二线方案、感染CRF85_BC亚型是更换二线方案后影响ART成功的危险因素。传播途径为母婴传播的HIV-1感染者多为儿童,说明儿童ART存在更多挑战。儿童体内病毒水平较高、药物的抗病毒效力不强、不能达到足够的血药浓度,这些都会导致儿童ART失败[25],虽然研究筛选了依从性较好的HIV-1感染者,但无法掌握这类HIV-1感染者是否规范服药。可能的原因,一是该人群多为在校学生和未成年人,因自律性相对较差和保护个人隐私原因,不愿规范服药;二是这些HIV-1感染者多来自凉山州,当地医疗资源及医疗服务质量受限,难以获得持续的医疗卫生服务,建议加强凉山地区儿童ART相关技术支持与医疗服务质量。更换二线方案如果不及时,HIV-1感染者将产生针对一线方案严重的交叉耐药而导致VL反弹,影响后续病毒抑制及时性。CRF85_BC亚型是2014年四川省HIV-1分子流行病学调查时发现的新毒株[26-27],主要集中在川南地区,尤其是宜宾市老年人群。由于该亚型HIV-1在四川省流行时间较短,目前多集中于HIV-1分子传播网络相关研究[28],而针对该亚型HIV-1感染者在ART的疾病监测,如免疫细胞进展、耐药突变特征分析等均较少。本研究发现,四川省除了要加强分子流行病学监测,降低CRF85_BC亚型的流行外,还需深入研究该亚型HIV-1感染者的行为特征,加强ART监测。当HIV-1感染者发生针对一线方案耐药时,其耐药程度不影响二线方案治疗效果。HIV-1感染者应及时更换二线方案,保持良好依从性,提高服药规范度,降低病死率[29]。
本研究存在不足。本研究时间仅2年,还需继续延长观察时间,如果二线方案ART失败,将为HIV-1感染者本人及社会带来严重后果。
综上所述,一线方案耐药差异不影响更换二线方案后的HIV-1感染者ART效果;及时更换二线方案并保持良好依从性,有助于提高HIV-1感染者免疫水平和持续保持较低VL水平。母婴传播、未及时更换二线方案和感染CRF85_BC亚型是HIV-1感染者更换二线方案后影响ART成功的危险因素。
利益冲突 所有作者声明无利益冲突
作者贡献声明 袁丹:现场调查实施、数据分析、论文撰写、论文修改、经费支持;李一平:数据整理、数据分析、论文修改;杨淑娟:研究指导、数据分析;刘芳、黄晓玲、姚亮:现场调查实施、数据整理;李玲、周玚、叶黎:数据整理;曾亚莉:研究指导、论文修改;梁姝:经费支持、行政支持
| [1] |
王启兴, 王霞, 陈彬, 等. 四川省凉山州HIV耐药毒株流行及其相关因素分析[J]. 中华流行病学杂志, 2011, 32(11): 1082-1086. Wang QX, Wang X, Chen B, et al. Drug resistance and associated factors on HIV in Liangshan prefecture, Sichuan province[J]. Chin J Epidemiol, 2011, 32(11): 1082-1086. DOI:10.3760/cma.j.issn.0254-6450.2011.11.006 |
| [2] |
张云桂, 周曾全, 刑辉, 等. 云南省140例HIV/AIDS患者抗病毒治疗效果和耐药检测分析[J]. 卫生软科学, 2012, 26(1): 38-41. Zhang YG, Zhou ZQ, Xing H, et al. The antiviral therapy efficiency and drug resistance analysis among 140 HIV/AIDS patients in Yunnan[J]. Soft Sci Health, 2012, 26(1): 38-41. DOI:10.3969/j.issn.1003-2800.2012.01.013 |
| [3] |
郑煜煌, 周华英, 何艳, 等. 艾滋病7年高效抗逆转录病毒治疗的多中心前瞻性观察[J]. 中国感染控制杂志, 2010, 9(5): 310-315. Zheng YH, Zhou HY, He Y, et al. A 7-year multicenter prospective study on highly active antiretroviral therapy in HIV-1 infected patients in China[J]. Chin J Infect Control, 2010, 9(5): 310-315. DOI:10.3969/j.issn.1671-9638.2010.05.002 |
| [4] |
郑本锋, 刘宏伟, 袁源, 等. HIV抗病毒治疗者病毒抑制失败影响因素及耐药[J]. 中国公共卫生, 2011, 27(6): 728-730. Zheng BF, Liu HW, Yuan Y, et al. Virological supperssion failure and drug resistance in HIV-infected patients receiving antiretroviral therapy in Xihua county, Henan province[J]. Chin J Public Health, 2011, 27(6): 728-730. DOI:10.11847/zgggws2011-27-06-23 |
| [5] |
Gsponer T, Petersen M, Egger M, et al. The causal effect of switching to second-line ART in programmes without access to routine viral load monitoring[J]. AIDS, 2012, 26(1): 57-65. DOI:10.1097/QAD.0b013e32834e1b5f |
| [6] |
袁丹, 黄俊, 赖文红, 等. 四川省HIV-1抗病毒治疗1年以上病例耐药性分析[J]. 预防医学情报杂志, 2011, 27(10): 777-781. Yuan D, Huang J, Lai WH, et al. HIV-1 drug-resistance in patients who received antiviral treatment over 1 year in Sichuan, 2010[J]. J Prev Med Inf, 2011, 27(10): 777-781. |
| [7] |
袁丹, 叶黎, 苏玲, 等. 四川省2011年HIV-1抗病毒治疗患者耐药情况及亚型分析[J]. 现代预防医学, 2013, 40(22): 4248-4251. Yuan D, Ye L, Su L, et al. Analysis of the drug resistance and subtype of HIV-1 in patients receiving highly active antiretroviral therapy in Sichuan Province in 2011[J]. Mod Prev Med, 2013, 40(22): 4248-4251. |
| [8] |
张燕, 李一平, 周玚, 等. 2016-2019年四川地区HIV-1抗病毒治疗患者治疗效果及耐药性分析[J]. 国际检验医学杂志, 2022, 43(8): 973-978. Zhang Y, Li YP, Zhou C, et al. Analysis of treatment efficacy and drug resistance of patients receiving HIV-1 antiretroviral therapy in Sichuan area from 2016 to 2019[J]. Int J Lab Med, 2022, 43(8): 973-978. DOI:10.3969/j.issn.1673-4130.2022.08.016 |
| [9] |
中国疾病预防控制中心性病艾滋病预防控制中心. 艾滋病病毒感染者及艾滋病患者CD4+T淋巴细胞检测质量保证指南[R]. 2013. National Center for AIDS/STD Control and Prevention, Chinese Center for Disease Control and Prevention. A guideline for CR4+T lymphocyte counting and quality assurance in people living with HIV/AIDS[R]. 2013. |
| [10] |
中国疾病预防控制中心性病艾滋病预防控制中心. HIV-1病毒载量测定及质量保证指南(2013版)[R]. 2013. National Center for AIDS/STD Control and Prevention, Chinese Center for Disease Control and Prevention. Guideline for HIV-1 viral load testing and quality assurance[R]. 2013. |
| [11] |
邵一鸣. HIV耐药监测策略和检测技术[M]. 北京: 人民卫生出版社, 2010. Shao YM. The strategy and methodology for HIV drug resistance surveillance and detection[M]. Beijing: People's Medical Publishing House, 2010. |
| [12] |
中国疾病预防控制中心. 中国艾滋病诊疗指南[M]. 2021. Chinese Center for Disease Control and Prevention. China AIDS diagnosis and treatment guidelines[M]. 2021. |
| [13] |
中国疾病预防控制中心性病艾滋病预防控制中心. 国家免费艾滋病抗病毒药物治疗手册[M]. 第4版. 北京: 人民卫生出版社, 2016. National Center for AIDS/STD Control and Prevention, Chinese Center for Disease Control and Prevention. National manual of free antiviral treatment for AIDS[M]. 4th edition. Beijing: People's Medical Publishing House, 2016. |
| [14] |
刘明斌, 熊志伟, 徐丹, 等. HIV耐药的研究进展[J]. 中国艾滋病性病, 2007, 13(6): 588-591. Liu MB, Xiong ZW, Xu D, et al. Research progress of HIV drug resistance[J]. Chin J AIDS STD, 2007, 13(6): 588-591. DOI:10.3969/j.issn.1672-5662.2007.06.040 |
| [15] |
Ge ZW, Feng Y, Li K, et al. CRF01_AE and CRF01_AE cluster 4 are associated with poor immune recovery in Chinese patients under combination antiretroviral therapy[J]. Clin Infect Dis, 2021, 72(10): 1799-1809. DOI:10.1093/cid/ciaa380 |
| [16] |
Jiang H, Lan GH, Zhu QY, et al. Impacts of HIV-1 subtype diversity on long-term clinical outcomes in antiretroviral therapy in Guangxi, China[J]. J Acquir Immune Defic Syndr, 2022, 89(5): 583-591. DOI:10.1097/QAI.0000000000002906 |
| [17] |
Little SJ, Frost SDW, Wong JK, et al. Persistence of transmitted drug resistance among subjects with primary human immunodeficiency virus infection[J]. J Virol, 2008, 82(11): 5510-5518. DOI:10.1128/JVI.02579-07 |
| [18] |
Kandathil AJ, Kannangai R, Verghese VP, et al. Drug resistant mutations detected by genotypic drug resistance testing in patients failing therapy in clade C HIV-1 infected individuals from India[J]. Indian J Med Microbiol, 2009, 27(3): 231-236. DOI:10.4103/0255-0857.53205 |
| [19] |
Gupta A, Saple DG, Nadkarni G, et al. One-, two-, and three-class resistance among HIV-infected patients on antiretroviral therapy in private care clinics: Mumbai, India[J]. AIDS Res Hum Retroviruses, 2010, 26(1): 25-31. DOI:10.1089/aid.2009.0102 |
| [20] |
Maiga AI, Fofana DB, Cisse M, et al. Characterization of HIV-1 antiretroviral drug resistance after second-line treatment failure in Mali, a limited-resources setting[J]. J Antimicrob Chemother, 2012, 67(12): 2943-2948. DOI:10.1093/jac/dks310 |
| [21] |
Fisher R, van Zyl GU, Travers SAA, et al. Deep sequencing reveals minor protease resistance mutations in patients failing a protease inhibitor regimen[J]. J Virol, 2012, 86(11): 6231-6237. DOI:10.1128/JVI.06541-11 |
| [22] |
Chetchotisakd P, Anunnatsiri S, Kiertiburanakul S, et al. High rate multiple drug resistances in HIV-infected patients failing nonnucleoside reverse transcriptase inhibitor regimens in Thailand, where subtype A/E is predominant[J]. J Int Assoc Physicians AIDS Care (Chic), 2006, 5(4): 152-156. DOI:10.1177/1545109706294288 |
| [23] |
Marconi VC, Sunpath H, Lu ZG, et al. Prevalence of HIV-1 drug resistance after failure of a first highly active antiretroviral therapy regimen in KwaZulu Natal, South Africa[J]. Clin Infect Dis, 2008, 46(10): 1589-1597. DOI:10.1086/587109 |
| [24] |
Sungkanuparph S, Manosuth W, Kiertiburanakul S, et al. Options for a second-line antiretroviral regimen for HIV type 1-infected patients whose initial regimen of a fixed-dose combination of stavudine, lamivudine, and nevirapine fails[J]. Clin Infect Dis, 2007, 44(3): 447-452. DOI:10.1086/510745 |
| [25] |
Rouet F, Fassinou P, Inwoley A, et al. Long-term survival and immuno-virological response of African HIV-1-infected children to highly active antiretroviral therapy regimens[J]. AIDS, 2006, 20(18): 2315-2319. DOI:10.1097/QAD.0b013e328010943b |
| [26] |
Su L, Feng Y, Liang S, et al. The origin and spread of CRF85_BC, driven by heterosexual transmission among older people in Sichuan, China[J]. BMC Infect Dis, 2020, 20(1): 772. DOI:10.1186/s12879-020-05488-4 |
| [27] |
苏玲, 杨洪, 胡莹, 等. 四川省2014年HIV-1分子流行病学调查[J]. 中国艾滋病性病, 2016, 22(12): 946-949. Su L, Yang H, Hu Y, et al. Molecular epidemiological study on HIV-1 in Sichuan province in 2014[J]. Chin J AIDS STD, 2016, 22(12): 946-949. DOI:10.13419/j.cnki.aids.2016.12.02 |
| [28] |
Yuan D, Yu B, Liang S, et al. HIV-1 genetic transmission networks among people living with HIV/AIDS in Sichuan, China: a genomic and spatial epidemiological analysis[J]. Lancet Reg Health West Pac, 2022, 18: 100318. DOI:10.1016/j.lanwpc.2021.100318 |
| [29] |
Li YP, Wang QJ, Liang S, et al. Effect of switching antiretroviral treatment regimen in patients with drug- resistant HIV-1 infection: retrospective observational cohort study[J]. JMIR Public Health Surveill, 2022, 8(6): e33429. DOI:10.2196/33429 |
 2023, Vol. 44
2023, Vol. 44