文章信息
- 赵星, 洪峰, 殷建忠, 唐文革, 张刚, 梁娴, 李景中, 崔超英, 李晓松.
- Zhao Xing, Hong Feng, Yin Jianzhong, Tang Wenge, Zhang Gang, Liang Xian, Li Jingzhong, Cui Chaoying, Li Xiaosong
- 西南区域自然人群队列简介与研究进展
- Introduction of general population cohort study in southwestern China
- 中华流行病学杂志, 2023, 44(1): 40-47
- Chinese Journal of Epidemiology, 2023, 44(1): 40-47
- http://dx.doi.org/10.3760/cma.j.cn112338-20221009-00864
-
文章历史
收稿日期: 2022-10-09
2. 贵州医科大学公共卫生学院环境污染与疾病监控教育部重点实验室, 贵阳 550025;
3. 昆明医科大学公共卫生学院, 昆明 650500;
4. 保山中医药高等专科学校, 保山 678000;
5. 重庆市疾病预防控制中心, 重庆 400042;
6. 四川省妇幼保健院, 成都 610045;
7. 成都市疾病预防控制中心, 成都 610041;
8. 西藏自治区疾病预防控制中心, 拉萨 850002;
9. 西藏大学医学院高原医学研究中心, 拉萨 850033
2. Ley Laboratory of Environmental Pollution Monitoring and Disease Control, School of Public Health, Guizhou Medical University, Kunming 550025, China;
3. School of Public Health, Kunming Medical University, Kunming 650500, China;
4. Baoshan Collede of Traditional Chinese Medicine, Baoshan 678000, China;
5. Chongqing Municipal Center for Disease Control and Prevention, Chongqing 400042, China;
6. Sichuan Provincial Maternity and Child Health Care Center, Chengdu 610045, China;
7. Chengdu Municipal Center for Disease Control and Prevention, Chengdu 610041, China;
8. Tibet Autonomous Region Center for Disease Control and Prevention, Lhasa 850002, China;
9. High Altitude Medical Research Center, School of Medicine, Tibet University, Lhasa 850033, China
常见高危慢性非传染性疾病(慢性病)如心血管疾病、癌症、糖尿病和慢性肺病,已成为全球主要死亡原因,合计占全球死亡人数近70%[1]。我国慢性病负担逐年增加,且存在区域异质性[2]。西南多民族地区经济欠发达,卫生资源相对匮乏,高危慢性病防控形势严峻。加强慢性病防控是《“健康中国2030”规划纲要》中的重要内容,然而目前我国慢性病流行率和危险因素研究多来自中部和东部[3-5]。西部地区是“一带一路”倡议的重要枢纽,因地理人文环境复杂,开展队列研究难度大,尚缺乏相关高质量大样本人群研究。
西南区域地域辽阔、民族众多,涵盖诸多特异性环境因素和多民族遗传背景,慢性病的发生可能具有遗传和环境易感性。西南地区既包括世界屋脊青藏高原,也包括大气污染严重的四川盆地。西南民族人群既具有特异性膳食习惯(如酥油茶、酸汤等民族食物),也具有区域特异多发疾病(如高原红细胞增多症、高原心脏病等特殊疾病)。此外,已有研究均表明不同慢性病的发生存在民族差异[6-8],但我国关于慢性病患病率、发病率及风险因素的民族差异研究证据尚不足。
“十三五”期间,针对我国高发高危疾病及若干流行率相对较高的罕见病,国家重点研发计划布局“精准医学研究”重点专项,该专项目标为实施精准医学研究的全创新链协同攻关,为显著提升人口健康水平、减少无效和过度医疗、避免有害医疗、遏制医疗费用支出快速增长提供科技支撑。专项提出构建百万人以上的自然人群国家大型健康队列和重大疾病专病队列,2017年四川大学联合西南地区15家单位共同启动了西南区域自然人群队列(西南队列)的建设。该项目在统一标准与信息化共享的基础上,基于社区人群,建成了10万成年人队列与2万人的出生队列,收集并分析了西南区域多民族慢性病相关问卷、体检及生化指标等多维度信息,为我国西南区域多民族地区慢性病防控研究提供了多中心、高质量、大规模队列研究平台,丰富了我国百万级自然人群队列的自然环境多样性、文化多样性和遗传多样性。
二、队列基本情况介绍西南队列项目组在统一标准与信息化共享的基础上,基于社区人群,建立了具有西南区域特色的十万人级多中心自然人群队列,并对队列人群长期随访。根据西南区域特点,下设4个子队列:少数民族聚居地世居自然人群队列(少数民族队列:分布在云南省和贵州省少数民族区域,包括西南区域主要少数民族—彝族、白族、苗族、布依族、侗族)、高海拔地区世居高原自然人群队列(高原队列:分布在西藏自治区、云南省和四川省的高原地区,包括高原汉族与藏族人群)、四川盆地大气重污染区域自然人群队列(盆地队列:分布在四川省和重庆市重污染城市区域,均为汉族)以及出生队列(分布在四川省、重庆市和贵州省城市地区,均为汉族)。见表 1。本研究通过四川大学医学伦理审查委员会审查(批准文号:K2016038,K2020022)。
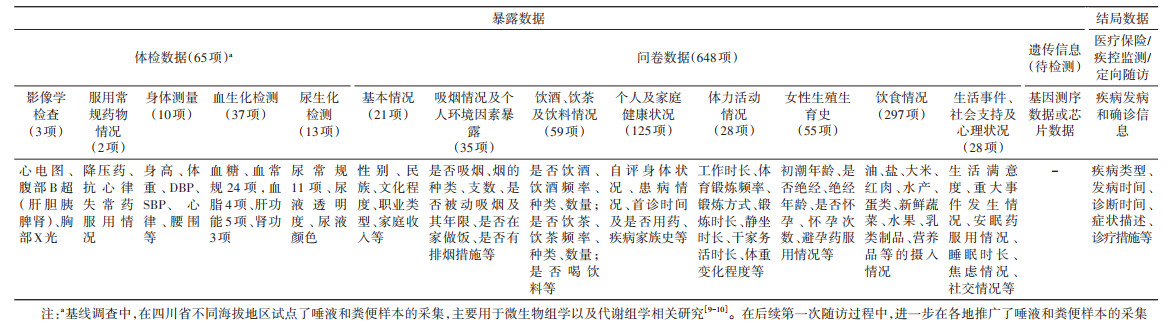
1. 基线调查:西南队列于2018年5月正式启动了基线调查工作。西南成年人队列于2019年9月完成了全部的基线数据采集工作。项目组采用了严格的纳入和排除标准,纳入年龄为30~79岁(拉萨市藏族人群18~79岁),要求当地户籍、居住半年以上的常住居民,无精神性疾患或其他相关疾病,表达和理解能力正常,并签署了知情同意书。少数民族和高原汉族除了满足上述条件,还要求直系三代亲属均居住在当地。项目采用了多阶段分层整群抽样的方式,在选定城市和农村社区后,事先获得当地人群性别和各年龄段人口比例,按照≤10%的误差选取相同比例的人群纳入队列研究。本项目按照统一的技术规范标准主要采集了调查对象3个方面的数据:体格检查、电子问卷以及生物样本。见表 2。
出生队列的建立依托于妇幼保健系统,于2020年12月底完成了全部基线数据采集工作。为保证入组研究对象具有代表性,选取妊娠13周+6以前到调查点进行第一次产检建卡的孕妇。其余纳入标准同西南成年人队列。问卷内容在参照成年人队列的基础上,还增加了孕期相关内容,主要包括孕前健康及体格检查情况、孕妇及配偶生育健康及治疗状况、避孕史、全身各系统疾病状况、孕期保健知识知晓情况。
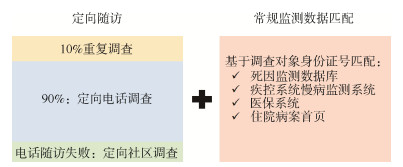
2. 第一次随访调查:2020年8月至2021年7月,队列开展了第一轮跟踪随访,建立随访数据库。见图 1。随访信息主要包括死亡事件、发病事件、住院事件、健康相关因素、迁移以及失访事件。随访方式则为现场重复调查、定向电话调查、定向社区调查、常规监测信息系统匹配等多种方式相结合。抽取基线10%的研究对象,开展面对面现场重复调查。除问卷内容在基线调查基础上做了进一步增加和优化外,该轮现场调查、体格检查和实验室检测的内容、步骤、实施过程与基线调查基本一致。对余下的90%研究对象开展定向电话调查,调查内容包括其基本信息、吸烟、饮酒等健康行为变化情况以及健康状况改变情况(含重大疾病发生情况)。出生队列随访调查通过面对面调查的方式开展,主要包括孕妇随访、儿童基线调查、儿童随访调查和儿童干血斑采集冻存。
|
| 图 1 西南区域自然人群队列随访方式示意图 |
3. 队列质量控制:西南队列建立了全过程、多维度、现代化的质控体系。①充分利用了现代信息化手段辅助质量控制。基线调查以及随访均基于平板电脑,实现调查数据的全程无纸化,问卷预制了逻辑查错体系和调查全过程录音与24 h质量抽查反馈机制。配合编码系统(包括个人编码、血样编码和尿样编码),实现了体检数据与生物样本的全流程电子化与质量控制。②血、尿生化指标检测统一委托第三方,确保各分中心检查结果的可比性。③从项目开展前对工作人员的统一培训,到项目过程中均实行了基于标准操作程序的现场实施单位自查—质控员现场检查—项目办不定期督导的多层级现场质量控制措施。
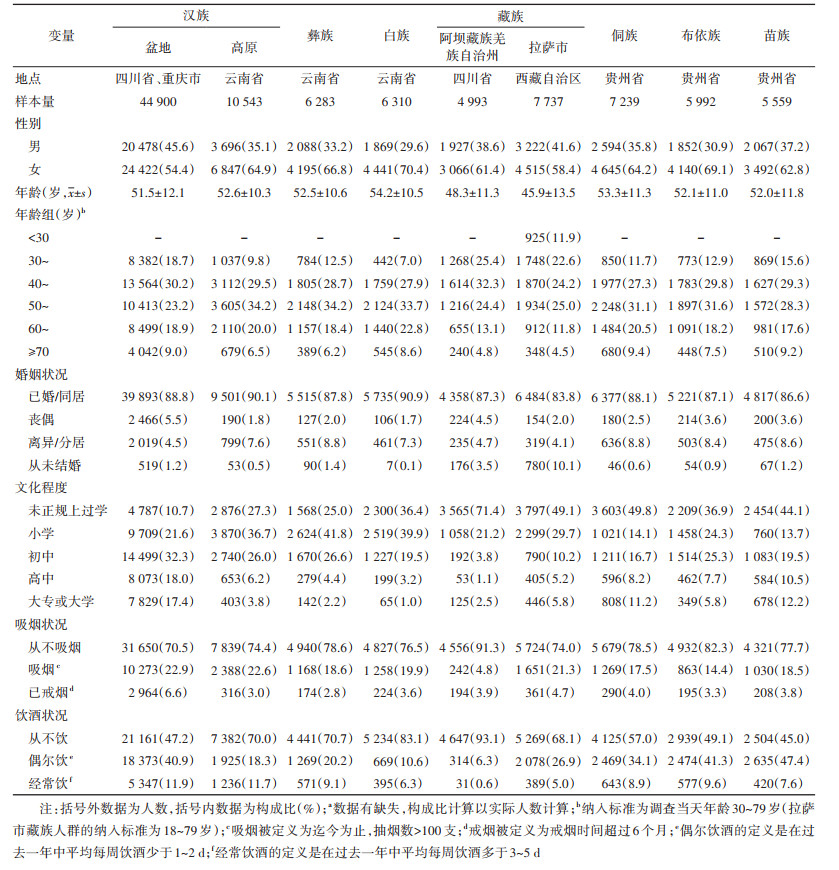
三、人群基本特征1. 人口学与生活行为方式特征:在西南成年人队列中,女性占60.0%,且在各民族中女性均多于男性。女性比例最低的民族为成都市和重庆市(盆地)汉族,约为54.4%,比例最高的民族为云南省(高原)白族,约为70.4%。不同民族调查对象的年龄分布和婚姻状况相似,都集中于40~59岁且已婚/同居,但在文化程度上存在差异,四川省阿坝藏族羌族自治州71.4%的藏族人未正规上过学,而成都市与重庆市汉族人群中未正规上过学的比例仅为10.7%,行为生活方式也存在差异。与其他人群相比,阿坝藏族羌族自治州藏族人中从不吸烟(91.3%)或饮酒(93.1%)的比例相对较高(表 3)。
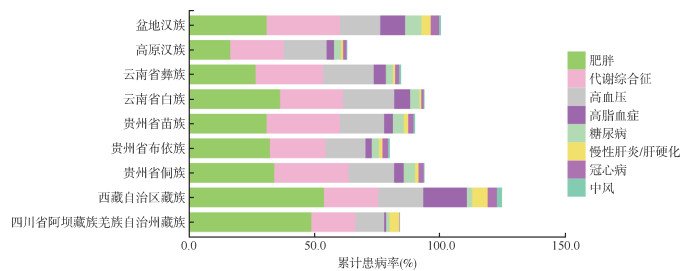
2. 疾病自我报告特征:根据西南成年人队列基线疾病自我报告数据发现,不同民族之间具有不同的疾病模式。高血压基线患病率最高的是白族(20.5%)和彝族(20.2%),而阿坝藏族羌族自治州的藏族患病率最低(11.4%)。糖尿病则以成都市、重庆市盆地汉族为主,基线患病率达6.5%。冠心病患病率在民族间差异较大,拉萨市藏族患病率最高(3.7%),而患病率最低的人群是来自四川省阿坝藏族羌族自治州的藏族(0.2%)。见图 2。
|
| 图 2 西南区域常见疾病自报患病率 |
针对不发达情形下高质量大型队列建立的需求与西南地区的自然环境暴露、生活行为方式的健康效应,基于西南队列的基线调查与第一次随访数据,项目组在各领域均产出了成果。
1. 欠发达地区大型队列的构建模式创新:西南队列地处多民族地区,地理环境复杂、文化习惯各异,对于队列的建立、实施与组织协调均提出了新的挑战。在参考国际国内前沿队列建立经验的前提下,项目组从技术规范、运行模式以及信息化建设多个维度进行了本土化创新:①严格依据国家示范队列研究的技术标准和规范,建立了适用于西南多民族地区高效率、高质量、本土化以及体系完整的项目实施操作技术规范体系;②在借鉴国家示范队列“中央协调式”组织管理模式的基础上,兼顾了队列研究的科学性、可实施性、创新性提出了条(5个课题)块(5个省级地区)结合的运行格局,实行了共同负责人制,有效组织协调了西南区域自然人群队列各参与单位间及各课题间的协作关系;③结合西南区域自然人群队列研究的实际工作需求,完成了适用于边远地区的信息系统自主开发,实现了西南区域自然人群队列数据的电子化规范化采集和质量控制;④基于“共建共享”原则建立了数据共享机制,并开展了多层次的数据使用以及科研能力培训,使得所有项目参与单位都可以及时全面地获取和利用队列数据,充分调动了项目成员和参与单位的积极性。上述研究成果为欠发达地区大规模自然人群队列的高质量建立提供了典型案例以及全程管理、技术支撑与协作模式的参考借鉴[9]。此外,西南队列还重点关注队列质量控制的方法体系研究。西南队列对于多中心大型队列调查中不可忽视的两种重要误差—调查误差、测量误差也展开了相关研究。系统研究了调查误差的流行规律特征,提出从问卷设计、调查员管理与培训等多角度控制调查误差[10],为提高大型队列的调查质量提供了科学依据。测量误差是营养流行病学研究领域中的重大挑战。西南队列在膳食模式研究基础上,阐明了测量误差对膳食模式研究的影响规律,对于合理评估膳食模式研究中的测量误差问题提供了科学依据[11]。
2. 西南区域自然环境的健康效应:开展对环境流行病学的研究是探索高危慢性病复杂病因及危险因素的重要组成部分。项目组聚焦心血管代谢性疾病及相关指标,结合外部环境数据集,从大气污染、气象、绿地、海拔等角度系统探讨了环境暴露与人群健康的关系。项目组揭示了大气污染与脉压差[12]、血脂[13]、肥胖[14]、骨密度[15]、肾功能[16]等代谢性指标之间的关联,发现大气污染与代谢相关脂肪性肝病存在关联[17],进一步探讨大气污染与糖尿病[18]、高尿酸血症[19]等代谢性疾病之间的关联机制。在此基础上,利用唾液和粪便的样本包含的微生物信息,揭示绿地对肠道菌群[20]和骨密度[21]的健康促进效应,发现海拔可能调节肠道菌群而影响骨密度[22],提出适当体力活动[23-24]、健康膳食模式[25]对大气污染的健康危害效应具有一定缓解作用。研究成果提供了丰富的环境暴露与心血管代谢性疾病关联证据,并为促进人群健康提供了科学支撑。
3. 西南区域特征生活行为方式的健康效应:近年来西南地区心脏代谢性疾病负担逐渐加重,膳食因素是心脏代谢疾病最重要的可干预因素之一。在膳食研究领域,项目组系统解析了西南地区的膳食分布规律,比较了不同民族间的膳食特点,并提取了3种西南区域特色膳食模式—盆地模式、云贵高原模式以及青藏高原模式,发现膳食模式特征与地理条件存在高度相关性。在此基础上,项目组进一步明确了西南区域膳食模式与代谢综合征[26]、肥胖类型[27]、高血压[28]、血脂谱[29]、代谢脂肪肝[30]等心血管疾病高危因素间的关联,为后续该类疾病的早期膳食干预提供了科学依据;将膳食和环境结合考虑后,进一步发现依从终止高血压膳食疗法可降低环境颗粒物引起的血压升高风险[25],以此提出基于膳食行为的大气污染相关代谢疾病防控的新干预靶点;除此之外,对睡眠方面的研究发现睡眠不足或睡眠-觉醒周期紊乱与代谢障碍有关,在中国人群中,较长的日间午睡时间(而非夜间睡眠时间)与高尿酸血症风险独立相关[31]。对体力活动和静坐时间方面的研究发现:中度体力活动降低高尿酸血症风险,减少静坐时间对预防女性高尿酸血症更有效[32]。
五、研究展望与挑战“十三五”期间,项目组已高质量建成西南多民族地区十万级规模自然人群队列,并初步揭示了西南地区常见高危慢性病的流行规律及其影响因素,取得了阶段性成果。后续,项目组将继续高质量推进队列发展,立足于西南地区的鲜明特色,为西南多民族地区慢性病复杂病因阐释以及防治策略研究贡献力量。主要将从以下几方面继续开展工作:
1. 长期可持续推进队列高质量追踪随访:持续开展长期追踪随访工作是大型自然人群队列发挥作用和取得成功的关键,同时也是队列发展所面临的首要挑战。为应对上述挑战,西南队列各参与单位均将维系队列发展纳入了本单位长期规划,将其作为义不容辞的责任,并通过多种举措来保障队列的可持续发展和高质量追踪随访,具体包括:根据不同单位特点积极整合资源,多途径争取各种层级和类型的科研项目及配套经费支持;将队列追踪随访与本单位其他科研及业务工作进行有机整合;充分依托医疗保险与疾病监测等数据维持低成本长期随访;延续开展全体项目参与单位的定期交流合作机制与信息共享等。
2. 基于国家健康战略需求开展特色研究:西南地区具有独特的地理文化以及多样的民族遗传背景,其健康需求与慢性病发生发展机制均存在特异性。因此,充分阐明西南区域特色暴露与慢性病之间的复杂关联,其对于提升少数民族人群健康水平、促进健康公平以及全面实现健康国家“十四五”规划均具有不可替代的作用。据此,西南队列将充分发挥其特色优势,一方面在既往研究的基础上,继续深入阐明膳食、环境、遗传等西南区域特色暴露的健康效应,聚焦于解决西南多民族地区突出的健康与公共卫生学问题,为常见高危慢性病的防控提供新的干预手段和思路;另一方面,逐步开展高原习服与脱习服、主动健康与老龄化科技应对等研究,积极响应当前国家对于西南地区迫切的健康战略需求。
3. 深入开展环境-基因交互及多组学研究:慢性病的发生发展是环境-基因复杂交互的共同作用,多组学研究则有助于深入明晰慢性病的发生机制。因此,西南队列也将开展慢性病多组学研究作为后续发展的重点领域。目前,西南队列已开始小规模的人类基因组以及肠道宏基因组测序,期望通过小规模组学数据的初步探索以明晰下一步重点聚焦的研究方向。
4. 稳步实现数据开放和推动高质量合作:西南队列独特的样本结构以及丰富的数据遗传资源,可以极大地丰富国家百万级人群队列的多样性,是人类共同的科研财富。因此,在保障数据安全和公民个人隐私的前提下,稳步实现西南队列研究数据向全社会开放,让西南队列成果能够服务于全人类的共同福祉,是西南队列建立之初的既定目标。目前,西南队列正在逐步完善数据开放所需的各项制度以及技术保障,预期在3年内逐步实现数据的社会全面开放。同时,西南队列也积极寻求国内外高水平合作,不仅期望汇集世界智慧解决西南区域健康问题,也期望能够为人类健康贡献西南力量。
六、总结西南队列的建成实现了我国西南大型队列平台从“0”到“1”的突破,为我国西南多民族人群常见高危慢性病的防控提供了坚实平台资源。由于多民族人群的特异环境行为暴露特征,队列研究成果预期具有两方面突出价值:揭示中国人群(尤其是多民族)的新多维易感特征;发现新的慢性病干预技术与策略。作为国家大型队列的重要组成部分,西南队列自建立之初就将开放共享作为基本原则之一,期待全国乃至全球研究者在国家相关法律法规内开展实质合作,共同为健康中国的实现贡献西南力量。
利益冲突 所有作者声明无利益冲突
作者贡献声明 赵星:研究设计、论文撰写、数据整理、统计学分析;洪峰、殷建忠、唐文革、张刚、梁娴、李景中、崔超英:研究设计、数据整理、统计学分析、论文修改;李晓松:研究设计
| [1] |
WHO. Noncommunicable diseases[EB/OL]. [2022-10-01]. https://www.who.int/health-topics/noncommunicable-diseases#tab=tab_1.
|
| [2] |
Zhou MG, Wang HD, Zeng XY, et al. Mortality, morbidity, and risk factors in China and its provinces, 1990-2017:a systematic analysis for the Global Burden of Disease Study 2017[J]. Lancet, 2019, 394(10204): 1145-1158. DOI:10.1016/s0140-6736(19)30427-1 |
| [3] |
何美安, 张策, 朱江, 等. 东风-同济队列研究: 研究方法及调查对象基线和第一次随访特征[J]. 中华流行病学杂志, 2016, 37(4): 480-485. He MA, Zhang C, Zhu J, et al. Dongfeng-Tongji cohort: methodology of the survey and the characteristics of baseline and initial population of follow-up program[J]. Chin J Epidemiol, 2016, 37(4): 480-485. DOI:10.3760/cma.j.issn.0254-6450.2016.04.008 |
| [4] |
李立明, 吕筠, 郭彧, 等. 中国慢性病前瞻性研究: 研究方法和调查对象的基线特征[J]. 中华流行病学杂志, 2012, 33(3): 249-255. Li LM, Lv J, Guo Y, et al. The China Kadoorie Biobank: related methodology and baseline characteristics of the participants[J]. Chin J Epidemiol, 2012, 33(3): 249-255. DOI:10.3760/cma.j.issn.0254-6450.2012.03.001 |
| [5] |
Wang XF, Lu M, Qian J, et al. Rationales, design and recruitment of the Taizhou longitudinal study[J]. BMC Public Health, 2009, 9: 223. DOI:10.1186/1471-2458-9-223 |
| [6] |
Gujral UP, Vittinghoff E, Mongraw-Chaffin M, et al. Cardiometabolic abnormalities among normal-weight persons from five racial/ethnic groups in the United States: a cross-sectional analysis of two cohort studies[J]. Ann Intern Med, 2017, 166(9): 628-636. DOI:10.7326/m16-1895 |
| [7] |
Ho FK, Gray SR, Welsh P, et al. Ethnic differences in cardiovascular risk: examining differential exposure and susceptibility to risk factors[J]. BMC Med, 2022, 20(1): 149. DOI:10.1186/s12916-022-02337-w |
| [8] |
Wang LM, Gao P, Zhang M, et al. Prevalence and ethnic pattern of diabetes and prediabetes in China in 2013[J]. JAMA, 2017, 317(24): 2515-2523. DOI:10.1001/jama.2017.7596 |
| [9] |
Zhao X, Hong F, Yin JZ, et al. Cohort profile: the China Multi-Ethnic Cohort (CMEC) study[J]. Int J Epidemiol, 2021, 50(3): 721-721l. DOI:10.1093/ije/dyaa185 |
| [10] |
Sun CY, Guo B, Liu X, et al. Interviewer error within the face-to-face food frequency questionnaire in large multisite epidemiologic studies[J]. Am J Epidemiol, 2022, 191(5): 921-929. DOI:10.1093/aje/kwac024 |
| [11] |
Hu YF, Tang D, Yang F, et al. The impacts of measurement errors on a dietary pattern analyses: a simulation study based on dietary data from the China Multi-Ethnic Cohort (CMEC) study[J]. Am J Clin Nutr, 2022, 116(2): 523-530. DOI:10.1093/ajcn/nqac092 |
| [12] |
Pan Q, Zha S, Li JZ, et al. Identification of the susceptible subpopulations for wide pulse pressure under long-term exposure to ambient particulate matters[J]. Sci Total Environ, 2022, 834: 155311. DOI:10.1016/j.scitotenv.2022.155311 |
| [13] |
Wang L, Chen GB, Pan YY, et al. Association of long-term exposure to ambient air pollutants with blood lipids in Chinese adults: the China multi-ethnic cohort study[J]. Environ Res, 2021, 197: 111174. DOI:10.1016/j.envres.2021.111174 |
| [14] |
Liu MJ, Tang WG, Zhang Y, et al. Urban-rural differences in the association between long-term exposure to ambient air pollution and obesity in China[J]. Environ Res, 2021, 201: 111597. DOI:10.1016/j.envres.2021.111597 |
| [15] |
Wu JL, Guo B, Guan H, et al. The association between long-term exposure to ambient air pollution and bone strength in China[J]. J Clin Endocrinol Metab, 2021, 106(12): e5097-5108. DOI:10.1210/clinem/dgab462 |
| [16] |
Li SC, Meng Q, Laba C, et al. Associations between long-term exposure to ambient air pollution and renal function in Southwest China: the China Multi-Ethnic Cohort (CMEC) study[J]. Ecotoxicol Environ Saf, 2022, 242: 113851. DOI:10.1016/j.ecoenv.2022.113851 |
| [17] |
Guo B, Guo YM, Nima Q, et al. Exposure to air pollution is associated with an increased risk of metabolic dysfunction-associated fatty liver disease[J]. J Hepatol, 2022, 76(3): 518-525. DOI:10.1016/j.jhep.2021.10.016 |
| [18] |
Wang X, Guo B, Yang XX, et al. Role of liver enzymes in the relationship between particulate matter exposure and diabetes risk: a longitudinal cohort study[J]. J Clin Endocrinol Metab, 2022, 107(10): e4086-4097. DOI:10.1210/clinem/dgac438 |
| [19] |
Zeng CM, Guo B, Wan Y, et al. The role of lipid profile in the relationship between particulate matters and hyperuricemia: a prospective population study[J]. Environ Res, 2022, 214: 113865. DOI:10.1016/j.envres.2022.113865 |
| [20] |
Wu KP, Guo B, Guo YM, et al. Association between residential greenness and gut microbiota in Chinese adults[J]. Environ Int, 2022, 163: 107216. DOI:10.1016/j.envint.2022.107216 |
| [21] |
Jiang Y, Kang Zhuo BM, Guo B, et al. Living near greenness is associated with higher bone strength: a large cross- sectional epidemiological study in China[J]. Sci Total Environ, 2022, 831: 155393. DOI:10.1016/j.scitotenv.2022.155393 |
| [22] |
Zuo HJ, Zheng TL, Wu KP, et al. High-altitude exposure decreases bone mineral density and its relationship with gut microbiota: results from the China multi-ethnic cohort (CMEC) study[J]. Environ Res, 2022, 215(Pt 2): 114206. DOI:10.1016/j.envres.2022.114206 |
| [23] |
Xu JY, Zhang YQ, Yao MH, et al. Long-term effects of ambient PM2.5 on hypertension in multi-ethnic population from Sichuan province, China: a study based on 2013 and 2018 health service surveys[J]. Environ Sci Pollut Res Int, 2021, 28(5): 5991-6004. DOI:10.1007/s11356-020-10893-y |
| [24] |
Ao LJ, Zhou JM, Han MM, et al. The joint effects of physical activity and air pollution on type 2 diabetes in older adults[J]. BMC Geriatr, 2022, 22(1): 472. DOI:10.1186/s12877-022-03139-8 |
| [25] |
Xu H, Guo B, Qian W, et al. Dietary pattern and long-term effects of particulate matter on blood pressure: a large cross-sectional study in Chinese adults[J]. Hypertension, 2021, 78(1): 184-194. DOI:10.1161/hypertensionaha.121.17205 |
| [26] |
Xiao X, Qin ZX, Lv XY, et al. Dietary patterns and cardiometabolic risks in diverse less-developed ethnic minority regions: results from the China Multi-Ethnic Cohort (CMEC) study[J]. Lancet Reg Health West Pac, 2021, 15: 100252. DOI:10.1016/j.lanwpc.2021.100252 |
| [27] |
Tang D, Xiao X, Chen LL, et al. Association of dietary patterns with obesity and metabolically healthy obesity phenotype in Chinese population: a cross-sectional analysis of China Multi-Ethnic Cohort Study[J]. Br J Nutr, 2022, 128(11): 2230-2240. DOI:10.1017/s0007114521005158 |
| [28] |
Dai SY, Xiao X, Xu CZ, et al. Association of dietary approaches to stop hypertension diet and Mediterranean diet with blood pressure in less-developed ethnic minority regions[J]. Public Health Nutr, 2022, 25(12): 3476-3486. DOI:10.1017/s1368980022000106 |
| [29] |
Zhang N, Xiao X, Xu JR, et al. Dietary Approaches to Stop Hypertension (DASH) diet, Mediterranean diet and blood lipid profiles in less-developed ethnic minority regions[J]. Br J Nutr, 2022, 128(6): 1137-1146. DOI:10.1017/s0007114521004013 |
| [30] |
Xie XF, Guo B, Xiao X, et al. Healthy dietary patterns and metabolic dysfunction-associated fatty liver disease in less-developed ethnic minority regions: a large cross-sectional study[J]. BMC Public Health, 2022, 22(1): 118. DOI:10.1186/s12889-021-12486-x |
| [31] |
Wang YJ, Zeng YL, Zhang XH, et al. Daytime napping duration is positively associated with risk of hyperuricemia in a Chinese population[J]. J Clin Endocrinol Metab, 2021, 106(5): e2096-2105. DOI:10.1210/clinem/dgab043 |
| [32] |
Hong RD, Huang J, Xu CZ, et al. Association of Sedentary behovior and physical Activity with hyperuricemia and sex diffierence: results from the China-Ethnic cohort Study[J]. Rheumatol, 2022, 45(5): 513-522. DOI:10.3899/jrheum.211180 |
 2023, Vol. 44
2023, Vol. 44