文章信息
- 秦莉, 陈波, 牛静雅, 王君, 王占国, 武鸣, 周金意, 张庆军, 周芳, 周正元, 张宁, 吕红艳, 盛红艳, 王文绢.
- Qin Li, Chen Bo, Niu Jingya, Wang Jun, Wang Zhanguo, Wu Ming, Zhou Jinyi, Zhang Qingjun, Zhou Fang, Zhou Zhengyuan, Zhang Ning, Lyu Hongyan, Sheng Hongyan, Wang Wenjuan
- 社区糖尿病患者的周围血管病变患病率及其影响因素研究
- The prevalence and risk factors of diabetic peripheral artery disease in Chinese communities
- 中华流行病学杂志, 2022, 43(12): 1932-1938
- Chinese Journal of Epidemiology, 2022, 43(12): 1932-1938
- http://dx.doi.org/10.3760/cma.j.cn112338-20211026-00823
-
文章历史
收稿日期: 2021-10-26
2. 北京市疾病预防控制中心结核病预防控制所, 北京 100035;
3. 江苏省疾病预防控制中心, 南京 210009;
4. 湖北省疾病预防控制中心, 武汉 430079;
5. 常熟市疾病预防控制中心, 常熟 215500;
6. 武汉市江岸区疾病预防控制中心, 武汉 430014
2. Center for Tuberculosis Control and Prevention, Beijing Center for Disease Prevention and Control, Beijing 100035, China;
3. Jiangsu Provincial Center for Disease Control and Prevention, Nanjing 210009, China;
4. Hubei Provincial Center for Disease Control and Prevention, Wuhan 430079, China;
5. Changshu Center for Disease Control and Prevention, Changshu 215500, China;
6. Jiang'an District Center for Disease Control and Prevention, Wuhan 430014, China
周围血管病变(peripheral arterial disease,PAD)是糖尿病大血管并发症的重要组成部分,表现为下肢动脉的硬化、狭窄或闭塞,极易导致糖尿病患者足部溃疡、周围神经病变甚至截肢,是患者致残的主要原因[1]。与非糖尿病患者相比,糖尿病患者发生PAD的风险高2倍,且发病年龄早、病情进展快、预后差、死亡率更高[2-4]。与未患PAD的糖尿病患者相比,并发PAD的患者发生心肌梗死、卒中、心血管死亡的风险高3~6倍[5]。2019年中国糖尿病患者的数量高达1.16亿,预示我国有数量庞大的潜在糖尿病PAD患者群体[6]。但国内糖尿病患者中的PAD患病率研究较少,且局限于大医院门诊或住院的糖尿病患者,由于存在选择偏倚,研究结果难以反映社区管理糖尿病患者的PAD流行状况。
2009年我国将“2型糖尿病患者健康管理服务”纳入基本公共卫生服务项目。糖尿病患者管理工作在基层逐年深入,但缺乏以社区管理糖尿病患者为研究对象、能较好反映PAD的流行病学研究报道。本研究以中国糖尿病足预防模式项目为基础,以社区管理的糖尿病患者为研究对象,分析其PAD的流行特征,为防治糖尿病患者PAD、促进社区糖尿病患者管理提供科学依据。
对象与方法1. 研究对象:数据来自中国糖尿病足预防模式项目的基线调查,研究对象为在基层卫生服务机构参加“2型糖尿病患者健康管理服务”的糖尿病患者。于2015年8-9月,在江苏省常熟市及武汉市江岸区分别随机抽取4个社区,共8个社区,在各社区卫生服务中心随机抽取符合纳入、排除标准的糖尿病患者。纳入标准:①符合WHO 1999年糖尿病诊断标准;②正在参加社区2型糖尿病患者健康管理(≥35岁);③能够正常交流且签署知情同意书。排除患有严重急、慢性疾病的糖尿病患者,包括恶性肿瘤、心肌梗死及脑卒中的急性期等不能参加调查的人。为满足干预项目的需要,采用随机对照试验公式
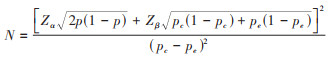
计算样本量,得到每个社区样本量为300人,8个社区应调查2 400人,实际调查2 528人。
样本量计算采用患病率调查多阶段抽样公式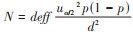
2. 研究方法:通过统一设计的结构化调查表,以面对面调查方式收集年龄、性别、文化程度、现在吸烟、现在饮酒、身体活动水平、糖尿病病程、降糖药物使用、高血压及心肌梗死或心绞痛史等信息;通过体格检查获得身高、体重、血压值;踝肱指数(ABI)测量为休息10 min后,以仰卧位进行,由经培训合格的临床医生使用Bidop ES-100V3多普勒仪(Hadeco,Kawasaki,日本)测量踝部和肱部的SBP,每侧ABI=同侧足背/胫骨后SBP较高者÷右臂/左臂SBP较高者,选择两侧ABI中较低值为该名患者的ABI。实验室检查采用己糖激酶法于采血后24 h内完成FPG、100 g标准馒头餐后2 h静脉血糖检测。
3. 质量控制(质控):基线调查采取全程质控。调查员为社区的医护人员,调查前采用统一调查方案对其培训且考核合格;充分动员调查对象,通知并提醒次日调查前应空腹8 h以上;检查工具统一提供并进行检查和校准。调查中,现场设协调员和质控员,发现问题及时纠正。调查后,数据双录入并进行一致性检验、数据清理和分析程序复核。
4. 相关指标定义:PAD:按照《中国2型糖尿病防治指南(2017版)》标准,患者静息ABI≤0.9或自报已被医疗机构诊断为PAD[8]。高血压:调查前自报高血压病史或调查时符合《中国高血压防治指南2010》诊断标准,即SBP≥140 mmHg(1 mmHg=0.133 kPa)和/或DBP≥90 mmHg[9]。血糖控制达标:根据《中国2型糖尿病防治指南(2017年版)》标准,将FPG≤7.0 mmol/L、餐后2 h血糖≤10.0 mmol/L分别定义为FPG控制达标和餐后血糖控制达标[8]。超重/肥胖分类:按照《中国成人超重和肥胖症预防控制指南》分类标准,体重过轻、体重正常、超重、肥胖的BMI(kg/m2)分别为 < 18.5、18.5~、24.0~、≥28.0[10]。身体活动水平:采用《国际身体活动量表短卷》(IPAQ-SF),对过去7 d身体活动种类、频率和时长进行调查。按照IPAQ-SF推荐标准,将身体活动水平分为高、中、低组[11]。现在吸烟指被调查时吸烟。现在饮酒指过去12个月内有饮酒行为。心肌梗死或心绞痛史:自报有既往心肌梗死或心绞痛病史。血脂异常史:自报被医疗机构诊断为血脂异常。
5. 统计学分析:用EpiData 3.1软件建数据库,用SAS 9.4软件进行数据清洗和统计学分析。不服从正态分布的计量资料用M(Q1,Q3)描述;计数资料用频数、构成比或率描述;率的差异性检验和趋势性检验分别采用Pearson χ2检验和Cochran-Armitage趋势检验;影响因素分析采用非条件多因素logistic回归方法。双侧检验,以P < 0.05为差异有统计学意义。
结果1. 基本情况:共调查2 528名糖尿病患者,剔除既往未诊断PAD中ABI检查缺失(8人)或ABI > 1.3且未自报被医疗机构诊断为PAD者(98人),共计106人,共收集有效问卷2 422份,有效调查率为95.8%。其中江岸区1 171人,常熟市1 251人;年龄M(Q1,Q3)为65.0(60.0,70.0)岁,女性偏多(59.7%),文化程度偏低,初中及以下文化程度者占71.8%;糖尿病病程M(Q1,Q3)为7.0(3.0,11.0)年,82.0%的患者使用降糖药物,但75.4%的患者餐后血糖控制未达标。见表 1。
2. PAD患病率:社区管理糖尿病患者的PAD患病率为11.2%(常熟市6.6%,江岸区16.1%),其中有87.5%(237/271)的患者为新诊断为PAD。< 55、55~、65~、≥75岁年龄组的患病率分别为7.8%、6.0%、12.9%、22.5%。共患高血压者(12.5%)高于非高血压患者(8.3%),自报血脂异常史者(13.2%)高于非异常者(10.4%),心肌梗死或心绞痛史者(23.9%)高于无心肌梗死或心绞痛史者(10.3%),餐后血糖控制不达标者(12.2%)高于控制达标者(8.2%),身体活动低水平者(12.7%)高于高水平者(7.3%),现在饮酒者(6.6%)低于不饮酒者(12.1%),均差异有统计学意义(P < 0.05);且趋势性检验显示,年龄越大(趋势χ2=-7.31,P < 0.001)、文化程度越高(趋势χ2=-3.95,P < 0.001)、糖尿病病程越长(趋势χ2=-3.91,P < 0.001),糖尿病患者PAD患病率越高;性别、现在吸烟、超重和肥胖、FPG控制达标的PAD患病率均差异无统计学意义(P > 0.05)。见表 2。
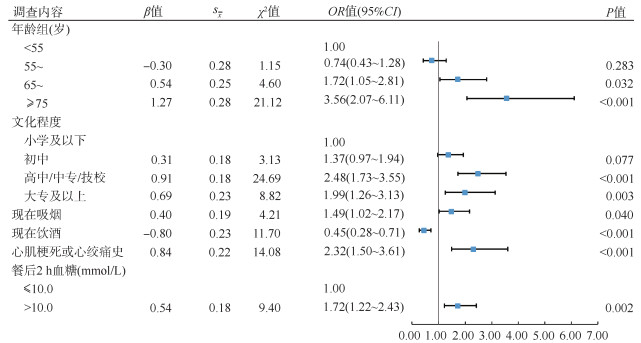
3. 糖尿病PAD的影响因素分析:采用非条件多因素logistic回归,以是否有PAD为因变量,将年龄、性别、文化程度、糖尿病病程、现在吸烟、现在饮酒、身体活动水平、高血压、血脂异常史、心肌梗死或心绞痛史、FPG、餐后血糖控制为自变量,纳入标准0.10,排除标准0.05,采用逐步回归方法进行分析。结果显示,年龄、文化程度、现在吸烟、现在饮酒、餐后血糖控制和心肌梗死或心绞痛史均是糖尿病PAD的相关因素。与 < 55岁年龄组相比,55~、65~、≥75岁年龄组糖尿病患者PAD患病的OR值分别为0.74(95%CI:0.43~1.28)、1.72(95%CI:1.05~2.81)、3.56(95%CI:2.07~6.11);与小学及以下文化程度相比,初中、高中/中专/技校、大专及以上文化程度的糖尿病患者PAD患病的OR值分别为1.37(95%CI:0.97~1.94)、2.48(95%CI:1.73~3.55)、1.99(95%CI:1.26~3.13);现在吸烟(OR=1.49,95%CI:1.02~2.17)、现在饮酒(OR=0.45,95%CI:0.28~0.71)、餐后血糖控制未达标(OR=1.72,95%CI:1.22~2.43)、心肌梗死或心绞痛史(OR=2.32,95%CI:1.50~3.61)均是糖尿病PAD的影响因素。见图 1。
|
| 图 1 社区糖尿病患者周围血管病变多因素logistic回归分析 |
PAD已成为严重的公共卫生问题,据估计2020年我国约有4 113万名PAD患者[3]。糖尿病是其重要的危险因素,主要通过炎症反应、内皮功能障碍和凝血功能障碍等机制引发PAD,而PAD同时也会加重糖尿病其他并发症的进展[12]。PAD的典型表现是间歇性跛行,但在糖尿病患者中通常由于合并周围神经病变,绝大多数患者是没有症状的[13]。因此,在糖尿病患者中,早期筛查PAD尤为重要。
国外调查发现,PAD患病率为7%~30%[2, 14-15]。本研究中社区管理2型糖尿病患者的PAD患病率为11.2%[年龄(64.9±8.7)岁,糖尿病病程(8.1±6.3)年]。该患病率低于诊断方法相同、调查对象糖尿病病程和年龄相似的2013年对国内15家三级医院糖尿病患者的调查,其PAD患病率为19.5%[年龄(63.8±8.3)岁,糖尿病病程(8.6±7.4)年][16],也低于2016年对国内30家医院糖尿病住院患者调查[年龄(64.6±9.21)岁]的患病率25.5%,但接近门诊糖尿病患者[年龄(63.4±8.57)岁]的患病率12.6%[7],原因可能是同门诊或社区管理的糖尿病患者相比,三级医院住院患者的病程偏长、病情较重及患者对医院有选择偏性。
采用ABI诊断周围血管疾病,灵敏度为68%~84%,特异度为84%~99%[17]。由于少数血管钙化的患者,ABI通常较高,容易出现假阴性错误,指南推荐ABI > 1.3的患者,需进一步采用测量趾肱指数或者二维超声成像来确定是否患有周围神经病变[7]。本研究未将ABI > 1.3的调查对象(98人)纳入分析,有可能使PAD患病率被低估。
多因素结果显示,年龄、现在吸烟、心肌梗死或心绞痛史、餐后血糖控制是PAD患病的相关因素,与过往研究结果类似[18-20]。《中国2型糖尿病防治指南(2017版)》建议 > 50岁的糖尿病患者应常规进行PAD的筛查[7]。本研究发现≥65岁糖尿病患者PAD患病率明显增加,和国内其他研究相似[18-19],建议针对社区管理的老年糖尿病患者进行PAD筛查,当医疗资源有限时优先关注≥65岁人群。研究发现控制糖化血红蛋白能够有效减少糖尿病血管病变的发生发展[21]。本研究中血糖控制未达标与PAD患病风险增加相关,并且多因素分析发现,餐后血糖比FPG与PAD患病率之间相关性更强,可能与血糖波动有关,急性血糖波动比慢性持续性高血糖更显著地促进氧化应激反应和损害内皮功能[22]。目前社区管理的糖尿病患者由国家免费提供每年4次的FPG检测,但是对于医疗条件较好地区,应提倡糖尿病患者的餐后血糖或糖化血红蛋白检测。其他研究显示心肌梗死或心绞痛、PAD都与动脉粥样硬化有关,约有25%的缺血性心脏病患者同时合并PAD,心脑血管疾病的发生也与低ABI有关[18, 20]。本研究中发现高血压患者PAD患病率较高,但多因素逐步回归模型分析过程中,当“心肌梗死或心绞痛史”放入模型后,“高血压”被排出模型,原因可能是“高血压”和“心肌梗死或心绞痛史”是PAD的共同危险因子,二者有共线性且心肌梗死或心绞痛史反映了严重的动脉粥样硬化,而动脉粥样硬化是PAD发生的病理基础。
多因素分析中发现现在饮酒者与不饮酒者相比PAD患病率较低。Yang等[23]发现中国2型糖尿病患者饮酒 > 64 g/d比不饮酒者有更高的患病风险(OR=6.35,95%CI:1.78~22.65);另一对中国男性的调查发现[24],饮酒 < 60 g/d时,酒精消耗与PAD患病呈负相关,饮酒≥60 g/d时,酒精消耗与PAD患病成正相关。本研究人群的酒精消耗M(Q1,Q3)为22(6,47)g/d,远低于上述研究中的危险剂量,这可能是本研究饮酒者反而患病率较低的原因。单因素分析时,糖尿病病程越长的患者有更高的PAD患病率,当糖尿病病程≥5年时,PAD患病率上升明显。但多因素分析显示,糖尿病病程不是PAD的独立影响因素,原因可能为糖尿病病程与年龄、餐后血糖控制相关,此结果可能受病程与上述自变量的共线性所致。本研究中发现文化程度较高者,PAD患病率反而越高,原因可能为文化程度较高者因工作性质静坐时间偏长、工作压力大等心脑血管疾病的危险因素较多。
本调查基于整群随机抽样,选择在基层医疗卫生机构管理的糖尿病患者,由培训合格的医生采用方便可靠的ABI检查进行筛查,可较好反映社区糖尿病患者的PAD患病率,为社区糖尿病并发症防控提供依据。但是,本研究采用的横断面研究方法,无法确定相关因素与PAD的因果关联;调查中心肌梗死或心绞痛史、血脂异常史和糖尿病患病时间均由调查对象自报,可能存在一定的回忆偏倚。
综上所述,本研究发现社区管理2型糖尿病患者中PAD有较高的患病率,且其中有87.5%的患者为新诊断为PAD,年龄增加、吸烟、餐后血糖控制未达标均可增加糖尿病PAD的患病风险。针对已在社区管理的糖尿病患者,应持续加强规范化管理;对≥65岁、合并心肌梗死或心绞痛史、高血压、吸烟、糖尿病病程≥5年或餐后血糖控制未达标的糖尿病患者要重点关注,落实常规PAD筛查。同时,可在基层医疗卫生机构大力推广方便、适宜的ABI筛查,加强基层医护人员关于糖尿病并发症筛查技术、操作方法的培训,进一步提升基层管理糖尿病患者的PAD常规筛查率,及早发现尽早治疗,更好地防控PAD,预防糖尿病足的发生。
利益冲突 所有作者声明无利益冲突
作者贡献声明 秦莉:论文撰写、数据整理、统计学分析;陈波、王文绢:研究指导、论文修改;牛静雅、王君:数据整理、统计学分析;王占国、武鸣、周金意、张庆军、周芳、周正元、张宁、吕红艳、盛红艳:数据收集
| [1] |
International Diabetes Federation. Clinical Practice Recommendations on the Diabetic Foot: A guide for health care professionals: International Diabetes Federation [EB/OL]. (2017-06-21)[2022-04-18]. https://www.idf.org/e-library/guidelines/119-idf-clinical-practice-recommendations-on-diabetic-foot-2017.html.
|
| [2] |
Berger JS, Hochman J, Lobach I, et al. Modifiable risk factor burden and the prevalence of peripheral artery disease in different vascular territories[J]. J Vasc Surg, 2013, 58(3): 673-681.e1. DOI:10.1016/j.jvs.2013.01.053 |
| [3] |
Song PG, Rudan D, Wang ML, et al. National and subnational estimation of the prevalence of peripheral artery disease (PAD) in China: a systematic review and meta-analysis[J]. J Glob Health, 2019, 9(1): 010601. DOI:10.7189/jogh.09.010601 |
| [4] |
Vrsalovic M, Vucur K, Presecki AV, et al. Impact of diabetes on mortality in peripheral artery disease: a meta-analysis[J]. Clin Cardiol, 2017, 40(5): 287-291. DOI:10.1002/clc.22657 |
| [5] |
Criqui MH, Langer RD, Fronek A, et al. Mortality over a period of 10 years in patients with peripheral arterial disease[J]. N Engl J Med, 1992, 326(6): 381-386. DOI:10.1056/NEJM199202063260605 |
| [6] |
International Diabetes Federation. IDF Diabetes Atlas Ninth Edition 2019[EB/OL]. [2022-04-18]. https://diabetesatlas.org/atlas/ninth-edition/.
|
| [7] |
Zhang XM, Ran XW, Xu ZR, et al. Epidemiological characteristics of lower extremity arterial disease in Chinese diabetes patients at high risk: a prospective, multicenter, cross-sectional study[J]. J Diabetes Complications, 2018, 32(2): 150-156. DOI:10.1016/j.jdiacomp.2017.10.003 |
| [8] |
中华医学会糖尿病学分会. 中国2型糖尿病防治指南(2017年版)[J]. 中华糖尿病杂志, 2018, 10(1): 4-67. Chinese Diabetes Society. Chinese guideline for the prevention and treatment of type 2 diabetes mellitus (2017 edition)[J]. Chin J Diabetes Mellit, 2018, 10(1): 4-67. DOI:10.3760/cma.j.issn.1674-5809.2018.01.003 |
| [9] |
中国高血压防治指南修订委员会. 中国高血压防治指南2010[J]. 中华心血管病杂志, 2011, 39(7): 579-616. Writing Group of 2010 Chinese Guidelines for the Management of Hypertension. 2010 Chinese guidelines for the management of hypertension[J]. Chin J Cardiol, 2011, 39(7): 579-616. DOI:10.3760/cma.j.issn.0253-3758.2011.07.002 |
| [10] |
中华人民共和国卫生部疾病控制司. 中国成人超重和肥胖症预防控制指南[M]. 北京: 人民卫生出版社, 2006.
|
| [11] |
Macfarlane DJ, Lee CCY, Ho EYK, et al. Reliability and validity of the Chinese version of IPAQ (short, last 7 days)[J]. J Sci Med Sport, 2007, 10(1): 45-51. DOI:10.1016/j.jsams.2006.05.003 |
| [12] |
Thiruvoipati T, Kielhorn CE, Armstrong EJ. Peripheral artery disease in patients with diabetes: Epidemiology, mechanisms, and outcomes[J]. World J Diabetes, 2015, 6(7): 961. DOI:10.4239/wjd.v6.i7.961 |
| [13] |
Bundó M, Muñoz L, Pérez C, et al. Asymptomatic peripheral arterial disease in type 2 diabetes patients: a 10-year follow-up study of the utility of the ankle brachial index as a prognostic marker of cardiovascular disease[J]. Ann Vasc Surg, 2010, 24(8): 985-993. DOI:10.1016/j.avsg.2010.06.001 |
| [14] |
Hirsch AT, Criqui MH, Treat-Jacobson D, et al. Peripheral arterial disease detection, awareness, and treatment in primary care[J]. JAMA, 2001, 286(11): 1317-1324. DOI:10.1001/jama.286.11.1317 |
| [15] |
Sanna G, Alesso D, Mediati M, et al. Prevalence of peripheral arterial disease in subjects with moderate cardiovascular risk: Italian results from the PANDORA study Data from PANDORA (Prevalence of peripheral Arterial disease in subjects with moderate CVD risk, with No overt vascular Diseases nor Diabetes mellitus)[J]. BMC Cardiovasc Disord, 2011, 11: 59. DOI:10.1186/1471-2261-11-59 |
| [16] |
Guan H, Li YJ, Xu ZR, et al. Prevalence and risk factors of peripheral arterial disease in diabetic patients over 50 years old in China[J]. Chin Med Sci J, 2007, 22(2): 83-88. |
| [17] |
Gerhard-Herman MD, Gornik HL, Barrett C, et al. 2016 AHA/ACC guideline on the management of patients with lower extremity peripheral artery disease: a report of the American College of Cardiology/American Heart Association task force on clinical practice guidelines[J]. Circulation, 2017, 135(12): e726-779. DOI:10.1161/CIR.0000000000000471 |
| [18] |
Li X, Wang YZ, Yang XP, et al. Prevalence of and risk factors for abnormal ankle-brachial index in patients with type 2 diabetes[J]. J Diabetes, 2012, 4(2): 140-146. DOI:10.1111/j.1753-0407.2011.00171.x |
| [19] |
Chen YJ, Lin MS, Hsu KY, et al. Prevalence of asymptomatic peripheral arterial disease and related risk factors in younger and elderly patients in Taiwan[J]. Angiology, 2013, 65(5): 396-401. DOI:10.1177/0003319713480842 |
| [20] |
Pang XH, Han J, Ye WL, et al. Lower extremity peripheral arterial disease is an independent predictor of coronary heart disease and stroke risks in patients with type 2 diabetes mellitus in China[J]. Int J Endocrinol, 2017, 2017, 9620513. DOI:10.1155/2017/9620513 |
| [21] |
Adler AI, Stevens RJ, Neil A, et al. UKPDS 59: hyperglycemia and other potentially modifiable risk factors for peripheral vascular disease in type 2 diabetes[J]. Diabetes Care, 2002, 25(5): 894-899. DOI:10.2337/diacare.25.5.894 |
| [22] |
母义明, 纪立农, 杨文英, 等. 中国2型糖尿病患者餐后高血糖管理专家共识[J]. 中国糖尿病杂志, 2016, 24(5): 385-392. Mu YM, Ji LN, Yang WY, et al. Chinese expert consensus on management of postprandial hyperglycemia for type 2 diabetes mellitus[J]. Chin J Diabetes, 2016, 24(5): 385-392. DOI:10.3969/j.issn.1006-6187.2016.05.001 |
| [23] |
Yang SS, Wang S, Yang B, et al. Alcohol consumption is a risk factor for lower extremity arterial disease in Chinese patients with T2DM[J]. J Diabetes Res, 2017, 2017, 8756978. DOI:10.1155/2017/8756978 |
| [24] |
Xie X, Ma YT, Yang YN, et al. Alcohol consumption and ankle-to-brachial index: results from the Cardiovascular Risk Survey[J]. PLoS One, 2010, 5(12): e15181. DOI:10.1371/journal.pone.0015181 |
 2022, Vol. 43
2022, Vol. 43



