文章信息
- 张泽云, 袁满琼, 石再兴, 方亚.
- Zhang Zeyun, Yuan Manqiong, Shi Zaixing, Fang Ya
- 中国中老年人共病发展轨迹及其对新发失能的影响
- Multimorbidity developmental trajectory among middle-aged and older adults and its impact on new-onset disability in China
- 中华流行病学杂志, 2022, 43(12): 1893-1899
- Chinese Journal of Epidemiology, 2022, 43(12): 1893-1899
- http://dx.doi.org/10.3760/cma.j.cn112338-20220519-00438
-
文章历史
收稿日期: 2022-05-19
人口老龄化已成为我国人口发展的主要趋势,截至2020年,≥65岁老年人口达1.9亿,占总人口的13.5%[1]。据估计,我国约有1.8亿老年人患慢性病,老年人患≥1种慢性病已超2/3,1/3以上的老年人同时患有≥2种慢性病[2]。随着生活方式的改变,慢性病患病年龄趋于年轻化,在中年人群中也越来越普遍[3]。共病(multimorbidity)指一个人同时患≥2种慢性病[4],其对个体功能、医疗卫生资源等造成的影响,远高于这些疾病单独产生的影响[5]。
目前有关共病的研究多局限于60岁以上老年人群[6-7],对中年人群的研究相对较少,且多数基于横断面数据[8],难以描述共病的动态变化过程,有关共病如何随时间发展的研究仍然不足[9-10]。由于中老年人群的人口学、行为学等特征存在差异,其慢性病累积过程可能存在异质性,共病发展轨迹的拟合将有助于识别具有相似特征和预后的同质群体,进而采取有针对性的干预措施。已有研究表明失能的风险随着慢性病数目的增加而升高[11],不同类别的共病发展轨迹对中老年人失能的影响可能存在差异。因此,本研究基于组基轨迹模型识别我国中老年群体中不同的共病发展轨迹,并分析其对新发失能的影响,揭示我国中老年人共病的进展过程对日常活动能力的影响,为预防中老年人失能提供理论依据。
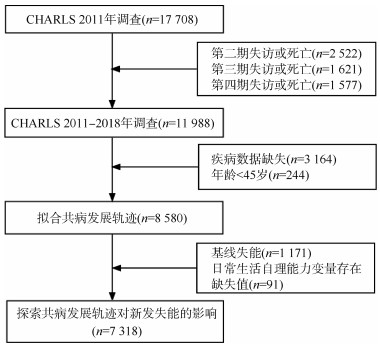
资料与方法1. 资料来源:本研究基于中国健康与养老追踪调查(China Health and Retirement Longitudinal Study,CHARLS)2011-2018年数据。CHARLS项目于2011年在全国范围内进行基线调查,每2或3年随访1次,覆盖了28个省份的150个县级单位的450个村级单位,是我国具有全国代表性的中老年人健康调查之一[12]。本研究以≥45岁中老年人作为研究对象,排除失访、死亡和关键变量缺失者,纳入8 580人用于识别共病发展轨迹。进一步排除基线失能或日常生活自理能力存在缺失值的人群,最终纳入7 318人探索共病发展轨迹对新发失能的影响。见图1。
|
| 注:CHARLS:中国健康与养老追踪调查 图 1 样本筛选流程 |
2. 研究内容:慢性病患病情况由“是否有医生曾经告诉过您有以下这些慢性病”获得,14种慢性病包括高血压、血脂异常、糖尿病或血糖升高、恶性肿瘤、慢性肺部疾病、肝脏疾病、心脏病、卒中、肾脏疾病、胃部或消化系统疾病、情感和精神障碍、与记忆相关疾病、关节炎或风湿病、哮喘。失能由日常生活能力活动量表测量,6项功能包括洗澡、穿衣、如厕、室内走动、起床、进食,如果在执行任意一项功能时有任何程度的困难,则被定义为失能。新发失能指基线未失能,随访时任一时期发生失能。协变量包括性别、年龄、文化程度、婚姻状况、居住地、职业、自评健康、BMI(体重过轻为<18.5 kg/m2、正常为18.5~kg/m2、超重为24.0~kg/m2、肥胖为≥28.0 kg/m2)[13]、吸烟、饮酒、睡眠时长、家庭年人均支出水平(按家庭年人均消费总额四分位数分组)、锻炼、社会活动(有无参加任一社会活动)、公共医疗保险。
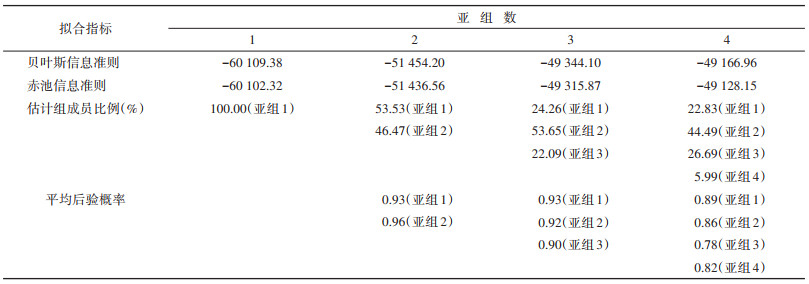
3. 组基轨迹模型:能够探索总体中含有多少发展趋势不同的亚组,并确定各亚组的发展轨迹。本研究将慢性病计数定义为组基轨迹模型中随时间变化的因变量,采用零膨胀泊松模型分析数据。通过比较不同亚组数(1~6组)和不同轨迹形状(线性、二次方和三次方)的模型,反复进行模型拟合。模型的评价与选取基于以下指标:①贝叶斯信息准则(Bayesian information criterion,BIC)和赤池信息准则(Akaike’s information criterion,AIC),BIC和AIC值越接近0,模型拟合效果越好;②平均后验概率>0.7表示模型拟合良好;③估计组成员数应大于总样本量的5%[14]。
4. 统计学分析:计数资料采用频数进行描述,计量资料采用x±s描述,并用χ2检验(分类变量)和方差分析(连续变量)进行组间比较。首先基于组基轨迹模型识别共病发展轨迹,进一步采用3个含时间依存协变量Cox回归模型探索共病发展轨迹对新发失能的影响,其中模型1未调整任何协变量,模型2调整了人口学特征(年龄、性别、文化程度、婚姻状况、居住地、职业、自评健康、BMI、家庭年人均支出水平),模型3进一步调整了吸烟、饮酒、睡眠时长、锻炼、社会活动和公共医疗保险等行为学特征。含时间依存协变量Cox回归模型是一种非比例风险回归模型,能够同时考虑到协变量随时间的变化对风险回归模型的影响。本研究中数据清理和分析采用Stata 16.0软件,统计图表的绘制采用R 4.1.2软件,双侧检验,以P<0.05为差异有统计学意义。
结果1. 基本情况:共纳入调查对象8 580人,其中女性4 452人(51.9%);年龄为(57.8±8.7)岁;自评健康差者占21.7%;小学以下文化程度者3 769人(43.9%);体重正常者占53.4%;52.0%的人从事农业工作;42.7%的人睡眠时长为7~8 h/d;不吸烟与不饮酒者分别占60.4%和60.5%;815人(9.5%)处于单身状态;3 017人(35.2%)居住在农村。共病患病率和慢性病数均呈现逐渐上升的趋势,共病患病率从2011年的35.5%上升到2018年的56.5%,而慢性病数从1.0增加到2.0。见表1。
2. 中老年人共病发展轨迹:通过拟合不同亚组数的模型,发现当亚组数>4时,模型无法收敛。当亚组数为4时,BIC值最接近于0,故确定共病发展轨迹的最佳亚组数为4。进一步拟合不同轨迹形状的模型,结合模型简约原则,得到轨迹形状为线性时模型最佳。此时每个亚组均符合平均后验概率>0.7,估计组成员数大于总样本量的5%的标准,表明当前拟合的模型可接受[15]。见表2。
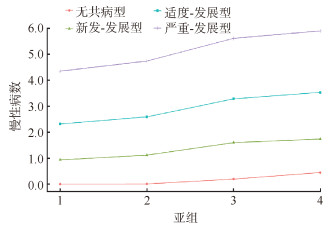
每个亚组的慢性病计数均随时间的增长而增多,亚组1~4呈现由低到高的分层分布。亚组1 (2 136人,24.90%)的慢性病计数最少,该组人群基线时无慢性病,随后缓慢增加至0.4种,定义为无共病型。亚组2(3 758人,43.80%)基线时有0.9种慢性病,逐渐增长到1.7种,定义为新发-发展型。亚组3(2 270人,26.45%)基线时已有共病,随后发展至3.5种,定义为适度-发展型。亚组4(416人,4.85%)人数最少,但该组的慢性病计数一直最高,从基线的4.3种发展至5.9种,定义为严重-发展型。见图2。
|
| 图 2 中国中老年人共病发展轨迹 |
3. 共病发展轨迹组基本情况:无共病型和新发-发展型人群中文化程度高、有工作、吸烟、饮酒、睡眠时长≥7 h/d的占比高,且平均年龄较小。而女性、自评健康差、超重/肥胖、单身、居住在农村、家庭年人均支出水平高在适度-发展型和严重-发展型中占比较高。新发失能发生率在严重-发展型最高,达到了74.0%,而无共病型最低,为15.2%。见表1。
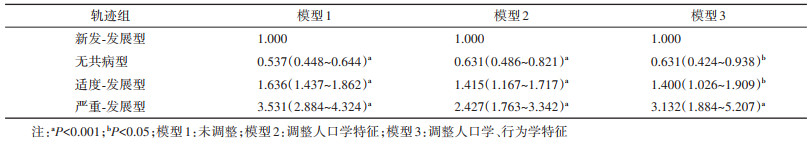
4. 共病发展轨迹与新发失能的关系:模型1 中,适度-发展型(HR=1.636,95%CI:1.437~1.862)和严重-发展型(HR=3.531,95%CI:2.884~4.324)的失能风险增加,而无共病型(HR=0.537,95%CI:0.448~0.644)失能风险降低。调整人口学、行为学特征后,尽管适度-发展型和严重-发展型的失能风险有所下降,无共病型有所上升,但严重-发展型(HR=3.132,95%CI:1.884~5.207)失能发生风险仍然最高,适度-发展型(HR=1.400,95%CI:1.026~1.909)次之,无共病型(HR=0.631,95%CI:0.424~0.938)最低。失能风险随着共病水平的升高而增加,提示共病发展轨迹升高是发生失能的危险因素。见表3。
本研究在我国中老年人群中识别出4类共病发展轨迹:无共病型、新发-发展型、适度-发展型和严重-发展型。高水平共病发展轨迹增加了我国中老年人群失能发生风险,并且随着疾病数量的增加,我国中老年人群失能的风险也随之上升。
本研究识别出的4种不同类型共病发展轨迹与基于韩国[16],英国[17]和中国[18]人群的研究结果类似。超过一半的参与者(68.70%)在随访期间共病发展轨迹处于相对低的水平,表明大部分中老年人处于健康老龄化进程。这一结果可能由于本研究选取完成4期随访的中老年人,纳入的参与者可能更健康,且平均年龄相对较小。此外,与既往研究结果一致[16-18],本研究发现存在共病水平持续较高的亚组,却无随着时间的推移而改善的轨迹(即随着时间的增加,共病水平降低),这可能是由于中老年人慢性病的病程长且病情迁延不愈。
共病发展轨迹对新发失能的影响结果显示,以新发-发展型为对照组,归属于严重-发展型的人群发生失能的风险是对照组的3倍左右,随着时间的推移,慢性病的累积数量越多可能表明健康状况下降越快,失能的风险随之增加。如既往文献所述,失能风险随着慢性病数量的增加而增加[11, 19-21]。慢性病促使身体结构和功能的恶化,进而影响日常活动能力导致失能[22]。且共病可能损害多个系统和器官而增加失能风险。Verbrugge和Jette[23]将慢性病到失能的过程视为从病理学变化到功能损伤,最终到失能的过程。在这一过程中,失能被认为是超出一定阈值的病理损伤,共病患者的病理变化可能更接近失能阈值,进而使共病患者更容易发生功能损伤甚至失能。本研究通过比较不同类型共病发展轨迹的失能风险进一步证实了既往研究结果。
本研究基于全国代表性的中老年人群数据,采用组基轨迹模型识别共病发展轨迹潜在类别,有效识别具有相似慢性病发展历程的人群亚组,并进一步研究其对新发失能的影响,为我国中老年人群的失能风险干预提供依据。本研究存在局限性。首先,慢性病信息基于自报的方式采集。尽管已有研究证明采用自我报告的疾病数据具有有效性[24],这种方式仍然可能会低估人群中的患病情况。其次,由于数据限制,本研究无法考虑疾病的严重程度和共病模式的变化,以及其他混杂因素(如饮食等)对研究结果的影响。由于某些慢性疾病具有共同的病理生理机制或危险因素[25],它们更可能以联合模式共存即共病模式——人群中高发的慢性病共病的组合模式[26],且不同共病模式对健康结局的影响可能不同[25]。因此,后续可通过研究共病模式的发生发展进一步优化研究。最后,本研究只纳入了完成4期随访的人群,患有多种慢性病的中老年人可能会因身体状况较差或死亡而退出调查,从而使结果外推性受到一定程度的影响,后续可将代表性更高的样本纳入分析。
综上所述,我国中老年人群的共病会随着时间的推移而动态变化,遵循不同的发展轨迹,且不同类型的共病发展轨迹的失能风险不同。共病发展轨迹可能有助于识别具有相似特征和预后的同质群体,根据共病发展轨迹类型的不同,合理地对共病患者进行预防控制、干预和管理是促进中老年人健康,降低失能风险的重点。
利益冲突 所有作者声明无利益冲突
作者贡献声明 张泽云:数据整理分析、论文撰写;袁满琼:研究指导、论文修改;石再兴、方亚:研究指导、论文修改、经费支持
| [1] |
中华人民共和国国家统计局. 中国统计年鉴(2021-09)[2022-05-19]. http://www.stats.gov.cn/tjsj/ndsj/2021/indexch.htm.
|
| [2] |
王丽敏, 陈志华, 张梅, 等. 中国老年人群慢性病患病状况和疾病负担研究[J]. 中华流行病学杂志, 2019, 40(3): 277-283. Wang LM, Chen ZH, Zhang M, et al. Study of the prevalence and disease burden of chronic disease in the elderly in China[J]. Chin J Epidemiol, 2019, 40(3): 277-283. DOI:10.3760/cma.j.issn.0254-6450.2019.03.005 |
| [3] |
廉萍, 李耀军. "健康长沙"战略下慢性病患者社区卫生服务需求的研究[J]. 甘肃科技纵横, 2022, 51(2): 62-64,74. Lian P, Li YJ. Research on community health service needs of chronic disease patients under the "Healthy Changsha" strategy[J]. Gansu Sci Technol, 2022, 51(2): 62-64,74. DOI:10.3969/j.issn.1672-6375.2022.02.019 |
| [4] |
van den Akker M, Buntinx F, Knottnerus JA. Comorbidity or multimorbidity: what's in a name? A review of literature[J]. Eur J General Pract, 1996, 2(2): 65-70. DOI:10.3109/13814789609162146 |
| [5] |
Marengoni A, Angleman SB, Melis RJF, et al. Aging with multimorbidity: A systematic review of the literature[J]. Ageing Res Rev, 2011, 10(4): 430-439. DOI:10.1016/j.arr.2011.03.003 |
| [6] |
Yarnall AJ, Sayer AA, Clegg A, et al. New horizons in multimorbidity in older adults[J]. Age Ageing, 2017, 46(6): 882-888. DOI:10.1093/ageing/afx150 |
| [7] |
Beard JR, Officer A, de Carvalho IA, et al. The World report on ageing and health: a policy framework for healthy ageing[J]. Lancet, 2016, 387(10033): 2145-2154. DOI:10.1016/S0140-6736(15)00516-4 |
| [8] |
Fortin M, Stewart M, Poitras ME, et al. A systematic review of prevalence studies on multimorbidity: toward a more uniform methodology[J]. Ann Family Med, 2012, 10(2): 142-151. DOI:10.1370/afm.1337 |
| [9] |
Head A, Fleming KM, Kypridemos C, et al. Multimorbidity: the case for prevention[J]. J Epidemiol Commun Health, 2021, 75(3): 242244. DOI:10.1136/jech-2020-214301 |
| [10] |
Xu XL, Mishra GD, Jones M. Evidence on multimorbidity from definition to intervention: An overview of systematic reviews[J]. Ageing Res Rev, 2017, 37: 53-68. DOI:10.1016/j.arr.2017.05.003 |
| [11] |
Rizzuto D, Melis RJF, Angleman SB, et al. Effect of chronic diseases and multimorbidity on survival and functioning in elderly adults[J]. J Am Geriatr Soc, 2017, 65(5): 1056-1060. DOI:10.1111/jgs.14868 |
| [12] |
Zhao YH, Hu YS, Smith JP, et al. Cohort profile: the China Health and Retirement Longitudinal Study (CHARLS)[J]. Int J Epidemiol, 2014, 43(1): 61-68. DOI:10.1093/ije/dys203 |
| [13] |
中华人民共和国国家卫生和计划生育委员会. WS/T 428-2013 成人体重判定[S]. 北京: 中国质检出版社, 中国标准出版社, 2013. State Health and Family Planning Commission of the People's Republic of China. WS/T 428-2013 Criteria of weight for adults[S]. Beijing: China Quality Inspection Press, Standards Press of China, 2013. |
| [14] |
Jones BL, Nagin DS. A note on a stata plugin for estimating group-based trajectory models[J]. Sociol Methods Res, 2013, 42(4): 608613. DOI:10.1177/0049124113503141 |
| [15] |
Nagin DS. Group-based modeling of development[M]. Cambridge: Harvard University Press, 2005.
|
| [16] |
Lee SA, Joo S, Chai HW, et al. Patterns of multimorbidity trajectories and their correlates among Korean older adults[J]. Age Ageing, 2021, 50(4): 1336-1341. DOI:10.1093/ageing/afab002 |
| [17] |
Saito J, Kondo N, Saito M, et al. Exploring 2.5-year trajectories of functional decline in older adults by applying a growth mixture model and frequency of outings as a predictor: a 2010-2013 JAGES longitudinal study[J]. J Epidemiol, 2019, 29(2): 65-72. DOI:10.2188/jea.JE20170230 |
| [18] |
Yao SS, Xu HW, Han L, et al. Multimorbidity measures differentially predicted mortality among older Chinese adults[J]. J Clin Epidemiol, 2022, 146: 97-105. DOI:10.1016/j.jclinepi.2022.03.002 |
| [19] |
Qiao YN, Liu SY, Li GC, et al. Longitudinal follow-up studies on the bidirectional association between ADL/IADL disability and multimorbidity: results from two national sample cohorts of middle-aged and elderly adults[J]. Gerontology, 2021, 67(5): 563-571. DOI:10.1159/000513930 |
| [20] |
王彦茹, 夏慧玲, 刘永兵. 乌鲁木齐市空巢老年人慢性病与日常生活自理能力的关系[J]. 中国老年学杂志, 2014, 34(7): 1908-1910. Wang YR, Xia HL, Liu YB. The relationship between chronic diseases and self-care ability of daily living among empty nesters in Urumqi[J]. Chin J Gerontol, 2014, 34(7): 1908-1910. DOI:10.3969/j.issn.1005-9202.2014.07.082 |
| [21] |
陈炜, 郝世超, 茅范贞, 等. 厦门市老年人失能现状及其影响因素研究[J]. 中国卫生统计, 2015, 32(5): 770-773. Chen W, Hao SC, Mao FZ, et al. Research on the Situation of elderly disability and its impact factors in Xiamen[J]. Chin J Health Stat, 2015, 32(5): 770-773. |
| [22] |
Durstine JL, Painter PL, Franklin BA, et al. Physical activity for the chronically Ill and disabled[J]. Sports Med, 2000, 30(3): 207-219. DOI:10.2165/00007256-200030030-00005 |
| [23] |
Verbrugge LM, Jette AM. The disablement process[J]. Soc Sci Med, 1994, 38(1): 1-14. DOI:10.1016/0277-9536(94)90294-1 |
| [24] |
Simpson F, Boyd CM, Carlson MC, et al. Agreement between self‐report of disease diagnoses and medical record validation in disabled older women: factors that modify agreement[J]. J Am Geriatr Soc, 2004, 52(1): 123-127. DOI:10.1111/j.1532-5415.2004.52021.X |
| [25] |
Prados-Torres A, Calderón-Larrañaga A, Hancco-Saavedra J, et al. Multimorbidity patterns: a systematic review[J]. J Clin Epidemiol, 2014, 67(3): 254-266. DOI:10.1016/j.jclinepi.2013.09.021 |
| [26] |
World Health Organization. The world health report 2008: primary health care now more than ever[M]. Geneva: World Health Organization, 2008.
|
 2022, Vol. 43
2022, Vol. 43