文章信息
- 贾小芳, 王志宏, 黄绯绯, 杜文雯, 姜红如, 苏畅, 张晓帆, 白晶, 张兵, 王惠君.
- Jia Xiaofang, Wang Zhihong, Huang Feifei, Du Wenwen, Jiang Hongru, Su Chang, Zhang Xiaofan, Bai Jing, Zhang Bing, Wang Huijun
- 中国4省份55岁及以上中老年人空腹血糖与轻度认知功能障碍的关联研究
- Association between fasting plasma glucose and mild cognitive impairment in Chinese 55 and older population from four provinces
- 中华流行病学杂志, 2022, 43(10): 1590-1595
- Chinese Journal of Epidemiology, 2022, 43(10): 1590-1595
- http://dx.doi.org/10.3760/cma.j.cn112338-20211223-01012
-
文章历史
收稿日期: 2021-12-23
2020年我国≥60岁人口占全人群的18.74%[1],提示我国人口老龄化加剧,年龄相关性疾病患病形势严峻。据报道,我国≥60岁老年人群轻度认知功能障碍(MCI)患病率为15.5%[2]。MCI是正常老化与痴呆之间的一种认知受损状态,阻止或延缓MCI发展有利于降低痴呆患病率及其疾病负担[3]。因此,识别并减少MCI可调节危险因素的暴露对健康老龄化具有重要意义。越来越多的研究证实不同程度的认知功能减退是糖尿病并发症之一[4-5]。高血糖和低血糖均可导致糖尿病相关的认知功能障碍[6]。FPG作为糖代谢和诊断糖尿病的一项重要生化指标,与MCI的相关研究较少且结果不尽相同[7]。因此,本研究拟利用神经系统疾病专病社区队列研究2018-2019年基线调查数据,分析我国≥55岁中老年人FPG与MCI的关联性,为确定MCI高危人群和采取有效防控措施提供一定的科学依据。
对象与方法1. 研究对象:利用神经系统疾病专病社区队列研究2018-2019年基线调查数据。该项目采用分层多阶段整群随机抽样的方法,在河北、浙江、陕西和湖南4省份抽取调查对象,旨在建立癫痫(> 1岁)、阿尔茨海默病和帕金森病(≥55岁)社区队列。具体研究设计见文献[8-9]。该项目通过中国CDC营养与健康所伦理审查委员会审查(审批号:2017020),调查对象在调查前均签署了知情同意书。本研究选择参加阿尔茨海默病社区队列的未患阿尔茨海默病,具有完整人口统计学、生活方式、疾病史、认知功能测试和心理评估信息及血生化检测数据、有基本日常生活能力的≥55岁中老年人作为研究对象,排除FPG < 3.9 mmol/L者[10],最终有3 272人纳入分析。
2. 研究方法:
(1)认知功能评估及MCI判定:采用简明精神状态检查(MMSE)[11]和蒙特利尔认知测验(MoCA)中文版量表[12]对所有调查对象进行认知功能评估。要求经培训合格的调查员严格按照指导语、采用面对面方式在规定的时长内完成认知评估(MMSE量表:5~10 min;MoCA量表:10~15 min)。MMSE与MoCA量表均有30个条目,所有条目得分之和即为总分,范围0~30分。当调查对象受教育年限≤12年且MoCA量表总分 < 30分时,则总分加1[13]。分数越高表示认知功能越好。首先按照不同文化程度的切点值判定MCI:MMSE量表总分≤19(小学以下),≤22(小学),≤26(中学及以上)[14];MoCA量表总分≤13(小学以下),≤19(受1~6年教育),≤24(受≥7年教育)[12]。为了提高MCI筛查准确性,本研究进一步将MCI患者定义为MMSE和MoCA量表均判定为MCI者。
(2)血样采集和指标检测:采集调查对象空腹静脉血,按照标准方法分离血清,使用德国罗氏试剂和瑞士罗氏C702全自动生化分析仪,采用酶法和胆固醇氧化酶法检测血清TG、TC、HDL-C、LDL-C和血糖[15]。
(3)FPG分组:为探讨不同FPG水平与MCI的相关性,本研究将FPG五等分为 < 4.98、4.98~、5.34~、5.71~和≥6.49 mmol/L。
(4)其他协变量及分组:经培训合格的调查员通过面对面询问采集人口统计学、生活方式、疾病史等信息;使用身高尺、体重计和水银血压计按照标准方法分别测量身高、体重和血压。采用老年抑郁量表(GDS-30)筛查抑郁症状,量表得分 > 11分则判定为抑郁[9]。根据《中国高血压防治指南(2018修订版)》,具有下列情况之一者,判定为高血压[16]:①SBP≥140 mmHg(1 mmHg=0.133 kPa)和(或)DBP≥90 mmHg;②有高血压史;③目前服用降压药。根据《中国成人血脂异常防治指南(2016年修订版)》[17],具有下列情况之一者,判定为血脂异常:①TG≥2.3 mmol/L;②TC≥6.2 mmol/L;③HDL-C < 1.0 mmol/L;④LDL-C≥4.1 mmol/L。
3. 统计学分析:采用SAS 9.4软件进行数据整理和分析。计量资料经Shapiro-Wilk检验不符合正态分布的用M(Q1,Q3)表示,组间比较采用Kruskal-Wallis检验。计数资料用构成比表示,组间比较采用χ2检验或Cochran-Armitage趋势检验。若多组间差异有统计学意义,则进一步采用Bonferroni法进行两两比较。采用多因素logistic回归模型分析FPG与MCI的关联性,将FPG五等分组转变为哑变量后作为研究变量,以是否患MCI为结局变量,参考有代表性或大规模的相关研究确定纳入模型的调整变量[2, 8, 18],包括年龄、性别、文化程度、家庭收入水平、居住地、目前吸烟、过去一年饮酒、高血压、卒中病史、心肌梗死病史、血脂异常、抑郁和BMI。双侧检验,检验水准α=0.05。
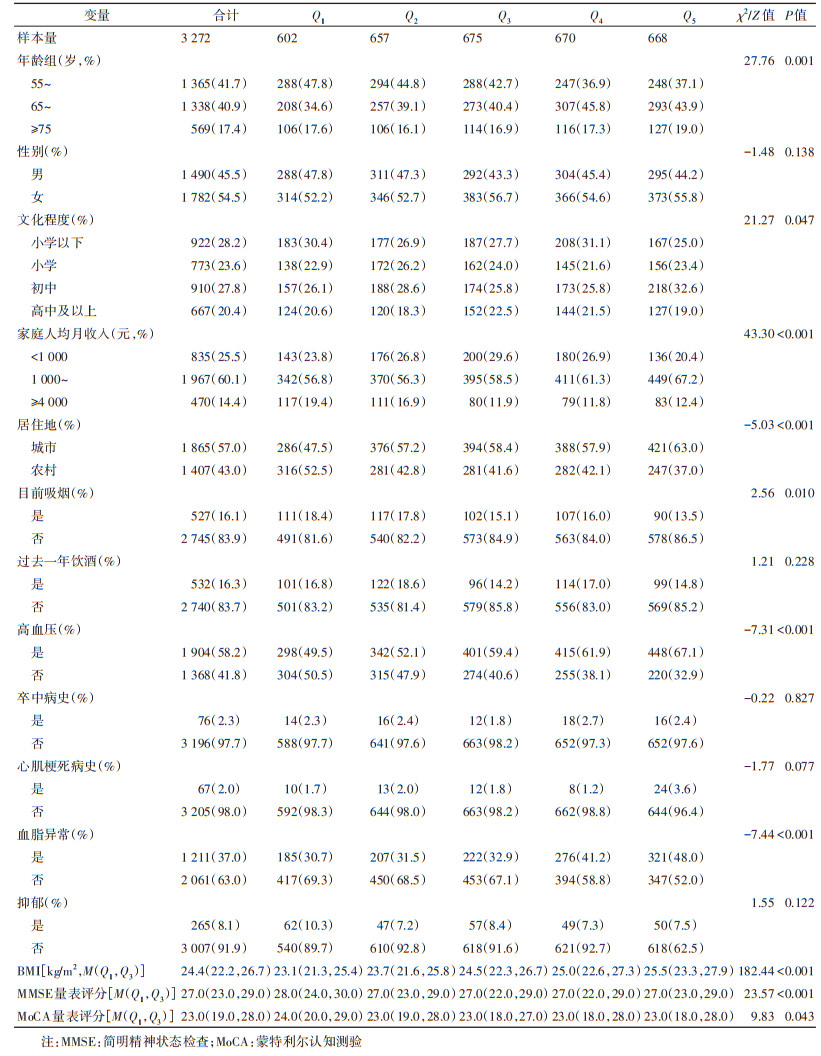
结果1. 一般特征:研究共纳入3 272名≥55岁中老年人。男性占45.5%,≥75岁年龄组比例最低,占17.4%,文化程度为高中及以上者占20.4%。57.0%的研究人群居住在城市。目前吸烟和过去一年饮酒者所占比例分别为16.1%和16.3%。研究人群中58.2%患高血压,37.0%有血脂异常;有卒中和心肌梗死病史者分别占2.3%和2.0%;有8.1%的人群检出抑郁症状;MMSE和MoCA量表中位得分分别为27.0和23.0分。见表 1。
2. 不同FPG组的特征比较:FPG五等分组间不同年龄、文化程度、家庭人均收入、居住地、目前吸烟、高血压和血脂异常组的人群比例差异有统计学意义(均P < 0.05)。其中,居住在城市、有高血压或血脂异常者的比例呈上升趋势,而目前吸烟者所占比例呈下降趋势。不同FPG分组BMI和MMSE、MoCA量表评分的分布差异有统计学意义(均P < 0.05)。见表 1。
3. MCI患病率和FPG水平:研究人群MCI患病率24.8%。FPG五等分组的MCI患病率分别为19.4%、22.2%、29.2%、26.6%和26.1%,组间差异有统计学意义且呈上升趋势(P=0.002)。其中,Q3和Q4组MCI患病率显著高于Q1组,Q3组显著高于Q2组。研究人群FPG中位水平为5.5 mmol/L,其中MCI患者为5.6 mmol/L,非患者为5.5 mmol/L,二者的分布差异有统计学意义(χ2=10.46,P=0.001)。
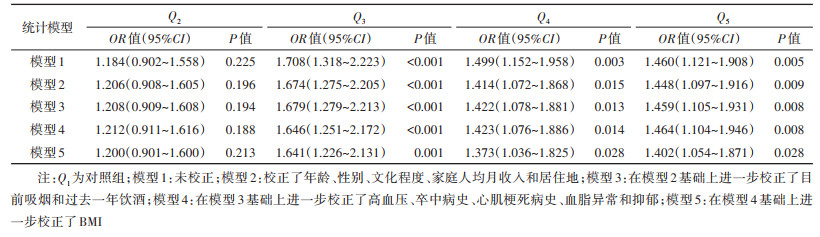
4. FPG和MCI的关联性:单因素logistic回归分析显示,FPG的Q3、Q4和Q5组中老年人MCI患病风险分别是Q1组的1.708(95%CI:1.318~2.223)、1.499(95%CI:1.152~1.958)和1.460(95%CI:1.121~1.908)倍(均P < 0.05)。调整所有混杂因素后,多因素logistic回归分析显示,与Q1组相比,FPG的Q3、Q4和Q5组中老年人MCI患病风险分别增加了64.1%(95%CI:1.226~2.131)、37.3%(95%CI:1.036~1.825)和40.2%(95%CI:1.054~1.871)(均P < 0.05)。见表 2。
MMSE和MoCA是认知相关流行病学调查中较为广泛使用的2种量表。与MoCA相比,MMSE量表筛查MCI具有天花板效应和较低的灵敏度[8]。但是,MoCA的条目较MMSE量表复杂,文化程度低的调查对象可能会出现假阳性的筛查结果[12]。因此,考虑到文化程度为小学及以下者比例较高(51.8%),本研究综合MMSE和MoCA量表筛查结果,将二者均判定为MCI者认定为MCI患者,结果显示我国4省份≥55岁中老年人MCI患病率为24.8%。近年来,我国单一地区如上海市、重庆市、武汉市和广州市开展的社区老年人群流行病学调查显示MCI患病率在12.6%~34.1%[19-22]。此外,2项包含我国多个地区的横断面调查分别报道了老年人群MCI患病率为20.8%[18]和15.5%[2]。尽管由于认知功能评估方法和调查对象特征(如年龄、性别和文化程度等)不同及地区差异等因素导致已报道的我国中老年人群MCI患病率不尽相同,但是以上研究均提示随着我国人口老龄化加剧,MCI已成为一个重要的公共卫生问题,全社会将面临防治MCI和痴呆的巨大挑战。因此,识别MCI相关可调节危险因素可以为制定有效防控措施提供一定的科学依据。
越来越多的研究报道了糖尿病可以增加认知功能减退、MCI以及痴呆患病风险[7, 23],这主要由长期高血糖(FPG或糖化血红蛋白)而引起,也可能与血糖波动和反复发生的低血糖有关[24]。FPG是诊断糖尿病的一项重要指标,其与认知功能的关联尚存在争议。横断面研究报道了FPG与瑞典中年女性情景记忆功能呈显著负相关[25]。以队列研究进行的Meta分析证明了较高的FPG是认知功能障碍及所有痴呆类型的危险因素[7]。本研究将FPG五等分作为分类变量处理,发现各组间MCI患病率存在显著差异,提示FPG与MCI可能存在相关性。调整人口统计学特征、生活方式、慢性病及BMI等混杂因素后,logistic回归分析发现与Q1组相比,FPG的Q3、Q4和Q5组研究人群患MCI的风险分别显著增加64.1%(95%CI:1.226~2.131)、37.3%(95%CI:1.036~1.825)和40.2%(95%CI:1.054~1.871)。已有研究报道我国北京市FPG受损的≥55岁社区中老年人MMSE量表评分低于血糖正常者[26];丹麦老年女性FPG受损导致认知功能障碍的可能性增加44%[27];非洲裔美国中老年人非糖尿病的FPG水平越高,执行功能和言语记忆功能越低[28]。这些发现一定程度上与本研究一致,均提示即使未达到糖尿病诊断标准,控制较高的血糖水平可能降低认知功能减退的风险。类似地,我国上海市对社区≥55岁中老年人开展的一项横断面研究也报道了较高的FPG增加MCI患病风险(OR=1.118,95%CI:1.014~1.233)[29]。但也有研究并未发现FPG与MCI的关联性[30],可能与研究对象的种族、年龄及相关的新陈代谢特征有较大的关系,也提示了进一步研究的必要性。有关较高的FPG增加MCI患病风险的机制尚不明确。长期高血糖对机体造成的氧化应激对血管有显著的负面影响,可加快动脉粥样硬化形成,而大脑的主要能量来源是持续的葡萄糖供应,血糖的变化会改变大脑局部血流而影响认知功能[24]。此外,较高的FPG与纹状体和海马区体积减小显著相关[31],也可导致体内炎性因子水平上升[29]。
本研究存在局限性。首先,横断面研究不能确定FPG与MCI之间的因果关系;此外,本研究没有探讨FPG对不同认知域功能及不同MCI类型的影响。
综上所述,我国4省份≥55岁中老年居民MCI患病率较高,较高的FPG可增加MCI患病风险,提示无论是否患糖尿病,监测和控制血糖对中老年人预防认知功能减退具有重要意义。
利益冲突 所有作者声明无利益冲突
作者贡献声明 贾小芳、黄绯绯:研究设计、论文撰写;王志宏、张兵、王惠君:研究指导、论文修改、经费支持;杜文雯、姜红如、苏畅:数据收集和整理;张晓帆、白晶:统计分析
志谢 感谢参加神经系统疾病专病社区队列研究2018-2019年基线调查的所有工作人员和调查对象
| [1] |
国家统计局. 中国统计年鉴-2021[M]. 北京: 中国统计出版社, 2021. Natioanl Bureau of Statistics of China. 2021 China statistical yearbook[M]. Beijing: China Statistics Press, 2021. |
| [2] |
Jia LF, Du YF, Chu L, et al. Prevalence, risk factors, and management of dementia and mild cognitive impairment in adults aged 60 years or older in China: a cross-sectional study[J]. Lancet Public Health, 2020, 5(12): e661-671. DOI:10.1016/S2468-2667(20)30185-7 |
| [3] |
Anderson ND. State of the science on mild cognitive impairment (MCI)[J]. CNS Spectr, 2019, 24(1): 78-87. DOI:10.1017/S1092852918001347 |
| [4] |
Biessels GJ, Despa F. Cognitive decline and dementia in diabetes mellitus: mechanisms and clinical implications[J]. Nat Rev Endocrinol, 2018, 14(10): 591-604. DOI:10.1038/s41574-018-0048-7 |
| [5] |
Kim HG. Cognitive dysfunctions in individuals with diabetes mellitus[J]. Yeungnam Univ J Med, 2019, 36(3): 183-191. DOI:10.12701/yujm.2019.00255 |
| [6] |
Kodl CT, Seaquist ER. Cognitive dysfunction and diabetes mellitus[J]. Endocr Rev, 2008, 29(4): 494-511. DOI:10.1210/er.2007-0034 |
| [7] |
Xue M, Xu W, Ou YN, et al. Diabetes mellitus and risks of cognitive impairment and dementia: A systematic review and meta-analysis of 144 prospective studies[J]. Ageing Res Rev, 2019, 55: 100944. DOI:10.1016/j.arr.2019.100944 |
| [8] |
Jia XF, Wang ZH, Huang FF, et al. A comparison of the mini-mental state examination (MMSE) with the Montreal cognitive assessment (MoCA) for mild cognitive impairment screening in Chinese middle-aged and older population: a cross-sectional study[J]. BMC Psychiatry, 2021, 21(1): 485. DOI:10.1186/s12888-021-03495-6 |
| [9] |
张晓帆, 刘峰, 刘万普, 等. 中国四省中老年人睡眠时长与抑郁症状的关联性研究[J]. 中华流行病学杂志, 2021, 42(11): 1955-1961. Zhang XF, Liu F, Liu WP, et al. Relationship between sleep duration and depressive symptoms in middle-aged and elderly people in four provinces of China[J]. Chin J Epidemiol, 2021, 42(11): 1955-1961. DOI:10.3760/cma.j.cn112338-20200930-01210 |
| [10] |
中华医学会糖尿病学分会. 中国2型糖尿病防治指南(2020年版)[J]. 中华内分泌代谢杂志, 2021, 37(4): 311-398. Chinese Diabetes Society. Guideline for the prevention and treatment of type 2 diabetes mellitus in China (2020 edition)[J]. Chin J Endocrinol Metab, 2021, 37(4): 311-398. DOI:10.3760/cma.j.cn311282-20210304-00142 |
| [11] |
Katzman R, Zhang MY, Qu OY, et al. A Chinese version of the mini-mental state examination; impact of illiteracy in a Shanghai dementia survey[J]. J Clin Epidemiol, 1988, 41(10): 971-978. DOI:10.1016/0895-4356(88)90034-0 |
| [12] |
Lu JH, Li D, Li F, et al. Montreal cognitive assessment in detecting cognitive impairment in Chinese elderly individuals: a population-based study[J]. J Geriatr Psychiatry Neurol, 2011, 24(4): 184-190. DOI:10.1177/0891988711422528 |
| [13] |
Nasreddine ZS, Phillips NA, Bédirian V, et al. The montreal cognitive assessment, MoCA: a brief screening tool for mild cognitive impairment[J]. J Am Geriatr Soc, 2005, 53(4): 695-699. DOI:10.1111/j.1532-5415.2005.53221.x |
| [14] |
张振馨, 洪霞, 李辉, 等. 北京城乡55岁或以上居民简易智能状态检查测试结果的分布特征[J]. 中华神经科杂志, 1999, 32(3): 149-153. Zhang ZX, Hong X, Li H, et al. The minimental state examination in the Chinese residents population aged 55 years and over in the urban and rural areas of Beijing[J]. Chin J Neurol, 1999, 32(3): 149-153. DOI:10.3760/j.issn:1006-7876.1999.03.006 |
| [15] |
苏畅, 王志宏, 白晶, 等. 中国四省55岁及以上人群血清尿酸与抑郁症状的关联[J]. 环境与职业医学, 2021, 38(8): 810-816. Su C, Wang ZH, Bai J, et al. Association between serum uric acid and depressive symptoms among people aged 55 years and above in four provinces of China[J]. J Environ Occup Med, 2021, 38(8): 810-816. DOI:10.13213/j.cnki.jeom.2021.21004 |
| [16] |
中国高血压防治指南修订委员会, 高血压联盟(中国), 中华医学会心血管病学分会, 等. 中国高血压防治指南(2018年修订版)[J]. 中国心血管杂志, 2019, 24(1): 24-56. Writing Group of 2018 Chinese Guidelines for the Management of Hypertension, Chinese Hypertension League, Chinese Society of Cardiology, et al. 2018 Chinese guidelines for the management of hypertension writing group of 2018[J]. Chin J Cardiovasc Med, 2019, 24(1): 24-56. DOI:10.3969/j.issn.1007-5410.2019.01.002 |
| [17] |
中国成人血脂异常防治指南修订联合委员会. 中国成人血脂异常防治指南(2016年修订版)[J]. 中国循环杂志, 2016, 31(10): 937-950. Joint Commmittee for Revising Chinese Guidelines on Prevention and Treatment of Dyslipidemia in Adults. 2016 Chinese Guidelins on prevention and treatment of dyslipidemia in adults[J]. Chin Circulat J, 2016, 31(10): 937-950. DOI:10.3969/j.issn.1000-3614.2016.10.001 |
| [18] |
Jia JP, Zhou AH, Wei CB, et al. The prevalence of mild cognitive impairment and its etiological subtypes in elderly Chinese[J]. Alzheimer's Dement, 2014, 10(4): 439-447. DOI:10.1016/j.jalz.2013.09.008 |
| [19] |
Ren LB, Zheng YT, Wu LZ, et al. Investigation of the prevalence of Cognitive Impairment and its risk factors within the elderly population in Shanghai, China[J]. Sci Rep, 2018, 8(1): 3575. DOI:10.1038/s41598-018-21983-w |
| [20] |
Giri M, Chen T, Yu WH, et al. Prevalence and correlates of cognitive impairment and depression among elderly people in the world's fastest growing city, Chongqing, People's Republic of China[J]. Clin Interv Aging, 2016, 11: 1091-1098. DOI:10.2147/CIA.S113668 |
| [21] |
Liu XJ, Yin X, Tan AR, et al. Correlates of mild cognitive impairment of community-dwelling older adults in Wuhan, China[J]. Int J Environ Res Public Health, 2018, 15(12): 2705. DOI:10.3390/ijerph15122705 |
| [22] |
Rao DP, Luo X, Tang MN, et al. Prevalence of mild cognitive impairment and its subtypes in community-dwelling residents aged 65 years or older in Guangzhou, China[J]. Arch Gerontol Geriatr, 2018, 75: 70-75. DOI:10.1016/j.archger.2017.11.003 |
| [23] |
Guo MY, Kang KJ, Wang AX, et al. Association of diabetes status with cognitive impairment in two Chinese rural communities[J]. J Neurol Sci, 2020, 415: 116894. DOI:10.1016/j.jns.2020.116894 |
| [24] |
Rizzo MR, Barbieri M, Boccardi V, et al. Dipeptidyl peptidase-4 inhibitors have protective effect on cognitive impairment in aged diabetic patients with mild cognitive impairment[J]. J Gerontol A Biol Sci Med Sci, 2014, 69(9): 1122-1131. DOI:10.1093/gerona/glu032 |
| [25] |
Backeström A, Eriksson S, Nilsson LG, et al. Glucose but not insulin or insulin resistance is associated with memory performance in middle-aged non-diabetic women: a cross sectional study[J]. Diabetol Metab Syndr, 2015, 7: 20. DOI:10.1186/s13098-015-0014-7 |
| [26] |
Xiu S, Zheng Z, Liao QJ, et al. Different risk factors for cognitive impairment among community-dwelling elderly, with impaired fasting glucose or diabetes[J]. Diabetes Metab Syndr Obes Targets Ther, 2019, 12: 121-130. DOI:10.2147/DMSO.S180781 |
| [27] |
Neergaard JS, Dragsbaek K, Christiansen C, et al. Metabolic syndrome, insulin resistance, and cognitive dysfunction: does your metabolic profile affect your brain?[J]. Diabetes, 2017, 66(7): 1957-1963. DOI:10.2337/db16-1444 |
| [28] |
Skinner JS, Morgan A, Hernandez-Saucedo H, et al. Associations between markers of glucose and insulin function and cognitive function in healthy African American elders[J]. J Gerontol Geriatr Res, 2015, 4(4): 232. DOI:10.4172/2167-7182.1000232 |
| [29] |
Li W, Yue L, Sun L, et al. Elevated fasting plasma glucose is associated with an increased risk of MCI: A community- based cross-sectional study[J]. Front Endocrinol, 2021, 12: 739257. DOI:10.3389/fendo.2021.739257 |
| [30] |
Tian S, Huang R, Han J, et al. Increased plasma Interleukin-1β level is associated with memory deficits in type 2 diabetic patients with mild cognitive impairment[J]. Psychoneuroendocrinology, 2018, 96: 148-154. DOI:10.1016/j.psyneuen.2018.06.014 |
| [31] |
Zhang TQ, Shaw M, Humphries J, et al. Higher fasting plasma glucose is associated with striatal and hippocampal shape differences: the 2 sweet project[J]. BMJ Open Diabetes Res Care, 2016, 4(1): e000175. DOI:10.1136/bmjdrc-2015-000175 |
 2022, Vol. 43
2022, Vol. 43