文章信息
- 杨淑娟, 贾鹏.
- Yang Shujuan, Jia Peng
- 空间全生命周期流行病学在慢性病研究中的应用
- Spatial lifecourse epidemiology in chronic non-communicable disease research
- 中华流行病学杂志, 2022, 43(5): 755-760
- Chinese Journal of Epidemiology, 2022, 43(5): 755-760
- http://dx.doi.org/10.3760/cma.j.cn112338-20220108-00013
-
文章历史
收稿日期: 2022-01-08
2. 武汉大学空间全生命周期流行病学国际研究中心,武汉 430072;
3. 武汉大学资源与环境科学学院,武汉 430072
2. School of Resource and Environmental Sciences, Wuhan University, Wuhan 430072, China;
3. International Institute of Spatial Life-course Epidemiology, Wuhan University, Wuhan 430072, China
随着危险因素谱和疾病谱的转变,慢性病流行病学研究领域逐步演化出新兴分支方向,从行为生活方式等非空间因素范畴向地理环境等空间因素范畴延伸,加深了对慢性病致病因素的多维度、多水平、时空异质性等特征的认识,也成为了健康地理学(health geography)的重点研究内容。两个始于21世纪初期的分支方向最为典型,全生命周期流行病学(lifecourse epidemiology)和空间流行病学(spatial epidemiology)。前者研究个体从生命之初到终止期间不同阶段的生物、行为、心理等因素的积累和相互作用对慢性病发生发展带来的影响[1];后者是健康地理学的一个分支方向,研究疾病及相关的环境、行为、社会经济等危险因素在地理空间中分布的异质性。
空间全生命周期流行病学(spatial lifecourse epidemiology)是健康地理学向精准健康(precision health)发展的一个分支方向。作为全生命周期流行病学和空间流行病学两个分支方向在大数据时代的新发展,结合先进的地理信息、测绘遥感、移动定位、人工智能等技术对个体的全生命周期暴露史(暴露组)进行精准回溯、测量及模拟,研究具有时空异质性的因素在人生不同阶段对健康的影响,为制定慢性病的精准健康干预政策提供依据[2-3]。相较于健康地理学的其他分支方向,空间全生命周期流行病学更关注个体在精细时空尺度下的暴露组及在全生命周期各个阶段与健康状况的因果关联。
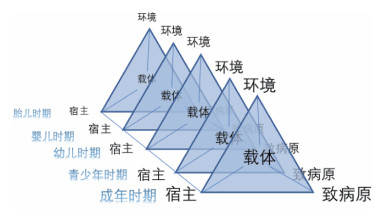
一、理论基础空间全生命周期流行病学基于地理信息、遥感和移动定位等技术,使传统的流行病学三角模型服务于慢性病研究,并在时间和空间上实现动态化(图 1)。三角模型的要素也有了新的含义,宿主指易感人群或个体;致病原的概念范畴则由病原微生物和寄生虫扩展到空间环境中一切潜在的致病因素。慢性病的发生是由于长期暴露于致病因素,因此准确估计宿主和致病原的交互程度需考虑个体所处空间环境长时间尺度下的暴露状况。空间环境因素不仅影响病原体与宿主的直接交互,还会通过影响宿主的行为习惯间接影响他们的交互过程。例如社区内开设的快餐店数量增加,不仅会直接增加居民在社区内食用快餐的次数,还会影响居民的饮食习惯,使他们在社区外也更倾向于选择食用快餐,最终可能导致肥胖等慢性病患病率增加。此外,传染病和慢性病在动态三角模型中还会发生交互作用,影响患病风险。例如长期处于慢性病致病原的暴露中,会降低宿主的免疫力,增加感染传染病的风险;而感染传染病也同样会增加慢性病的患病风险。
|
| 图 1 全生命周期流行病学三角模型 |
空间全生命周期流行病学主要基于纵向设计和监测设计,沿用Ben-Shlomo和Kuh[1]提出的针对长期暴露因素的研究范式,如累积风险模型和关键期/敏感期风险模型,并结合空间数据和基础模型的空间拓展研究累积或不同生命时期空间暴露因素对健康的影响。
1. 累积风险模型(accumulation of risk model):空间暴露具有长期性、累积性,目前常用两种方法研究不同暴露类型对个体健康产生的累积效应。
(1)潜类别增长模型(latent growth model,LGM):传统的LGM基于纵向、重复测量的数据集来反映长期空间与非空间暴露因素对个体健康的长期影响,并通过潜在变量建模方法,捕捉个体间发展轨迹的差异[4]。LGM假设样本所有个体的发展轨迹相似,且协变量以相同方式影响个体[5],根据潜变量的均值、方差分别描述群体增长趋势和个体差异。但当数据集中存在潜类别(latent class,即发展趋势不同质的群体)或未观察到同质性时,潜类别增长分析(latent class growth analysis,LCGA)展现出更高的适用性[6]。
LCGA假设各类别内的个体增长轨迹是同质的,但允许潜类别之间存在潜在变量的差异。LCGA采用数据驱动方法识别出的疾病类别还可与地理环境暴露进一步结合,通过回归等方法探究地理环境因素对各类群体的健康效应,探讨不同种类的疾病发展的异质性以及暴露对各种类疾病的不同影响,但目前仅有少量研究利用该方法探讨环境暴露与健康结局的关系。例如,Gonzalez-Casanova等[7]采用LCGA识别出儿童出生后的认知发展类别,再通过logistic回归模型描述孕妇产前氮氧化物(如NO2)和挥发性有机化合物(如苯)的户外空气污染物暴露等环境暴露与各类儿童认知发展轨迹的关联。
(2)多成员模型(multiple-membership model,MMM):关注区域空间与非空间暴露对全生命周期不同阶段的影响,适用于个体同时属于多个空间区域的研究场景,模型中还考虑了人口流动性[8]。MMM包含了个体暴露特征的固定效应和区域随机效应,通过对个体特征向量、区域暴露与健康结局的关联进行建模。模型需要指定个体在不同单元的权重,如可根据个体在不同区域逗留的时间长短来定义权重。假设每个个体的健康结局服从伯努利分布,伯努利分布的参数π与个体特征向量以logit函数建立关系,则MMM结构如下:
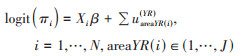
式中,X代表个体特征向量,β系数包括固定效应和区域的随机效应。uareaYR(i)(YR)表示在YR年,居住在areaYR(i)区域对健康结局的影响。
在长期暴露效应研究中,人口流动可能导致单一地址暴露效应估计的不准确甚至无效,因此应将地理位置变化情况纳入暴露研究,以有效提高累积暴露风险的描述准确性,现在已有少量研究应用MMM分析个体空间累积暴露与健康及相关行为的关系[9]。例如,Petrof等[10]构建了空间MMM,讨论石棉接触对间皮瘤患病的影响,该研究将居住地理位置变化纳入暴露研究,将个体历史居住地理位置集作为计算健康结局分布的参数之一,并加入空间随机效应,以描述地理位置变化导致的空间异质性。
2. 关键期/敏感期风险模型(critical/sensitive period model):目前常用以下几类模型探索在生命发育的关键时期,空间环境暴露因素对人体组织、器官及系统的结构或功能产生的短期或长期的健康效应。
(1)多水平回归模型(multilevel regression model):该模型适用于个体间不具备独立性、但在一定空间范围内或人群中具有聚集性的数据类型[11],例如人口普查数据在省(市、县)的多层数据等。多水平回归模型通过社区、家庭和个体层次的随机误差项解释各层次结构的聚类,使得个体的随机误差估计更精准。多水平线性回归模型应用于关键期/敏感期风险建模时,需要收集相应时间段的社会经济数据和环境暴露数据进行回归分析。假设结果变量服从二项分布,描述个体和社区两层关系的logit多水平模型可构建如下[12]:
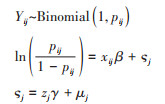
式中,pij是第i个生活在第j个区域的人不患病的概率;x是个体层面的暴露。在区域层面,ς表示空间单位j在对个体的影响,通过区域层面协变量z计算得到,μ是区域水平的随机残差。该模型拟合社区层面的暴露与个体层面的暴露共同影响个体的患病概率。例如,Jimenez等[13]应用多水平线性回归模型,探究了敏感期(出生、童年和成年)绿色空间暴露与成年血压、体重的关联。
(2)空间多水平模型(spatial multilevel model):多水平数据中如存在空间依赖或自相关现象,纳入空间权重矩阵或其他邻域结构计算空间随机效应的空间多水平模型能更好地体现区域层面因素对个体健康状况的影响[14]。例如,Leroux等[15]通过空间多水平模型研究了环境污染与健康结局的关联,模型如下:
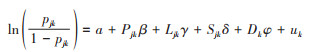
其中,P表示各类环境污染,L表示个体位置相关的变量,S表示个体的社会经济变量,D表示社区相关变量,a,β,γ,δ,φ为系数,u表示社区层面的空间随机效应。该模型已广泛应用到了慢性病相关研究中,但较少用于探讨空间暴露对关键期/敏感期健康效应研究。
(3)交叉分类的多水平模型:交叉分类模型(cross-classified model)针对个体的不同的身份及活动范围,将个体划分到不同的群体中,并假设同一群体内部的个体暴露水平固定,暴露和随机效应随群体变化而变化[16]。当应用于关键期/敏感期风险建模时,交叉分类多水平模型允许个体在某个年龄段嵌套于不同的社区单元,反映空间层面的暴露因素对个体健康水平的影响。模型如下:
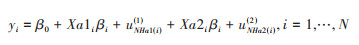
式中,X为协变量,a1,a2表示假设中不同敏感期年龄段,uNHa表示对应年龄段的社区随机效应。与空间多水平模型的拓展方式相似,也可以通过定义不同群体的空间随机效应建立交叉分类的空间多水平模型,并基于各社区单元区划层次构建空间权重矩阵,将相邻区域的潜在影响通过空间随机效应表示,目前仅有较少研究应用该模型探讨空间暴露因素对个体和群体水平健康的影响[17]。
3. 综合模型:是对累积暴露、关键期暴露和敏感期暴露进行不同方式量化,通过对比三种暴露模式的效果推断最适合描述健康结局的模型,避免了在研究中“先假设暴露模式,再进行建模分析”可能带来的潜在偏倚,目前常采用以下模型:
(1)最小角度回归(least angle regression,LARS):是一种结构化方法,可用于探索已有假设,通过最小绝对收缩和选择算子(lasso)来识别与结果关联最强的变量或变量组合[18]。首先通过有向无环图描述全生命周期中空间暴露因素与健康结局之间的潜在因果关系,再将可能的关联路径编码到一个或多个暴露量化的组合中进行识别。暴露量化方法包括:①累积暴露:暴露随时间变化曲线下面积或平均暴露;②关键期暴露:假设某一时期的暴露与健康结局的关联,用该时期多次测量的平均暴露表示;③敏感期暴露:即特定时期的暴露与健康结局关联更强,用时间相关的加权表示。
LARS目前主要应用于精神和心理健康的相关研究[19-20]。由于空气污染、绿地暴露、交通噪音等空间暴露与个体慢性病发生发展密切相关[21],在LARS模型框架下评估空间暴露对人生不同阶段健康的影响将是一个潜在的研究方向。需要注意的是,LARS没有考虑数据中可能存在的多水平结构,因此在模型评估时可能存在偏倚。
(2)相关生命周期暴露模型(relevant life course exposure model,RLM):是将累积暴露(不同时期的暴露重要性相同)和关键期暴露(某些特殊时期更重要)看作敏感期(不同时期具有不同的重要性)的特例进行建模[22],该模型的优点:不需要模型或变量选择、可用于连续或分类结果变量、可容纳缺失值和测量误差等。相关生命周期暴露定义为所有时间段暴露的加权和,相关暴露变量和健康结局之间的关系可通过广义线性模型等方法建模。
目前仅有少量出生队列将RLM应用在生命早期非空间暴露因素对健康的长期和敏感期影响的探究中[23-24],尚未将其应用于空间暴露因素与健康效应关系相关研究。RLM提供的是时间维度简化生命周期暴露模式的思路,未来可考虑将RLM与空间全生命周期研究框架结合应用。
三、重点研究内容及展望1. 统一空间暴露指标的量化标准:随着空间数据源和数据信息量的急剧增加,在个体的全生命周期研究中选择哪种空间暴露指标以及如何量化都会对暴露评价产生重要的影响[25]。随着生态环境保护、卫生健康等各项业务及信息化建设的不断发展,对基本数据集的需求会越来越多。然而国内外的研究机构、数据生产或管理部门制定的数据采集标准各不相同,标准的不一致导致难以综合分析复杂环境暴露对健康的影响。例如在食品营养环境暴露的相关研究中,如何定义食品零售商(例如餐馆、杂货店和当地的食品店)及其暴露程度(如何确定个体周围缓冲区的半径)都会对研究结论产生不同的影响[26-28]。已有研究证明不同暴露指标评价体系的使用是导致研究结果不一致的重要因素[29-30]。因此,在使用多源空间数据时,需要统一的暴露指标选择及量化标准,遵循报告准则(spatial lifecourse epidemiology reporting standards statement),有利于后续进行环境暴露对健康的影响程度的科学评价,并增强研究之间的可比较性[31]。
2. 基于前瞻性研究的全生命周期空间暴露测量:空间暴露的准确测量是全生命周期健康效应评估的一项重要挑战。目前许多队列研究在建立时没有采集个体的位置和移动轨迹信息,研究者往往使用个体不同时期的家庭住址替代位置信息进行后续研究。而有研究表明个体的平均每天只有6%的活动发生在居住地,21%的活动发生在居住地周围,剩下73%的活动则发生在城市的其他区域[29]。因此,基于居住地址的空间暴露研究往往忽略个体的日常活动模式对健康的影响,导致测量误差。其次,一些国家的地址系统不够规范,地理编码的不确定性较高,容易存在测量误差。因此,可以在人群队列研究期间利用移动定位技术,精确记录个体的地理位置、日常活动模式,前瞻性动态收集时间-空间信息,进行个体连续性暴露精准测量。比如生命早期暴露组出生队列(human early-life exposome)中建立了约150名儿童的面板研究,每半年持续一周使用智能手机、其他个体监测传感器获取个体的动态活动轨迹和问卷环境暴露数据[32],动态分析环境因素对儿童生长发育的影响。此外,色散模型、化学运输模型、混合模型以及谷歌街景车载空气污染探测器等新兴空间技术评估方法也可为动态监测个体暴露提供技术手段,为研究提供更精准的暴露信息[25]。
3. 融合多元数据源挖掘空间暴露信息:当前大样本的流行病学研究中最常用的环境暴露数据主要来自遥感手段。遥感数据是一种全天时数据,可作为地面环境监测变量因子的补充,获取暴露特征,以分析时间序列上的环境暴露特征与健康之间的关系[33-34]。长时间序列的多源遥感数据可进一步与环境监测、社会经济等数据相结合,实现对多种环境变量的反演。例如,可以利用由卫星观测的气溶胶光学厚度数据、气象数据以及每小时的PM2.5地面监测浓度数据实时估算大气中PM2.5浓度。
当前,具有空间信息的大数据可实时通过电子病历、智能手机、网络设备、社交媒体、积分卡、街景数据、物联网传感器数据等方式以前所未有的速度和规模累积。研究者可利用这些数据来创建暴露和行为的密集纵向测量数据,并利用计算机科学技术,通过庞大的多源数据分析揭示数据所反映的现象、其发展趋势及数据间的相互联系。例如,谷歌地球引擎是一个新的云计算平台[35],研究者可借助它调用机器学习的相关算法,从全球大规模的卫星数据中提取长时间的环境变量,并将其与长期健康监测或调查数据匹配,研究这些环境暴露因素与不同阶段健康状况的因果关系,从而基于实时环境暴露数据预测健康结局。
4. 发展复杂系统科学模型:空间暴露因素通过行为影响健康是一个漫长的过程,常是非线性并存在多种因素交互的复杂关系。因此,结合其他领域的统计学方法,发展复杂系统科学模型成为必然趋势。例如,环境暴露组学研究根据全基因组关联研究(genome-wide association study)的原则,即对基因组的每个基因标志物与感兴趣的基因表型进行关联,提出了一种基于数据驱动设计的分析方法,即全环境关联研究(environment-wide association study,EWAS),对暴露组的每个环境变量与疾病结局进行关联,并通过多重验证降低虚假关联的可能性。最新一项研究采用EWAS从139个邻里层面的环境暴露中,筛选出21个与居民的幸福感相关的环境因素[36]。此外,还可利用分子生物统计学中的网络分析和聚类分析等方法用于构建多因子间复杂的相互作用的系统模型[37],以揭示实验背后复杂的空间暴露因素与健康之间的关系。
四、结论空间全生命周期流行病学在健康地理学和全生命周期流行病学的基础上,结合先进科学技术进一步探索暴露组和个体健康状况之间的复杂关系。然而,空间全生命周期流行病学当前的理论和技术偏重于外暴露的研究,对内暴露的精准测量及模拟还有待加强[2],亟需结合生物与遗传学、生态学等学科内容,不断改进自身的理论框架和方法论,以更好地认识疾病及其不断演化的致病因素,实现对慢性病的精准防控。
利益冲突 所有作者声明无利益冲突
作者贡献声明 杨淑娟:论文构思、文献检索、论文撰写、修改;贾鹏:研究指导、论文构思、论文撰写、修改
| [1] |
Ben-Shlomo Y, Kuh D. A life course approach to chronic disease epidemiology: conceptual models, empirical challenges and interdisciplinary perspectives[J]. Int J Epidemiol, 2002, 31(2): 285-293. DOI:10.1093/ije/31.2.285 |
| [2] |
Jia P. Spatial lifecourse epidemiology[J]. Lancet Planet Health, 2019, 3(2): e57-59. DOI:10.1016/S2542-5196(18)30245-6 |
| [3] |
Jia P, Dong WH, Yang SJ, et al. Spatial lifecourse epidemiology and infectious disease research[J]. Trends Parasitol, 2020, 36(3): 235-238. DOI:10.1016/j.pt.2019.12.012 |
| [4] |
MacCallum RC, Austin JT. Applications of structural equation modeling in psychological research[J]. Annu Rev Psych ol, 2000, 51: 201-226. DOI:10.1146/annurev.psych.51.1.201 |
| [5] |
Berlin KS, Parra GR, Williams NA. An introduction to latent variable mixture modeling (part 2): longitudinal latent class growth analysis and growth mixture models[J]. J Pediatr Psychol, 2014, 39(2): 188-203. DOI:10.1093/jpepsy/jst085 |
| [6] |
刘源, 骆方, 刘红云. 多阶段混合增长模型的影响因素: 距离与形态[J]. 心理学报, 2014, 46(9): 1400-1412. Liu Y, Luo F, Liu HY. Factors of piecewise growth mixture model: distance and pattern[J]. Acta Psychol Sin, 2014, 46(9): 1400-1412. DOI:10.3724/SP.J.1041.2014.01400 |
| [7] |
Gonzalez-Casanova I, Stein AD, Barraza-Villarreal A, et al. Prenatal exposure to environmental pollutants and child development trajectories through 7 years[J]. Int J Hyg Environ Health, 2018, 221(4): 616-622. DOI:10.1016/j.ijheh.2018.04.004 |
| [8] |
Leyland AH, Næss Ø. The effect of area of residence over the life course on subsequent mortality[J]. J R Stat Soc Ser A Stat Soc, 2009, 172(3): 555-578. DOI:10.1111/j.1467-985X.2008.00581.x |
| [9] |
Cafri G, Hedeker D, Aarons GA. An introduction and integration of cross-classified, multiple membership, and dynamic group random-effects models[J]. Psychol Methods, 2015, 20(4): 407-421. DOI:10.1037/met0000043 |
| [10] |
Petrof O, Neyens T, Nuyts V, et al. On the impact of residential history in the spatial analysis of diseases with a long latency period: A study of mesothelioma in Belgium[J]. Stat Med, 2020, 39(26): 3840-3866. DOI:10.1002/sim.8697 |
| [11] |
李佳萌. 多水平模型及其在卫生领域的应用[J]. 中国慢性病预防与控制, 2007, 15(5): 514-515. Li JM. Multilevel models and their applying in health field[J]. Chin J Prev Control Chron Non-Commun Dis, 2007, 15(5): 514-515. DOI:10.3969/j.issn.1004-6194.2007.05.052 |
| [12] |
Goldstein H. Multilevel statistical models[M]. London, England: John Wiley & Sons, 2011. DOI:10.1002/9780470973394
|
| [13] |
Jimenez MP, Wellenius GA, James P, et al. Associations of types of green space across the life-course with blood pressure and body mass index[J]. Environ Res, 2020, 185: 109411. DOI:10.1016/j.envres.2020.109411 |
| [14] |
Arcaya M, Brewster M, Zigler CM, et al. Area variations in health: a spatial multilevel modeling approach[J]. Health Place, 2012, 18(4): 824-831. DOI:10.1016/j.healthplace.2012.03.010 |
| [15] |
Leroux BG, Lei XY, Breslow N. Estimation of disease rates in small areas: a new mixed model for spatial dependence[M]//Halloran ME, Berry D. Statistical models in epidemiology, the environment, and clinical trials. New York: Springer, 2000. DOI: 10.1007/978-1-4612-1284-3_4.
|
| [16] |
Ding C, Lin YY, Liu C. Exploring the influence of built environment on tour-based commuter mode choice: A cross-classified multilevel modeling approach[J]. Trans Res D: Transp Environ, 2014, 32: 230-238. DOI:10.1016/j.trd.2014.08.001 |
| [17] |
Jephcote C, Mah A. Regional inequalities in benzene exposures across the European petrochemical industry: A Bayesian multilevel modelling approach[J]. Environ Int, 2019, 132: 104812. DOI:10.1016/j.envint.2019.05.006 |
| [18] |
Smith AD, Hardy R, Heron J, et al. A structured approach to hypotheses involving continuous exposures over the life course[J]. Int J Epidemiol, 2016, 45(4): 1271-1279. DOI:10.1093/ije/dyw164 |
| [19] |
Marini S, Davis KA, Soare TW, et al. Adversity exposure during sensitive periods predicts accelerated epigenetic aging in children[J]. Psychoneuroendocrinology, 2020, 113: 104484. DOI:10.1016/j.psyneuen.2019.104484 |
| [20] |
Kessing LV, Rytgaard HC, Ekstrøm CT, et al. Antidiabetes agents and incident depression: a nationwide population-based study[J]. Diabetes Care, 2020, 43(12): 3050-3060. DOI:10.2337/dc20-1561 |
| [21] |
Helbich M. Toward dynamic urban environmental exposure assessments in mental health research[J]. Environ Res, 2018, 161: 129-135. DOI:10.1016/j.envres.2017.11.006 |
| [22] |
Madathil S, Joseph L, Hardy R, et al. A Bayesian approach to investigate life course hypotheses involving continuous exposures[J]. Int J Epidemiol, 2018, 47(5): 1623-1635. DOI:10.1093/ije/dyy107 |
| [23] |
O'Hare C, Kuh D, Hardy R. Association of early-life factors with life-course trajectories of resting heart rate: more than 6 decades of follow-up[J]. JAMA Pediatr, 2018, 172(4): e175525. DOI:10.1001/jamapediatrics.2017.5525 |
| [24] |
Armstrong MK, Fraser BJ, Hartiala O, et al. Association of Non-High-Density Lipoprotein Cholesterol Measured in Adolescence, Young Adulthood, and Mid-Adulthood With Coronary Artery Calcification Measured in Mid-Adulthood[J]. JAMA Cardiol, 2021, 6(6): 661-668. DOI:10.1001/jamacardio.2020.7238 |
| [25] |
Jia P, Lakerveld J, Wu JG, et al. Top 10 research priorities in spatial lifecourse epidemiology[J]. Environ Health Perspect, 2019, 127(7): 074501. DOI:10.1289/EHP4868 |
| [26] |
Jia P, Yang HX, Cao XX, et al. Association between access to full-service restaurants and childhood obesity[J]. Obes Rev, 2021, 22 Suppl 1(Suppl 1): e13076. DOI:10.1111/obr.13076 |
| [27] |
Yang SJ, Zhang X, Feng P, et al. Access to fruit and vegetable markets and childhood obesity: A systematic review[J]. Obes Rev, 2021, 22 Suppl 1(Suppl 1): e12980. DOI:10.1111/obr.12980 |
| [28] |
Li YM, Luo MY, Wu XY, et al. Grocery store access and childhood obesity: A systematic review and meta-analysis[J]. Obes Rev, 2021, 22 Suppl 1(Suppl 1): e12945. DOI:10.1111/obr.12945 |
| [29] |
Matthews SA, Detwiler JE, Burton LM. Geo-ethnography: coupling geographic information analysis techniques with ethnographic methods in urban research[J]. Cartograph: Int J Geograph Inf Geovisualizat, 2005, 40(4): 75-90. DOI:10.3138/2288-1450-w061-r664 |
| [30] |
Jia P, Cheng X, Xue H, et al. Applications of geographic information systems (gis) data and methods in obesity-related research[J]. Obes Rev, 2017, 18(4): 400-411. DOI:10.1111/obr.12495 |
| [31] |
Jia P, Yu C, Remais JV, et al. Spatial Lifecourse Epidemiology Reporting Standards (ISLE-ReSt) statement[J]. Health Place, 2020, 61: 102243. DOI:10.1016/j.healthplace.2019.102243 |
| [32] |
Vrijheid M, Slama R, Robinson O, et al. The human early-life exposome (HELIX): project rationale and design[J]. Environ Health Perspect, 2014, 122(6): 535-544. DOI:10.1289/ehp.1307204 |
| [33] |
Jia P, Stein A. Using remote sensing technology to measure environmental determinants of non-communicable diseases[J]. Int J Epidemiol, 2017, 46(4): 1343-1344. DOI:10.1093/ije/dyw365 |
| [34] |
Jia P, Stein A, James P, et al. Earth observation: Investigating noncommunicable diseases from space[J]. Annu Rev Public Health, 2019, 40: 85-104. DOI:10.1146/annurev-publhealth-040218-043807 |
| [35] |
Khan R, Gilani H. Global drought monitoring with big geospatial datasets using Google Earth Engine[J]. Environ Sci Pollut Res, 2021, 28(14): 17244-17264. DOI:10.1007/s11356-020-12023-0 |
| [36] |
van de Weijer MP, Baselmans BML, Hottenga JJ, et al. Expanding the environmental scope: an environment-wide association study for mental well-being[J]. J Expo Sci Environ Epidemiol, 2021 Jun 14. DOI: 10.1038/s41370-021-00346-0.
|
| [37] |
Silverman EK, Schmidt HHHW, Anastasiadou E, et al. Molecular networks in Network Medicine: Development and applications[J]. WIREs Syst Biol Med, 2020, 12(6): e1489. DOI:10.1002/wsbm.1489 |
 2022, Vol. 43
2022, Vol. 43


