文章信息
- 武媛婷, 姚添, 石璟, 王建民, 刘广明, 王富珍, 冯永亮, 王素萍.
- Wu Yuanting, Yao Tian, Shi Jing, Wang Jianmin, Liu Guangming, Wang Fuzhen, Feng Yongliang, Wang Suping
- 维持性血液透析患者60 μg高剂量乙型肝炎疫苗免疫持久性及影响因素
- Immunity persistence of 60 μg high dose hepatitis B vaccine and influencing factors in maintained hemodialysis patients
- 中华流行病学杂志, 2021, 42(9): 1566-1572
- Chinese Journal of Epidemiology, 2021, 42(9): 1566-1572
- http://dx.doi.org/10.3760/cma.j.cn112338-20210319-00221
-
文章历史
收稿日期: 2021-03-19
2. 山西医科大学临床流行病学与循证医学中心, 太原 030001;
3. 临汾市中心医院肾内科 041000;
4. 长治医学院附属和平医院检验科 046000;
5. 中国疾病预防控制中心免疫规划中心, 北京 100050
2. Center of Clinical Epidemiology and Evidence Based Medicine, Shanxi Medical University, Taiyuan 030001, China;
3. Department of Nephrology, Linfen Central Hospital, Linfen 041000, China;
4. Department of Clinical Laboratory, Heping Hospital Affiliated to Changzhi Medical College, Changzhi 046000, China;
5. Department of National Immunization Program, Chinese Center for Disease Control and Prevention, Beijing 100050, China
乙型肝炎(乙肝)是全球重大的公共卫生问题,据WHO报道,截至2015年,全球约有2.57亿慢性HBV感染者[1]。而目前我国1~59岁一般人群HBsAg阳性率为5.7%[2],这与WHO[3]提出的2030年消除病毒性肝炎这一公共卫生威胁的目标还有较大差距。维持性血液透析患者由于频繁输注血液制品、反复穿刺、共用透析机等原因,其HBV感染率(11.9%)远高于一般人群[4-6],加之血液透析患者人数众多,截至2016年我国血液透析患者已有约57.8万人,且数量持续增加[7],预防和控制维持性血液透析患者HBV感染是实现2030年消除病毒性肝炎这一目标的重要内容。接种乙肝疫苗是降低HBV感染最有效的措施,但由于长期接受血液透析,免疫系统损伤较为严重,维持性血液透析患者按常规免疫方案(0-1-6月20 μg)接种乙肝疫苗后抗-HBs阳转率(50%~70%)远低于一般人群(90%~95%),且相较于一般人群,维持性血液透析患者疫苗接种后1年内抗-HBs下降速度更快,免疫持久性不佳[8-11]。提高乙肝疫苗免疫效果及持久性是降低该人群HBV感染的关键举措。增加接种剂量是提高免疫效果最便捷措施,然而,国外有研究显示,双倍剂量(40 μg)乙肝疫苗接种不能有效提高维持性血液透析患者的免疫效果及持久性[12-13]。课题组前期进行了高剂量(60 μg)乙肝疫苗免疫的随机对照试验研究[14],明显提高了该人群抗-HBs阳转率,但免疫持久性如何,未见国内外报道。为此,在既往研究基础上,本研究前瞻性随访分析该人群乙肝疫苗免疫后1年抗-HBs情况,探讨免疫持久性的影响因素及其交互作用,以期为优化高危人群乙肝疫苗免疫接种策略和乙肝消除策略提供参考依据。
对象与方法1. 研究对象:2014年2月在山西省13家二甲及以上医院,选取18~70岁、HBsAg和抗-HBs阴性的维持性血液透析患者352例,随机分为20 μg组和60 μg组,按0-1-6月程序接种乙肝疫苗,并于全程接种后1个月、6个月和1年采集血液标本,定量检测抗-HBs[14]。完成乙肝疫苗全程接种后1年随访者为研究对象,共249例(20 μg组125例、60 μg组124例)。本研究已获得山西医科大学伦理委员会审批,研究对象均签署知情同意书。
2. 资料收集:由培训合格的专业人员,通过面对面调查和病历查阅的方式收集研究对象年龄、性别、民族、职业、文化程度、BMI等人口学特征和导致肾衰的原发性疾病、血液透析时间、乙肝疫苗接种史、现患疾病等信息。
3. 标本采集和检测:乙肝疫苗接种后1年,采集研究对象静脉血5 ml,采用化学发光微粒子免疫分析法定量检测抗-HBs几何平均浓度(geometric mean concentration,GMC),严格按照说明书进行操作,实验室检测委托第三方医学检测公司(太原金域临床检验有限公司)完成。
4. 相关定义:
(1)抗-HBs划分标准[14]:①阴性:抗-HBs < 10 mIU/ml;②阳性:抗-HBs≥10 mIU/ml;③强阳性:抗-HBs≥100 mIU/ml。
(2)维持性血液透析[15]:是指利用血液透析或腹膜透析挽救患者的生命,延长终末期肾脏疾病患者生命的方法。
5. 统计学分析:采用EpiData 3.1软件进行数据双录入,采用SAS 9.4软件整理数据和分析。计量资料符合正态分布采用x±s表示,偏态分布则采用M(P25,P75)表示,计数资料以例数(构成比或率,%)表示。采用χ2检验比较20 μg组和60 μg组一般情况及抗-HBs阳性率的差异;采用t检验比较两组抗体GMC水平(对数转换后)的差异。采用非条件logistic回归进行多因素分析,入选标准为0.10,剔除标准为0.15。采用logistic回归模型分析相乘交互作用,采用Andersson等编制的交互作用计算表分析相加交互作用,计算超额相对危险度(RERI)、交互作用归因比(AP)、交互作用指数(S)及其95%CI。双侧检验,以P < 0.05为差异有统计学意义。
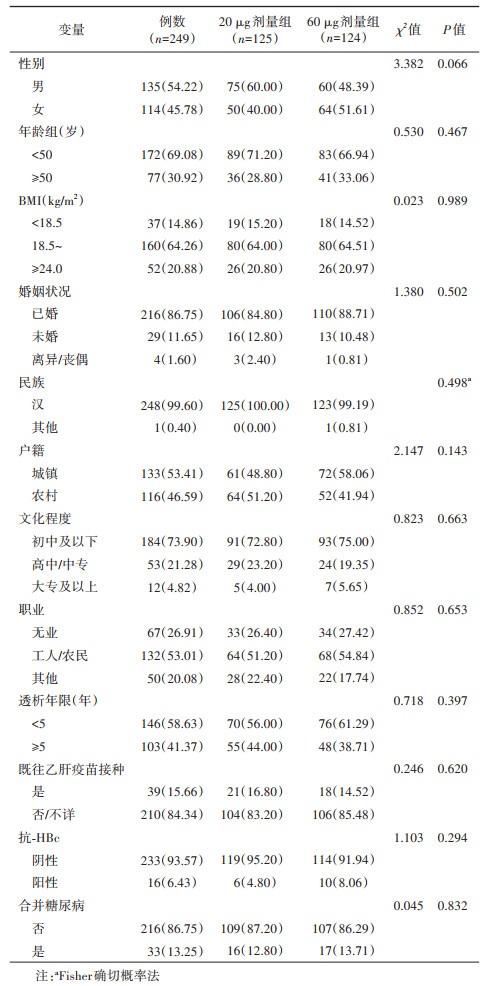
结果1. 一般情况:完成乙肝疫苗全程接种后1年的患者共249例,20 μg组和60 μg组分别为125和124例。其中,男性135人,女性114人,男女比例1.18∶1;年龄(43.55±12.04)岁,年龄范围18~70岁;BMI范围13.8~45.0 kg/m2,其中18.5~23.9 kg/m2者占64.26%;婚姻状况以已婚者为主(86.75%);汉族为主(99.60%);透析年限≥5年患者占41.37%;抗-HBc阳性比例为6.43%;合并糖尿病占13.25%。均衡性检验结果显示:两组在性别、年龄、BMI、婚姻状况、民族、户籍、文化程度、职业、透析年限、既往乙肝疫苗接种史、抗-HBc、合并糖尿病等差异均无统计学意义(P > 0.05)。见表 1。研究对象与失访对象在性别、年龄、BMI、接种剂量、透析年限和合并糖尿病等差异无统计学意义(P > 0.05)。
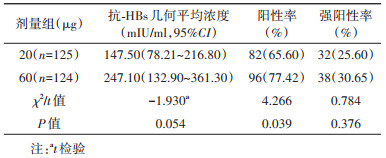
2. 免疫持久性分析:全程接种后1年时,60 μg组抗-HBs阳性率(77.42%,96/124)明显高于20 μg组(65.60%,82/125)(P < 0.05);60 μg组抗-HBs的GMC高于20 μg组(247.10 mIU/ml比147.50 mIU/ml),抗-HBs强阳性率(30.65%,38/124)高于20 μg组(25.60%,32/125),差异无统计学意义(P > 0.05)。见表 2。
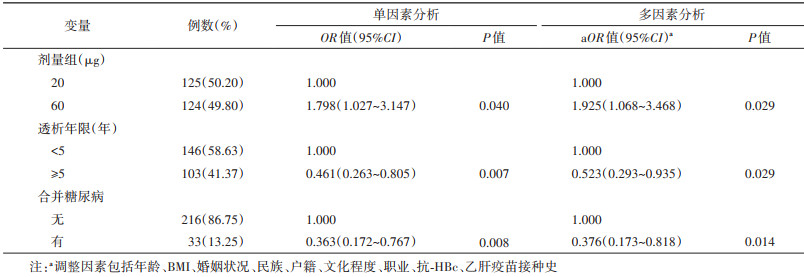
3.免疫持久性影响因素分析:以维持性血液透析患者乙肝疫苗接种后1年的抗-HBs阳性情况为因变量,将单因素有意义的自变量和相关文献报道的自变量进行非条件logistic回归模型分析,结果显示,全程接种后1年时,60 μg组抗-HBs阳性的概率是20 μg组的1.925倍(95%CI:1.068~3.468);透析年限≥5年(OR=0.523,95%CI:0.293~0.935)和合并糖尿病(OR=0.376,95%CI:0.173~0.818)的患者抗-HBs阳性的概率较低。见表 3。
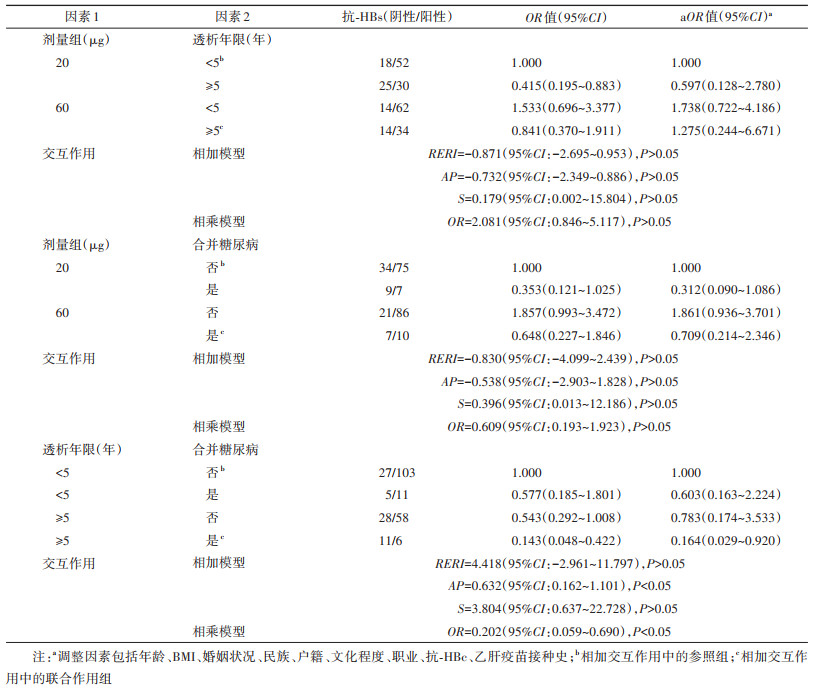
4.免疫持久性影响因素交互作用分析:相加模型中,透析年限≥5年与合并糖尿病存在相加交互作用(AP=0.632,95%CI:0.162~1.101)(P < 0.05);相乘模型中,透析年限≥5年且合并糖尿病的患者疫苗接种后1年抗-HBs阳性的概率明显降低,存在相乘交互作用(OR=0.202,95%CI:0.059~0.690)(P < 0.05)。接种剂量与透析年限、接种剂量与合并糖尿病未发现相加和相乘交互作用(P > 0.05)。见表 4。
结合WHO、美国CDC及我国技术指南建议,对于血液透析、器官移植、免疫功能低下者,应使用高剂量(40 μg或60 μg)、多针次(0-1-2-6月)的乙肝疫苗免疫方案[16]。然而,目前我国关于血液透析患者高剂量多针次乙肝疫苗免疫效果的相关研究甚少,尚无免疫持久性研究。前期研究发现,维持性血液透析患者按0-1-6月60 μg乙肝疫苗接种后1个月时抗-HBs阳性率(92.3%)明显高于20 μg组(83.7%),可有效提高该人群的免疫效果[14]。苏伟等[17]增加针次(0-1-6-9月)接种乙肝疫苗后,血液透析患者抗体阳转率为78.12%。国外对维持性血液透析患者多使用0-1-6月或0-1-2-6月40 μg免疫程序进行接种,结果显示,乙肝疫苗免疫后1年,抗-HBs阳性率为57.10%~81.10%不等,免疫持久性不佳[5, 11, 18]。本研究中,按0-1-6月接种高剂量(60 μg)乙肝疫苗后1年抗-HBs阳性率提高至77.42%(96/124),明显高于常规剂量(20 μg)接种(65.60%,82/125),但仍低于一般人群按常规免疫程序接种乙肝疫苗1年后抗-HBs阳性率(82.60%~92.30%)[19-21]。提示,高剂量(60 μg)乙肝疫苗接种一定程度上有助于维持性血液透析患者在全程接种后1年继续维持其抗体保护作用,可考虑使用高剂量(60 μg)乙肝疫苗延长抗-HBs对机体的保护时间,以降低我国维持性血液透析患者HBV感染率,为实现我国2030年消除乙肝的目标奠定基础。
有关透析年限与乙肝疫苗免疫效果的关系,目前尚无定论,且未见与免疫持久性的研究。Asan等[22]一项回顾性研究发现,维持性血液透析患者按0-1-2-6月40 μg乙肝疫苗接种后1个月时,透析年限≥5年的患者抗-HBs阴性的概率较高(OR=3.50),免疫效果不佳。而Afsar[23]和Erdoğdu等[24]分别对97例和197例患者进行的回顾性研究中,透析年限与乙肝疫苗免疫应答无关,分析其原因,可能与研究对象的纳入标准(接受血液透析治疗≥12个月)[23]、年龄分布不均(≥65岁者占51.2%)[24]等有关。本研究发现,透析年限≥5年的患者疫苗接种后1年的抗-HBs阳性率低,免疫持久性差。随着透析时间的延长,维持性血液透析患者的免疫损伤越严重[25],提示透析年限越长,乙肝疫苗的免疫效果及持久性可能越差。因此,透析中心加强维持性血液透析患者定期检测乙肝标志物至关重要,尤其是透析年限长者,既可以有效避免该人群HBV感染暴发,降低医源性感染发生率,也可以在抗-HBs消减至保护性水平之下时,及时提醒患者接种乙肝疫苗,减少HBV感染的发生。
目前关于维持性血液透析患者合并糖尿病与乙肝疫苗免疫应答的研究较少,且结果不一。El-Charabaty等[26]和Chin[27]对血液透析患者进行的乙肝疫苗免疫效果影响因素的回顾性研究均发现,合并糖尿病的患者接种乙肝疫苗后抗-HBs阴性的概率较高(OR=3.15和OR=3.40),免疫效果差。而沙特阿拉伯某大型血液透析中心的研究[28],进行了乙肝疫苗免疫应答影响因素的单因素分析后,结果显示,糖尿病未对维持性血液透析患者乙肝疫苗免疫应答产生影响。关于合并糖尿病与乙肝疫苗免疫持久性的研究,仅有美国纽约1项回顾性队列研究发现,合并糖尿病与乙肝疫苗接种后1年的免疫持久性无关[29]。而本研究发现,合并糖尿病的血液透析患者乙肝疫苗接种后1年抗-HBs阳性率低,免疫持久性差,分析其结果不同的原因,可能与研究地区、民族及研究方法不同等有关。现有研究表明,维持性血液透析患者合并糖尿病不仅会影响透析效果,而且会引起机体免疫功能的进一步低下[30-31]。因此,积极预防糖尿病以降低机体免疫损伤程度对乙肝疫苗免疫效果的提高可能有积极作用。
本研究发现,透析年限与糖尿病二者之间存在相加及相乘交互作用,提示维持性血液透析患者乙肝疫苗免疫持久性不佳可能是多种因素联合作用的结果。透析年限≥5年且合并糖尿病的患者可能存在更严重的免疫功能低下,致使其乙肝疫苗免疫持久性更差。从经济学角度来讲,过去10年我国实施的乙肝免疫预防策略避免了大量HBV感染和乙肝相关疾病的发生,具有较高的成本效益和成本效果价值,而要达到2030年WHO消除病毒性肝炎的目标,就需要更多的投入[32]。建议应进一步优化维持性血液透析患者尤其是透析年限较长和/或并发糖尿病者乙肝疫苗接种策略,定期检测乙肝标志物,并积极预防糖尿病的发生,降低HBV感染的风险。
本研究存在不足。一是仅分析了乙肝疫苗接种后1年的抗-HBs情况及影响因素,随访时间较短;二是失访率为29.26%的失访偏倚;三是仅分析了血清抗-HBs的免疫持久性,细胞免疫等指标难以测定和统一标准。
综上所述,维持性血液透析患者0-1-6月高剂量(60 μg)乙肝疫苗接种1年后免疫持久性优于20 μg,接种剂量、透析年限和合并糖尿病是免疫持久性的影响因素,透析年限≥5年与合并糖尿病存在相加及相乘交互作用。
利益冲突 所有作者均声明不存在利益冲突
| [1] |
WHO. Global hepatitis report, 2017[EB/OL]. (2017-04-19)[2021-04-20]. https://www.who.int/publications/i/item/global-hepatitis-report-2017.
|
| [2] |
张维璐, 吉兆华, 付婷, 等. 中国2007-2016年59岁以下普通人群HBsAg阳性率的Meta分析[J]. 中华流行病学杂志, 2017, 38(9): 1278-1284. Zhang WL, Ji ZH, Fu T, et al. Meta analysis on HBsAg-positive rate among general populations aged 1-59 years, 2007-2016, China[J]. Chin J Epidemiol, 2017, 38(9): 1278-1284. DOI:10.3760/cma.j.issn.0254-6450.2017.09.027 |
| [3] |
WHO. Global health sector strategy on viral hepatitis 2016-2021[EB/OL]. (2016-05-17)[2021-04-20]. https://www.who.int/publications/i/item/WHO-HIV-2016.06.
|
| [4] |
Almueilo SH. Evaluation of response to hepatitis B vaccination in chronic hemodialysis patients[J]. Saudi J Med Med Sci, 2017, 5(3): 218-223. DOI:10.4103/1658-631x.213302 |
| [5] |
Wang CY, Sun JH, Zhu B, et al. Hepatitis B virus infection and related factors in hemodialysis patients in China-systematic review and Meta-analysis[J]. Ren Fail, 2010, 32(10): 1255-1264. DOI:10.3109/0886022x.2010.517354 |
| [6] |
陈卿, 石璟, 冯永亮, 等. 血液透析者乙肝和丙肝感染情况及影响因素分析[J]. 中国公共卫生, 2013, 29(11): 1577-1580. Chen Q, Shi J, Feng YL, et al. Prevalence rates and influencing factors of hepatitis B and hepatitis C virus infection among hemodialysis patients in Taiyuan, China[J]. Chin J Public Health, 2013, 29(11): 1577-1580. DOI:10.11847/zgggws2013-29-11-06 |
| [7] |
Zhang LX, Zhao MH, Zuo L, et al. China Kidney Disease Network (CK-NET) 2016 annual data report[J]. Kidney Int Suppl, 2020, 10(2): e97-185. DOI:10.1016/j.kisu.2020.09.001 |
| [8] |
Reddy S, Chitturi C, Yee J. Vaccination in chronic kidney disease[J]. Adv Chronic Kidney Dis, 2019, 26(1): 72-78. DOI:10.1053/j.ackd.2018.10.002 |
| [9] |
Pan LP, Zhang L, Zhang W, et al. A genome-wide association study identifies polymorphisms in the HLA-DR region associated with non-response to hepatitis B vaccination in Chinese Han populations[J]. Hum Mol Genet, 2014, 23(8): 2210-2219. DOI:10.1093/hmg/ddt586 |
| [10] |
Leuridan E, van Damme P. Hepatitis B and the need for a booster dose[J]. Clin Infect Dis, 2011, 53(1): 68-75. DOI:10.1093/cid/cir270 |
| [11] |
Peces R, Laurés AS. Persistence of immunologic memory in long-term hemodialysis patients and healthcare workers given hepatitis B vaccine: role of a booster dose on antibody response[J]. Nephron, 2001, 89(2): 172-176. DOI:10.1159/000046064 |
| [12] |
Mulley WR, Le ST, Ives KE. Primary seroresponses to double-dose compared with standard-dose hepatitis B vaccination in patients with chronic kidney disease: a systematic review and Meta-analysis[J]. Nephrol Dial Transplant, 2017, 32(1): 136-143. DOI:10.1093/ndt/gfv443 |
| [13] |
Chaves SS, Daniels D, Cooper BW, et al. Immunogenicity of hepatitis B vaccine among hemodialysis patients: effect of revaccination of non-responders and duration of protection[J]. Vaccine, 2011, 29(52): 9618-9623. DOI:10.1016/j.vaccine.2011.10.057 |
| [14] |
Feng YL, Shi XH, Shi J, et al. Immunogenicity, antibody persistence, and safety of the 60μg hepatitis B vaccine in hemodialysis patients: a multicenter, randomized, double-blind, parallel-controlled trial[J]. Exp Rev Vaccines, 2017, 16(10): 1045-1052. DOI:10.1080/14760584.2017.1367667 |
| [15] |
Abe M, Okada K, Maruyama T, et al. Efficacy and safety of mitiglinide in diabetic patients on maintenance hemodialysis[J]. Endocr J, 2010, 57(7): 579-586. DOI:10.1507/endocrj.k09e-318 |
| [16] |
中华预防医学会, 中国疾病预防控制中心免疫规划中心. 中国成人乙型肝炎免疫预防技术指南[J]. 中国病毒病杂志, 2012, 2(1): 11-16. Chinese Prevention Medicine Association, Department of National Immunization Program, Chinese Center for Disease Control and Prevention. Technical guide for adult hepatitis B immunization in China[J]. Chin J Viral Dis, 2012, 2(1): 11-16. DOI:10.16505/j.2095-0136.2012.01.005 |
| [17] |
苏伟, 张焕巧, 尚有全, 等. 血液透析患者两种方法接种乙型肝炎疫苗的疗效分析[J]. 中国血液净化, 2010, 9(5): 261-264. Su W, Zhang HQ, Shang YQ, et al. Therapeutic effect of two inoculation methods for hepatitis B vaccination in hemodialysis patients[J]. Chin J Blood Purif, 2010, 9(5): 261-264. |
| [18] |
Ramezani A, Velayati AA, Eslamifar A, et al. Persistence of hepatitis B vaccine immunity in hemodialysis patients[J]. Ther Apher Dial, 2008, 12(2): 143-146. DOI:10.1111/j.1744-9987.2008.00560.x |
| [19] |
Yang LN, Yao J, Li J, et al. Suitable hepatitis B vaccine for adult immunization in China[J]. Immunol Res, 2016, 64(1): 242-250. DOI:10.1007/s12026-015-8742-1 |
| [20] |
王存祯, 邢秀生, 王晓芳, 等. 重组乙型肝炎疫苗(酿酒酵母)免疫后15年的持久性效果研究[J]. 中国疫苗和免疫, 2013, 19(2): 147-149, 182. Wang CZ, Xing XS, Wang XF, et al. Study on antibody persistence of the neonatal after vaccinated the hepatitis B vaccine made by recombinant deoxyribonucleic acid technigues saccharomyces cerevisiae yeast for 15 years[J]. Chin J Vacc Immun, 2013, 19(2): 147-149, 182. |
| [21] |
翟如方, 常少英, 齐秀香, 等. 重组酵母乙型肝炎疫苗免疫4年的效果观察[J]. 中华流行病学杂志, 2001, 22(3): 233. Zhai RF, Chang SY, Qi XX, et al. Study on immune effect of recombinant yeast-derived hepatitis B vaccine 4 years after immunization[J]. Chin J Epidemiol, 2001, 22(3): 233. DOI:10.3760/j.issn:0254-6450.2001.03.023 |
| [22] |
Asan A, Demirhan H, Sorkun HÇ, et al. Factors affecting responsiveness to hepatitis B immunization in dialysis patients[J]. Int Urol Nephrol, 2017, 49(10): 1845-1850. DOI:10.1007/s11255-017-1616-9 |
| [23] |
Afsar B. The relationship between erythropoietin resistance and antibody response to hepatitis B vaccine in hemodialysis patients[J]. Nephrourol Mon, 2013, 5(3): 806-812. DOI:10.5812/numonthly.8919 |
| [24] |
Erdoğdu Hİ, Atalay E, Gürsoy G, et al. Factors affecting inadequate response to HBV vaccine in hemodialysis patients: northeast anatolia survey with six hemodialysis centers[J]. Clin Exp Nephrol, 2019, 23(4): 530-536. DOI:10.1007/s10157-018-1676-x |
| [25] |
孟建中, 李丹丹, 彭侃夫, 等. 血液透析患者血浆PGE2含量与T细胞亚群和NK细胞活性的关系[J]. 中国血液净化, 2003, 2(6): 295-297, 337. Meng JZ, Li DD, Peng KF, et al. Influence of hemodialysis on peripheral blood prostaglandin E2(PGE2)、NK cell and T cell subsets in uremia patients[J]. Chin J Blood Purif, 2003, 2(6): 295-297, 337. DOI:10.3969/j.issn.1671-4091.2003.06.002 |
| [26] |
El-Charabaty E, Saifan C, Samarneh MM, et al. Variability in response to hepatitis B vaccine in hemodialysis patients[J]. J Clin Med Res, 2015, 7(5): 315-318. DOI:10.14740/jocmr1999w |
| [27] |
Chin AI. Hepatitis B virus vaccine response in hemodialysis: baseline patient characteristics[J]. Hemodial Int, 2003, 7(4): 296-303. DOI:10.1046/j.1492-7535.2003.00053.x |
| [28] |
Al Saran K, Sabry A, Al Halawany Z, et al. Factors affecting response to hepatitis B vaccine among hemodialysis patients in a large Saudi Hemodialysis Center[J]. Saudi J Kidney Dis Transpl, 2014, 25(1): 185-191. DOI:10.4103/1319-2442.124572 |
| [29] |
Elwell RJ, Neumann M, Bailie GR. Factors associated with long-term antibody production induced by hepatitis B vaccine in patients undergoing hemodialysis: a retrospective cohort study[J]. Pharmacotherapy, 2003, 23(12): 1558-1563. DOI:10.1592/phco.23.15.1558.31954 |
| [30] |
张洪源, 冯现竹. 高通量血液透析对糖尿病肾病血液透析患者细胞免疫功能的影响[J]. 中国中西医结合肾病杂志, 2015, 16(10): 905-907. Zhang HY, Feng XZ. Effect of High-flux hemodialysis on cellular immune function in diabetic nephropathy patients with hemodialysis[J]. Chin J Integr Tradit Western Nephrol, 2015, 16(10): 905-907. |
| [31] |
冯雪芳, 张芸, 周蓉. 糖尿病肾病维持性血液透析患者血糖控制对并发症的影响[J]. 中国血液净化, 2007, 6(5): 257-259. Feng XF, Zhang Y, Zhou R. The impact of blood glucose on complications in diabetic nephropathy on maintenance hemodialysis[J]. Chin J Blood Purif, 2007, 6(5): 257-259. DOI:10.3969/j.issn.1671-4091.2007.05.008 |
| [32] |
张顺祥, 孙盼盼, 夏云. 我国2006-2030年乙肝免疫预防经济学效果的评价和预测[J]. 中华疾病控制杂志, 2018, 22(7): 741-746. Zhang SX, Sun PP, Xia Y. Evaluation and forecast for economic outcomes of hepatitis B immunoprophylaxis strategies in China from 2006 to 2030[J]. Chin J Dis Control Prev, 2018, 22(7): 741-746. DOI:10.16462/j.cnki.zhjbkz.2018.07.020 |
 2021, Vol. 42
2021, Vol. 42