文章信息
- 郭兰伟, 李江, 陈亚敏, 刘茵, 李贺, 曹毛毛, 何思怡, 张韶凯, 陈万青.
- Guo Lanwei, Li Jiang, Chen Yamin, Liu Yin, Li He, Cao Maomao, He Siyi, Zhang Shaokai, Chen Wanqing
- 全球上消化道癌筛查指南的质量评价
- Quality assessment of guidelines on upper gastrointestinal cancer screening
- 中华流行病学杂志, 2021, 42(7): 1318-1324
- Chinese Journal of Epidemiology, 2021, 42(7): 1318-1324
- http://dx.doi.org/10.3760/cma.j.cn112338-20200805-01023
-
文章历史
收稿日期: 2020-08-05
2. 国家癌症中心/国家肿瘤临床医学研究中心/中国医学科学院/北京协和医学院肿瘤医院癌症早诊早治办公室, 北京 100021;
3. 兰州大学循证护理中心/兰州大学护理学院 730000
2. Office of Cancer Screening, National Cancer Center/National Clinical Research Center for Cancer/Cancer Hospital, Chinese Academy of Medical Sciences and Peking Union Medical College, Beijing 100021, China;
3. Evidence-Based Nursing Center of Lanzhou University/School of Nursing of Lanzhou University, Lanzhou 730000, China
上消化道癌(包括食管癌和胃癌)是临床最常见的恶性肿瘤之一。2018年,全世界估计新发病例160.6万例,占所有癌症病例的8.9%;全世界估计死亡病例129.1万例,占所有癌症病例的13.5%[1]。亚洲地区上消化道癌发病和死亡人数最多,2018年分别为121.4万(占全球发病例数的75.6%)和98.2万(占全球死亡例数的76.1%),中国、日本、印度、美国和俄罗斯发病位列前五位[1]。中国肿瘤登记地区数据显示,2015年我国食管癌发病率和死亡率分别居恶性肿瘤的第6位和第4位,胃癌发病率和死亡率分别居恶性肿瘤的第2位和第3位[2],疾病负担较重。有研究表明,早期食管癌或胃癌的5年生存率可达到90%左右[1, 3],而进展期食管癌或胃癌的5年生存率低于30%[4]。由于早期胃癌多无症状或症状轻微,难以诊断易被忽视,目前我国的早期食管癌或胃癌诊断率不到10%,远低于日本、韩国等,导致大多数确诊患者已到达病程的中期甚至晚期,预后较差[5]。因此,若能开展上消化道癌早期筛查,则有望提高食管癌或胃癌患者的5年生存率[6]。
循证实践指南和共识是基于现有资料和证据的全面、客观的总结,是改善上消化道癌筛查质量和使上消化道癌筛查得以推广的重要基础。因此,本研究基于系统文献检索,利用国际广泛使用的指南研究和评估工具(Appraisal of Guidelines for Research and Evaluation,AGREE Ⅱ)和国际实践指南报告标准(Reporting Items for Practice Guidelines in Healthcare,RIGHT)[7]评价全球范围内现有的食管癌和胃癌筛查指南,为我国上消化道癌筛查循证指南的制定提供参考依据。
资料与方法1. 文献检索:系统检索中国知网、万方数据知识服务平台、中国生物医学文献数据库、中国临床指南文库、PubMed、The Cochrane Library和Embase数据库。自数据库截至2020年8月31日发表的食管癌或胃癌筛查领域所有相关的指南/共识,语种限定为中文和英文。中文检索词包括指南、共识、规范、标准、食管癌、食管肿瘤、胃癌、胃部肿瘤、筛查、筛检、诊断;英文检索词包括Guideline、Recommendation、Esophagus Cancer、Esophagus Neoplasm、Gastric Cancer、Gastric Tumor、Early Detection of Cancer、Screening。采用主题词和自由词相结合的方法进行检索,同时手工检索国际癌症研究机构(International Agency for Research on Cancer)、国际指南协作网(Guideline International Network)等机构官网刊登的指南作为补充。
2. 纳入/排除标准:对检索的文献进行筛选,纳入标准:①食管癌或胃癌筛查的独立指南文件;②符合美国医学研究所(Institute of Medicine)对指南的定义。排除标准:①文章语言非中文或英文;②指南摘要、解读及评价类文献;③已更新的原始版指南;④重复发表;⑤食管癌或胃癌临床治疗或实践指南。
3. 评价方法:采用AGREE Ⅱ和RIGHT评价指南质量。AGREE Ⅱ对指南的范围和目的、参与人员、严谨性、清晰性、应用性和独立性6个领域的23个条目分别进行评分,从很不同意到很同意划分为7个态度等级,按照1~7分打分。得分越高,说明该指南在此领域的方法学质量越高[8-10]。评价结束后,综合考虑上述评价标准和最终得分将指南的推荐分为4个等级:A级即推荐(≥4个领域的分值≥60分)、B级即在一定条件下推荐(3个领域的分值≥60分且≤2个领域的分值< 30分)、C级即修改完善后可推荐(2个领域的分值≥60分且≤3个领域的分值< 30分)、D级即不推荐(≤2个领域的分值≥60分且 > 3个领域的分值< 30分)。RIGHT对纳入指南在22个条目的35个具体标准“是/否”报告进行评价,共涵盖了基本信息、背景、证据、推荐意见、评审和质量保证、资金资助和利益冲突、其他方面7个领域。
4. 质量控制:由2名研究人员分别开展信息摘录。在实施评价前,由项目组对其进行方法学、食管癌和胃癌筛查背景、AGREE Ⅱ和RIGHT使用等方面的培训,评价过程中2人不进行相关交流,待评价结束后,共同评价结果,意见出现不一致时,由小组讨论决定。使用Endnote X9软件进行文献资料管理。
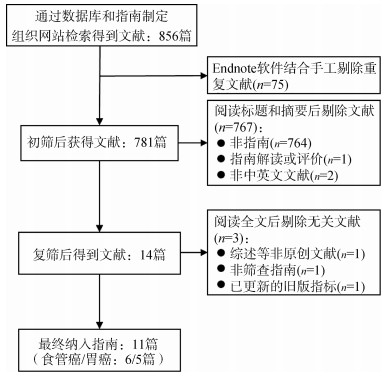
结果1. 基本情况:通过各数据库共检索到相关文献856篇,排除重复、无关、旧版指南等文献后,最终筛选出11篇文献[11-21],其中食管癌筛查指南6篇[15-19, 21]、胃癌筛查指南5篇[11-14, 20]。见图 1。纳入的11部指南均为各国的相关协会发布,指南发布时间为2014-2020年。见表 1。
|
| 图 1 文献检索流程图 |
2.食管癌筛查指南AGREE Ⅱ和RIGHT评价情况:
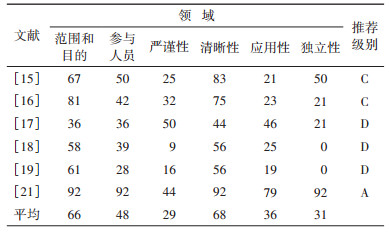
(1)AGREE Ⅱ:6篇指南中,推荐等级为A级的1篇、等级为C级的2篇、等级为D级的3篇。纳入指南在6个领域的具体得分:①范围和目的:得分最高的为加拿大筛查指南(92分),其次为中国巴雷特食管及其早期腺癌筛查与诊治共识(81分)。②参与人员:仅加拿大筛查指南得分 > 60分。③严谨性:所有筛查指南得分均 < 60分,其中3篇得分 < 30分。④清晰性:3篇指南得分 < 60分,其中早期食管癌及癌前病变筛查专家共识[17]得分最低(44分)。⑤应用性:仅加拿大筛查指南得分 > 60分,国内4篇指南得分 < 30分。⑥独立性:仅加拿大筛查指南得分 > 60分,4篇指南得分 < 30分,其中有2篇指南得分为0分。见表 2。
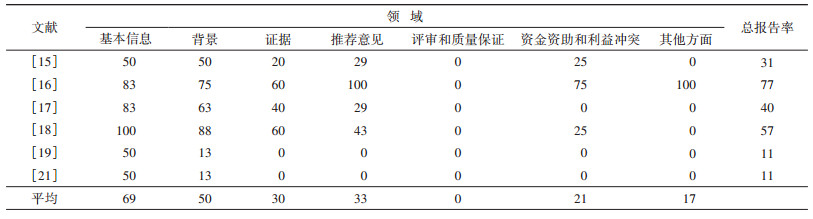
(2)RIGHT:在所评价的7个领域中,除基本信息外,其他6个领域报告率均较低。整体的不足主要集中在评审和质量控制、资金资助和利益冲突和其他方面3个领域。纳入指南在7个领域的报告情况:①基本信息:仅2部指南在标题中报告了指南的发表年份,以及对指南推荐意见进行汇总呈现。②背景:问题突出的条目集中出现在对指南制定贡献值角色描述不清晰(5篇)。③证据:6部指南未描述系统评价如何制作。④推荐意见:大多数指南未描述形成推荐意见的原理和解释说明(5部),指南制定工作组的决策过程和方法(5部)。⑤评审和质量保证:本领域各指南表现最差,所有指南均未报告。⑥资金资助和利益冲突:该领域仅1篇指南提到了资金来源以及作用,以及描述了利益冲突的管理方法。⑦其他方面:该领域仅1篇指南描述了指南的可及性、对未来的建议和局限性。见表 3。
3. 胃癌筛查指南AGREE Ⅱ和RIGHT评价情况:
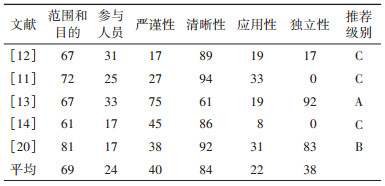
(1)AGREE Ⅱ:4篇指南中,推荐等级为A级的1篇,等级为C级的3篇。纳入指南在6个领域的具体得分:①范围和目的:5篇指南得分均 > 60分,得分最高的亚太地区胃癌防治共识(81分),其次为中国上海胃癌共识(72分)。②参与人员:3篇指南得分 < 30分,得分较低。③严谨性:仅日本指南得分 > 60分,国内2篇共识意见得分均 < 30分。④清晰性:5篇指南得分均 > 60分。⑤应用性:3篇指南得分 < 30分,为得分最低的领域,其中韩国胃癌筛查指南得分最低(8分)。⑥独立性:2篇指南得分 > 60分,3篇指南得分 < 30分,其中有2篇指南得分为0分。见表 4。
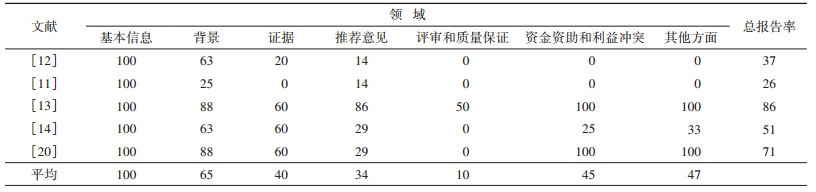
(2)RIGHT:在评价体系的7个领域中,除了基本信息篇外,其他6个领域中均有不同数量的指南回答“否”,整体的不足主要集中在证据、推荐意见、评审和质量控制3个领域。①基本信息:本领域各指南表现最好。②背景:问题突出的条目集中出现在缺乏对指南主要使用者和具体应用环境的描述(3篇)以及对指南贡献者的角色和责任描述不清晰(2篇)。③证据:5篇指南在使用文献综述和系统评价的方法时,没能明确呈现关键问题(4篇)和分类方法(3篇)。④推荐意见:在对推荐意见的描述中大多数指南未关注到目标人群中亚组人群的差异(4篇)以及其价值观和偏好(4篇),并缺乏对成本和资源的考虑(4篇)。此外,国内指南对决策过程和方法的描述欠佳。⑤评审和质量保证:该领域整体情况较差,仅1篇指南提及独立评审。⑥资金资助和利益冲突:该领域国内外差异较大,国外3篇指南在各项条目中均只有1篇指南缺少相关内容,但国内2篇指南均未涉及此领域的4项内容。⑦其他方面:只有2篇指南描述了指南制定过程中存在的局限性。见表 5。
食管癌和胃癌是我国最常见的消化道恶性肿瘤,其5年生存率较低,癌症的二级预防(早发现、早诊断和早治疗)已成为潜在患者提高生存率和生活质量的关键。本研究通过分析和评价目前已发表的食管癌和胃癌筛查指南,可以更好地为临床工作者选择合适的指南提供参考和依据。
本研究共纳入6篇食管癌筛查指南和5篇胃癌筛查指南,通过AGREE Ⅱ评价后,仅加拿大食管癌指南[21]和日本胃癌指南[13]涉及的内容全面,所形成的意见的证据可靠性强、过程的方法学严谨、利益相关者及冲突透明,符合A级推荐指南/推荐意见。而其他9篇多采用参考已发表的系统综述、指南或专家共识,它们的推荐等级分别为B、C和D级。
食管癌筛查指南纳入的6篇指南在独立性和严谨性领域存在普遍问题。指南的独立性是指指南必须在文中声明指南制定和资金赞助者之间及指南制定人员之间无利益冲突,大部分纳入的食管癌指南未进行利益冲突的声明和管理。指南制定的严谨性主要考察指南制定者对方法学的研究、认知和重视程度,包括对证据的检索、证据选择标准的描述、推荐意见形成的描述、形成推荐意见时是否考虑了对健康的风险及副作用、推荐意见与证据之间的关系、专家的外部评审和指南更新的步骤,但纳入的大部分食管癌指南未提供系统的证据检索步骤、筛选过程,在发表前也未经过专家的外部评审,并且随着医学的不断发展,筛查新技术、新疗法不断出现,筛查指南必须根据新出现的证据及时更新,大部分食管癌指南均未提及指南更新计划。
胃癌筛查指南纳入的5篇指南在参与人员和应用性领域存在普遍问题。指南参与人员是指指南制定组包括所有相关专业的人员,考虑到目标人群(患者、公众等)的观点和选择,并明确规定指南的适用者。虽然5篇指南均公布了参与制定的人员,但很少对其具体职责和角色进行详细描述[22],其报告的开发组织中以临床专家为主,缺乏公共政策、流行病、卫生经济、卫生法律等多学科的专业人士。指南应用性是指指南制定过程中需考虑指南推行的潜在障碍、推行指南推荐意见所需成本和监测指南使用的标准。纳入的指南没有从不同亚组人群的角度系统地收集实用性的数据,较少地考虑不同亚组的目标人群的价值观念、选择偏好[22],也就没有关注到指南在应用时可能存在的阻碍和促进实施的工具及额外资源,削弱了指南的应用性。因此,指南制定小组如果能有多学科的专家组成综合团队,由接受过专业培训的内部审核人员(含能对可用的证据进行系统评价、能运用指南研究和评估工具)协同撰写,针对实际的公共卫生状况,提出系统指导意见,会使指南更加科学严谨,从而能够引导使用者在当前的最佳证据、知识经验和临床判断与亚组人群的特别需求之前寻求平衡,最大程度满足个体患者的卫生服务需要[23],增强指南在实践中的适用性。
中国的食管癌和胃癌指南尽管在范围和目的、清晰性两个领域得分较高,但其余4个领域方法学质量总体偏低,有较大的提升空间。尤其对于得分最低的“独立性”领域,提示出受社会文化背景的影响,我国在指南制定时对赞助单位、利益冲突的公开声明环节认识缺位。如果能提供公开透明的项目资金资助来源和外部赞助支持,可以让指南用户避免因利益冲突导致的阳性偏倚,进而提高其可信度和权威性。
评审和质量保证是确保指南准确性和严谨性的核心,外审是指在指南全文正式发表前,制定小组外的专家或其他利益相关方对指南及其推荐意见进行的发布前评审[24]。评审专家小组应对指南方法学、指南推荐内容以及指南相关因素进行评估,对指南制定小组提出质疑,对每条推荐意见均无疑问才能予以公开发布。而所纳入的指南中仅有1部指南提及同行评审,但均未详细说明评审内容及评审结果。该领域仍需加强汇报的规范化和透明化。
高质量的循证医学指南对于我国高发的上消化道癌防控具有重大意义,不仅可以为临床实践提供重要的参考依据,也是引导居民养成健康的生活方式的重要工具。我国上消化道癌筛查指南的制定应基于我国人群的上消化道癌筛查研究和系统综述,在借鉴其他国家指南的同时充分考虑我国国情,参考AGREE Ⅱ和RIGHT,完善指南制定的各个环节。
利益冲突 所有作者均声明不存在利益冲突
| [1] |
Ferlay J, Colombet M, Soerjomataram I, et al. Estimating the global cancer incidence and mortality in 2018:Globocan sources and methods[J]. Int J Cancer, 2019, 144(8): 1941-1953. DOI:10.1002/ijc.31937 |
| [2] |
郑荣寿, 孙可欣, 张思维, 等. 2015年中国恶性肿瘤流行情况分析[J]. 中华肿瘤杂志, 2019, 41(1): 19-28. Zheng RS, Sun KX, Zhang SW, et al. Report of cancer epidemiology in China, 2015[J]. Chin J Oncol, 2019, 41(1): 19-28. DOI:10.3760/cma.j.issn.0253-3766.2019.01.005 |
| [3] |
Ferlay J, Soerjomataram I, Dikshit R, et al. Cancer incidence and mortality worldwide: Sources, methods and major patterns in globocan 2012[J]. Int J Cancer, 2015, 136(5): E359-386. DOI:10.1002/ijc.29210 |
| [4] |
Isobe Y, Nashimoto A, Akazawa K, et al. Gastric cancer treatment in Japan: 2008 annual report of the JGCA nationwide registry[J]. Gastric Cancer, 2011, 14(4): 301-316. DOI:10.1007/s10120-011-0085-6 |
| [5] |
Ajani JA, Bentrem DJ, Besh S, et al. Gastric cancer, version 2.2013:Featured updates to the NCCN guidelines[J]. J Natl Compr Canc Netw, 2013, 11(5): 531-546. DOI:10.6004/jnccn.2013.0070 |
| [6] |
房静远, 陈萦晅, 高琴琰. 重视慢性萎缩性胃炎癌变的预警、早诊与预防[J]. 中华消化杂志, 2018, 38(3): 145-148. Fang JY, Chen YX, Gao QY. Pay attention to early warning, early diagnosis and prevention of canceration of chronic atrophic gastritis[J]. Chin J Dig, 2018, 38(3): 145-148. DOI:10.3760/cma.j.issn.0254-1432.2018.03.001 |
| [7] |
Chen YL, Yang KH, Marušic A, et al. A reporting tool for practice guidelines in health care: the right statement[J]. Ann Intern Med, 2017, 166(2): 128-132. DOI:10.7326/m16-1565 |
| [8] |
Leung WK, Wu MS, Kakugawa Y, et al. Screening for gastric cancer in Asia: current evidence and practice[J]. Lancet Oncol, 2008, 9(3): 279-287. DOI:10.1016/S1470-2045(08)70072-X |
| [9] |
姜玢杉, 要鹏韬, 戈一冰, 等. 胃癌筛查领域指南方法学质量和报告质量的系统评价[J]. 中华预防医学杂志, 2020, 54(3): 314-319. Jiang FS, Yao PT, Ge YB, et al. Systematic review of methodological quality and reporting quality in gastric cancer screening guidelines[J]. Chin J Prev Med, 2020, 54(3): 314-319. DOI:10.3760/cma.j.issn.0253-9624.2020.03.013 |
| [10] |
李江, 杨珂璐, 蔡依彤, 等. 全球乳腺癌筛查指南质量评价[J]. 中华流行病学杂志, 2021, 42(2): 219-226. Li J, Yang KL, Cai YT, et al. Quality assessment of global breast cancer screening guidelines[J]. Chin J Epidemiol, 2021, 42(2): 219-226. DOI:10.3760/cma.j.cn112338-20200806-01032 |
| [11] |
国家消化系统疾病临床医学研究中心, 中华医学会消化内镜学分会, 中华医学会健康管理学分会, 等. 中国早期胃癌筛查流程专家共识意见(草案, 2017年, 上海)[J]. 中华消化杂志, 2018, 38(2): 87-92. National Clinical Research Center for Digestive Diseases, Digestive Endoscopy Branch of Chinese Medical Association, Health Management Branch of Chinese Medical Association, et al. Expert consensus on screening process of early gastric cancer in China (draft, 2017, Shanghai)[J]. Chin J Dig, 2018, 38(2): 87-92. DOI:10.3760/cma.j.issn.0254-1432.2018.02.006 |
| [12] |
中华医学会消化内镜学分会, 中国抗癌协会肿瘤内镜专业委员会. 中国早期胃癌筛查及内镜诊治共识意见(2014年, 长沙)[J]. 中华消化杂志, 2014, 34(7): 433-448. Digestive Endoscopy Branch of Chinese Medical Association, Cancer Endoscopy Committee of Chinese Anti Cancer Association. Consensus on screening and endoscopic diagnosis and treatment of early gastric cancer in China (Changsha, 2014)[J]. Chin J Dig, 2014, 34(7): 433-448. DOI:10.3760/cma.j.issn.0254-1432.2014.07.001 |
| [13] |
Hamashima C, Systematic Review Group and Guideline Development Group for Gastric Cancer Screening Guidelines. Update version of the Japanese guidelines for gastric cancer screening[J]. Jpn J Clin Oncol, 2018, 48(7): 673-683. DOI:10.1093/jjco/hyy077 |
| [14] |
Park HA, Nam SY, Lee SK, et al. The Korean guideline for gastric cancer screening[J]. J Korean Med Assoc, 2015, 58(5): 373-384. DOI:10.5124/jkma.2015.58.5.373 |
| [15] |
中国抗癌协会食管癌专业委员会, 中国下咽与食管癌协同诊疗工作组. 下咽与食管多原发癌筛查诊治中国专家共识[J]. 中华外科杂志, 2020, 58(8): 589-595. Committee of Esophageal Cancer in China Anti Cancer Association, Chinese Working Group on Cooperative Diagnosis and Treatment of Hypopharyngeal and Esophageal Cancer. Chinese expert consensus on multiple primary cancers of hypopharynx and esophagus[J]. Chin J Surgery, 2020, 58(8): 589-595. DOI:10.3760/cma.j.cn112139-20200311-00210 |
| [16] |
国家消化系统疾病临床医学研究中心, 中华医学会消化内镜学分会, 中国医师协会消化医师分会. 中国巴雷特食管及其早期腺癌筛查与诊治共识(2017年, 万宁)[J]. 中华消化内镜杂志, 2017, 34(9): 609-620. National Clinical Research Center for Digestive System Diseases, Digestive Endoscopy Branch of Chinese Medical Association, Digestive Physicians Branch of Chinese Medical Association. Consensus on screening, diagnosis and treatment of Barrett's esophagus and its early adenocarcinoma in China (Wanning, 2017)[J]. Chin J Dig Endosc, 2017, 34(9): 609-620. DOI:10.3760/cma.j.issn.1007-5232.2017.09.001 |
| [17] |
国家消化内镜专业质控中心, 国家消化系统疾病临床医学研究中心(上海), 国家消化道早癌防治中心联盟, 等. 中国早期食管癌及癌前病变筛查专家共识意见(2019年, 新乡)[J]. 中华健康管理学杂志, 2019, 13(6): 465-473. National Quality Control Center of Digestive Endoscopy, National Clinical Research Center for Digestive Diseases (Shanghai), National Early Gastrointestinal-Cancer Prevention & Treatment Center Alliance(GECA), et al. China experts consensus on the protocol of early esophageal cancer and pre-cancerous lesion screening (2019, Xinxiang)[J]. Chin J Health Manag, 2019, 13(6): 465-473. DOI:10.3760/cma.j.issn.1674-0815.2019.06.001 |
| [18] |
中华医学会消化内镜学分会, 中国抗癌协会肿瘤内镜专业委员会. 中国早期食管癌筛查及内镜诊治专家共识意见(2014年, 北京)[J]. 中华消化内镜杂志, 2015(4): 205-224. Digestive Endoscopy Branch of Chinese Medical Association, Cancer Endoscopy Committee of Chinese Anti Cancer Association. Chinese expert consensus on screening and endoscopic management of early esophageal cancer (Beijing, 2014)[J]. Chin J Dig Endosc, 2015(4): 205-224. DOI:10.3760/cma.j.issn.1007-5232.2015.04.001 |
| [19] |
中华医学会消化内镜学分会消化系早癌内镜诊断与治疗协作组, 中华医学会消化病学分会消化道肿瘤协作组, 中华医学会消化病学分会消化病理学组. 中国早期食管鳞状细胞癌及癌前病变筛查与诊治共识(2015年, 北京)[J]. 中华消化内镜杂志, 2016, 33(1): 3-18. Cooperation Group of Endoscopic Diagnosis and Treatment for Early Gastrointestinal Cancer of Digestive Endoscopy Branch of Chinese Medical Association, Digestive Tract Cancer Collaboration Group of Gastroenterology Branch of Chinese Medical Association, Digestive Pathology Group of Gastroenterology Branch of Chinese Medical Association. Consensus on screening, diagnosis and treatment of early esophageal squamous cell carcinoma and precancerous lesions in China (2015, Beijing)[J]. Chin J Dig Endosc, 2016, 33(1): 3-18. DOI:10.3760/cma.j.issn.1007-5232.2016.01.002 |
| [20] |
Fock KM, Talley N, Moayyedi P, et al. Asia-pacific consensus guidelines on gastric cancer prevention[J]. J Gastroenterol Hepatol, 2008, 23(3): 351-365. DOI:10.1111/j.1440-1746.2008.05314.x |
| [21] |
Groulx S, Limburg H, Doull M, et al. Guideline on screening for esophageal adenocarcinoma in patients with chronic gastroesophageal reflux disease[J]. CMAJ, 2020, 192(27): E768-777. DOI:10.1503/cmaj.190814 |
| [22] |
宋霄杨, 高玉婷, 王小琴, 等. 制订卫生研究报告指南的方法学指导[J]. 中国循证儿科杂志, 2017, 12(3): 204-208. Song XY, Gao YT, Wang XQ, et al. Methodological guidance for developing guidelines for health research reports[J]. Chin J Evid Based Pediatr, 2017, 12(3): 204-208. DOI:10.3969/j.issn.1673-5501.2017.03.010 |
| [23] |
李涛, 张勇, 陈凛. NCCN临床实践指南在胃癌外科进修医师培训中的应用[J]. 武警后勤学院学报: 医学版, 2014, 23(4): 362-364, 368. Li T, Zhang Y, Chen L. Application of NCCN clinical practice guidelines in postgraduates' training of gastric cancer surgery[J]. J Logist Univ CAPF: Med Sic, 2014, 23(4): 362-364, 368. DOI:10.3969/j.issn.2095-3720.2014.4.036 |
| [24] |
谭力铭, 薛竑飏, 范曼如, 等. 临床实践指南制订方法——指南发布前的外部评审[J]. 中国循证心血管医学杂志, 2019, 11(7): 771-773. Tan LM, Xue HY, Fan MR, et al. Methodology for clinical practice guidelines-external review of guidelines prior to publication[J]. Chin J Evid Based Cardiovasc Med, 2019, 11(7): 771-773. DOI:10.3969/j.issn.1674-4055.2019.07.02 |
 2021, Vol. 42
2021, Vol. 42