文章信息
- 杨琼英, 黄勇, 王雯, 张春焕, 许建雄, 张周斌.
- Yang Qiongying, Huang Yong, Wang Wen, Zhang Chunhuan, Xu Jianxiong, Zhang Zhoubin
- 2008年和2018年广州市乙型肝炎流行病学特征比较
- Comparative analysis on seroprevalence of hepatitis B in Guangzhou in 2008 and 2018
- 中华流行病学杂志, 2021, 42(6): 1061-1066
- Chinese Journal of Epidemiology, 2021, 42(6): 1061-1066
- http://dx.doi.org/10.3760/cma.j.cn112338-20200928-01195
-
文章历史
收稿日期: 2020-09-28
WHO于2016年通过全球病毒性肝炎策略,要求“到2030年前消除病毒性肝炎这一公共卫生威胁”。广州市于1992年开始新生儿乙型肝炎(乙肝)疫苗大规模接种,2002年将乙肝疫苗纳入计划免疫,2008年HBsAg流行率已有较大幅度下降,但仍属乙肝高发地区[1]。2006-2013年广州市累计报告乙肝病例199 318例,死亡病例297例[2]。为控制乙肝的高发态势,广州市2008-2011年开展≤15岁人群乙肝疫苗查漏补种工作,2011年启动预防乙肝母婴传播项目。为了解乙肝防控措施改变下的广州市人群乙肝血清流行病学特征变化,于2008年和2018年在全市范围内进行1~59岁人群乙肝血清流行病学调查,为制定WHO推行的全球消除病毒性肝炎目标计划提供科学依据。
对象与方法1. 调查方法:两次调查均采用分层二阶段整群抽样法,第1阶段均以区为单位将广州市分层,每层以与人口容量大小成比例的概率(probability proportional to size,PPS)抽取一定数目的居委会或行政村。2008年第2阶段在已抽取的居委会或行政村中随机抽取一定数目的住户,对住户中1~59岁常住人口(居住时间≥6个月)全部进行调查。2018年第2阶段在已抽取的居委会或行政村中随机抽取1~59岁常住人口进行调查。
2. 样本量估计:参考2006年全国乙肝血清流行病学调查,本研究两次调查以不同年龄组HBsAg流行率为确定样本量的计算标识,分别计算各年龄组所需样本量,合并得到总样本量。计算公式:

式中,n为所需样本量;p为总体概率π(参数)的估计值;Ⅰ类错误概率α取值0.05,则zα/2=1.96;绝对最大允许误差δ = p - π,为估计值95%CI的半宽度;设计效应值
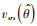
3. 调查内容:两次调查均采用入户或集中调查的方式,对研究对象进行问卷调查。调查内容包括出生日期、性别、民族、地区、乙肝疫苗接种史等信息。调查后采集静脉血3~5 ml,血清分离后置于-20 ℃冰箱中冻存待检。
4. 标本检测:2008年采用上海科华生物技术有限公司生产的酶联免疫测定试剂进行检测,HBsAg S/N(样本孔A值/阴性对照孔A值)≥2为阳性,对HBsAg单独阳性及HBsAg和抗-HBs同时阳性的血样用放射免疫试剂确认。2018年采用Cobase 602电化学发光全自动免疫分析仪进行检测,仪器和试剂均采购自罗氏诊断产品(上海)有限公司。
为保证两种检测方法结果的可比性,随机抽取2008年20份阳性标本和50份阴性标本,采用2018年的检测方法重新检测。结果显示,阳性标本一致率为100%,阴性标本一致率为98%,不一致的标本处于临界值,经比较两种检测方法差异无统计学意义(P=0.999)。
5. 相关定义:
(1)HBV感染:血清HBsAg、抗-HBc、HBeAg和抗-HBe至少有1项为阳性[3]。
(2)乙肝流行地区[4-5]:①高流行区:HBsAg阳性率≥8%;②低流行区:HBsAg阳性率≤2%;③中流行区:HBsAg阳性率为2%~8%。
6. 年龄组划分:2008年调查的1~6岁人群为乙肝疫苗纳入免疫规划实施后的人群;7~16岁人群为开始实施新生儿乙肝疫苗接种但未纳入计划免疫管理,即自费接种乙肝疫苗的人群;17~59岁人群为实施计划免疫管理前人群。2018年调查的1~6岁人群为启动预防乙肝母婴传播项目后的人群;7~16岁人群为纳入计划免疫管理但未启动母婴传播项目的人群;17~59岁人群大部分为实施计划免疫管理前人群。
7. 统计学分析:采用EpiData 3.1软件进行数据双录入,核对无误后使用SPSS 24.0软件进行复杂抽样数据统计分析。2008年和2018年调查数据均按调查设计权重加权估计率及其95%CI。采用复杂抽样的χ2检验进行率的比较。双侧检验,以P < 0.05为差异有统计学意义。
结果1. 乙肝疫苗接种率:2008年调查1~59岁人群4 989名,其中,乙肝疫苗接种史有、无及不详的分别有3 088名(61.90%)、923名(18.50%)及978名(19.60%)。2018年调查1~59岁人群3 980名,其中,乙肝疫苗接种史有、无及不详的分别为2 735名(68.72%)、479名(12.04%)及不详766名(19.25%)。2018年广州市各年龄组人群的乙肝疫苗接种率均较2008年升高(表 1)。
2. HBsAg阳性率变化情况:2008年和2018年1~59岁人群HBsAg阳性率分别为12.45%和9.50%,其中1~6岁人群HBsAg阳性率最低,分别为0.48%和0.28%,17~59岁人群HBsAg阳性率最高,分别为14.72%和11.28%。有乙肝疫苗接种史人群的HBsAg阳性率分别为5.81%和3.90%,无乙肝疫苗接种史人群的HBsAg阳性率分别为18.26%和18.95%,有、无乙肝疫苗接种史人群HBsAg阳性率差异有统计学意义(表 2)。
与2008年相比,2018年1~59岁人群HBsAg阳性率略有下降,但差异无统计学意义。7~16岁人群HBsAg阳性率下降(降幅为80.62%),差异有统计学意义。
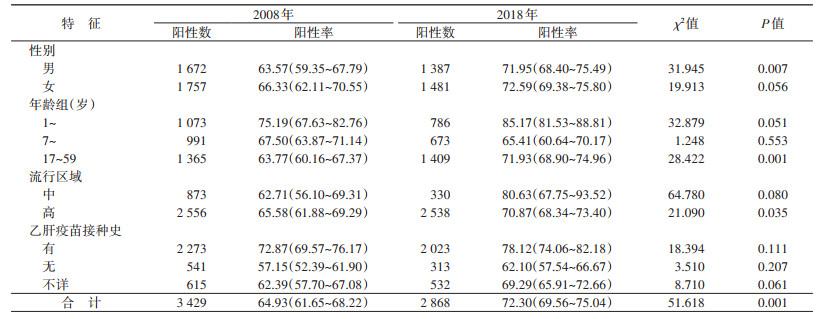
3. 抗-HBs阳性率变化情况:2008年和2018年1~59岁人群抗-HBs阳性率分别为64.93%和72.30%,其中1~6岁人群抗-HBs阳性率最高,分别为75.19%和85.17%。具有乙肝疫苗接种史的人群抗-HBs阳性率分别为72.87%和78.12%,无乙肝疫苗接种史的人群抗-HBs阳性率分别为57.15%和62.10%,有、无乙肝疫苗接种史人群抗-HBs阳性率差异有统计学意义(表 3)。
与2008年相比,2018年1~59岁人群抗-HBs阳性率升高(升幅11.35%),差异有统计学意义。其中17~59岁人群抗-HBs阳性率升高(升幅12.80%),差异有统计学意义。
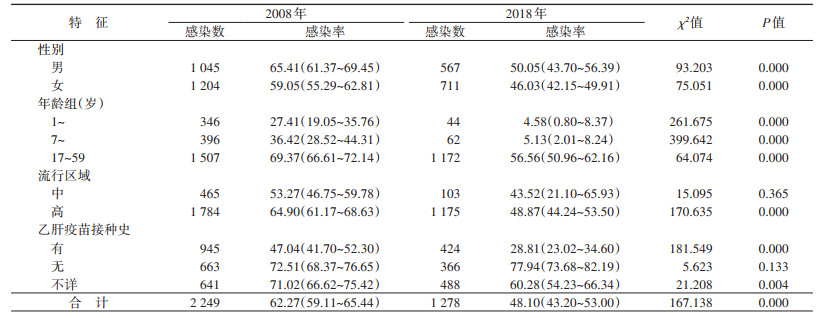
4. HBV感染率变化情况:2008年和2018年1~59岁人群HBV感染率分别为62.27%和48.10%,其中17~59岁人群HBV感染率最高,分别为69.37%和56.56%。中流行区、高流行区人群HBV感染率分别为53.27%、64.90%和43.52%、48.87%。具有乙肝疫苗接种史的人群HBV感染率分别为47.04%和28.81%,无乙肝疫苗接种史的人群HBV感染率分别为72.51%和77.94%,有、无乙肝疫苗接种史的人群HBV感染率差异有统计学意义(表 4)。
与2008年相比,2018年人群HBV感染率明显下降(降幅22.76%),差异有统计学意义。其中,1~、7~和17~59岁人群HBV感染率均明显下降(降幅分别为81.83%、85.91%和18.47%)。高流行区人群HBV感染率降低(降幅24.70%),差异有统计学意义,中流行区人群HBV感染率差异无统计学意义。具有乙肝疫苗接种史人群的HBV感染率下降(降幅38.75%)。
讨论HBV感染是全球重大公共卫生问题,接种乙肝疫苗是最经济有效的预防控制措施之一[4-5]。2008年广州市1~16岁人群HBsAg阳性率为0.48%,2018年下降为0.28%,均达到≤5岁儿童HBsAg流行率继续控制 < 1%的指标要求[6]。与2008年相比,2018年广州市1~59岁人群乙肝疫苗接种率升高,抗-HBs阳性率升高,HBV感染率下降(降幅为22.76%),其中1~16岁人群下降幅度较大,且主要为有乙肝疫苗接种史的人群感染率下降。表明广州市实施儿童乙肝疫苗免疫接种的成效显著。
2008年广州市1~59岁人群HBsAg阳性率为12.45%,2018年HBsAg阳性率与2008年比有所下降,为9.50%,提示从全人群角度看,广州市依然属于乙肝高流行区。从全国乙肝流行情况看,2006年我国1~59岁人群HBsAg阳性率为7.2%[7],乙肝流行已降为中流行强度。2014年我国1~29岁人群HBsAg阳性率为2.64%[8],且有研究估计2016年我国人群HBsAg阳性率为6.1%[9]。与全国比较,广州市乙肝流行情况不容乐观,乙肝防控工作任重道远。与2008年相比,2018年广州市HBsAg的下降主要表现在7~16岁(2002-2011年出生)人群,这部分人群HBsAg的下降,一方面与广州市2011年启动预防乙肝母婴传播项目的乙肝免疫措施密切相关,另一方面可能与2008-2011年开展≤15岁儿童乙肝疫苗查漏补种工作,减少易感人群的数量有关。2018年7~16岁人群的乙肝疫苗接种率(96.20%)比2008年(77.58%)接种率明显升高,也支持此推断。
2008年广州市1~59岁人群抗-HBs阳性率为64.93%,2018年有所升高,但主要为17~59岁人群升高有统计学意义。广州市自1992年开展新生儿乙肝疫苗免疫接种至今,17~59岁人群在疫苗免疫保护的大环境下经历的时间最长,防控效果最为显著。从研究结果看,与2008年相比,2018年1~59岁人群乙肝疫苗接种率升高11.67%,而抗-HBs阳性率仅上升7.37%,说明人群抗体阳性率提高缓慢,与其他研究结果一致[8, 10],且不同性别、年龄组、流行区域的人群抗-HBs阳性率虽在点估计上有一定的升高,但差异均无统计学意义,侧面反映免疫接种对于群体建立保护屏障需要更长的时间。2018年广州市1~59岁人群HBV感染率(48.10%)较2008年(62.27%)有明显下降,但按广州市2018年1~59岁户籍人口数663.6万估算,广州市1~59岁人群中约有319.2万人感染HBV。数量庞大的HBV感染者对完成消除乙肝的目标是一大挑战,需要引起重视,应开展慢性HBV感染者的科学管理和规范的抗病毒治疗。
从年龄分组看,1~6岁人群抗-HBs阳性率最高(2008、2018年分别为75.19%、85.17%),HBV感染率最低(2008、2018年分别为27.41%、4.58%),而17~59岁人群抗-HBs阳性率和7~16岁人群接近,但HBV感染率最高(2008、2018年分别为69.37%、56.56%)。2008年和2018年的1~6岁人群均为乙肝纳入免疫规划实施后的人群,且2018年1~6岁人群还为乙肝母婴传播项目实施的儿童,而17~59岁人群中绝大多数为实施计划免疫管理前人群。因此,低年龄组人群抗体阳性率高而感染率低,与高年龄组人群抗体阳性率低而感染率高,符合计划免疫在婴幼儿人群中实施所产生的效果,也表明计划免疫确实是有效的。
2018年1~、7~16岁人群的乙肝疫苗接种率分别为100.00%、96.20%,抗-HBs阳性率分别为85.17%、65.41%,而1~和7~16岁人群无乙肝保护性抗体的分别占14.83%和34.59%。广州市2012年将儿童乙肝疫苗接种剂量从5 µg调整为10 µg,而多数无乙肝保护性抗体的1~6岁人群对乙肝疫苗存在无/低应答情况,7~16岁人群是接种5 µg剂量的人群,随着年龄增长,抗-HBs水平逐步下降有可能导致无保护性抗体。说明5 µg剂量的疫苗免疫持久性不够理想,与既往研究结果一致[11-12]。与2008年比,2018年17~59岁人群抗-HBs阳性率略有升高,HBV阳性率下降,但此现象可能是2008年7~16岁接种乙肝疫苗的人群经过10年进入到这一年龄组人群所致。成年人社会活动频繁且性需求旺盛[13],20~39岁人群为性活跃人群[14-15],是HBV感染的重点人群。成年人按照0-1-6程序接种3剂次10 µg或20 µg均能产生较好的抗体应答[16-17]。因此,在新生儿乙肝疫苗普及接种的基础上,应重点加强对成年人群的监测,鼓励其到医疗机构定期体检筛查,补种、加强或重新接种乙肝疫苗。
本研究存在不足,收集成年人的乙肝疫苗接种史存在回忆偏倚,影响资料分析的可靠性。
综上所述,自2008年以来,广州市乙肝防控取得显著成效,儿童HBV感染率达到WHO消除乙肝2020年的目标,但仍属于高流行区,降低乙肝死亡率的目标任务艰巨,需继续做好新生儿乙肝疫苗接种工作和成年人的监测筛查工作。
利益冲突 所有作者均声明不存在利益冲突
| [1] |
王鸣, 刘建华, 蔡衍珊, 等. 广州市乙型肝炎流行特征研究[J]. 中华流行病学杂志, 2009, 30(12): 1317-1318. Wang M, Liu JH, Cai YS, et al. An investigation on the epidemiological characteristics of hepatitis B in Guangzhou[J]. Chin J Epidemiol, 2009, 30(12): 1317-1318. DOI:10.3760/cma.j.issn.0254-6450.2009.12.028 |
| [2] |
李建杰, 洪佳冬. 2006-2013年广州市乙型病毒性肝炎流行病学分析[J]. 现代预防医学, 2015, 42(8): 1363-1366. Li JJ, Hong JD. Epidemiological analysis of hepatitis B in Guangzhou City between 2006 and 2013[J]. Mod Prev Med, 2015, 42(8): 1363-1366. |
| [3] |
朱渭萍, 王远萍, 费怡, 等. 上海市浦东新区不同人群乙肝病毒感染现状与免疫策略研究[J]. 中华疾病控制杂志, 2014, 18(2): 112-116. Zhu WP, Wang YP, Fei Y, et al. Study on HBV infection situation and vaccination in different population in Pudong New Area of Shanghai[J]. Chin J Dis Control Prev, 2014, 18(2): 112-116. |
| [4] |
World Health Organization. Global hepatitis report 2017[R]. Geneva: WHO, 2017.
|
| [5] |
World Health Organization. Hepatitis B vaccines: WHO position paper, July 2017-Recommendations[J]. Vaccine, 2019, 37(2): 223-225. DOI:10.1016/j.vaccine.2017.07.046 |
| [6] |
国家卫生和计划生育委员会, 国家发展和改革委员会, 教育部, 等. 中国病毒性肝炎防治规划(2017-2020年)[EB/OL]. (2017-11-10)[2020-08-01]. http://www.nhc.gov.cn/ewebeditor/uploadfile/2017/11/20171113134002475.pdf. National Health and Family Planning Commission, National Development and Reform Commission, Ministry of Education, et al. Prevention and Control program of Viral Hepatitis in China (2017-2020)[EB/OL]. (2017-11-10)[2020-08-01]. http://www.nhc.gov.cn/ewebeditor/uploadfile/2017/11/20171113134002475.pdf. |
| [7] |
Liang XF, Bi SL, Yang WZ, et al. Epidemiological serosurvey of Hepatitis B in China-Declining HBV prevalence due to Hepatitis B vaccination[J]. Vaccine, 2009, 27(47): 6550-6557. DOI:10.1016/j.vaccine.2009.08.048 |
| [8] |
王富珍, 张国民, 沈立萍, 等. 1992和2014年中国不同流行地区1~29岁人群乙型肝炎血清流行病学调查结果对比分析[J]. 中华预防医学杂志, 2017, 51(6): 462-468. Wang FZ, Zhang GM, Shen LP, et al. Comparative analyze on hepatitis B seroepidemiological surveys among population aged 1-29 years in different epidemic regions of China in 1992 and 2014[J]. Chin J Prev Med, 2017, 51(6): 462-468. DOI:10.3760/cma.j.issn.0253-9624.2017.06.002 |
| [9] |
The Polaris Observatory Collaborators. Global prevalence, treatment, and prevention of hepatitis B virus infection in 2016:a modelling study[J]. Lancet Gastroenterol Hepatol, 2018, 3(6): 383-403. DOI:10.1016/S2468-1253(18)30056-6 |
| [10] |
苏颖, 唐继海, 柴瑜. 2014年安徽省1-29岁人群乙型病毒性肝炎血清流行病学调查[J]. 现代预防医学, 2017, 44(9): 1553-1556, 1560. Su Y, Tang JH, Chai Y. Sero epidemiological survey of hepatitis B virus among people aged 1-29 in Anhui Province, 2014[J]. Mod Prev Med, 2017, 44(9): 1553-1556, 1560. |
| [11] |
肖敏. 北京市新生儿高剂量乙肝疫苗免疫效果及其影响因素研究[D]. 北京: 北京协和医学院, 2015. Xiao M. Immune response in infants after universal high-dose hepatitis B vaccination: a community-based study in Beijing. [D]. Beijing: Peking Union Medical College, 2015. |
| [12] |
张丽, 张卫, 翟祥军, 等. 新生儿5μg和10μg重组酵母乙型肝炎疫苗初免后抗体免疫应答比较[J]. 中华流行病学杂志, 2012, 33(3): 305-308. Zhang L, Zhang W, Zhai XJ, et al. Comparison on the antibody response after primary immunization of 5μg and 10μg hepatitis B vaccine made bv recombinant DNA techniques among newborns[J]. Chin J Epidemiol, 2012, 33(3): 305-308. DOI:10.3760/cma.j.issn.0254-6450.2012.03.013 |
| [13] |
张国民, 孙校金, 王富珍, 等. 中国18~59岁人群乙型病毒性肝炎流行病学特征分析及乙型肝炎疫苗免疫策略探讨[J]. 中国疫苗和免疫, 2013, 19(3): 266-270. Zhang GM, Sun XJ, Wang FZ, et al. Analysis of epidemiological characteristics of Hepatitis B among the population of 18-59 year-old and HepB immunization Strategies[J]. Chin J Vaccin Immun, 2013, 19(3): 266-270. |
| [14] |
龚向东, 岳晓丽, 滕菲, 等. 2000-2013年中国梅毒流行特征与趋势分析[J]. 中华皮肤科杂志, 2014, 47(5): 310-315. Gong XD, Yue XL, Teng F, et al. Syphilis in China from 2000 to 2013:epidemiological trends and characteristics[J]. Chin J Dermatol, 2014, 47(5): 310-315. DOI:10.3760/cma.j.issn.0412-4030.2014.05.002 |
| [15] |
岳晓丽, 龚向东, 李婧, 等. 2008-2016年中国性病监测点尖锐湿疣流行特征分析[J]. 中华皮肤科杂志, 2017, 50(5): 321-325. Yue XL, Gong XD, Li J, et al. Epidemiological features of condyloma acuminatum in national sexually transmitted disease surveillance sites in China from 2008 to 2016[J]. Chin J Dermatol, 2017, 50(5): 321-325. DOI:10.3760/cma.j.issn.0412-4030.2017.05.003 |
| [16] |
刘甲野, 颜丙玉, 张丽, 等. 成人接种20微克重组乙型肝炎疫苗免疫应答及其影响因素的比较研究[J]. 中国疫苗和免疫, 2013, 19(2): 142-146, 153. Liu JY, Yan BY, Zhang L, et al. Comparison on the antibody response and influenced factors of hepatitis B vacine made by recombinant dexyribonucleic acid techniques among adults[J]. Chin J Vaccin Immun, 2013, 19(2): 142-146, 153. |
| [17] |
颜丙玉, 张丽, 吕静静, 等. 成人重组酿酒酵母和汉逊酵母乙型肝炎疫苗免疫应答及相关因素研究[J]. 中华流行病学杂志, 2012, 33(9): 988-989. Yan BY, Zhang L, Lv JJ, et al. Comparison of the antibody response and related influencing factors after primary immunization by 10μg hepatitis B vaccine made from recombinant DNA techniques in saccharomyces and hansenula polymorpha among adults[J]. Chin J Epidemiol, 2012, 33(9): 988-989. DOI:10.3760/cma.j.issn.0254-6450.2012.09.025 |
 2021, Vol. 42
2021, Vol. 42