文章信息
- 宗俊, 丁晟, 田国忠, 夏光辉, 熊长辉, 王鹏, 徐晓倩, 徐建民.
- Zong Jun, Ding Sheng, Tian Guozhong, Xia Guanghui, Xiong Changhui, Wang Peng, Xu Xiaoqian, Xu Jianmin
- 江西省羊种布鲁氏菌分子流行病学特征分析
- Characteristics on molecular epidemiology of Brucella melitensis in Jiangxi province
- 中华流行病学杂志, 2020, 41(8): 1341-1344
- Chinese Journal of Epidemiology, 2020, 41(8): 1341-1344
- http://dx.doi.org/10.3760/cma.j.cn112338-20191225-00916
-
文章历史
收稿日期: 2019-12-25
2. 中国疾病预防控制中心传染病预防控制所, 北京 102206
2. National Institute for Communicable Disease Control and Prevention, Chinese Center for Disease Control and Prevention, Beijing 102206, China
布鲁氏菌病(布病)是由布鲁氏菌引起的一种人畜共患传染病,布鲁氏菌属有6个生物种(羊种、牛种、猪种、绵羊附睾种、犬种、沙林鼠种),传统分类方法仍为鉴定布鲁氏菌的金标准,该方法比较费时费力,尤其是遇到不典型或表型特征不稳定的菌株鉴定更为复杂,由于布鲁氏菌各型之间同源程度非常高,分型方法少。随着科技水平的提高,出现了DNA为基础的分子分型方法,多位点可变数目串联重复序列分析(MLVA)是基于PCR技术方法,通过区分基因组上多个具有多态性串联重复序列位点(VNTR)的重复数来区分菌株,该项技术在国际上广泛运用在布鲁氏菌基因分型[1-3]。
MLVA16方案将16个VNTR分为Panel1(Bruce06、Bruce08、Bruce11、Bruce12、Bruce42、Bruce43、Bruce45、Bruce55)、Panel2A(Bruce18、Bruce19、Bruce21)和Panel2B(Bruce04、Bruce07、Bruce09、Bruce16、Bruce30),根据VNTR组合又可分为MLVA8型(Panel1)、MLVA11型(Panel1+Panel2A)、MLVA16型(Panel1+Panel2A+Panel2B)3个型。Panel1的VNTR其多态性较低,仅用于遗传关系较远菌株的鉴别,尤其是布鲁氏菌在种水平上的鉴别。Panel2 8个VNTR又细分为具有高度多态性,用于遗传关系较近的菌株鉴别,其中Panel2B有非常高的分辨力,能将菌株最细微的差异表现出来,也是MLVA16分型中的关键VNTR位点,因此,MLVA16方案已被证明是在流行病学中追溯特定区域的菌株来源的重要工具之一[4-5]。运用MLVA16对江西省的羊种布鲁氏菌进行分子流行病学研究,了解菌株间流行病学相关性,掌握布病防控关键技术,为防控布病提供新的模式打下基础。
对象与方法1.数据来源:中国疾病预防控制系统传染病报告信息管理系统2011-2017年江西省布病疫情资料,其他数据来源于《江西统计年鉴-2018》[6]。
2.实验菌株:25株布鲁氏菌于2012-2017年由江西省部分医院从布病患者血液分离,均采用经典微生物学方法进行表型特征鉴定,即需要CO2,产生H2S,尿素水解,单特异性血清凝集(A、M、R),染料敏感性(硫堇、碱性复红)和噬菌体分型(Tb、Wb BK2、Fi)。
3.细菌培养与核酸提取:将待检菌株接种于布氏琼脂培养基上,37 ℃培养48 h,使用细菌核酸提取试剂盒(北京天根生化科技有限公司),按照说明书进行核酸提取,-20 ℃保存。
4.分型方法:VNTR位点的选择及引物设计实验方法参考文献[7],引物由北京擎科新业生物技术公司合成,并在上游引物5′端标记荧光基团。
5. VNTR位点扩增:采用多重PCR法扩增各VNTR位点。①反应体系:PCR均采用30 μl反应体系,包括2×EasyTaqPCR Super Mix:15 μl,引物(10 μmol/L)2 μl,DNA模板1 μl,去离子水12 μl;②扩增条件:预变性96 ℃3 min,94 ℃30 s,60 ℃90 s、72 ℃30 s,35个循环,最后72 ℃延伸5 min,PCR产物4 ℃保存。
6. PCR产物检测与测序:产物送北京擎科新业生物技术公司,采用ABI Prism 3130自动荧光毛细管DNA测序仪(Applied Biosystems)通过毛细管电泳确定PCR产物的大小,采用Gene-Mapper 4.0软件进行分析并计算检测位点中各VNTR重复次数。
7.数据分析:将VNTR转换为串联重复单元的数量,将该数据提交给网络数据库(http://mlva.u-psud.fr),通过比对得到布鲁氏菌基MLVA8、MLVA11基因型。聚类分析将重复单元数据导入BioNumerics 7.5软件中提供的算术平均值(UPGMA)方法,基于分类系数和非加权对组方法。布鲁氏菌菌株多态性分析使用辛普森指数多样性指数来表达,Hunter和Gaston[8]1988年提出使用辛普森指数(1949)来辨别物种多态性,辛普森指数越大,物种多样性越丰富。多样性指数是每个VNTR重复数变异性的量度。它的范围可以从0(无多样性)到1(极端多样性)。因此,样品具有相似VNTR重复数的基因具有较低的多样性指数,而样品几乎全部具有不同VNTR重复数的基因,具有非常高的多样性指数。此外,为每个检查的参数生成的95%CI通过提供上边界和下边界来指示ID的精度。将MLVA串联重复单元的数据导入在线工具http://www.comparingpartitions.info/?link=Tool计算多样性指数。
结果1.菌株分离地区和时间分布:25株布鲁氏菌分布于江西省17个县(区)(表 1),分别从2012-2017年布病住院患者血培养获得。
2.生物型鉴定:25株布鲁氏菌经表型特征鉴定为羊种布鲁氏菌,其中羊3型23株、羊1型2株(图 1)。

|
| 注:MLVA:多位点可变数目串联重复序列分析方法 图 1 江西省25株羊种布鲁氏菌MLVA聚类分析 |
3. MLVA分型:将所有VNTR数据导入在线数据库后,经比较数据库的数据得到的结果,25株菌株在聚类后分析,菌株间相似度在67.00%~100.00%(图 1)。
MLVA16基因型有24个独立基因型,其中JX1201株与JX1711株相似度为100.00%。MLVA8有3个基因型,42型(1-5-3-13-2-2-3-2),占60.00%(15/25)、43型(1-5-3-13-3-2-3-2)占32.00%(8/25)和63型(1-5-3-13-2-3-3-2),占8.00%(2/25)。
MLVA11有7个基因型(104、111、116、121、122、125、179),其中116和125型为主要基因型,占菌株的56.00%(14/25),另有20.00%(5/25)无比对结果。
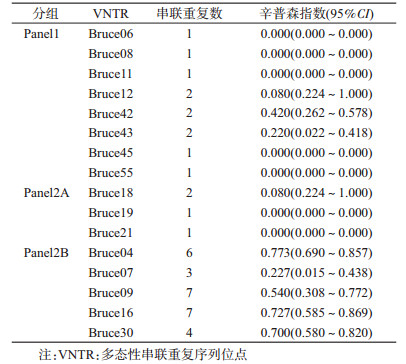
4.辛普森指数:25株羊种布鲁氏菌MLVA16辛普森指数在0.000~0.773之间,Panel1和Panel2A多样性较低,除了Bruce42指数高一点外其余非常小甚至为0,而Panel2B的Bruce04、Bruce09、Bruce16和Bruce30多样性指数分别为0.700、0.727、0.540、0.773。见表 1。
讨论江西省地处鄱阳湖畔,牧草资源丰富,畜牧业发达,近年来随着市场对羊肉的需求量增加,养殖户越来越多,截至2017年底,羊年末存栏952 800只,比2016年增长7.5%[6],随着养殖户增加和大量羊群进入江西省,由于检疫措施不完善,使江西省布病疫情越来越多,是导致江西省布病疫情上升的主要原因,与国内学者阐述中国南方布病的出现,很可能起源于中国其他地方动物引进的表述一致[9]。
江西省时隔30年于2011年再次报告布病病例,并在2012年首次在患者血液分离到布鲁氏菌[10],从病原学证实江西省存在布病,至2017年共报告布病239例,发病率由2011年的0.002/10万到2017年的0.159/10万,上升趋势非常明显。从2011年开始在7年内,报告病例从1个县(市、区)增加到69个,病例报告及地区增长非常明显,与文献报道南方布病疫情发展相一致[11],然而,布病的人间疫情控制乏力,与传染源管理有关,亟需加强监测,与农业部门联防联控,是控制人间布病疫情的最佳手段。
本研究数据经在线数据库比较后分析,MLVA8型有3个基因型,42、43和63(基因)型,其中以42型为江西省主要布鲁氏菌流行菌株。国内学者报道MLVA8的基因42、43型在我国最常见[9],是典型的“东地中海”型,有文献报道63型较少,仅在新疆维吾尔自治区、内蒙古自治区、青海省和山西省流行[12],但江西省25株布鲁氏菌中有2株63型菌株,与江西省相邻的福建省也有63型菌株存在[13],不排除江西省种羊及羊群从其他省份引进而致人感染该基因型菌株[9, 14]。
MLVA11型有7个基因型,分布于江西省17个县(区),且有明显的地理分布特征,以116、125型为主流基因型,并有各自的流行区域,其分布特点是以南昌地区为中心,分布在周边市(县),116型以南昌市东湖区、青山湖区为中心北向九江的永修县、都昌县,南向宜春市丰城市、吉安市峡江县,125型从南昌市新建区往江西省的东部地区的上饶市万年县、上饶县,南向抚州市南城县、赣州市信丰县,2个基因型在江西省的地理分布均为从北到南的2条线路,且116、125型布鲁氏菌株在流行县(区)不重叠,是否与羊群的贩运、转场养殖活动有关,值得我们重视。
本研究数据中,另有5株菌株在网络数据库中MLVA11基因型无比对结果,需要进一步通过数据分析和实验来判断其基因型。
将VNTR数据经网络在线工具计算辛普森指数显示,MLVA16的Panel1和Panel2A的VNTR多态性指数非常低甚至无,但关键点在Panel2B的VNTR上,辛普森指数非常高,显示菌株的多态性高,因此,其区分能力也高。将25株羊种布鲁氏菌MLVA16基因型的全部VNTR聚类后,可分为24个独立基因型,经调查后发现,24株菌株之间无明显流行病学相关性,这与江西省病例高度散发,没有聚集性疫情相吻合,说明江西省人感染布鲁氏菌的传染源的来源复杂。25株菌株中新建区的2株布鲁氏菌JX1201/JX1711,有100.00%相同的MLVA16图谱,其分别从2名患者血液分离的菌株,也是同一地区、不同养殖场、不同年份、不同疫情中的分离菌株,但2株布鲁氏菌分离时间相差5年,其遗传基因不变,表明两者可能存在流行病学联系,由此可见,MLVA16分型方法能准确判断菌株基因,追踪疫情的起源,在流行病学中有其重要的意义。
综上所述,25株人分离羊种布鲁氏菌基因具有高度遗传多样性,菌株基因型繁多,各菌株间无明显流行病学相关性,显示江西省布鲁氏菌传染来源复杂,染疫动物为江西省人布鲁氏菌病感染的主要特征。
利益冲突 所有作者均声明不存在利益冲突
志谢 中国CDC传染病预防控制所布鲁氏菌病室姜海、崔步云、田国忠、朴东日、赵鸿雁等老师提供实验室技术帮助,崔志刚老师提供聚类分析图制作帮助
| [1] |
Le Flèche P, Jacques I, Grayon M, et al. Evaluation and selection of tandem repeat loci for a Brucella MLVA typing assay[J]. BMC Microbiol, 2006, 6: 9. DOI:10.1186/1471-2180-6-9 |
| [2] |
Al Dahouk S, Le Flèche P, Nöckler K, et al. Evaluation of Brucella MLVA typing for human brucellosis[J]. J Microbiol Methods, 2007, 69(1): 137-145. DOI:10.1016/j.mimet.2006.12.015 |
| [3] |
Kattar MM, Jaafar RF, Araj GF, et al. Evaluation of a multilocus variable-number tandem-repeat analysis scheme for typing human Brucella isolates in a region of brucellosis endemicity[J]. J Clin Microbiol, 2008, 46(12): 3935-3940. DOI:10.1128/JCM.00464-08 |
| [4] |
Mustafa AS, Habibi N, Osman A, et al. Species identification and molecular typing of human Brucella isolates from Kuwait[J]. PLoS One, 2017, 12(8): e0182111. DOI:10.1371/journal.pone.0182111 |
| [5] |
田国忠, 崔步云, 赵鸿雁, 等. 一起羊种布鲁氏菌病暴发的流行病学和分子特征研究[J]. 疾病监测, 2017, 32(3): 211-215. Tian GZ, Cui BY, Zhao HY, et al. Studies on epidemiology and molecular characteristics of Brucella melitensis during an outbreak of brucellosis[J]. Dis Surveill, 2017, 32(3): 211-215. DOI:10.3784/j.issn.1003-9961.2017.03.011 |
| [6] |
江西省统计局. 江西统计年鉴-2018[M]. 北京: 中国统计出版社, 2018: 268. Statistics Bureau of Jiangxi. Jiangxi statistical yearbook-2018[M]. Beijing: China Statistics Press, 2018: 268. |
| [7] |
姜海, 荣蓉, 田国忠, 等. 利用多重聚合酶链反应和多色毛细管电泳分析布氏菌多位点可变数目串联重复序列[J]. 中国人兽共患病学报, 2015, 31(4): 303-310. Jiang H, Rong R, Tian GZ, et al. MLVA-16 Loci panel on Brucella spp. using multiplex PCR and multicolor capillary electrophoresis[J]. Chin J Zoonoses, 2015, 31(4): 303-310. DOI:10.3969/cjz.j.issn.1002-2694.2015.04.003 |
| [8] |
Hunter PR, Gaston MA. Numerical index of the discriminatory ability of typing systems:an application of Simpson's index of diversity[J]. J Clin Microbiol, 1988, 26(11): 2465-2466. DOI:10.1128/JCM.26.11.2465-2466.1988 |
| [9] |
Jiang H, Fan MG, Chen JD, et al. MLVA genotyping of Chinese human Brucella melitensis biovar 1, 2 and 3 isolates[J]. BMC Microbiol, 2011, 11: 256. DOI:10.1186/1471-2180-11-256 |
| [10] |
徐建民, 宗俊, 杨梦, 等. 江西省首次从当地人群中分离出布鲁氏菌及其流行病学分析[J]. 中华流行病学杂志, 2014, 35(5): 616. Xu JM, Zong J, Yang M, et al. Isolation of Brucella from human specimen and epidemiological analysis in Jiangxi province[J]. Chin J Epidemiol, 2014, 35(5): 616. DOI:10.3760/cma.j.issn.0254-6450.2014.05.035 |
| [11] |
施玉静, 赖圣杰, 陈秋兰, 等. 我国南北方2015-2016年人间布鲁氏菌病流行特征分析[J]. 中华流行病学杂志, 2017, 38(4): 435-440. Shi YJ, Lai SJ, Chen QL, et al. Analysis on the epidemiological features of human brucellosis in northern and southern areas of China, 2015-2016[J]. Chin J Epidemiol, 2017, 38(4): 435-440. DOI:10.3760/cma.j.issn.0254-6450.2017.04.005 |
| [12] |
Sun MJ, Jing ZG, Di DD, et al. Multiple locus variable-number tandem-repeat and single-nucleotide polymorphism-based Brucella typing reveals multiple lineages in Brucella melitensis currently endemic in China[J]. Front Vet Sci, 2017, 4: 215. DOI:10.3389/fvets.2017.00215 |
| [13] |
韩腾伟, 林代华, 刘菁, 等. 福建省2008-2017年人间布鲁氏菌病流行特征及分离株MLVA分型研究[J]. 中国人兽共患病学报, 2019, 35(5): 382-388. Han TW, Lin DH, Liu J, et al. Epidemiological characteristic of human brucellosis and MLVA genotyping for Brucella isolates in Fujian, China, 2008-2017[J]. Chin J Zoonoses, 2019, 35(5): 382-388. |
| [14] |
王月, 陈红, 李沛丽, 等. 贵州省一起人间布鲁氏菌病疫情高危人群调查及分离菌遗传特征分析[J]. 中国媒介生物学及控制杂志, 2016, 27(4): 345-349. Wang Y, Chen H, Li PL, et al. Investigation and genetic characteristic analysis of Brucella strain isolated from high-risk population in a human Brucellosis epidemic in Guizhou province[J]. Chin J Vector Biol Control, 2016, 27(4): 345-349. DOI:10.11853/j.issn.1003.8280.2016.04.008 |
 2020, Vol. 41
2020, Vol. 41