文章信息
- 刘英, 黄荷, 张翠彩, 姚光海, 徐飞, 马青, 王月, 唐光鹏, 王定明, 李世军.
- Liu Ying, Huang He, Zhang Cuicai, Yao Guanghai, Xu Fei, Ma Qing, Wang Yue, Tang Guangpeng, Wang Dingming, Li Shijun
- 贵州省不明原因发热病例钩端螺旋体病原体分离鉴定研究
- Isolation and identification of Leptospira in patients with fever of unknown origin in Guizhou province
- 中华流行病学杂志, 2020, 41(7): 1110-1114
- Chinese Journal of Epidemiology, 2020, 41(7): 1110-1114
- http://dx.doi.org/10.3760/cma.j.cn112338-20191014-00733
-
文章历史
收稿日期: 2019-10-14
2. 中国疾病预防控制中心传染病预防控制所, 北京 102206
2. National Institute for Communicable Disease Prevention and Control, Chinese Center for Disease Control and Prevention, Beijing 102206, China
钩端螺旋体(钩体)病是由致病性钩体感染引起的全球流行的人兽共患传染病[1]。2007-2018年,贵州省共报告249例病例,其中死亡22例,高于全国平均水平,疫情主要集中在黔东南地区[2]。近年来的血清学监测结果显示,人间钩体病例抗体主要为黄疸出血群抗体,贵州省自2009年以来未曾从钩体病例标本分离到钩体,人间钩体病的病原学特征不清楚。多数钩体病初期以发热、乏力等不典型症状为主,实验室血清学确诊周期长,难以与其他感染性疾病鉴别,易造成误诊、漏诊,导致患者失去接受及时有效治疗的机会。本研究以钩体病高发的贵州省黔东南州黎平县为监测点,于2017年在钩体病高发的9-10月对当地主要医疗机构收治的不明原因发热病例进行调查并采集血液和尿液标本进行钩体分离培养,对钩体分离株采用致病性钩体特异性G1/G2-PCR方法,钩体血清群特异性PCR和多位点序列分型(MLST)技术进行鉴定和分型,了解当地高发季节不明原因发热患者中钩体感染情况,分析钩体病原学特征,为钩体病的防控提供病原学依据。
材料与方法1.标本采集:在贵州省黔东南州黎平县于钩体病高发的2017年9-10月对当地主要医疗机构(县人民医院、中潮卫生院、高屯卫生院)收治的不明原因发热病例进行流行病学调查。纳入标准:①体温>38 ℃;②至少具备以下症状体征2项:头痛、乏力、肌肉痛、结膜充血、寒战、黄疸、出血、皮疹、咳嗽、咳血、呼吸困难、脑膜刺激征及肾衰竭相关症状。排除标准:①确诊上呼吸道感染、肺炎、伤寒及其他明确病因(如外伤感染)的发热病例;②拒绝配合的病例;③5周岁以下的患者。采集病例血液和尿液标本用于钩端螺旋体分离培养。
2.钩体分离与培养:无菌操作采集不明原因发热病例血液标本5滴和清洁中段尿液标本1 ml接种于EMJH培养基(Becton Dickinson and Company),置28 ℃通风培养箱(Binder)内培养5~7 d,挑取少量培养液涂于载玻片上采用暗视野显微镜(OLYMPUS)观察是否具有疑似钩体生长,对观察到疑似钩体生长的菌液进行传代并继续培养5~7 d后用于后续鉴定[3]。若未见生长,继续培养至60 d,仍观察不到钩体生长者则判为阴性。
3.钩体菌株DNA提取:对经培养5~7 d的钩体疑似菌株及参考菌株采用细菌DNA提取试剂盒(北京索莱宝生物科技公司)提取其基因组DNA。
4.钩体菌株G1/G2-PCR鉴定:应用致病性钩体特异的G1/G2-PCR方法对从不明原因发热病例全血或尿液标本分离的菌株进行鉴定[4]。采用25 μl PCR反应体系进行PCR扩增,其中含Pre MixTaq(北京索莱宝生物科技公司)12.5 μl,正向引物G1(5′-CTG AAT CGC TGT ATA AAA GT)和反向引物G2(5′- GGA AAA CAA ATG GTC GGA AG)各2 μl,DNA模板1 μl,去离子水7.5 μl。PCR扩增参数为:95 ℃预变性5 min;94 ℃ 60 s、55 ℃ 60 s、72 ℃ 90 s,35个循环;72 ℃延伸10 min,产物采用1.2%琼脂糖凝胶对扩增产物进行电泳检测,根据扩增条带判断分离菌株是否为致病性钩体菌株。
5.钩体菌株血清群PCR鉴定:参照Cheng等[5]建立的黄疸出血群、赛罗群、犬群、秋季群、流感伤寒群和七日热群特异PCR鉴定方法对3株致病性钩体菌株进行常见的6个血清群鉴定,同时采用6个钩体血清群对应的参考菌株DNA做阳性对照,去离子水做空白对照,非钩体样本做阴性对照。扩增体系为25 μl,其中含Pre MixTaq 12.5 μl,正反向引物各2 μl,DNA模板1 μl,去离子水7.5 μl,PCR扩增参数为95 ℃预变性2 min,95 ℃ 30 s、退火30 s(退火温度见表 1)、72 ℃ 1 min,30个循环,产物进行电泳检测。
6.钩体菌株MLST分析:参考MLST网站(https://pubmlst.org/leptospira/)推荐的钩体7个管家基因位点(PntA、SucA、PfkB、TpiA、MreA、GluM、CaiB)对3株致病性钩体进行MLST[6]。7个管家基因位点及引物信息见表 2。采用50 μl PCR反应体系:Pre MixTaq 25 μl,正反向引物各2 μl,DNA模板2 μl,去离子水19 μl。PCR扩增参数:94 ℃预变性10 min;94 ℃ 30 s,退火30 s(退火温度见表 2),72 ℃ 60 s共25个循环;72 ℃延伸10 min。PCR产物进行电泳检测。将条带清晰的PCR产物进行双向测序,测得序列采用contig软件进行拼接,拼接完成的序列采用DNAStar的MegAlig软件进行序列截取,将7个管家基因位点序列与MLST共享网站(https://pubmlst.org/leptospira/)上相应等位基因进行比较,获得每株菌的各等位基因位点的序列号,根据7个等位基因的基因谱确定序列型(ST型)。对3株菌及参考菌株的7个管家基因位点数据采用NTsys 2.10e软件进行聚类分析,了解菌株间的聚类关系。
1.钩体菌株分离培养:共采集发热病例血液标本35份,其中的3例病例血液标本出现疑似钩体菌生长阳性率为8.6%;3株疑似菌株分别命名为17BX002、17BX003和17AJX008。同时采集35例发热病例的尿液标本经培养均未观察到疑似钩体生长。
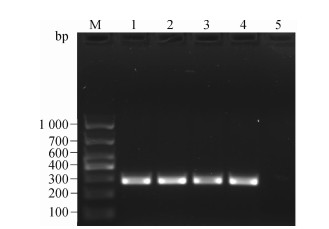
2.钩体G1/G2-PCR鉴定:G1/G2-PCR检测结果显示,3株分离株DNA和阳性对照菌株DNA均出现致病性钩体预期大小的285 bp的目标条带,阴性对照未出现任何DNA条带。见图 1。
|
| 注:M:DNA分子量标准;1~3:分别为菌株17BX002、17BX003和17AJX008;4:阳性对照;5:阴性对照 图 1 贵州省不明原因发热病例致病性钩端螺旋体分离株G1/G2-PCR检测结果 |
3.钩体血清群PCR鉴定:3株钩体菌株中17BX002株经流感伤寒群钩体特异性引物检测出现352 bp的预期扩增片段,而其余的赛罗群、犬群、秋季群和七日热群特异性引物扩增后均未获得扩增条带。17BX003和17AJX008菌株经6个血清群特异引物扩增均未出现预期扩增条带。对应血清群的参考菌株(阳性对照)经扩增均出现了预期扩增条带,而阴性对照均未出现扩增条带(图 2)。

|
| 注:M:DNA分子量标准;1~3:分别为菌株17BX002、17BX003和17AJX008;4:对应血清群钩体菌株阳性对照;5:阴性对照 图 2 贵州省不明原因发热病例钩端螺旋体血清群PCR检测结果 |
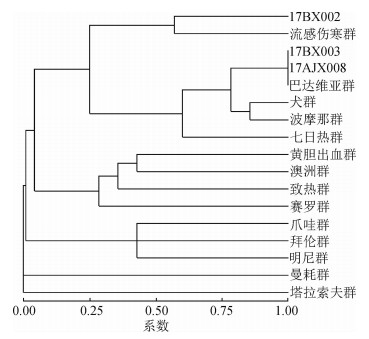
4. MLST分析:3株菌株经钩体7个管家基因位点特异引物扩增,获得了每株菌的等位基因谱(表 3)。经与MLST网站(http://www.mlst.net/)数据库比对显示,17BX002菌株为ST106型,与流感伤寒群参考菌株ST92型存在差异。17BX003和17AJX008菌株为ST96型,与巴达维亚群属同一序列型。MLST聚类分析结果显示,菌株17BX002与流感伤寒群参考菌株属同一分支亲缘关系最近;17BX003和17AJX008与巴达维亚群参考菌株相似性为100%。见图 3。
|
| 图 3 贵州省不明原因发热病例钩端螺旋体菌株及参考菌株多位点序列分型聚类图 |
致病性钩体血清群、型众多,分布广泛,我国已发现18个血清群76个血清型[1]。国外有研究显示在高发地区不明原因发热病例中20%可能是由于钩体感染[7]。钩体病也被WHO称为“被忽视的人畜共患病”,钩体病缺少及时有效的监测系统,可能造成疫情被低估的现状。因此,早期钩体菌株分离培养对揭示钩体人群流行菌株的菌群结构和钩体病防控方案的制定至关重要。
贵州省黎平县35例不明原因发热病例中分离到3株钩体菌株,带菌率为8.6%,提示高发季节该地区存在钩体感染病例。贵州省于1958年首次报道从病原学角度证实了钩体病在人群中的流行,到1993年全省87%的县(市)有钩体病疫情报告,36年共发病80 474例,病死3 458例[1]。2007-2018年,贵州省共报告249例病例,其中死亡22例,近10年贵州省钩体病发病率、死亡率均显著降低。由于钩体病发病症状不典型,基层医疗机构的医疗人员对钩体病缺乏认识,实验室诊断能力有限,贵州省早期钩体病病例并未发现。这类病例作为隐性感染者或轻症感染者在其他诊疗过程后痊愈,人群中钩体发病情况可能被低估。
本研究采用血清群PCR技术对3株致病性钩体菌株进行血清群鉴定,结果显示17BX002株为流感伤寒群,其余的17BX003和17AJX008菌株经该方法检测为阴性,提示这2株菌为该方法检测范围以外的血清群,通过MLST方法检测17BX003和17AJX008菌株与巴达维亚群相似性为100%。近年来贵州省对鼠类动物钩体带菌监测结果显示携带钩体菌群为黄疸出血群[8]。本研究从发热病例标本分离的菌株为流感伤寒和巴达维亚群,与贵州省、江西省、安徽省鼠类动物携带钩体主要菌群为黄疸出血群结果不一致[9-10],并非钩体在我国的主要流行型别。
MLST结果显示17BX002株为ST106型与流感伤寒群56609参考菌株聚类关系最近,查询MLST网站仅有江西省于1941年分离该ST型人源菌株。其他研究2001年浙江省曾在鼠肾中分离出流感伤寒群菌株[11];2017年报道海南省不明原因发热患者调查检出流感伤寒群抗体阳性[12],但病例并未分离培养出该菌。贵州省地处我国西南部云贵高原,有必要进一步了解这些不同地区、不同来源分离的同群菌株之间是否具有同源性。其余2株为ST96型与我国56612钩体参考株型别一致。长沙地区钩体监测猪、牛感染以巴达维亚群为主[13],提示病例的巴达维亚群菌株是否来源于猪、牛。因此,除了鼠类动物外,其他钩体宿主动物如猪、牛、犬等家畜和其他野生动物可能是人间钩体病的重要传染源[13-14],有必要了解除鼠类动物以外的宿主动物钩体带菌情况。本研究结果提示,贵州省人间钩体流行的菌株ST型别少见,应加强人间和动物间钩体病病原学监测。
综上所述,贵州省钩体病疫区不明原因发热病例血液和尿液标本进行钩体分离培养,分离得到3株钩体疑似菌株,经特异性G1/G2-PCR方法鉴定为致病性钩体,进一步的钩体血清群PCR鉴定和MLST分析显示其中1株为流感伤寒群菌株,其余2株为巴达维亚群菌株。本研究提示,高发季节贵州省疫区发热病例中存在钩体感染病例,流感伤寒群和巴达维亚群为本省新发现钩体流行菌群,研究结果将为贵州省钩体病的预防和控制提供科学依据。
利益冲突 所有作者均声明不存在利益冲突
| [1] |
严杰, 戴保民, 余恩庶. 钩端螺旋体病学[M]. 3版. 北京: 人民卫生出版社, 2006: 1-3, 327. Yan J, Dai BM, Yu ES. Leptospirosis[M]. 3rd ed. Beijing: People's Medical Publishing House, 2006: 1-3, 327. |
| [2] |
刘英, 陈峥宏, 李世军, 等. 贵州省2010-2014年钩端螺旋体病流行特征分析[J]. 中国人兽共患病学报, 2016, 32(11): 1034-1038. Liu Y, Chen ZH, Li SJ, et al. Epidemic characteristics of leptospirosis in Guizhou Province from 2010 to 2014[J]. Chin J Zoonoses, 2016, 32(11): 1034-1038. DOI:10.3969/j.issn.1002-2694.2016.011.017 |
| [3] |
Fraga TR, Carvalho E, Isaac L, et al. Leptospira and leptospirosis//Tang YW, Sussman M, Schwartzman J. Molecular medical microbiology[M]. 2nd ed. Melbourne: Elsevier Ltd. All. DOI: 10.1016/B978-0-12-397169-2.00107-4.
|
| [4] |
中华人民共和国卫生部. WS290-2008钩端螺旋体病诊断标准[S].北京: 人民卫生出版社, 2008. Ministry of Health, PRC. WS290-2008 Diagnostic criteria for leptospirosis[S]. Beijing: People's Medical Publishing House, 2008. |
| [5] |
Cheng SC, Yong ZZ, Yi Z, et al. Development of O-antigen gene cluster-specific PCRs for rapid typing six epidemic serogroups of Leptospira in China[J]. BMC Microbiol, 2010, 10: 67. DOI:10.1186/1471-2180-10-67 |
| [6] |
Ahmed N, Devi SM, de Los á Valverde M, et al. Multilocus sequence typing method for identification and genotypic classification of pathogenic Leptospira species[J]. Ann Clin Microbiol Antimicrob, 2006, 5: 28. DOI:10.1186/1476-0711-5-28 |
| [7] |
Colt S, Pavlin BI, Kool JL, et al. Erratum To:Human leptospirosis in the Federated States of Micronesia:a hospital-based febrile illness survey[J]. BMC Infect Dis, 2014, 14: 267. DOI:10.1186/1471-2334-14-186 |
| [8] |
李世军, 张翠彩, 唐光鹏, 等. 2011年贵州省钩端螺旋体病疫区鼠类动物带菌监测与菌株分型[J]. 中华预防医学杂志, 2013, 47(3): 280-281. Li SJ, Zhang CC, Tang GP, et al. Surveillance and strain classification of rodents in leptospirosis epidemic area of Guizhou Province in 2011[J]. Chin J Prev Med, 2013, 47(3): 280-281. DOI:10.3760/cma.j.issn.0253-9624.2013.03.020 |
| [9] |
张翠彩, 张汀兰, 徐建民, 等. 2016-2018年江西省钩端螺旋体病鼠类动物流行病学调查与分离菌株鉴定[J]. 中国人兽共患病学报, 2019, 35(12): 1080-1084. Zhang CC, Zhang TL, Xu JM, et al. Epidemiological survey and identification of pathogenic Leptospira isolated from rats in Jiangxi Province during 2016-2018[J]. Chin J Zoonoses, 2019, 35(12): 1080-1084. DOI:10.3969/j.issn.1002-2694.2019.00.185 |
| [10] |
任军, 顾黎莉, 刘红, 等. 安徽省沿江沿淮地区洪涝灾害前后钩端螺旋体病监测[J]. 中华流行病学杂志, 2005, 26(9): 690-693. Ren J, Gu LL, Liu H, et al. Study on a monitoring program regarding leptospirosis in some fore-and-after flood-affected areas along Large rivers in Anhui province[J]. Chin J Epidemiol, 2005, 26(9): 690-693. DOI:10.3760/j.issn:0254-6450.2005.09.017 |
| [11] |
龚震宇, 姜理平, 王臻. 浙江省2001年钩端螺旋体病监测分析[J]. 疾病监测, 2002, 17(8): 287-289. Gong ZY, Jiang LP, Wang Z. Surveillance of Leptospirosis in Zhejiang Province in 2001[J]. Dis Surveill, 2002, 17(8): 287-289. DOI:10.3784/j.issn.1003-9961.2002.08.006 |
| [12] |
吴捷, 王丹, 王少玲, 等. 海南省不明原因发热病人中钩端螺旋体病的实验检测结果分析[J]. 中国人兽共患病学报, 2017, 33(3): 276-279. Wu J, Wang D, Wang SL, et al. Leptospirosis detection among patients with fever in Hainan Province, China[J]. Chin J Zoonoses, 2017, 33(3): 276-279. DOI:10.3969/j.issn.1002-2694.2017.03.016 |
| [13] |
Thaipadungpanit J, Wuthiekanun V, Chierakul W, et al. A dominant clone of Leptospira interrogans associated with an outbreak of human leptospirosis in Thailand[J]. PLoS Negl Trop Dis, 2007, 1(1): e56. DOI:10.1371/journal.pntd.0000056 |
| [14] |
Han HJ, Wen HL, Liu JW, et al. Pathogenic Leptospira species in insectivorous bats, China, 2015[J]. Emerg Infect Dis, 2018, 24(6): 1123-1126. DOI:10.3201/eid2406.171585 |
 2020, Vol. 41
2020, Vol. 41





