文章信息
- 吴雨霏, 沈智勇, 杨新宇, 李荣健, 梁能秀, 蓝光华.
- Wu Yufei, Shen Zhiyong, Yang Xinyu, Li Rongjian, Liang Nengxiu, Lan Guanghua
- 广西壮族自治区男男性行为者HIV非职业暴露后预防效果分析
- Non-occupational post-exposure prophylaxis in men who have sex with men in Guangxi Zhuang Autonomous Region
- 中华流行病学杂志, 2020, 41(7): 1086-1091
- Chinese Journal of Epidemiology, 2020, 41(7): 1086-1091
- http://dx.doi.org/10.3760/cma.j.cn112338-20191008-00719
-
文章历史
收稿日期: 2019-10-08
2. 美国疾病预防控制中心全球艾滋病防治合作项目中国办事处, 北京 100600
2. U. S. CDC Global AIDS Program, China Office, Beijing 100600, China
艾滋病已成为全球严重的公共卫生问题和社会问题。自2010-2015年,全球艾滋病治疗人数从750万增加到1 700万,艾滋病病死率下降25%[1]。从2010-2018年,尽管全球艾滋病新感染人数已从210万下降至170万,减少16%[2],但中国每年报告的HIV/AIDS中男男同性性传播所占比例不断上升,从2006年的2.5%上升至2015年的28.3%[3];艾滋病哨点监测数据显示,中国MSM的HIV感染率一直呈上升趋势,从2006年的3.0%上升到2015年的8.0%[3]。非职业暴露后预防(non-occupational post-exposure prophylaxis,nPEP)是1种降低高危人群感染HIV风险的策略,指发生HIV暴露后72 h内开始服用抗病毒药物并持续28 d[4-6],以阻断HIV感染。近年有关MSM的HIV nPEP日益受到国际关注,而我国MSM高危人群的nPEP需求与相关医疗支持不足之间的矛盾尚未得到充分解决[7]。Mitchell等[8]研究发现,HIV阳性者的性伴中有73%愿意使用nPEP;2016年4-10月对广西壮族自治区(广西)部分地区MSM进行nPEP服务需求和态度等问题的调查发现,MSM对nPEP服务存在一定的需求[9]。为应对艾滋病疫情蔓延,在中美艾滋病防治合作项目等的支持下,在南宁、柳州市MSM中使用抗病毒药物进行nPEP服务试点研究,评价暴露后预防效果,为nPEP策略在中国推广提供依据。
对象与方法1.研究对象:以常住南宁、柳州市≥18周岁的发生HIV非职业暴露并服用抗病毒药物的MSM为研究对象。纳入标准:①未使用安全套的性行为(包括同性性行为和异性性行为、肛交、口交并射精);②与HIV感染者共用针具吸毒;③被血液、精液、阴道分泌液、直肠液、带血的唾液、创伤渗出液等液体喷溅到眼睛、鼻子、口腔,或黏膜破损处。排除标准:①暴露者已经感染HIV;②暴露源为HIV抗体阴性并排除窗口期;③暴露于HIV感染风险小的体液(如不含血的唾液、尿液及汗液等);④暴露时间超过72 h。研究开始前,所有参加者签署了知情同意书。本研究获得广西伦理审查委员会的批准(批件号:GW-2017-0012)。
2.研究方法:2017年9月至2019年3月,以MSM社会组织南宁市益同行健康服务中心、柳州市虹影工作组和CDC为工作平台,通过线上(微信公众号、微博、Blued、QQ群)和线下(卡片、海报、手册)宣传nPEP知识,招募研究对象。建立社会组织-CDC/医院-药店“三位一体”的服务合作模式,其中CDC和医院抗病毒治疗门诊医生组织MSM同伴教育员统一培训,解读实施方案;经过培训的同伴教育员对发生HIV非职业暴露后求询的MSM进行初步风险评估,包括利用第四代HIV抗体检测试剂检测HIV抗原抗体[10]。对符合nPEP用药的目标人群陪同转介至CDC艾滋病关爱门诊或医院抗病毒治疗门诊做进一步风险评估和血常规、肝肾功能、乙肝五项和HIV抗体检测。医生为符合nPEP条件者开处方及检验项目。医院药房或商业药店凭处方卖药给目标人群。在整个nPEP服务中,MSM社会组织实行“首询负责制”原则,即尽可能让第1个接待目标人群的咨询员“一对一”陪同转介,提供药物依从性教育和心理支持,督促随访检测,登记病历信息等。
3.用药方案:研究对象承担药费。医生向研究对象解释现有用药方案,研究对象根据自身经济能力选择其中1个方案。为保证预防效果,用药时机为暴露后越早服用越好,原则上不超过暴露后72 h,连续服药28 d[11-12]。①替诺福韦(TDF)300 mg+恩曲他滨(FTC)200 mg复合片剂,每次1片,每日1次+拉替拉韦片(RAL)400 mg,每次1片,每日2次;3 960元1个疗程。②替诺福韦(TDF)300 mg+恩曲他滨(FTC)200 mg复合片剂,每次1片,每日1次+多替拉韦(DTG)50 mg,每次1片,每日1次;3 960元1个疗程。③阿巴卡韦(ABC)50 mg+拉米夫定(3TC)600 mg +多替拉韦(DTG)300 mg复合片剂,每次1片,每日1次;2 880元1个疗程。④根据当地药物可及性,参照WHO等国际相关指南的其他用药组合,如替诺福韦(TDF)+恩曲他滨(FTC)复合片剂或艾考恩丙替片(E/C/F/TAF),每次1片,每日1次;分别为1 980和2 980元一个疗程。
4.相关检测及随访:①基线检测:血常规和肝肾功能、乙肝五项、HIV抗体;②服药4~6周后检测:血常规和肝肾功能、HIV抗体;③服药3个月后检测:HIV抗体;④其他检测:在随访过程中发现HIV阳性,按当地发现阳性病例常规流程,进行确证、CD4+T淋巴细胞计数及病毒载量检测,并转诊接受抗病毒治疗。研究对象出示血常规、肝肾功能相关检测报告单,可领取100元交通费补助。
5.服药满28 d的确定:通过随访时研究对象自我报告或电话询问来确定是否连续服药满28 d。
6.质量控制:项目工作人员定期到MSM社会组织开展技术指导并核查数据质量,对存在问题及时进行纠正。
7.资料收集与分析:设计nPEP病历记录表,登记研究对象的社会人口学信息、药物使用(含用药方案及28 d服药情况)、报告的药物副作用和随访检测情况。采用EpiData 3.1软件建立“nPEP病历记录表”数据库并进行数据录入,核对无误后运用SPSS 23.0软件进行统计学分析,以P<0.05为差异有统计学意义。对资料进行描述性统计。
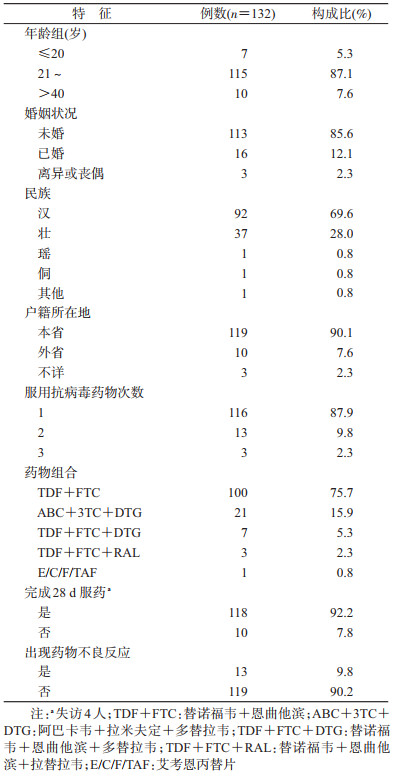
结果1.基本情况:2017年9月至2019年3月,在广西南宁和柳州市共有213名MSM咨询nPEP用药,其中159人符合标准,接受nPEP用药154人、5人因承担不起药费放弃治疗;54人不符合纳入标准(含29人经评估无风险、10人暴露时间超过72 h、11人只咨询不接受检测、3人HIV抗体检测结果阳性、1人拒绝参加)。入组nPEP满28 d及以上132人,主要暴露方式为性接触,年龄中位数为29岁,其中最小的18岁、最大的56岁;年龄段以21~40岁为主,占总数87.1%(115/132);未婚占总数的85.6%(113/132);民族以汉族为主,占69.6%(92/132);户籍属于广西的占90.1%(119/132)(表 1)。
2.药物使用情况:入组nPEP满28 d的132名参加者中,87.9%(116/132)为第1次接受nPEP用药,9.8%(13/132)为第2次使用,2.3%(3/132)为第3次使用;75.7%(100/132)使用TDF+FTC,15.9%(21/132)使用ABC+3TC+DTG,5.3%(7/132)使用TDF+FTC+DTG,2.3%(3/132)使用TDF+FTC+RAL。92.2%(118/128)连续服药满28 d;10.6%(14/132)未连续或无法证实服药满28 d,包括4.5%(6/132)因后来暴露源经检测证实未感染HIV且已排除窗口期而停药、3.0%(4/132)因失访无法证实是否完成服药、1.5%(2/132)由于工作原因不愿继续服药、0.8%(1/132)因副作用停药、0.8%(1/132)购买不起整瓶药。服药者中有9.8%(13/132)报告有不同程度的药物副作用,症状主要表现为恶心、呕吐、头晕、困倦和无法集中注意力等(表 1)。
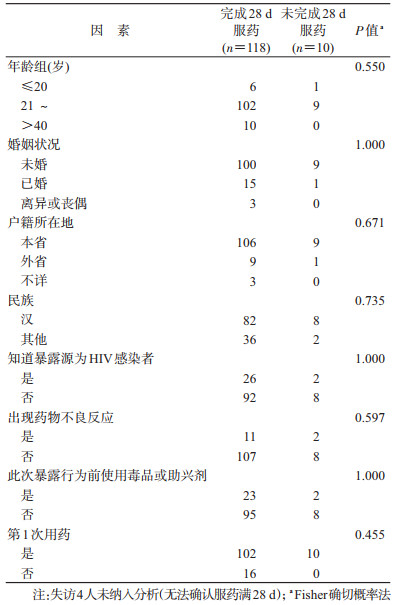
3.服药满28 d的影响因素分析:采用Fisher精确检验法,没有发现完成服药者和未完成服药者在年龄、婚姻状况、户籍所在地、民族、是否知晓暴露源为HIV感染者、是否出现药物不良反应、暴露行为前是否使用毒品或助兴剂以及是否第1次服药的差异有统计学意义(P<0.05)(表 2)。
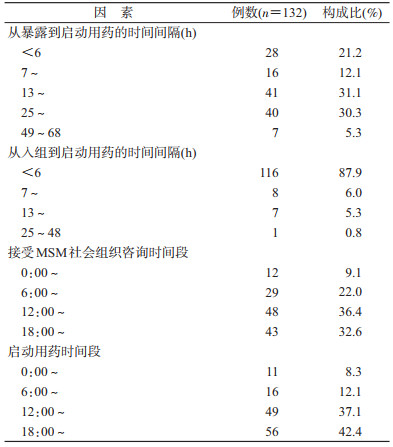
4.咨询及启动用药时间:入组满28 d的132名研究对象中,分别有21.2%(28/132)、12.1%(16/132)、31.1%(41/132)和30.3%(40/132)于暴露后的6 h内、7~、13~和25~48 h启动服药;仅有5.3%(7/132)于暴露后49~68 h启动服药。从入组到启动用药的时间间隔来看,87.9%(116/132)于入组后的6 h内启动服药。分别有36.4%(48/132)、32.6%(43/132)和22.0%(29/132)暴露者在12:00~前、18:00~前和6:00~前来MSM社会组织求询;也有9.1%(12/132)在0:00~前求询。从启动服药的时间来看,分别有42.4%(56/132)、37.1%(49/132)、12.1%(16/132)在18:00~、12:00~和6:00~的时间段启动用药;而8.3%(11/132)则在0:00~的时间段开始服药(表 3)。
5.随访检测情况:132名研究对象在服药前有47.7%(63/132)进行了HBV检测,发现6人为HBsAg阳性,并跟踪随访3个月,未发现因药物导致肝损伤问题;75.0%(99/132)进行了基线血常规及血生化检测。服药4~6周后有44.7%(59/132)进行了血常规及血生化检测,未发现指标异常者;85.6%(113/132)在暴露后4~6周进行了HIV抗体检测,未发现阳转者。73.5%(97/132)在暴露后3个月随访进行了HIV抗体检测,其中1人出现HIV抗体阳转,调查发现此人于服药两周后因性伴检测结果阴性而停药并在暴露后6周检测HIV抗体阴性,之后再次发生高危行为未进行药物阻断。此外,单从连续服药满28 d来看,94.1%(111/118)在暴露后4~6周接受HIV抗体检测、75.4%(89/118)在暴露后3个月接受检测,结果均为阴性。
讨论MSM由于存在多性伴和无保护性肛交行为而成为感染HIV的高危人群,即使在发生性行为时坚持使用安全套还可能出现安全套滑脱和破裂等情况,因而运用生物医学预防进行暴露后阻断显得十分必要。本研究中,连续服药满28 d的参加者中,分别有94.1%、75.4%于暴露后4~6周和3个月的HIV随访检测阴性,这与Chomchey等[13]的研究结果相类似;值得注意的是,其中26人知晓暴露源为HIV感染者,除5人在暴露后3个月后未接受HIV抗体检测外,其余21人复检HIV抗体均为阴性。仅1人出现HIV抗体阳转但不归咎于nPEP失败。WHO对全球15个国家nPEP研究进行Meta分析发现,在总共2 209名nPEP使用者中,有19人发生HIV抗体阳转,只有1人归咎于nPEP失败,其他18人或没有完成28 d治疗或在3个月随访期间存在高危行为[14]。Mitchell等[8]的研究结果也表明,nPEP具有可能减少MSM人群感染HIV的风险,提示暴露后预防用药可降低HIV感染风险。
本次研究服药完成率为92.2%,高于McDougal等[6]研究结果(5%);而Ford等[15]的Meta分析显示,MSM作为nPEP的主要对象,完成率仅为67.3%。这可能与我们的前期宣传分不开,广西CDC通过微信公众号、广西防艾宣传管理平台发布多篇文章,普及nPEP知识;南宁市益同行健康服务中心通过其微信公众号(wwwnnchcn)设置nPEP专栏,开展社区宣传与倡导;柳州市虹影工作组通过QQ群、微博、Blued,采用图片、文字、视频、动画等形式介绍和宣传nPEP知识;制作nPEP宣传材料,在南宁和柳州市CDC艾滋病自愿咨询检测点、医疗机构抗病毒治疗点、MSM社会组织、男同酒吧等地发放,促使研究对象对nPEP用药有正确的认识和强烈的使用要求。此外,MSM社会组织“一对一”跟踪随访服务也可能是良好用药依从性的关键因素之一。
研究结果发现,分别有9.8%、2.3%的人第2次和第3次使用nPEP。根据WHO指南中所提及的,对于可能反复暴露于HIV感染风险而多次使用nPEP的人群,应建议改用暴露前预防用药(PrEP),这样可以增加预防效果[16]。nPEP使用者中有9.8%出现药物副作用,主要表现为头疼、乏力和胃肠道反应等轻微症状,在及时有效地进行对症处理后得到较好恢复,无严重不良事件发生;仅1人出现不良反应而停药,这些结果与其他研究相符[17-19],并提示这是药物常见的副作用。有研究表明,抗病毒药物的副作用会导致治疗中断或不依从性的问题,从而限制整个nPEP的疗效[15]。
所有参加者中,绝大部分在暴露后的48 h内启动用药,无一例因风险评估等环节妨碍了服药时间;大部分人在入组后的6 h内启动用药。值得一提的是,分别有32.6%、9.1%的人于18:00~和0:00~的时间段来MSM社会组织求询;42.4%、8.3%分别于18:00~和0:00~的时间段启动用药。这提示,MSM可能常在夜间发生高危行为,社会组织工作时间的灵活性恰好满足了目标人群对nPEP服务的需求。“三位一体”模式下社会组织的主导性作用,反映出委托MSM社会组织开展nPEP,目标人群或许更容易接受,因为同伴教育员与目标人群有着天然的联系,能与他们建立起更好的信任关系。这可能是CDC和医疗机构难以达到的地方。
由于nPEP所用药物对HBV有抑制作用,对服药者需进行肝肾功能及HBV检测;对HBsAg阳性患者在完成预防用药后,需密切关注其有无HBV复燃造成的急性肝损伤问题[20-21],提供血常规、肝肾功能相关检测报告单可获取100元交通费补助,但可能因服药前咨询没有强调基线血生化和HBV检测的重要性,导致仅有75.0%(99/132)的药物使用者接受基线血生化检测、47.7%(63/132)接受基线HBV检测;而在服药4~6周后,仅有44.7%(59/132)接受了血生化随访。虽然本研究没有发现因服药导致的肝肾功能损伤问题,但并不意味着无风险存在。这也提示中国nPEP指南制定者在未来指南制定时应对检测内容予以规范,强调检测的重要性。
本研究样本量少,也许代表性不够充分,但还是能够反映研究结果的价值。研究结束时,还有部分研究对象服药未满28 d,未能追踪到后续的结果,这也是影响样本量的一个因素。其次,目前预防药物价格昂贵,对部分人特别是学生群体而言是一个较大的经济负担,本研究就有5人因承担不起药费放弃治疗;而参加者中75.7%选择服用价格相对低廉的“TDF+FTC复合片剂”(1 980元/瓶)。因此,建议探索包括药物价格谈判、医保覆盖、药品国产化等多种途径力求将药价降至更多使用者可接受的范围。
综上所述,MSM使用抗病毒药物进行nPEP可以降低HIV感染的风险,一定程度上减少艾滋病的新发感染数,为我国积极推广nPEP服务提供科学依据。同时应发挥社会组织的优势,加强与MSM社会组织合作,继续强化nPEP宣传,促进MSM暴露后及时获取规范化nPEP服务,确保良好的服药依从性并按时随访检测。
利益冲突 所有作者均声明不存在利益冲突
| [1] |
W HO. Guideline on when to start antiretroviral therapy and on pre-exposure prophylaxis for HIV[M]. Geneva: World Health Organization, 2015.
|
| [2] |
UNAIDS. Global HIV & AIDS statistics-2019 fact sheet[EB/OL]. (2019-09-01)[2019-10-01]. https://www.unaids.org/en/resources/fact-sheet.
|
| [3] |
中国疾病预防控制中心性病艾滋病预防控制中心.男男性行为人群预防艾滋病干预工作指南(2016)[EB/OL].(2016-09-13)[2019-09-30]. http://www.chinacdc.cn/jkzt/crb/gjfd/zl/azb/jszl_2219/201609/t20160922_134279.html. National Center for AIDS/STD Control and Prevention, Chinese Center for Disease Control and Prevention. Guideline for HIV/AIDS Interventions for Men who Have Sex with Men (2016)[EB/OL].(2016-09-13)[2019-09-30]. http://www.chinacdc.cn/jkzt/crb/gjfd/zl/azb/jszl_2219/201609/t20160922_134279.html. |
| [4] |
Koyama A, Middlebrooks L, Bullock A. Updates on HIV non-occupational postexposure prophylaxis[J]. Curr Opin Pediatr, 2019, 31(4): 454-461. DOI:10.1097/MOP.0000000000000775 |
| [5] |
Kuhar DT, Henderson DK, Struble KA, et al. Updated US public health service guidelines for the management of occupational exposures to human immunodeficiency virus and recommendations for postexposure prophylaxis[J]. Infect Control Hosp Epidemiol, 2013, 34(9): 875-892. DOI:10.1086/672271 |
| [6] |
McDougal SJ, Alexander J, Dhanireddy S, et al. Non-occupational post-exposure prophylaxis for HIV:10-year retrospective analysis in Seattle, Washington[J]. PLoS One, 2014, 9(8): e105030. DOI:10.1371/journal.pone.0105030 |
| [7] |
陆天意, 毛翔, 彭二磊, 等. 2000-2017年国际HIV暴露后预防研究热点的文献计量分析[J]. 中华流行病学杂志, 2018, 39(11): 1501-1506. Lu TY, Mao X, Peng EL, et al. Bibliometric analysis on research hotspots on HIV post-exposure prophylaxis related articles in the world, 2000-2017[J]. Chin J Epidemiol, 2018, 39(11): 1501-1506. DOI:10.3760/cma.j.issn.0254-6450.2018.11.016 |
| [8] |
Mitchell JW, Sophus AI, Petroll AE. HIV-negative partnered men's willingness to use non-occupational post-exposure prophylaxis and associated factors in a U.S. sample of HIV-negative and HIV-discordant male couples[J]. LGBT Health, 20116, 3(2): 146-152. DOI:10.1089/lgbt.2015.0065 |
| [9] |
曾梓, 黎芝, 蓝光华, 等. 广西壮族自治区男男性行为者对艾滋病非职业暴露后预防服务需求的定性研究[J]. 中华疾病控制杂志, 2018, 22(12): 1274-1277. Zeng Z, Li Z, Lan GH, et al. Qualitative study on the demand for non-occupational post-exposure prophylaxis among MSM in Guangxi Zhuang Autonomous Region[J]. Chin J Dis Control Prev, 2018, 22(12): 1274-1277. DOI:10.16462/j.cnki.zhjbkz.2018.12.017 |
| [10] |
Tan DHS, Hull MW, Yoong D, et al. Canadian guideline on HIV pre-exposure prophylaxis and non-occupational postexposure prophylaxis[J]. Canad Med Assoc J, 2017, 189(47): E1448-1458. DOI:10.1503/cmaj.170494 |
| [11] |
齐唐凯, 卢洪洲. 加拿大人免疫缺陷病毒暴露前预防和非职业性暴露后预防指南解读[J]. 世界临床药物, 2018, 39(11): 727-731. Qi TK, Lu HZ. Interpretation for Canadian guideline on HIV pre-exposure prophylaxis and non-occupational postexposure prophylaxis[J]. World Clin Drugs, 2018, 39(11): 727-731. DOI:10.13683/j.wph.2018.11.002 |
| [12] |
O'Donnell S, Tan DHS, Hull MW. New Canadian guideline provides evidence-based approach to non-occupational HIV prophylaxis[J]. Canad J Emerg Med, 2019, 21(1): 21-25. DOI:10.1017/cem.2018.462 |
| [13] |
Chomchey N, Woratanarat T, Hiransuthikul N, et al. Factors associated with intention to take non-occupational HIV post-exposure prophylaxis among Thai men who have sex with men[J]. J Virus Erad, 2017, 3(3): 128-139. |
| [14] |
World Health Organization. Joint WHO/ILO guidelines on post-exposure prophylaxis (PEP) to prevent HIV infection[R]. 2007. http://www.who.int/hiv/pub/guidelines/PEP/en/index.html.
|
| [15] |
Ford N, Irvine C, Shubber Z, et al. Adherence to HIV postexposure prophylaxis:a systematic review and Meta-analysis[J]. AIDS, 2014, 28(18): 2721-2727. DOI:10.1097/QAD.0000000000000505 |
| [16] |
Jain S, Krakower DS, Mayer KH. The transition from postexposure prophylaxis to preexposure prophylaxis:an emerging opportunity for biobehavioral HIV prevention[J]. Clin Infect Dis, 2015, 60 Suppl 3: S200-204. DOI:10.1093/cid/civ094 |
| [17] |
Chauveau M, Raffi F, Allavena C. Tenofovir DF/emtricitabine/rilpivirine as HIV post-exposure prophylaxis:results from a multicentre prospective study-authors' response[J]. J Antimicrob Chemother, 2019, 74(11): 3403-3404. DOI:10.1093/jac/dky547 |
| [18] |
Kowalska JD, Pietraszkiewicz E, Firląg-Burkacka E, et al. Suspected unexpected and other adverse reactions to antiretroviral drugs used as post-exposure prophylaxis of HIV infection-five-year experience from clinical practice[J]. Arch Med Sci, 2018, 14(3): 547-553. DOI:10.5114/aoms.2016.59701 |
| [19] |
Li HC, Cheng YP, Yang CJ. Safety, tolerability and effectiveness of HIV non-occupational prophylaxis in Taiwan[J]. J Int AIDS Soc, 2014, 17(4 Suppl 3): 19736. DOI:10.7448/IAS.17.4.19736 |
| [20] |
Ford N, Mayer KH, World Health Organization Postexposure Prophylaxis Guideline Development Group. World Health Organization guidelines on postexposure prophylaxis for HIV:recommendations for a public health approach[J]. Clin Infect Dis, 2015, 60 Suppl 3: S161-164. DOI:10.1093/cid/civ068 |
| [21] |
Jain S, Mayer KH. Practical guidance for non-occupational postexposure prophylaxis to prevent HIV infection:an editorial review[J]. AIDS, 2014, 28(11): 1545-1554. DOI:10.1097/QAD.0000000000000301 |
 2020, Vol. 41
2020, Vol. 41