文章信息
- 王天雷, 牟育彤, 阚慧, 李亚欣, 范伟, 戴江红, 郑英杰.
- Wang Tianlei, Mou Yutong, Kan Hui, Li Yaxin, Fan Wei, Dai Jianghong, Zheng Yingjie
- 基于大自然时间轴的测量时序分类法
- A new classification of measured temporalities: based on the time axis in nature
- 中华流行病学杂志, 2020, 41(5): 782-787
- Chinese Journal of Epidemiology, 2020, 41(5): 782-787
- http://dx.doi.org/10.3760/cma.j.cn112338-20190929-00711
-
文章历史
收稿日期: 2019-09-29
2. 新疆医科大学公共卫生学院流行病与卫生统计学教研室, 乌鲁木齐 830011
2. Department of Epidemiology and Biostatistics, School of Public Health, Xinjiang Medical University, Urumqi 830011, China
因果推断研究中,对代表因和果的变量进行测量必不可少。观察和实验是其基本方法,前者观察事件的自然发生,而后者通过干预以改变产生结局的原因[1]。研究者一般根据现实情况决定因变量和果变量之间的测量顺序,即测量时序:如由“因”及“果”是指真实因已存在并可优先测量“因”,之后去测量“果”的过程;而由“果”及“因”是指真实果已存在并可优先测量“果”,之后去测量“因”的过程。习惯上,将这两个测量顺序分别称为前瞻性(prospective)和回顾性(retrospective),由William Farr于1851年首先提出[2]。
这种提法存在着问题或歧义:①真实的因果时序是唯一和单向性,而测量时序则是多向和非唯一的;同时,亦存在着“因”和“果”同时测量的情形,如记录联结研究或时点横断面研究;由“果”及“因”的提法违背了因果时序的单向性。②在因果推断研究中,无效假设通常是暴露与结局之间为零效应,研究获得的非零关联将推翻无效假设,从而得出暴露和结局之间可能存在着效应。因此,由“因”及“果”的提法容易造成“暴露和结局已存在因果律”的误解。③这种提法容易混淆对研究设计的认识:如病例对照研究和历史性队列研究到底有何不同?这是学生们最容易混淆的问题。④1990年前后,在流行病学界,研究者们围绕“时序(或方向性)对研究设计的分类是否有用”这一问题进行讨论:支持者们Kramer、Feinstein和Abramsom等[3-8],认为时序对偏倚来源和病因推断是重要的;而反对者们Greenland、Miettinen等[9-14],认为时序与设计类型无关。究其原因,两种观点对立的根源是其时序立场不同,这正如Greenland和Morgenstern[10]指出的“到底什么是方向性”这一问题未能得以明确。因果律是真实因以单向时序影响真实果的规律,这是大自然客观存在的、不以人的意志为转移。测量不能改变大自然因果律的两个基本特征:时间序和因果序,但测量有助于实现对这种因果律的认识。
基于时序的确切含义未能明确,本文从因果思维的角度,围绕观察和实验中真实因、真实果及其对应的测量因和测量果这4个变量之间的时序进行研究,以明确时序的含义、分类及其特征。
2、真实因、真实果、测量因与测量果的关系在观察的情况下,真实因(以变量A表示)或果(Y)的发生或存在,是其被测量的前提,此处以测量因(A*)或测量果(Y*)分别来表示A和Y的测量版。一个变量的测量值通常决定于其真实值和测量系统[15],除非采用随机方法对该变量进行测量,如以抛硬币后的正面或反面来诊断个体是否患有癌症。
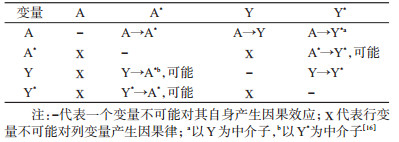
若A→Y因果律(以“→”代表A对Y产生效应)的确存在,则其因果序和时间明确。此外,这两对4个变量(A与A*、Y与Y*)之间还有6种可能的因果序和时间序(表 1),其中A→A*、Y→Y*、A→Y*一般来说成立(随机测量情形除外),因此这3种关系的因果序和时间序同样明确;而Y→A*、Y*→A*、A*→Y*的关系则不明确[16]。值得注意的是,A*一般不能直接影响Y*,而是通过间接的形式,如日光浴(A*)导致皮肤晒伤(中间变量),而后者更可能就诊,这有助于皮肤癌的诊断(Y*)率提高。同样地,Y*通常间接影响着A*,如在孕期暴露与先天性畸形间的关系研究中,是婴儿畸形已被诊断(Y*)并为孕妇所知晓(中间变量),从而影响了孕妇过高或过低地回忆其过去的暴露情况(A*),即Y*→中间变量→A*,或称之为“反向因果关系”。
实际研究中,仅A*和Y*是已知的,明确这二者的关系显得尤为重要。A*-Y*之间的时间序和因果序不确定情况可有3种(表 1):在时间序上,这两者间可出现3种情形,①A*先于Y*,②Y*先于A*,③A*与Y*的同时性;由此对应的因果序也分别有3种情形,即①A*可能影响Y*,②Y*可能影响A*,③A*与Y*间无因果序。
3、因果时序与测量时序——A和Y从未被测量过在观察的情况下,若A→Y因果律存在,依据A和Y的发生时间,郑英杰等[17]曾将大自然的时间轴(自左向右)划分为3个时域和2个时点。见图 1。A只能在第2时域(包括第2时点)和第3时域得以测量,而Y只能在第3时域(不包括第2时点)得以测量。因此,A和Y的发生时间位置从理论上锚定了因果推断实际研究的可能时间范围,即因果推断只能在第3时域得以实现。因果律的时间序(或因果时序,Causal Temporality,CT)是唯一的,即因先果后,或A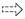
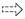
|
| 注:A和A*分别代表真实因及测量因;Y和Y*分别代表真实果及测量果;I*代表实验中测量的干预措施(此时与其对应的真实干预变量为A,A=I);黑色长条状单箭头代表着大自然时间轴;按照A和Y的发生时间划分时间轴为2个时点和3个时域;含黑点长条代表A或Y可被测量的时间;含蓝点长条代表I*可被测量的时间范围;实线单箭头联结A和Y或I*和A代表二者间存在因果律;双虚线单箭头代表箭头两端变量的测量时序(MT),其上标识相应的MT类型;双虚线无箭头竖条代表两端变量不存在方向的MT,其右侧标识MT类型;以数字标识每种MT。蓝色字母I*、蓝色单箭头、I*→A代表着实验中的干预,此时A加蓝色框代表着人群的限制,如预防性疫苗干预措施针对的仅是易感人群,而治疗性药物针对的仅是患者。去除蓝色部分的图形即观察 图 1 真实因(A)和真实果(Y)及其测量版或干预版(首次)之间的关系示意图 |
假定A和Y从未曾被测量过,基于A和Y的发生时间及其与时域(点)的关系(图 1),可以得出在观察的情况下A*与Y*的测量时序,或称之为观察性时序,有以下情形:
(1)第1种:跨第2和3时域纵向时序(图 1①):
A*测量发生于第2时域,而Y*只能在第3时域得以测量,为跨时域测量。因此,A*与Y*间的时间差提供了前瞻性追踪人群、观察结局出现(或测量)的机会,本文将其命名为跨第2和3时域纵向时序,即A*
另外3种时序是A和Y均已发生的情形(图 1②、③和④),研究者已无可能对人群进行追踪。A*和Y*的测量只能在第3时域进行,可被视为同时域测量,对其测量意味着历史的重建、回溯或“考古”。从这点看来,针对A*和Y*的测量,谁先谁后没有什么区别;然而,A*和Y*能否得到正确的测量,则显得更为重要。虽然这样,考虑到实际研究的可行性和便利性,有3种测量时序可供选择,即先测量A*(纵向)、先测量Y*(逆纵向)和同时测量A*与Y*(横向)。对应于这3种情形,相应地有3种测量时序:即,同时域纵向时序、同时域逆纵向时序和同时域横向时序。
(2)第2种:同时域纵向时序(图 1②):
类似于第1种时序,第2种时序亦为纵向,测量时序与因果时序的方向也是一致的;然而二者不同的是,第2种时序中A和Y已然发生,A*和Y*的测量同时在第3时域进行,即同时域的测量,研究者已经失去对人群进行追踪观察的机会。因此,本文将其命名为同时域纵向时序。例如,某社区普及接种疫苗一段时间后,想要知道该疫苗的短期副作用,但当时疫苗接种和副作用发生情况均没有记录,因此,需首先获知该社区中哪些人接种过疫苗?然后,再调查接种者和未接种者是否出现副作用。通常,进行因果推断研究时,对因和果及其测量已有所了解,因或果的发生或出现之后,研究者很快对因(或果)进行测量。在因和果均已发生后,过了一段时间才想起对其进行测量,这种测量策略在实践中较少被采纳。
(3)第3种:同时域逆纵向时序(图 1③):
第3种时序中,A*测量晚于Y*,此为同时域逆纵向时序。例如,职业研究中,发现某个职业人群出现高频率的癌症,此时需要调查其职业的暴露信息。而这种暴露信息并没有历史记录可以参考,因此,在该职业人群癌症测量已经完成后,研究者再去测量其暴露信息。
(4)第4种:同时域横向时序(图 1④):
第4种时序中,A*和Y*同时测量(横向或截面测量)而无测量时间差,即同时域横向时序。如在某个时间点,同时进行人群的体重和高血压的测量,以进行二者间关系的研究。
(5)第5种:跨第1和3时域纵向时序(图 1⑤),或实验性时序:
与观察不同,实验以干预为特征。干预意味着改变,即实验通过干预措施改变人群中产生结局的原因,进而间接地影响结局的发生,如疫苗接种提高了人群对疾病的免疫力(或降低了易感性),从而相应地降低了疾病的发生风险。这种干预措施是自然或人为预先设置[18];换句话说,其测量值(I*,代表对A的测量,以示与观察中的A*区别;此处I=A)是已知的,可视为“首次测量”,并出现在大自然时间轴的第1时域。如临床试验中,评估药物按照一定的分配机制给予研究对象,药物及其剂量、施加于研究对象的时机及治疗程序一般明确;然而研究对象真实地接受了多少药物(A)则是未知或未测量的,因此,I*(测量值变量)通过中介子A(真实值变量)可能影响着Y,进而影响着Y*,即I*→A→Y→Y*[15]。因此,I*-Y*间亦表现为跨时域纵向时序;但与观察中跨越第2和3时域的时序不同,实验中这种时序跨越第1和3时域。
4、因果时序与测量时序——A和/或Y曾被测量过在观察的情况下,A*和/或Y*曾经不经意地被测量过,如婴儿体重,从其出生时已被接生医生记录在出生证上;或妊娠期糖尿病,医生已经做出诊断并登记在出院记录上。重新获取这些已测量的结果,为再测量或重复测量。测量意味着变量值的空间位置转移[19],如婴儿体重,首次测量时,变量值从婴儿转移到出生记录;再次测量时,变量值从出生记录转移到新的记录工具,如调查表。
在“因果时序与测量时序——A和Y从未被测量过”论述的基础上,若进行观察,依据A和/或Y曾被首次测量并进行再次测量的情况,可有以下3种情形:
(1)仅真实因(A)已被测量,真实果未知,测果:A已被测量,意味着A已发生,则A*可出现于第2时域后任何时间。而Y何时测量,取决于其是否已发生。若A再次被测量时Y尚未发生,Y*只能在未来获得,即A*和Y*的测量为观察性跨时域测量;若A再次被测量时Y已发生,则A*-Y*间表现为观察性同时域时序。因此,A*-Y*间仍然可能具有上述4种观察性测量时序。
(2)仅真实果(Y)已被测量,真实因未知,测因:Y已被测量,意味着因果效应在人群中的作用已经完成。此时对A*的测量相当于A的历史重建,只能在第3时域进行,A*和Y*属于同时域测量。因此,A*-Y*间可能有上述3种观察性同时域时序。
(3)真实因和果均已被测量过,再测量/空间位置改变:A和Y均已测量,意味着图 1中的过程已经完成,已经获得了A*和Y*。在此基础上,重新获取A*和Y*,均发生在第3时域。因此,A*-Y*间可能有3种观察性同时域时序。
(4)3次及以上测量:A和/或Y可出现首次测量、二次测量或多次测量。按照“真实因和果均已被测量过,再测量/空间位置改变”中的思想,3次及以上测量时,A*-Y*间可有3种观察性同时域时序。
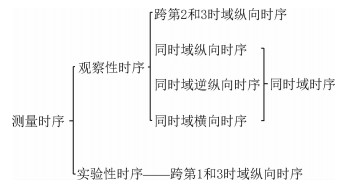
以上内容阐述了在观察的情形下再次测量时可能出现的测量时序。实验法中,首次测量表现为跨越第1和3时域的纵向时序。与观察的情形类似,Y只能在第3时域测量,而I*的再测量理论上可跨越第1、2和3时域,因此,I*的再测量取决于其测量时机与A之间的关系:若I*的再测量在时序上先于A,即干预措施施加于研究对象后,在其真实值效应(I*对A的效应)未出现之前再次进行测量,则同样地表现为上述第5种时序(实验性时序),这种情形在实践中罕见;若I*的再测量在时序上晚于A的发生,则I*-Y*之间的时序可表现为类似于上述4种观察性时序,3次及以上测量则表现为3种观察性同时域时序。为方便读者理解,本文将测量时序汇总。见图 2。
|
| 图 2 观察和实验情形下测量时序分类法 |
大自然只有一种因果律。研究设计是研究具体的计划或实际实施过程,是对人群因果律的复制,或认识上的实现。大自然不会告诉我们,该采用什么样设计可以获得因果律。实践中,对同一因果推断问题,研究者对于因和果的认识及其信息的可及性,而采取不同的测量策略。这些测量策略均应以测量因与测量果之间的关系能真实地反映真实因与真实果的关系为唯一金标准。因此,研究设计是否真实复制这种因果律?有没有失真?失真多少?这是研究者需要优先考虑的问题。在充分掌握研究背景及设计实施的数据产生机制,研究者需形成其对大自然因果律的认知或假设[16, 20-24],这是正确进行因果推断的前提。
无论是观察还是实验,为实现因果推断研究的目的,研究者必然要对因和果进行测量[1]。本文采用因果思维分析方法,在因果律存在的前提下,以大自然因和果的时域为基础,首先明确定义测量时序,接着分析对因和果进行测量(或干预)的时域特征,结合跨时域和测量方向,提出了5种测量时序并分析了其特点。
因果时序是唯一,理论上锚定了因、果及其测量(或干预)、以及因果推断可能实现的时域;而测量时序则非唯一,可有5种类型:即2种跨时域纵向时序、3种同时域时序(纵向、逆纵向和横向)。其中,无论是观察和实验中跨第2和3时域还是实验中跨第1和3时域的纵向时序,均可为人群的追踪、协变量的测量及偏倚调整所需的参数估计提供机会[25-26]。而同时域(第3时域)中因和果已然发生,对研究人群的追踪已无可能,而对人群的测量相当于历史重建或“考古”。因此,测量时序的重要性已次于测量的准确性。无论对因和果是首次、二次或多次测量,真实因发生前的干预(仅出现在实验中)、真实因(或果)发生后的及时或延后测量,实际研究中的测量时序均包含在本文提出的5种时序中。
本文是基于因果律成立的基础上在观察和实验时对测量时序进行阐述,全文并不涉及具体的研究设计。虽然这样,跨第2和3时域纵向时序或是当前认识的前瞻性队列研究、巢式病例对照研究、病例队列研究等常见的特征,跨第1和3时域纵向时序或是干预研究、临床实验、现场实验等的特征,同时域逆纵向时序或是暴发调查、病例对照研究、历史性队列研究等常见的特征,同时域横向时序或是时点横断面研究的特征;同时域横向时序和逆纵向时序的结合是横断面队列研究的特征[27];而记录联结研究或历史性队列研究均为二手数据(再测量),可有多种测量时序。虽然这样,因各种研究设计类型本身内涵的模糊性[18, 28-29],这种以时序为基础的研究设计分类并非确定无误的[28, 30]。如在讨论出生体重与婴儿感染之间关系的病例对照研究中,获取体重的信息来自于接生医生的出生记录(首次测量),本次研究为体重信息的第二次测量(从出生记录过录到调查表),因此二次测量婴儿体重与婴儿感染为同时域逆纵向时序,而首次测量与婴儿感染理论上为跨时域纵向时序。应具体分析研究设计实施过程的具体要素,而不仅仅局限于简单的一个设计的名字。因此,由“因”及“果”或由“果”及“因”与设计类型联系的提法,值得商榷。
虽然测量时序与研究设计间的关系存在争议,然而时序对判断研究过程中出现偏倚的重要性不言而喻。因果时序与纵向测量时序方向的一致性,并不代表着因果推断的准确性[16, 31]。与横向时序不同,有向时序(第1~3、5种)存在的测量时间差,为因果推断中因测量过程所产生的偏倚埋下伏笔[16, 32]。如跨时域纵向时序,虽然有助于对人群进行追踪和测量,然而在测量过程中,这种追踪可能导致研究者和研究对象在测量上出现偏倚:如研究对象可因意识到自己参与研究的过程,而有意地改变了暴露或影响暴露的行为,从而产生霍桑效应[32];而研究者更多地关注暴露组的结局,从而更多地进行观察和进行结局判断,产生检出偏倚或暴露怀疑偏倚[33-34],这种偏倚也可能发生在同时域纵向时序中。此外,同时域时序均有因“历史重建”而导致信息偏倚的可能;然而,同时域有向时序的时间差可能导致的测量偏倚,则不会出现在横向时序中。
6、结语综上所述,基于大自然时间轴,结合真实因和果的发生时间,本文提出了5种测量时序的分类,该分类法适用于首次或多次测量、及时和延后测量等所有测量策略及各种不同设计类型。从研究设计应整合偏倚设计的观点来看,实际研究过程中因果律总是交织地与偏倚产生的来源形成一个统一的因果框架。本文提出基于大自然时间轴的测量时序五分类法,概念清晰并有助于判断研究中可能出现的偏倚,为正确进行因果推断研究奠定基础。
利益冲突 所有作者均声明不存在利益冲突
| [1] |
Hill AB. Observation and experiment[J]. N Engl J Med, 1953, 248(24): 995-1001. DOI:10.1056/NEJM195306112482401 |
| [2] |
Lilienfeld DE. "The greening of epidemiology":sanitary physicians and the London Epidemiological Society (1830-1870)[J]. Bull Hist Med, 1978, 52(4): 503-528. |
| [3] |
Kramer MS, Boivin JF. Toward an "unconfounded" classification of epidemiologic research design[J]. J Chronic Dis, 1987, 40(7): 683-688. DOI:10.1016/0021-9681(87)90104-4 |
| [4] |
Kramer MS, Boivin JF. Directionality, timing, and sample selection in epidemiologic research design[J]. J Clin Epidemiol, 1989, 42(9): 827-828. DOI:10.1016/0895-4356(89)90094-2 |
| [5] |
Kramer MS, Boivin JF. The importance of directionality in epidemiologic research design[J]. J Clin Epidemiol, 1988, 41(8): 717-718. DOI:10.1016/0895-4356(88)90156-4 |
| [6] |
Feinstein AR. Directionality and scientific inference[J]. J Clin Epidemiol, 1989, 42(9): 829-833. DOI:10.1016/0895-4356(89)90095-4 |
| [7] |
Feinstein AR. Directionality in epidemiologic research[J]. J Clin Epidemiol, 1988, 41(8): 705-707. DOI:10.1016/0895-4356(88)90153-9 |
| [8] |
Abramson JH. Classification of epidemiologic research[J]. J Clin Epidemiol, 1989, 42(9): 819-820. DOI:10.1016/0895-4356(89)90091-7 |
| [9] |
Greenland S, Morgenstern H. Classification schemes for epidemiologic research designs[J]. J Clin Epidemiol, 1988, 41(8): 715-716. DOI:10.1016/0895-4356(88)90155-2 |
| [10] |
Greenland S, Morgenstern H. What is directionality?[J]. J Clin Epidemiol, 1989, 42(9): 821-824. DOI:10.1016/0895-4356(89)90092-9 |
| [11] |
Miettinen OS. "Directionality" in epidemiologic research[J]. J Clin Epidemiol, 1989, 42(9): 825-826. DOI:10.1016/0895-4356(89)90093-0 |
| [12] |
Greenland S. Multivariate estimation of exposure-specific incidence from case-control studies[J]. J Chronic Dis, 1981, 34(9/10): 445-453. DOI:10.1016/0021-9681(81)90004-7 |
| [13] |
Greenland S, Morgenstern H. Design versus directionality[J]. J Clin Epidemiol, 1991, 44(2): 213-214. DOI:10.1016/0895-4356(91)90269-f |
| [14] |
Greenland S. Science versus advocacy:the challenge of Dr. Feinstein[J]. Epidemiology, 1991, 2(1): 64-72. |
| [15] |
Hernán MA, Cole SR. Invited commentary:causal diagrams and measurement bias[J]. Am J Epidemiol, 2009, 170(8): 959-962. DOI:10.1093/aje/kwp293 |
| [16] |
郑英杰, 蔡倩莹, 范伟, 等. 因果思维在效应估计若干问题中的应用[J]. 中华流行病学杂志, 2019, 40(10): 1314-1323. Zheng YJ, Cai QY, Fan W, et al. The application of causal thinking in several issues in estimation of effects[J]. Chin J Epidemiol, 2019, 40(10): 1314-1323. DOI:10.3760/cma.j.issn.0254-6450.2019.10.026 |
| [17] |
郑英杰, 赵耐青, 何一宁. 客观世界的因果关系:基于有向无环图的结构解析[J]. 中华流行病学杂志, 2018, 39(1): 90-93. Zheng YJ, Zhao NQ, He YN. Causality in objective world:Directed Acyclic Graphs-based structural parsing[J]. Chin J Epidemiol, 2018, 39(1): 90-93. DOI:10.3760/cma.j.issn.0254-6450.2018.01.019 |
| [18] |
唐金陵. 再论观察与实验:大数据现实世界研究不能取代随机对照试验[J]. 中华流行病学杂志, 2018, 39(8): 1121-1124. Tang JL. Revisit to observation and experiment:real world study cannot replace randomized controlled trial[J]. Chin J Epidemiol, 2018, 39(8): 1121-1124. DOI:10.3760/cma.j.issn.0254-6450.2018.08.021 |
| [19] |
Shahar E, Shahar DJ. Causal diagrams, information bias, and thought bias[J]. Pragmat Obs Res, 2010, 1: 33-47. DOI:10.2147/POR.S13335 |
| [20] |
Glymour MM, Hamad R. Causal thinking as a critical tool for eliminating social inequalities in health[J]. Am J Public Health, 2018, 108(5): 623. DOI:10.2105/AJPH.2018.304383 |
| [21] |
Kaufman JS, Poole C. Looking back on "causal thinking in the health sciences"[J]. Annu Rev Public Health, 2000, 21: 101-119. DOI:10.1146/annurev.publhealth.21.1.101 |
| [22] |
Pearl J. Causal diagrams for empirical research[J]. Biometrika, 1995, 82(4): 669-688. DOI:10.1093/biomet/82.4.669 |
| [23] |
郑英杰, 赵耐青. 有向无环图:语言、规则及应用[J]. 中华流行病学杂志, 2017, 38(8): 1140-1144. Zheng YJ, Zhao NQ. Directed acyclic graphs:languages, rules and applications[J]. Chin J Epidemiol, 2017, 38(8): 1140-1144. DOI:10.3760/cma.j.issn.0254-6450.2017.08.029 |
| [24] |
Hernán MA, Hernández-Diaz S, Werler MM, et al. Causal knowledge as a prerequisite for confounding evaluation:an application to birth defects epidemiology[J]. Am J Epidemiol, 2002, 155(2): 176-184. DOI:10.1093/aje/155.2.176 |
| [25] |
Lash TL, Fox MP, Fink AK. Applying quantitative bias analysis to epidemiologic data[M]. New York: Springer-Verlag, 2009: 13-32.
|
| [26] |
Lash TL, Fox MP, MacLehose RF, et al. Good practices for quantitative bias analysis[J]. Int J Epidemiol, 2014, 43(6): 1969-1985. DOI:10.1093/ije/dyu149 |
| [27] |
Hudson JI, Pope HG Jr, Glynn RJ. The cross-sectional cohort study:an underutilized design[J]. Epidemiology, 2005, 16(3): 355-359. DOI:10.1097/01.ede.0000158224.50593.e3 |
| [28] |
Feinstein AR. Clinical biostatistics.Ⅻ. The architecture of cross-sectional research (Part Ⅰ)[J]. Clin Pharmacol Ther, 1978, 23(1): 81-96. DOI:10.1002/cpt197823181 |
| [29] |
White C, Bailar III JC. Retrospective and prospective methods of studying association in medicine[J]. Am J Public Health Nations Health, 1956, 46(1): 35-44. DOI:10.2105/ajph.46.1.35 |
| [30] |
Feinstein AR. Clinical biostatistics.ⅩⅢ. The architecture of cross-sectional reserach (conclusion)[J]. Clin Pharmacol Ther, 1978, 23(4): 481-493. DOI:10.1002/cpt1978234481 |
| [31] |
Taris TW, Kompier M. Challenges in longitudinal designs in occupational health psychology[J]. Scand J Work Environ Health, 2003, 29(1): 1-4. DOI:10.5271/sjweh.697 |
| [32] |
Mangione-Smith R, Elliott MN, McDonald L, et al. An observational study of antibiotic prescribing behavior and the Hawthorne effect[J]. Health Serv Res, 2002, 37(6): 1603-1623. DOI:10.1111/1475-6773.10482 |
| [33] |
Rundle A, Wang Y, Sadasivan S, et al. Larger men have larger prostates:Detection bias in epidemiologic studies of obesity and prostate cancer risk[J]. Prostate, 2017, 77(9): 949-954. DOI:10.1002/pros.23350 |
| [34] |
Sjölander A, Humphreys K, Palmgren J. On informative detection bias in screening studies[J]. Stat Med, 2008, 27(14): 2635-2650. DOI:10.1002/sim.3091 |
 2020, Vol. 41
2020, Vol. 41