文章信息
- 朱军礼, 吕梅斋, 骆淑英, 陈高尚, 庞志峰, 章光明, 吴晓虹.
- Zhu Junli, Lyu Meizhai, Luo Shuying, Chen Gaoshang, Pang Zhifeng, Zhang Guangming, Wu Xiaohong
- 2017-2018年流感流行季儿童接种流感疫苗效果社区队列研究
- Evaluation of influenza vaccine effectiveness in 2017-2018 influenza season based on community children cohort study
- 中华流行病学杂志, 2020, 41(5): 747-752
- Chinese Journal of Epidemiology, 2020, 41(5): 747-752
- http://dx.doi.org/10.3760/cma.j.cn112338-20190730-00563
-
文章历史
收稿日期: 2019-07-30
2. 永康市疾病预防控制中心传染病防制科 321300;
3. 义乌市疾病预防控制中心免疫规划科 322000
2. Division of Communicable Disease Prevention and Control, Yongkang County Center for Disease Control and Prevention, Yongkang 321300, China;
3. Department of Immunization Program, Yiwu County Center for Disease Control and Prevention, Yiwu 322000, China
流感是对我国儿童产生较重疾病负担的传染病之一,但也是疫苗可预防疾病[1]。接种流感疫苗是预防流感及并发症的最有效手段,在我国大部分省份,流感疫苗为非免疫规划疫苗,公民自愿、自费接种,年平均接种率为2%~3%[2]。随流感病毒持续演变,流感疫苗株也在不停改变,人群需要不断接种来维持免疫屏障。开展流感疫苗人群预防效果评价,可为筛选流感疫苗株、指导人群免疫预防提供重要流行病学证据[3-4]。在2017-2018年流感流行季,开展儿童接种流感疫苗效果社区队列研究,评估流感疫苗对6~72月龄儿童流感样病例(influenza-like illness,ILI)及诊疗负担的预防效果。
对象与方法1.研究现场:本研究采用两阶段抽样方法,在浙江省永康市和义乌市共30家乡镇/街道儿童接种门诊中,随机抽取10家门诊(根据2市0~6岁儿童人口数比例,永康市4家、义乌市6家),再由该10家接种门诊医生招募研究对象,组建队列。
2.研究对象:①纳入标准:在接种门诊完成儿童免疫接种、6~72月龄、身体健康的儿童;②剔除标准:儿童家长或监护人无法配合完成研究的儿童。根据相关参数[1](如流感流行季儿童ILI发病率、流感疫苗暴露的RR值等),并考虑失访,最终确定进入队列的儿童为1 752人。
3.研究方法:采用社区队列研究设计,招募时间从2017年10月1日至12月31日。随访观察时间是从进入队列始,至2018年4月30日止(主要依据流感病原学监测,确定2017-2018年流感流行季为2017年10月至2018年4月)。
(1)调查与随访:儿童进入队列时,由接种门诊医生开展问卷调查(主要包括儿童的基本信息,流感疫苗接种史等),然后随访观察至2018年4月30日。其间,每月月末,由接种门诊医生完成一次随访,观察记录儿童ILI发病、门诊就诊、住院治疗、自行服药、是否接种流感疫苗、失访等。
(2)推广接种流感疫苗:2017-2018年流感流行季,永康和义乌两市均在2017年9月至2018年1月间推广接种三价灭活流感疫苗(trivalent inactivated influenza vaccine,TIV)。儿童接种门诊发放“流感疫苗接种对象告知书”,建议6月龄至3岁儿童接种2剂次,间隔1个月;≥3岁人群接种1剂次。本队列1 752名儿童中,有643名自愿、全程接种了TIV,接种率为36.70%。
(3)观测变量(指标)定义:ILI,发热(体温≥38 ℃),伴咳嗽或咽痛之一者[5]。①ILI发病次数:若研究对象在随访期报告ILI次数≥2次,发病时间间隔不足1周的记录,将其与上次发病时间合并后,再记发病次数。②门诊就诊次数:每次ILI发病后,去医院就诊的,不论其就诊次数,门诊就诊次数均记为1次;若被收入院的,则住院治疗次数记为1次。③自行服药次数:每次ILI发病后,未就诊而自行服药治疗的,则记为1次。既未就诊也未服药治疗,则门诊就诊和自行服药次数均记为0次。
(4)流感疫苗免疫史判定:通过查询“浙江省儿童免疫规划信息管理系统”或“儿童预防接种证”获取。根据疫苗接种日期(6月龄至3周岁儿童,则为接种第2剂次日期)与ILI发病日期(或随访日期)的间隔时间t来判定,若t≥14 d,则该时点判定为“有免疫史”状态,反之为“无免疫史”状态。
4.质量控制:参与招募、调查随访的医生接受统一培训,掌握研究对象纳入与剔除标准,获得儿童家长或监护人的知情同意,提高研究对象依从性;随访前,医生给每名研究对象配发体温计,并培训儿童家长或监护人测量儿童体温;随访工作中,确定专人分组包干(两人一组),月末随访,采用电话或面对面访问方式,若采取电话随访,每名儿童随访时间≥3 min。每月随访结束后,抽取一定比例对象复核。
5.统计学分析:采用EpiData 3.1软件建立数据库,双录入核对。使用SPSS 19.0和Excel 2017软件分析包括研究对象基本情况,观察期间ILI、门诊就诊、自行服药发生人次数及影响因素,疫苗效果(vaccine effectiveness,VE)等指标。对于影响ILI、门诊就诊、自行服药发生人次数的因素分析,采用广义线性模型(generalized linear models,GLM)进行拟合,以各观测变量为因变量,自变量为各因子或协变量,构建泊松分布或负二项分布模型,为消除观察时间长短的影响,将研究对象的“随访观察天数的自然对数值”作为拟合模型的偏移量(offset),获得接种流感疫苗及其他自变量的RR值(95%CI)。根据公式:VE=(1-RR)×100%得到VE值(95%CI),以95%CI值是否在单侧,判断差异是否有统计学意义。双侧检验,以P<0.05为差异有统计学意义。
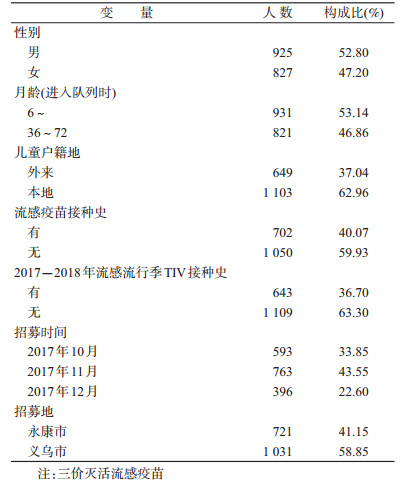
结果1.基本情况:1 752名儿童参加研究,进入队列时年龄为6.00~72.00月龄(M=30.00,P25~P75:14.00~48.00),男童925人,占52.80%。见表 1。随访到2018年4月30日,有139名儿童先后失访,占7.93%。累计观察了308 166人天,ILI发病1 625人次,平均每天有5.27‰发生ILI;门诊就诊1 052人次,平均每天有3.41‰因ILI去就诊;住院治疗11人次,平均每天有0.04‰因ILI住院;自行服药448人次,平均每天有1.45‰因ILI自行服药治疗。
2. ILI、门诊就诊和自行服药发生人次数的影响因素分析:在1 752名儿童中,分别按性别(男、女)、年龄(6~35月龄、36~72月龄)、招募地(永康市、义乌市)、儿童户籍地(外来、本地)、流感疫苗接种史(有、无)分组,分析各组儿童2017-2018年流感流行季ILI、门诊就诊和自行服药发生人次数的差异。结果显示,影响ILI发生人次数的变量有:年龄、招募地、儿童户籍地、流感疫苗接种史;影响门诊就诊发生人次数的变量有:年龄、招募地、儿童户籍地、流感疫苗接种史;影响自行服药发生人次数的变量有:年龄、招募地、流感疫苗接种史。见表 2。
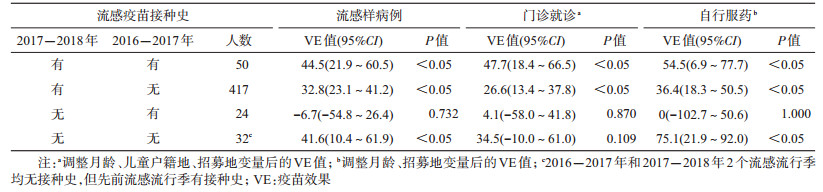
3. 2个流感流行季流感疫苗不同接种情况的VE值:选取入队列时,≥18月龄的1 265名均可接种流感疫苗儿童组成分析样本,其中有接种史的儿童523人,无接种史的儿童742人。与无接种史的儿童相比,2个流感流行季均有接种史的儿童中,流感疫苗针对2017-2018年流感流行季ILI、门诊就诊和自行服药的VE值差异有统计学意义;2017-2018年流感流行季有接种史、2016-2017年流感流行季无接种史的儿童中,流感疫苗针对ILI、门诊就诊和自行服药的VE值差异有统计学意义;而2017-2018年流感流行季无接种史、2016-2017年流感流行季有接种史的儿童,流感疫苗针对上述3类观测事件的VE值差异均无统计学意义。见表 3。
4. 2017-2018年流感流行季TIV的VE值:
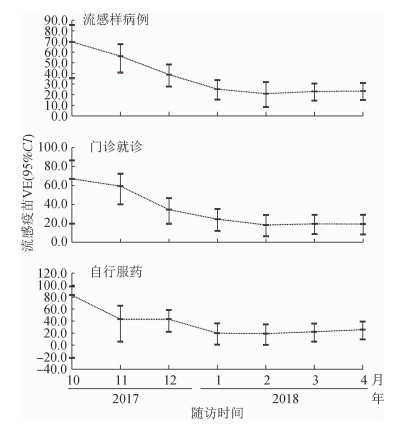
(1)不同时点的VE值评估:在1 752名队列儿童中,分别在7次随访时点(2017年10-12月,2018年1-4月),以未接种2017-2018年流感流行季TIV的儿童作为参照组,评估了2017-2018年流感流行季TIV的VE值,结果显示,TIV针对ILI、门诊就诊和自行服药的VE点估计值分别为21.0%~69.7%、18.3%~67.1%、19.2%~83.2%。VE点估计值随月份而降低,其95%CI趋于稳健。至2018年4月30日,TIV针对ILI、门诊就诊和自行服药总的VE值(95%CI)分别为23.5%(95%CI:15.1%~31.1%)、19.3%(95%CI:8.2%~29.1%)和25.8%(95%CI:9.3%~39.3%),均有统计学意义。见图 1。
|
| 注:VE:疫苗效果 图 1 2017-2018年流感流行季不同时间、不同观测指标的流感疫苗VE值 |
(2)流感疫苗接种前/后VE值:以接种2017-2018年流感流行季TIV的643名儿童为分析样本。接种前,平均每天有5.15‰发生ILI(158/30 671),3.52‰人因ILI去门诊就诊(108/30 671),1.50‰因ILI自行服药治疗(46/30 671);接种后,平均每天有4.30‰发生ILI(439/102 015),2.90‰因ILI去门诊就诊(296/102 015),1.13‰因ILI自行服药治疗(115/102 015)。以接种前为对照,流感疫苗针对ILI、门诊就诊和自行服药的VE值(95%CI)均无统计学意义。在分组分析中,仅36~72月龄儿童组的流感疫苗针对ILI、门诊就诊和自行服药的VE值均有统计学意义。见表 4。
本研究采用前瞻性队列研究设计,以ILI、门诊就诊和自行服药次数为观测指标,采用GLM模型进行拟合计算2017-2018年流感流行季TIV的VE值。结果显示,与未接种儿童相比,TIV针对该流行季6~72月龄儿童ILI发病、门诊就诊和自行服药的VE值(95%CI)分别为23.5%(95%CI:15.1%~31.1%)、19.3%(95%CI:8.2%~29.1%)和25.8%(95%CI:9.3%~39.3%);接种前、后相比,TIV对ILI、门诊就诊和自行服药的VE值(95%CI)分别为16.5%(95%CI:-0.2%~30.4%)、17.6%(95%CI:-2.7%~33.9%)和24.8%(95%CI:-5.8%~46.6%),差异均无统计学意义,且均低于过往类似研究所得相关指标的VE值[6-9]。
本研究中接种前、后比较发现,对于36~72月龄儿童,流感疫苗对ILI、门诊就诊和自行服药的VE值分别为31.9%(95%CI:12.7%~46.9%)、32.6%(95%CI:8.6%~50.3%)和44.3%(95%CI:11.9%~64.8%),差异均有统计学意义;而对于6~35月龄儿童组,VE值均差异无统计学意义,提示流感疫苗VE值存在年龄组差异[10-11]。从不同评估时点来看VE值变化,随着月份推移,流感疫苗VE值(95%CI)趋于稳健,与Kavanagh等[6-7]研究结果相仿。可能原因为随着时间推移,队列中观测事件发生次数和接种流感疫苗儿童数在增加,VE值精确度也随之提高,但不排除受到流感流行强度消长的影响。
在2016-2018年2个流感流行季中,流感疫苗不同接种组合的VE值研究发现,和未曾接种儿童比较,仅2017-2018年流感流行季有接种史或2016-2018年2个流感流行季均有接种史的儿童中,流感疫苗对2017-2018年流感流行季ILI、门诊就诊和自行服药的VE值有统计学意义,仅2016-2017年流感流行季有接种史的儿童流感疫苗VE值无统计学意义,提示流行季均要接种流感疫苗,与过往研究结论一致[12-13]。
综上所述,每年接种流感疫苗可以减轻儿童ILI发病、门诊就诊和自行服药治疗等疾病负担,且对36~72月龄儿童保护效果优于6~35月龄儿童。与以流感发病为观测指标的VE值评估研究相比,本研究可能低估了流感疫苗VE值[11]。但是,用ILI、门诊就诊和自行服药等作为观测指标,更具有经济适用性和推广前景。本研究局限性为未考虑流感感染史、流感流行强度消长、流感疫苗接种覆盖率等对人群VE值评估的影响[12, 14-15]。
利益冲突 所有作者均声明不存在利益冲突
| [1] |
冯录召, 彭质斌, 王大燕, 等. 中国流感疫苗预防接种技术指南(2018-2019)[J]. 中华预防医学杂志, 2018, 52(11): 1101-1114. Feng LZ, Peng ZB, Wang DY, et al. Technical guidelines for seasonal influenza vaccination in China (2018-2019)[J]. Chin J Prev Med, 2018, 52(11): 1101-1114. DOI:10.3760/cma.j.issn.0253-9624.2018.11.003 |
| [2] |
彭质斌, 王大燕, 杨娟, 等. 中国流感疫苗应用现状及促进预防接种的政策探讨[J]. 中华流行病学杂志, 2018, 39(8): 1045-1050. Peng ZB, Wang DY, Yang J, et al. Current situation and related policies on the implementation and promotion of influenza vaccination, in China[J]. Chin J Epidemiol, 2018, 39(8): 1045-1050. DOI:10.3760/cma.j.issn.0254-6450.2018.08.007 |
| [3] |
李娟, 卢莉. 上市后疫苗流行病学效果评价方法[J]. 中国疫苗和免疫, 2013, 19(3): 274-278. Li J, Lu L. Evaluation methods of vaccine epidemiological effectiveness for the vaccines of post-maketing[J]. Chin J Vacc Imm, 2013, 19(3): 274-278. |
| [4] |
Minodier L, Blanchon T, Souty C, et al. Influenza vaccine effectiveness:best practice and current limitations of the screening method and their implications for the clinic[J]. Exp Rev Vacc, 2014, 13(8): 1039-1048. DOI:10.1586/14760584.2014.930666 |
| [5] |
中华人民共和国国家卫生和计划生育委员会.关于印发全国流感监测方案(2017年版)的通知[EB/OL]. (2017-09-27)[2019-07-01]. http://www.chinaivdc.cn/cnic/zyzx/jcfa/201709/t20170927_153830.htm. National Health and Family Planning Commission of the People's Republic of China. The notice of the national influenza surveillance program (2017 edition)[EB/OL]. (2017-09-27)[2019-07-01]. http://www.chinaivdc.cn/cnic/zyzx/jcfa/201709/t20170927_153830.htm. |
| [6] |
Kavanagh K, Robertson C, McMenamin J. Assessment of the variability in influenza A(H1N1) vaccine effectiveness estimates dependent on outcome and methodological approach[J]. PLoS One, 2011, 6(12): e28743. DOI:10.1371/journal.pone.0028743 |
| [7] |
Kavanagh K, Robertson C, McMenamin J. Estimates of influenza vaccine effectiveness in primary care in Scotland vary with clinical or laboratory endpoint and method-Experience across the 2010/11 season[J]. Vaccine, 2013, 31(41): 4556-4563. DOI:10.1016/j.vaccine.2013.07.056 |
| [8] |
Wang Y, Chen LL, Yu J, et al. The effectiveness of influenza vaccination among nursery school children in China during the 2016/17 influenza season[J]. Vaccine, 2018, 36(18): 2456-2461. DOI:10.1016/j.vaccine.2018.03.039 |
| [9] |
Yu LL, Wilfred HSW, Hattangdi-Haridas R, et al. Evaluating impact of school outreach vaccination programme in Hong Kong influenza season 2018-2019[J]. Hum Vaccin Immunother, 2019, 1-4. DOI:10.1080/21645515.2019.1678357 |
| [10] |
Sugaya N, Shinjoh M, Nakata Y, et al. Three-season effectiveness of inactivated influenza vaccine in preventing influenza illness and hospitalization in children in Japan, 2013-2016[J]. Vaccine, 2018, 36(8): 1063-1071. DOI:10.1016/j.vaccine.2018.01.024 |
| [11] |
骆淑英, 朱军礼, 吕梅斋, 等. 基于实验室检测结果病例-对照研究评价6~72月龄儿童流感疫苗效果[J]. 中华预防医学杂志, 2019, 53(6): 576-580. Luo SY, Zhu JL, Lyu MZ, et al. Evaluation of the influenza vaccine effectiveness among children aged 6 to 72 months based on the test-negative case control study design[J]. Chin J Prev Med, 2019, 53(6): 576-580. DOI:10.3760/cma.j.issn.0253-9624.2019.06.007 |
| [12] |
Shinjoh M, Sugaya N, Yamaguchi Y, et al. Inactivated influenza vaccine effectiveness and an analysis of repeated vaccination for children during the 2016/17 season[J]. Vaccine, 2018, 36(37): 5510-5518. DOI:10.1016/j.vaccine.2018.07.065 |
| [13] |
Zhang L, van der Hoek W, Krafft T, et al. Influenza vaccine effectiveness estimates against influenza A(H3N2) and A(H1N1) pdm09 among children during school-based outbreaks in the 2016-2017 season in Beijing, China[J]. Hum Vaccin Immunother, 2019, 1: 1-7. DOI:10.1080/21645515.2019.1677438 |
| [14] |
Syrjänen RK, Jokinen J, Ziegler T, et al. Effectiveness of pandemic and seasonal influenza vaccines in preventing laboratory-confirmed influenza in adults:a clinical cohort study during epidemic seasons 2009-2010 and 2010-2011 in Finland[J]. PLoS One, 2014, 9(9): e108538. DOI:10.1371/journal.pone.0108538 |
| [15] |
Jang H, Ross TM. Preexisting influenza specific immunity and vaccine effectiveness[J]. Expert Rev Vaccine, 2019, 18(10): 1043-1051. DOI:10.1080/14760584.2019.1675519 |
 2020, Vol. 41
2020, Vol. 41