文章信息
- 付凯钰, 乔峰, 孟革, 张卿, 刘莉, 宋崑, 牛凯军.
- Fu Kaiyu, Qiao Feng, Meng Ge, Zhang Qing, Liu Li, Song Kun, Niu Kaijun
- 缺失牙数与非酒精性脂肪肝的相关研究
- Association between tooth missing and non-alcoholic fatty liver disease
- 中华流行病学杂志, 2020, 41(5): 716-721
- Chinese Journal of Epidemiology, 2020, 41(5): 716-721
- http://dx.doi.org/10.3760/cma.j.cn112338-20190621-00457
-
文章历史
收稿日期: 2019-06-21
2. 天津医科大学营养流行病学研究所 公共卫生学院 300070;
3. 天津医科大学总医院健康管理中心 300052
2. Nutritional Epidemiology Institute and School of Public Health, Tianjin Medical University, Tianjin 300070, China;
3. Health Management Centre, Tianjin Medical University General Hospital, Tianjin 300052, China
非酒精性脂肪肝(NAFLD)是一种以肝细胞内脂肪过度堆积为主要特征的非酒精性消耗性疾病[1]。根据流行病学调查结果表明,NAFLD的全球发病率已经达到6%~33%,包括中国在内的亚洲多数国家患病率已达25%以上[2]。龋病和牙周病是常见的口腔细菌性感染疾病,是造成牙缺失的主要原因,牙缺失的数目可能反映了口腔内及全身的炎症积累状态[3]。有学者提出,牙周炎患者体内细胞因子和炎症介质增加,其机体长期处于低水平的炎症状态[4]。此外,牙周炎的感染会增加体内的氧化应激反应和胰岛素抵抗,导致肝内脂质蓄积,进而加速NAFLD的发生和发展[5-6]。除牙周炎外,以变异链球菌(Streptococcus mutans)为主要致病菌的龋病也是导致牙齿脱落的另一个原因[7]。有研究证明,变异链球菌与动脉粥样硬化、心血管疾病等多种系统性疾病有关,其特定菌株可以在小鼠体内诱发NAFLD[8]。同时,口腔内细菌在肠道的异位定植与全身炎症性疾病也密切相关[9]。这些数据表明,缺失牙齿的数目与NAFLD之间可能存在关联,其机制可能与全身炎症、菌血症、胰岛素抵抗或氧化应激反应等原因相关。本研究旨在探讨评价成年人群中缺失牙的数量和NAFLD之间的关联,为NAFLD相关的预防和控制工作提供科学依据。
资料与方法1.资料来源:来源于2014-2018年天津营养流行病学队列(TCLSIH研究)。所有对象均自愿参加并且签署知情同意书,本研究通过天津医科大学伦理委员会审查(批准文号:TMUhMEC 201430)。排除酒精性脂肪肝患者1 820名、肝脏相关疾病患者(病毒性肝炎、慢性乙型或丙型肝炎、肝脏术后、自身免疫性肝脏疾病及肝癌)213名、心血管疾病患者1 317名、癌症患者276名、无效问卷者2 776名。本研究纳入人群为18~65岁成年人。最终共纳入26 983名,男性13 626名,女性13 357名。
2.诊断标准:
(1)NAFLD:诊断依据肝脏超声检查:①肝肾回声差异:肝脏前场回声增加(“明亮肝”);②肝内管道模糊不清;③肝前后回声差异:肝脏远场回声逐渐减弱;符合上述腹部超声表现至少2项者诊断为脂肪肝。在此基础上,男性和女性饮酒量分别 < 140 g/周和 < 70 g/周者定义为NAFLD[10]。血清指标:肝脏酶超过正常水平,ALT升高标准:男性>41 U/L,女性>33 U/L。腹部超声检查诊断NAFLD的敏感度为92%,特异度为100%。
(2)缺失牙:采用自行设计的调查问卷确定缺失牙数。缺失牙数定义为除第三磨牙外,口内余留牙数的总和,包括健康、龋坏、充填治疗后的牙体[11]。如果整颗牙或牙冠缺失,则记录为缺牙,计算缺失牙齿的总数。根据最新的美国健康和营养调查中成年人牙齿缺失数目的数据,35~49岁的平均缺失牙齿数为3[12]。因此,根据缺失牙齿的数目分为4组:0、1~、3~和≥ 6颗。
(3)实验室检查:血液样本采集对象空腹12 h的静脉血,采用全自动生化分析仪(德国曼海姆Roche Cobas8000模块化分析仪)测定FPG(采用葡萄糖氧化酶法),TC和TG测定采用酶法,LDL-C测定采用聚乙烯硫酸沉淀法,HDL-C测定采用化学沉淀法,ALT测定采用IFCC法及白细胞数目测定。
(4)其他变量:人体测量参数(身高和体重)采用标准方法测量,BMI为体重(kg)/身高(m)2。测量腰围时,受试者正常站立呼吸,测量呼气末脐部位置。使用自动血压测定仪(中国天津安东)测量SBP和DBP,受试者坐位休息5 min后,测量2次左上臂血压。以这2次测量的平均值作为血压值。
MS的诊断依据美国心脏协会2009年的诊断标准定义,且符合以下≥ 3种标准:①腰围增加(男性≥ 85 cm;女性≥ 80 cm);②TG水平升高(≥ 150 mg/dl),或进行相关药物治疗;③HDL-C水平降低(男性 < 1.0 mmol/L,女性 < 1.3 mmol/L),或进行相关药物治疗;④血压升高[SBP ≥ 130 mmHg(1 mmHg=0.133 kPa)和/或DBP ≥ 85 mmHg]或服用降压药物治疗。⑤FPG升高(≥ 5.56 mmol/L)或服用降糖药物治疗。
年龄、性别、文化程度、职业状况、吸烟和饮酒状况社会人口学资料通过填写问卷获得。根据国际身体活动问卷(IPAQ)评估过去1周的身体活动量(PA)[13]。代谢当量(MET)(h/w)=代谢当量系数×活动持续时间(h)×频率(d)。累计不同活动的得分以计算PA值。采用改良食物频度问卷(FFQ)进行膳食结构调查,以中国食物成分表作为营养素的基础数据库,结合FFQ的信息计算每名对象一日总能量的摄入量(kJ/d)以及蛋白质、碳水化合物、脂肪和二十碳五烯酸(EPA)和二十二碳六烯酸(DHA)的摄入量。针对该问卷进行因子分析确定因子负荷,生成主要膳食模式[13],因子负荷>0.30的食物项目是该饮食模式的主要组成部分,代表每种模式的特征。
3.统计学分析:采用SAS 9.3软件进行统计学分析。使用Kolmogorov-Smirnov(n>2 000)和Shapiro-Wilk(n ≤ 2 000)检验对连续变量的分布进行正态性评估。由于在本研究中,所有连续变量的分布都不是正态分布,所以在分析数据之前,应用自然对数对数据进行归一化处理,经过对数变换后的连续协变量接近正态分布。分类变量表示为百分比,连续变量表示为M(P25~P25)。对连续分布变量和有序分布变量进行Kruskal-Wallis检验(2组以上的比较)和分类变量的χ2检验。为了进一步分析,以NAFLD的存在为因变量,以缺失牙齿的种类为自变量。调整可能的混杂因素后,采用logistic回归分析缺牙数与NAFLD之间的关系。通过在回归模型中加入交叉积项,检验缺牙数目与潜在混杂因素之间的交互作用。为避免多重共线性,分别将MS的单一变量输入模型,并对膳食结构进行因子分析。计算OR值及其95%CI。所有检验均为双侧检验,以P < 0.05为差异有统计学意义。
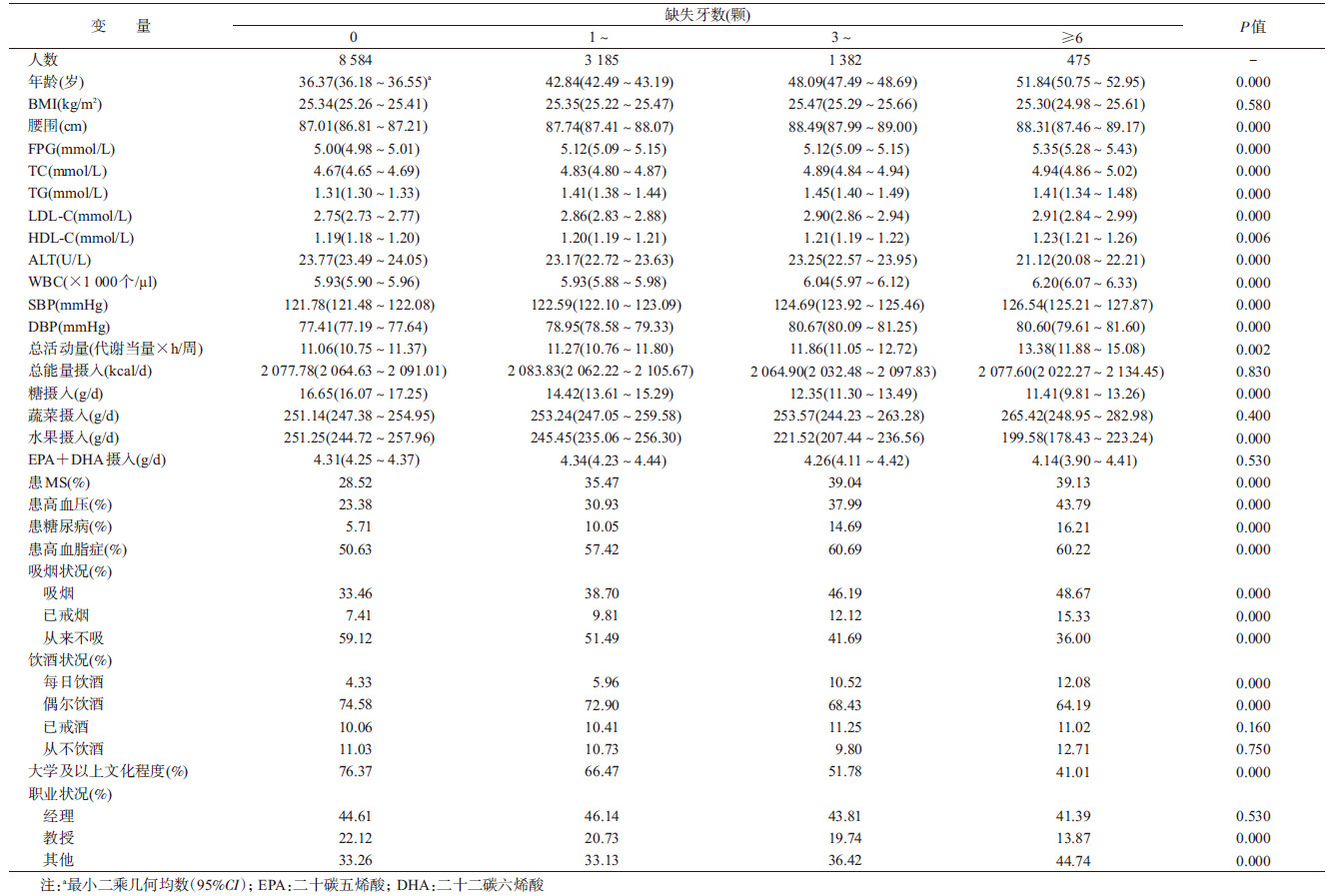
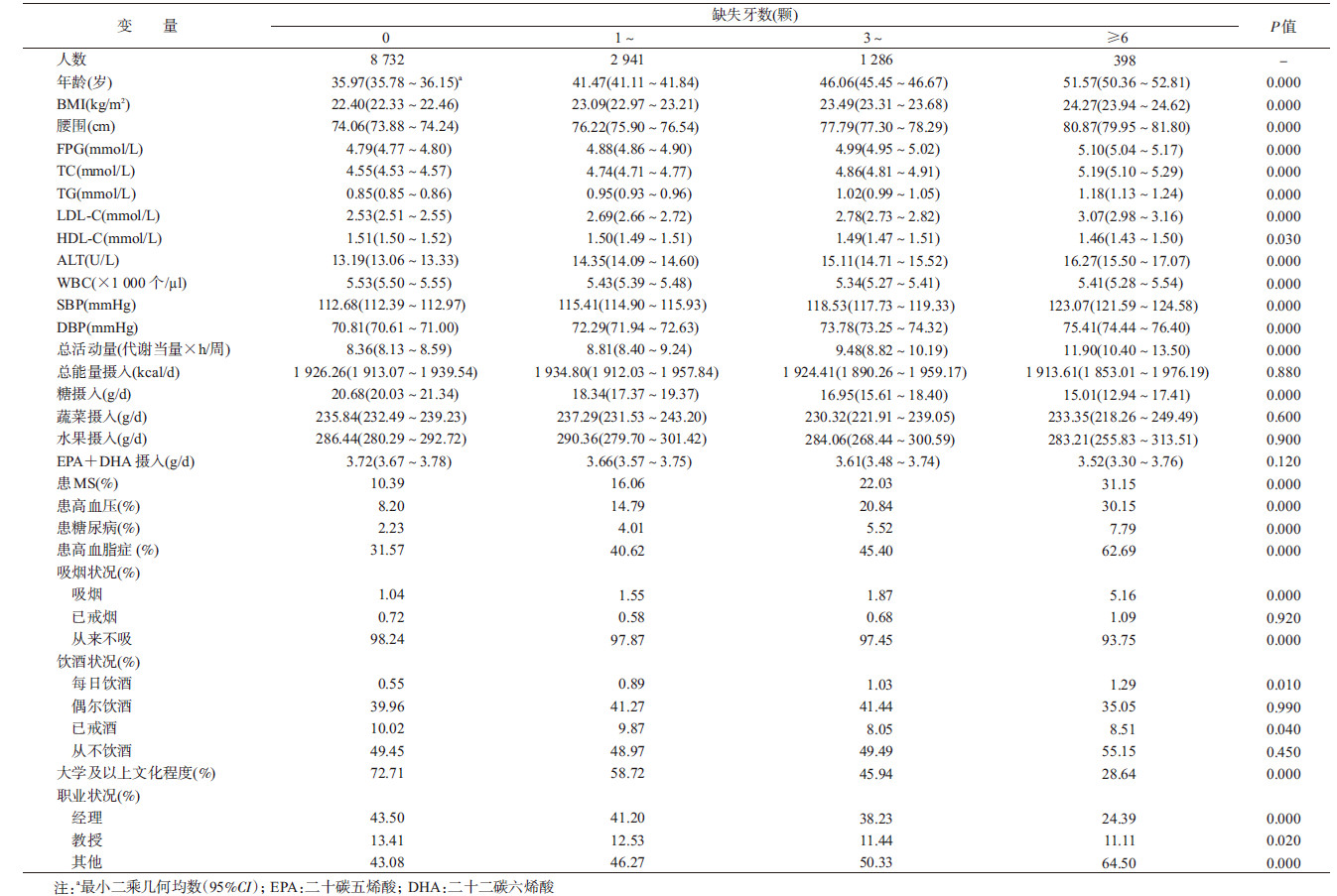
结果1.基本情况:共纳入26 983名研究对象,其中男性13 626名(50.1%),年龄为(40.4±10.6)岁,女性13 357名(49.9%),年龄为(39.4±10.4)岁。男性缺失牙数0、1~、3~和≥ 6颗的比例为63.0%、23.4%、10.1%和3.5%,女性为65.4%、22.0%、9.6%和3.0%。NAFLD的总发生率为26.9%(7 270/26 983),男性NAFLD发生率为39.9%,女性NAFLD发生率为13.8%。在男性中,至少有1颗牙齿缺失者年龄、腰围较大,总活动量、TC、TG、LDL-C、HDL-C、SBP、DBP等水平更高(P < 0.050),当缺失牙数≥ 6颗时,患有MS、糖尿病、高血压和高脂血症的比例更高(P=0.000);女性中,至少有1颗牙齿缺失的人群腰围较大,BMI、TC、LDL-C、SBP、DBP、ALT等水平较高(P < 0.05)。在缺失牙数≥ 6颗的组中,患有MS、高血压、高脂血症和糖尿病的女性比例较高(表 1,2)。
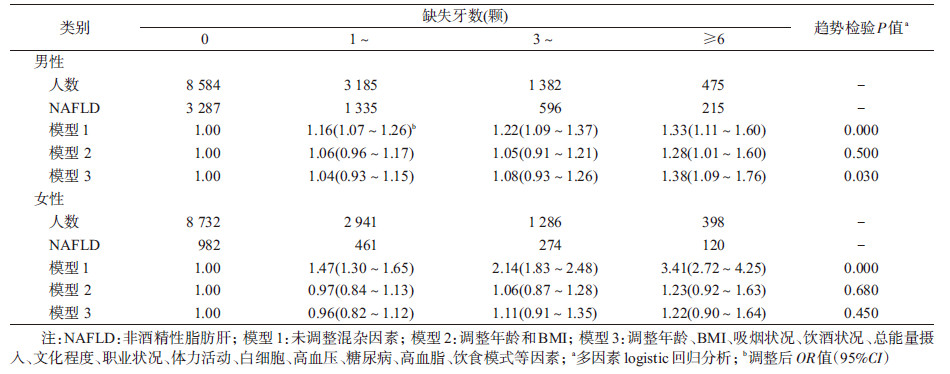
2.缺失牙和NAFLD的关系:采用logistic回归对缺牙数与NAFLD进行分析,调整年龄、BMI、吸烟状况、饮酒状况、总能量摄入、文化程度、职业状况、体力活动、白细胞、高血压、糖尿病、高血脂、饮食模式等因素后,缺失牙数≥ 6颗的男性NAFLD患病率比完整牙列者高38.0%(OR=1.38,95%CI:1.09~1.76,P=0.030)(表 3)。性别与缺牙数之间存在显著交互作用(P=0.040),而在最终模型中未观察到其他显著交互作用(年龄:P=0.250;BMI:P=0.260;吸烟状况:P=0.800;饮酒状况:P=0.770;总能量摄入:P=0.540;文化程度:P=0.330;职业状况:P=0.500;总活动量:P=0.780;白细胞:P=0.960;高血压:P=0.370;糖尿病:P=0.170;高血脂:P=0.300;饮食模式:P=0.500)。排除年龄 < 40岁的受试者(n=13 572)后进行敏感性分析,差异无统计学意义。同完整牙列组相比,缺失牙数≥ 6颗组的男、女性校正OR值(95%CI)分别为1.42(1.08~1.87)(趋势检验P=0.040)和1.13(0.80~1.58)(趋势检验P=0.150)。此外,调整性别因素后,结果为阴性(趋势检验P=0.070)。
本研究表明,在完整牙列组与缺失牙组的男性人群中,缺失牙数目和NAFLD发病率相关,在女性人群中无明显相关性,但随着缺失牙数的增加,NAFLD患病风险有上升趋势。
牙周炎是牙齿脱落的主要原因之一,人群研究显示,牙周炎与重症肝脏疾病显著相关,其患病史是NAFLD发病率的独立危险因素[14-15]。日本的一项横断面研究发现,深牙周袋(pd ≥ 4 mm)患者血液中的ALT高于健康对照组[16]。动物研究证实牙周炎主要致病菌牙龈卟啉单胞菌的感染会促进NAFLD的进展,若牙周病的NAFLD患者进行牙周治疗干预可降低其血清中AST和ALT水平,同时改善NAFLD的状况[17]。口腔内细菌与肠道内菌群关系密切[18],多项流行病学研究显示缺失牙的数目与心血管疾病、糖尿病等相关[19-20],这些疾病都与NAFLD有着共同的危险因素。广泛存在于龋病和牙周病患者口中的牙菌斑生物膜是以由革兰阴性菌为主的多种菌属组成三维结构[21]。其入血后经血液循环在肝脏异位定植,使血清中内毒素、脂多糖(LPS)和促炎细胞因子水平的增加,导致慢性、全身性的低度炎症[9],引起体内胰岛素抵抗,加速NAFLD的发生和发展[22]。因此,牙齿脱落与NAFLD之间的联系可能反映牙菌斑生物膜对口腔和全身健康的危害。此外,缺失牙数目过多降低了其咀嚼功能,改变其饮食模式,使纤维摄入量减少,碳水化合物的摄入量增加,使体内游离脂肪酸增加,也可能引起NAFLD的发生[23]。
本研究结果在不同性别间存在差异,其原因可能是NAFLD在男性中的患病率显著高于女性。其次,饮食摄入量和食物偏好的性别差异也可能是造成这种差异的原因。此外,吸烟和饮酒等危害健康的行为也有显著的性别差异,其也是NAFLD的常见危险因素。
本研究存在局限性。一是缺失牙数的统计来源于自我报告的问卷调查,存在报告偏倚,可能影响结果。二是横断面研究不能判断因果关系,需进一步的队列研究验证。第三,尽管本研究调整了大量的混杂因素,但尚不能完全消除其他潜在因素对NAFLD的影响。
综上所述,缺失牙齿的数目与NAFLD在男性中呈正相关,其主要机制可能是由口腔炎症引起的全身慢性炎症。牙周炎可能增加NAFLD的患病风险,严格的日常口腔护理和定期口腔检查对NAFLD患者有潜在的益处。
利益冲突 所有作者均声明不存在利益冲突
| [1] |
中华医学会肝脏病学分会脂肪肝和酒精性肝病学组. 非酒精性脂肪性肝病诊断标准[J]. 中华肝脏病杂志, 2003, 11(2): 71. Fatty Liver and Alcoholic Liver Disease Study Group of Chinese Liver Disease Association. Diagnostic criteria of nonalcoholic fatty liver disease[J]. Chin J Hepatol, 2003, 11(2): 71. DOI:10.3760/j.issn:1007-3418.2003.02.002 |
| [2] |
Younossi ZM, Koenig AB, Abdelatif D, et al. Global epidemiology of nonalcoholic fatty liver disease Meta-analytic assessment of prevalence, incidence, and outcomes[J]. Hepatology, 2016, 64(1): 73-84. DOI:10.1002/hep.28431 |
| [3] |
Kassebaum NJ, Bernabé E, Dahiya M, et al. Global burden of severe tooth loss:a systematic review and Meta-analysis[J]. J Dent Res, 2014, 93(7 Suppl): S20-28. DOI:10.1177/0022034514537828 |
| [4] |
Pizzo G, Guiglia R, Lo Russo L, et al. Dentistry and internal medicine:From the focal infection theory to the periodontal medicine concept[J]. Eur J Intern Med, 2010, 21(6): 496-502. DOI:10.1016/j.ejim.2010.07.011 |
| [5] |
Demmer RT, Breskin A, Rosenbaum M, et al. The subgingival microbiome, systemic inflammation and insulin resistance:the oral infections, glucose intolerance and insulin resistance study[J]. J Clin Periodontol, 2017, 44(3): 255-265. DOI:10.1111/jcpe.12664 |
| [6] |
Chapple ILC, Genco R. Diabetes and periodontal diseases:consensus report of the Joint EFP/AAP workshop on periodontitis and systemic diseases[J]. J Clin Periodontol, 2013, 84(4 Suppl): S106-112. DOI:10.1902/jop.2013.1340011 |
| [7] |
Selwitz RH, Ismail AI, Pitts NB. Dental caries[J]. Lancet, 2007, 369(9555): 51-59. DOI:10.1016/S0140-6736(07)60031-2 |
| [8] |
Nakano K, Nemoto H, Nomura R, et al. Detection of oral bacteria in cardiovascular specimens[J]. Oral Microbiol Immunol, 2009, 24(1): 64-68. DOI:10.1111/j.1399-302X.2008.00479.x |
| [9] |
Naka S, Wato K, Hatakeyama R, et al. Longitudinal comparison of Streptococcus mutans-induced aggravation of non-alcoholic steatohepatitis in mice[J]. J Oral Microbiol, 2018, 10(1): 1428005. DOI:10.1080/20002297.2018.1428005 |
| [10] |
中华医学会肝病学分会脂肪肝和酒精性肝病学组. 非酒精性脂肪性肝病诊疗指南(2010年修订版)[J]. 胃肠病学和肝病学杂志, 2010, 19(6): 483-487. Fatty Liver and Alcoholic Liver Disease Study Group of Chinese Liver Disease Association. Guidelines for diagnosis and treatment of nonalcoholic fatty liver diseases[J]. Chin J Gastroenterol Hepatol, 2010, 19(6): 483-487. DOI:10.3969/j.issn.1006-5709.2010.06.001 |
| [11] |
Saito M, Shimazaki Y, Fukai K, et al. Risk factors for tooth loss in adult Japanese dental patients:8020 Promotion Foundation Study[J]. J Invest Clin Dent, 2019, 10(2): e12392. DOI:10.1111/jicd.12392 |
| [12] |
NIDCR. Tooth loss in Adults (Age 20 to 64)[EB/OL].[2019-06-20]. https://www.nidcr.nih.gov/research/data-statistics/tooth-loss/adults#table1.
|
| [13] |
Xia Y, Gu YQ, Yu F, et al. Association between dietary patterns and metabolic syndrome in Chinese adults:a propensity score-matched case-control study[J]. Sci Rep, 2017, 6(1): 34748. DOI:10.1038/srep34748 |
| [14] |
Akinkugbe AA, Slade GD, Barritt AS, et al. Periodontitis and non-alcoholic fatty liver disease, a population-based cohort investigation in the Study of Health in Pomerania[J]. J Clin Periodontol, 2017, 44(11): 1077-1087. DOI:10.1111/jcpe.12800 |
| [15] |
Helenius-Hietala J, Suominen AL, Ruokonen H, et al. Periodontitis is associated with incident chronic liver disease-a population-based cohort study[J]. Liver Int, 2019, 39(3): 583-591. DOI:10.1111/liv.13985 |
| [16] |
Morita T, Yamazaki Y, Fujiharu C, et al. Serum γ-glutamyltransferase level is associated with periodontal disease independent of drinking habits in Japanese adults[J]. Med Sci Monit, 2014, 20: 2109-2116. DOI:10.12659/MSM.891204 |
| [17] |
Yoneda M, Naka S, Nakano K, et al. Involvement of a periodontal pathogen, Porphyromonas gingivalis on the pathogenesis of non-alcoholic fatty liver disease[J]. BMC Gastroenterol, 2012, 12: 16. DOI:10.1186/1471-230X-12-16 |
| [18] |
Cao XT. Intestinal inflammation induced by oral bacteria[J]. Science, 2017, 358(6361): 308-309. DOI:10.1126/science.aap9298 |
| [19] |
Liljestrand JM, Havulinna AS, Paju S, et al. Missing teeth predict incident cardiovascular events, diabetes, and death[J]. J Dent Res, 2015, 94(8): 1055-1062. DOI:10.1177/0022034515586352 |
| [20] |
Furuta M, Liu A, Shinagawa T, et al. Tooth loss and metabolic syndrome in middle-aged Japanese adults[J]. J Clin Periodontol, 2016, 43(6): 482-491. DOI:10.1111/jcpe.12523 |
| [21] |
周学东, 施文元. 人体口腔微生物组群与牙菌斑生物膜[J]. 华西口腔医学杂志, 2010, 28(2): 115-118. Zhou XD, Shi WY. Human oral microbial community and dental plaque biofilm[J]. West China J Stomatol, 2010, 28(2): 115-118. DOI:10.3969/j.issn.1000-1182.2010.02.001 |
| [22] |
Alam S, Mustafa G, Alam M, et al. Insulin resistance in development and progression of nonalcoholic fatty liver disease[J]. World J Gastrointest Pathophysiol, 2016, 7(2): 211-217. DOI:10.4291/wjgp.v7.i2.211 |
| [23] |
Neuschwander-Tetri BA. Non-alcoholic fatty liver disease[J]. BMC Med, 2017, 15(1): 45. DOI:10.1186/s12916-017-0806-8 |
 2020, Vol. 41
2020, Vol. 41