文章信息
- 牟笛, 崔金朝, 殷文武, 李昱, 陈秋兰.
- Mu Di, Cui Jinzhao, Yin Wenwu, Li Yu, Chen Qiulan
- 2015-2018年我国登革热暴发流行病学特征分析
- Epidemiological characteristics of dengue fever outbreaks in China, 2015-2018
- 中华流行病学杂志, 2020, 41(5): 685-689
- Chinese Journal of Epidemiology, 2020, 41(5): 685-689
- http://dx.doi.org/10.3760/cma.j.cn112338-20190715-00523
-
文章历史
收稿日期: 2019-07-15
登革热正成为威胁全球公共健康的疾病之一。尽管各国在登革热疫苗、暴发预警、媒介控制和流行控制策略等核心控制环节做了大量努力,但该病仍迅速蔓延[1]。据WHO统计,目前全球已有128个国家或地区,约39亿人口处于疾病风险之中,年发病数3.9亿人[2]。WHO将登革热排在“2019年全球健康面临最大威胁”清单中第9位,排在艾滋病之前[3]。1970-1989年,我国东南沿海地区曾多次出现较大规模的登革热暴发[4-5]。1989年后,疫情得到控制,呈整体低位散发,偶有小规模暴发态势。自2012年以来,疫情再次上升,连续7年发生较大规模的本地暴发。我国已建立了被动监测、哨点监测及媒介监测的综合监测系统,但尚无针对暴发早期的预警系统研究。为促进我国登革热防控工作,本研究对近年暴发特征进行分析,为暴发预警系统的建立提供参考。
资料与方法1.数据来源:病例个案、暴发事件来自2015-2018年中国疾病预防控制信息系统、突发公共卫生事件报告管理信息系统及病媒生物监测系统上报的登革热发病及媒介监测数据。我国31个省份报告的登革热病例信息,按照发病日期、现住址统计。
2.定义和标准[6]:①本地感染病例:发病前14 d内未离开过所在县(区),或未到过有登革热疫情报告的地区,其感染地点位于报告地区。②输入病例:包括境内和境外输入病例。境内输入病例:发病前14 d内离开本县(区)(现住址),到过本县(区)外的境内登革热流行地区的病例。境外输入病例:发病前14 d内到过登革热流行的国家或地区的病例。③暴发:1个最长潜伏期(14 d)内,在人口相对集中的地点(一个社区、居委会、村庄、学校或其他集体单位等),发生≥ 3例本地感染的登革热实验室诊断病例。④暴发持续时间:突发事件关联个案表中,首例发病病例和末例发病病例的发病时间差。⑤暴发地区分类:Ⅰ类地区为近年常有登革热暴发的省份(广东、云南、广西、海南、福建和浙江);Ⅱ类地区为近年出现过本地病例或根据伊蚊分布情况,暴发风险相对较高的省份(上海、重庆、江苏、安徽、江西、河南、湖北、湖南、四川和贵州);Ⅲ类地区为近年有输入病例报告,且有媒介伊蚊分布,具有登革热暴发风险的省份(北京、河北、山西、天津、山东、陕西和辽宁)。
3.统计学分析:应用Excel 2010和SPSS 20.0软件进行数据整理和分析,暴发持续时间采用M(P25~P75)描述,并描述疫情各类血清学检测结果、暴发发生场所、蚊媒监测结果的频数,各省份病例的性别、职业等人口学特征的频数及和采用χ2检验分析比较不同省份年龄组和职业构成比。采用ArcGIS 10.5软件绘制地图。以P < 0.05为差异有统计学意义。
结果1.全国疫情概况:2015-2018年,我国共报告登革热病例16 936例,累计死亡3人。病例主要分布在广东省(7 204例)、云南省(5 558例)、浙江省(1 584例)、福建省(1 275例)、湖南省(241例)和山东省(159例),占病例总数的94.6%(图 1)。其中本地病例12 894例,占总病例数的76.1%;输入病例主要来自于东南亚和南亚,其中缅甸(1 305例)、柬埔寨(489例)、泰国(381例)、马来西亚(265例)和菲律宾(205例)为主要输入国。72.0%的输入病例分布在云南省、广东省、浙江省、福建省、广西壮族自治区和江苏省。
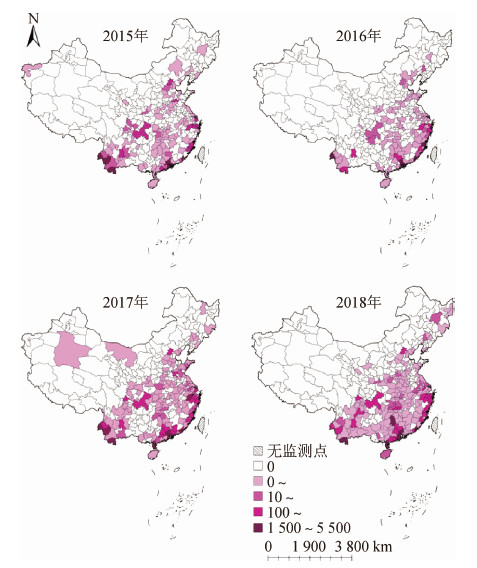
|
| 图 1 2015-2018年我国登革热报告发病数分布 |
2.暴发概况:2015-2018年全国累计报告登革热暴发111起,共涉及病例12 490例,占全国病例总数的73.7%,占本地报告病例的96.9%。
3.疫情规模及地区分布:2015-2018年全国报告登革热暴发累计县(区)数分别为15、25、39和54个,分别在广东省(77起)、云南省(14起)、浙江省(8起)、福建省(8起)、海南省(2起)、湖南省和山东省(各1起),共涉及85个县(区)。登革热暴发县(区)占各省份总县(区)的比例分别为广东(40%,48/121)、浙江(18%,16/89)、福建(13%,11/85)、海南(9%,2/23)、云南(5%,6/129)、湖南(1%,1/122)和山东(1%,1/139),差异有统计学意义(χ2=12.820,P < 0.001)。其中云南省瑞丽市和广东省佛山市顺德区、广州市海珠区连续4年均有暴发报告,云南省景洪市和勐腊县,广东省广州市白云区、花都区、南海区、南沙区、天河区、湘桥区和越秀区4年中有3年发生暴发。见图 2。
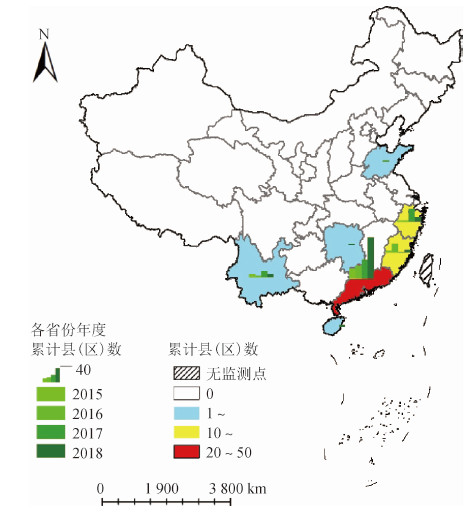
|
| 图 2 2015-2018年我国各省份登革热暴发病例数及波及县(区)数 |
2015-2018年,病例数>1 000例的大规模暴发有4起,分别为云南省景洪市(2015年1 046例和2017年1 040例)、广东省潮州市(2015年1 382例)、浙江省杭州市(2017年1 138例)(表 1)。涉及的省份依次为广东(5 166例)、云南(4 943例)、浙江(1 226例)、福建(971例)、湖南(96例)、山东(79例)和海南(9例),分别占各省份报告病例总数的72.0%、89.0%、77.0%、76.0%、40.0%、50.0%和23.0%(表 1,图 3)。
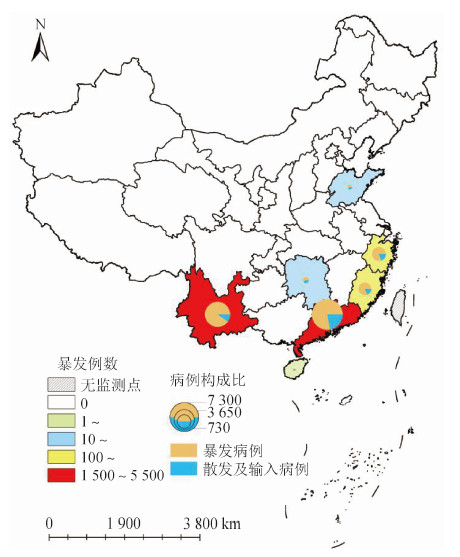
|
| 图 3 2015-2018年我国登革热暴发病例地区分布与病例构成比情况 |
4.暴发时间分布:2015-2018年,全国分别报告暴发13、20、27和51起。暴发集中在5-11月,其中9月最多,共报告36起,其次8月报告27起。病例≤ 10例的小规模暴发多于30 d内终止(82.4%,28/34),较大规模的暴发可持续数月。Ⅰ类省份中,云南省暴发自5月开始,明显早于其他省份,报告高峰为5-7月,病例>100例的暴发持续时间的M(P25~P75)为139(103~210)d,较大规模疫情多延续至当年11月底至12月;广东省暴发自6月下旬始,报告高峰为7-9月,报告病例数>100例的疫情持续时间的M(P25~P75)为111(40~173)d,较大规模疫情多持续至11月,偶尔持续至12月上旬;福建和浙江省疫情集中于7-9月,基本于10月终止,偶尔持续至11月初,有2个省各发生1起病例>100例的较大规模疫情,其中浙江省疫情持续时间为110 d,福建省为31 d;湖南和山东省分别发生1起暴发,于2018年9月初和2017年8月中旬发生,持续时间分别为27 d和28 d,于9月底和9月中旬终止。
5.血清学检测:共95起疫情报告血清学检测结果,其中流行株为1型的暴发46起,2型的暴发21起,3型的暴发1起,同时检出3种血清型的暴发2起,同时检出4种血清型的暴发1起。广东和云南省均发现有≥ 2年时间的流行株血清型一致的情况(1型和2型)。
6.疫情溯源及暴发场所:仅3起疫情通过分子学检测方法实现了疫情溯源,其中2起由东南亚输入病例引发,1起由外省输入病例引发。有67起暴发报告了疫情发生的主要场所,其中30起暴发来自社区、城中村或群租房等人口密集、卫生环境较差的城市居民区,12起疫情来自乡村或农场等乡镇人群聚居地,11起来自建筑工地,5起来自市场、商业街、健身房等人流量大的商业服务区域。
7.人口学特征:除山东省的男女性别比为0.68:1外,其余各省份的男女性别比均为1:1。整体上,25~34岁占21.0%,35~44岁占18.0%,45~54岁占17.0%,广东、云南、浙江、福建和湖南省的病例年龄组构成差异有统计学意义(χ2=1 084.068,P < 0.001)。职业上,家务及待业占20.0%,商业服务占16%.0,农民占13.0%,广东、云南、浙江和福建省病例的职业构成差异有统计学意义(χ2=3 805.576,P < 0.001)。
讨论本研究发现,2015-2018年我国登革热疫情呈现以暴发为主,输入及本地散发病例并存的态势。疫情仍高度集中在Ⅰ类省份,输入疫情来源国以东南亚地区为主,与既往登革热疫情特征相同[6-8]。有限的溯源分析结果提示,我国登革热暴发由输入病例引起。
登革热暴发报告起数及累计县(区)范围逐年增多,整体呈扩散趋势且向高纬度地区蔓延。暴发呈高度时空聚集特征,主要集中在Ⅰ类省份部分县(区),时间集中在5-11月,特别是7-9月;Ⅱ、Ⅲ类省份亦可发生较大规模暴发;同地区不同年度主要流行株呈现一致性。云南和广东省登革热暴发持续时间长于其他省份。暴发多发生在卫生条件较差且人口密度大的区域。不同省份间病例年龄、人群分布差异有统计学意义。
近年我国登革热报告发病数并未显著上升,但暴发在地域上呈扩散趋势,可能因为气候变迁导致的埃及伊蚊扩散,人口流动性增加,尤其是城市人口快速增长和城市化扩张,导致媒介孳生空间增加[9]。我国的埃及伊蚊分布已扩展至北纬24°左右,白纹伊蚊则在我国广泛分布[10-11]。2015-2018年我国城镇化率由56.1%上升至59.6%[12],且在2014年疫情高峰后,我国各级政府加强了登革热防控工作[13],登革热监测系统灵敏度升高也可能是相关因素。
根据我国暴发疫情的流行病学特征,可将暴发疫情大致分为口岸型、乡村型和城市型。口岸型以云南省为代表,疫情高度集中于口岸地区,疫情规模、持续时间与输入疫情水平密切相关,最初疫点多为人员复杂的市场,呈多点暴发;乡村型以山东省嘉祥县和湖南省祁阳县为代表,疫情由外地务工人员返乡后播散,疫情早期扩散迅速,但如果疫区与其他聚集性住宅区相隔较远,可形成地理屏障,疫情规模得以局限;城市型以杭州和福州市为代表,疫情由单一或少量疫点起始,并以此为中心迅速向四周扩散,疫情后期,首发疫点已鲜有病例报告,但外周不断出现新发疫点,防控难度大,疫情往往持续至气温下降。
Ⅰ类省份仍为我国登革热暴发重点,但Ⅱ、Ⅲ类省份均具备暴发条件。各省可根据本省暴发特点,重点布置防控工作。建议在暴发高峰来临前,开展媒介抗药性评估及媒介孳生地调查、医务人员培训及防蚊防病宣教工作,至高峰期结束前均应保持警惕。发病人群中,家务及待业和农民均占较高比例,提示宣教方式应以简明易懂为主,突出行为指导功能,可选用横幅、短信、小视频等重点人群接受度较高的宣教途径。城中村、工地、老旧社区疫情暴发风险较高,应作为防控重点,必要时可提前开展孳生地清理。对于云南省等口岸型为主的省份,建议在基本防控策略的基础上,着重加强出境人员宣教和入境人员症状监测,如有条件建议开展与周边国家的疫情通报和联防联控,将防控关口前移,尽量降低本地传播机会。浙江、广东省等城市型为主的省份,建议在疫情高峰期来临前开展医务人员培训,提高监测系统灵敏性,以及时发现和控制疫情;及时发布疫情通报,避免城区间输出和扩散。劳务输出为主的地区,发生乡村型疫情的风险较高,除做好疫情处置外,应避免疫情突破城乡界限传入邻近城区。
本研究存在不足。数据源于监测报告,无法避免报告意识和能力的影响。且未能观察到干预措施的及时性、有效性对暴发规模的影响。再者,本研究获得的蚊媒监测数据有限,不足以开展有关疫情暴发与媒介密度的关联分析。本研究仍为我国登革热暴发研究提供了本底数据,有助于进一步研究暴发早期预警和输入引起暴发的可能因素。
综上所述,我国登革热暴发呈地域扩散、甚至向高纬度扩散态势,不同省份暴发特征各异,总体分为口岸型、乡村型和城市型,各省应针对性调整防控策略。
利益冲突 所有作者均声明不存在利益冲突
志谢 本研究得到各省、市、县级CDC的积极支持
| [1] |
Runge-Ranzinger S, Kroeger A, Olliaro P, et al. Technical handbook for dengue surveillance, dengue outbreak prediction/detection and outbreak response ("model contingency plan")[M]. Geneva: World Health Organization, 2016.
|
| [2] |
Brady OJ, Gething PW, Bhatt S, et al. Refining the global spatial limits of dengue virus transmission by evidence-based consensus[J]. PLoS Negl Trop Dis, 2012, 6(8): e1760. DOI:10.1371/journal.pntd.0001760 |
| [3] |
WHO. Ten threats to global health in 2019[EB/OL]. (2019-02-20)[2019-07-01]. https://www.who.int/emergencies/ten-threats-to-global-health-in-2019.
|
| [4] |
黎正伦. 海南省昌江县第2次登革热流行与防制[J]. 中国媒介生物学及控制杂志, 2000, 11(4): 303-306. Li ZL. The 2nd Dengue epidemic and prevention in Changjiang, Hainan[J]. Chin J Vector Biol Control, 2000, 11(4): 303-306. DOI:10.3969/j.issn.1003-4692.2000.04.025 |
| [5] |
王永亮, 钱成, 左锋. 中国内陆口岸登革热流行势态及风险评述[J]. 口岸卫生控制, 2018, 23(5): 17-22. Wang YL, Qian C, Zuo F. A review on the prevalence and risk of dengue fever in China's Inland ports[J]. Port Health Control, 2018, 23(5): 17-22. DOI:10.3969/j.issn.1008-5777.2018.05.004 |
| [6] |
Lai SJ, Huang ZJ, Zhou H, et al. The changing epidemiology of dengue in China, 1990-2014:a descriptive analysis of 25 years of nationwide surveillance data[J]. BMC Med, 2015, 13: 100. DOI:10.1186/s12916-015-0336-1 |
| [7] |
牟笛, 李昱, 殷文武, 等. 中国登革热病例流行病学特征及传播媒介监测数据分析[J]. 国际病毒学杂志, 2016, 23(3): 177-180, 196. Mu D, Li Y, Yin WW, et al. Analysis on the epidemiological characteristics of dengue fever in China[J]. Int J Virol, 2016, 23(3): 177-180, 196. DOI:10.3760/cma.j.issn.1673-4092.2016.03.009 |
| [8] |
牟笛, 何泱霓, 陈秋兰, 等. 我国2016年登革热输入和本地病例流行病学特征比较[J]. 疾病监测, 2017, 32(3): 184-189. Mu D, He YN, Chen QL, et al. Comparison of epidemiological features between imported and indigenous dengue fever cases in China[J]. Dis Surveill, 2017, 32(3): 184-189. DOI:10.3784/j.issn.1003-9961.2017.03.004 |
| [9] |
WHO. Summary of evaluation of dengue strategic plan for the Asia pacific region 2008-2015[EB/OL].(2016-10-14)[2019-07-15]. https://iris.wpro.who.int/handle/10665.1/13457.
|
| [10] |
谢晖, 周红宁, 杨亚明. 我国登革热重要媒介埃及伊蚊的研究进展[J]. 中国媒介生物学及控制杂志, 2011, 22(2): 194-197. Xie H, Zhou HN, Yang YM. Advances in the research on the primary dengue vector Aedes aegypti in China[J]. Chin J Vector Biol Control, 2011, 22(2): 194-197. |
| [11] |
樊景春, 刘起勇. 气候变化对登革热传播媒介影响研究进展[J]. 中华流行病学杂志, 2013, 34(7): 745-749. Fan JC, Liu QY. Research progress on the effect of climate change on dengue vector[J]. Chin J Epidemiol, 2013, 34(7): 745-749. DOI:10.3760/cma.j.issn.0254-6450.2013.07.020 |
| [12] |
国家统计局.中国统计年鉴2018年[EB/OL]. (2019-01-01)[2019-02-20]. http://www.stats.gov.cn/tjsj/ndsj/2018/indexch.htm. National Bureau of Statistics of China. China Statistical Yearbook 2018[EB/OL]. (2019-01-01)[2019-02-02]. http://www.stats.gov.cn/tjsj/ndsj/2018/indexch.htm. |
| [13] |
中国疾病预防控制中心.登革热防治技术指南(2014版)[EB/OL]. (2014-09-29)[2019-02-20]. http://www.chinacdc.cn/jkzt/crb/zl/dgr/jszl_2235/201409/t20140929_104958.html. Chinese Centre for Disease Control and Prevention. Guideline for dengue prevention and control[EB/OL]. (2014-09-29)[2019-02-20]. http://www.chinacdc.cn/jkzt/crb/zl/dgr/jszl_2235/201409/t20140929_104958.html. |
 2020, Vol. 41
2020, Vol. 41



