文章信息
- 王莹, 尤心怡, 王奕婧, 彭丽萍, 杜志成, Gilmour Stuart, Yoneoka Daisuke, 顾菁, 郝春, 郝元涛, 李菁华.
- Wang Ying, You Xinyi, Wang Yijing, Peng Liping, Du Zhicheng, Gilmour Stuart, Yoneoka Daisuke, Gu Jing, Hao Chun, Hao Yuantao, Li Jinghua
- 中国新型冠状病毒肺炎疫情基本再生数评估
- Estimating the basic reproduction number of COVID-19 in Wuhan, China
- 中华流行病学杂志, 2020, 41(4): 476-479
- Chinese Journal of Epidemiology, 2020, 41(4): 476-479
- http://dx.doi.org/10.3760/cma.j.cn112338-20200210-00086
-
文章历史
收稿日期: 2010-02-10
2. 圣路加国际大学公共卫生学院, 东京104-0045, 日本;
3. 中山大学全球卫生研究中心, 广州 510275
2. Graduate School of Public Health, St. Luke's International University, Tokyo 104-0045, Japan;
3. Sun Yat-sen Global Health Institute, Sun Yat-sen University, Guangzhou 510275, China
2019年12月,湖北省武汉市发生不明原因肺炎疫情,流行病学调查发现,大部分病例与华南海鲜批发市场有关联[1],该市场存在出售野生动物的非法行为[2]。经检测,国家卫生健康委表示,收治的患者对常见的呼吸道病毒和细菌检测呈阴性,但对一种新型冠状病毒检测呈阳性[3]。患者常见体征有呼吸道症状、发热、咳嗽、气促和呼吸困难等,重症患者中,病毒感染可导致肺炎、严重急性呼吸综合征、肾衰竭,甚至死亡。病毒分离后,研究者们对其进行了基因组测序,WHO初步将新型冠状病毒所致肺炎命名为COVID-19[4]。
在“不明原因的病毒性肺炎”病原体初步判定为新型冠状病毒后,国家、省市专家组立即对COVID-19诊疗、监测等方案进行了修订和完善,于1月10日确认,武汉市已有累计41例病例被确诊为新型冠状病毒感染,截至2月8日24:00,全国31个省份累计确诊病例已上升至37 198例[5],累计死亡病例811例,确诊人数远超2003年SARS感染病例数。
目前,全国范围内确诊和疑似病例的数量仍在增加。基本再生数(basic reproduction number,R0)是决定传染病内在传播率的最重要参数,是指没有干预的情况下,全部是易感人群的环境中,平均一个患者可以传染的人数[6]。及时准确评估COVID-19的R0对于评估病毒的传播能力、预测未来流行趋势以及调整一系列控制措施具有重要意义。但目前相关R0的研究均基于发病早期的疫情通报数据计算得出,早期报告的病例数据可能存在较大波动,由此计算得出的数值也可能存在不稳定性,同时自1月23日武汉市政府宣布城市各类交通工具出行限制后,COVID-19的传播率可能发生了一定变化。因此,本研究旨在利用疫情通报相对稳定后的病例数据计算COVID-19的R0值,并且对政府控制措施实施前后R0值的变化进行评估,将所得结果与已有相关研究的结果进行比较分析。
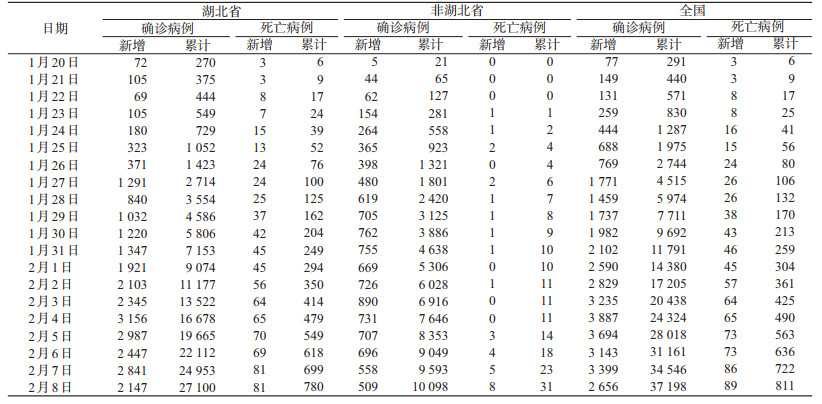
资料与方法本研究收集2020年1月17日到2月8日24:00国家卫生健康委员会报告的湖北省每天确诊COVID-19病例数等数据(表 1)。根据Li等[1]对COVID-19潜伏期的分析显示潜伏期均值为5.2(95%CI:4.1~7.0)。分别采用指数增长方法(exponential growth,EG)、极大似然法(maximum likelihood estimation,ML)、序贯贝叶斯方法(sequential Bayesian method,SB)和时间相关基本再生数(time dependent reproduction numbers,TD)计算得R0[7]。此外,湖北省各个城市分别于1月23-24日开始实施封城措施,本研究也计算了封城控制期间R0的估计值。
EG方法通过暴发早期的发病人数指数增长率与时间分布来估算R0值[8]。计算公式: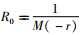
ML方法通过各个时间点报告的发病数以及时间来估算R0值[9]。计算公式: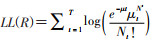
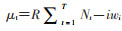
SB方法通过感染期的平均持续时间来估算R0值,并且每一时点R0的先验分布都是上一时点的后验分布[10],在t+1时刻的发病数Nt+1近似于Nte(γ(R-1))均值的泊松分布,其中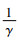
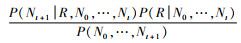
TD方法通过计算所有符合观察实际的传播网络的平均传播情况来估算R0值[11]。在ti时发病的病例i是由在tj时发病的病例j传染的概率为Pij,Pij= 


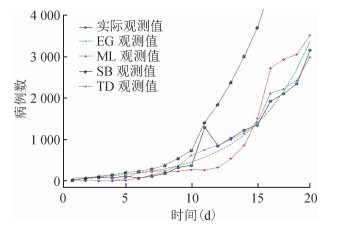
根据湖北省1月17日到2月8日每天确诊的COVID-19病例数(表 1),EG计算得R0=3.49(95%CI:3.42~3.58);ML计算得R0=2.99(95%CI:2.93~3.06);SB和TD方法计算得R0=2.80(95%CI:2.42~3.15)和4.48(95%CI:4.26~4.71)。由观测到的病例数和4种方法预测病例数的拟合情况(图 1)可知,EG方法的拟合效果最优。
|
| 图 1 观测病例数和4种方法预测的病例数的拟合情况 |
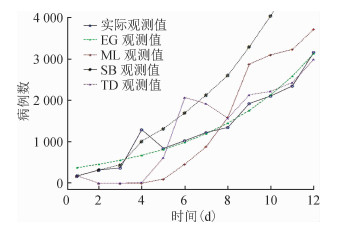
湖北省的各个城市分别于2020年1月23-24日开始实施封城措施,收集1月24日开始到2月8日期间每天确诊的COVID-19病例数,计算有效控制阶段R0的估计值。EG计算得R0=2.95(95%CI:2.86~3.03);ML计算得R0=3.16(95%CI:3.09~3.23);SB和TD方法计算得R0=2.65(95%CI:2.45~2.85)和3.61(95%CI:3.52~3.70)。由观测病例数和4种方法预测病例数的拟合情况(图 2)可知,EG方法的拟合效果最优。
|
| 图 2 控制阶段观测病例数和4种方法预测的病例数的拟合情况 |
全国范围内COVID-19的病例数在持续增加,本研究收集1月17日到2月8日期间国家卫生健康委报告的湖北省每天确诊病例数等数据,采用EG、ML、SB和TD方法评估COVID-19的R0值,评估COVID-19的传播速率,为疾病的预防和控制提供科学依据。
R0是判断传染病是否流行的重要参量,R0值越大,代表该类传染病传播速度越快。由观测病例数和4种方法预测的病例数的拟合情况可知,EG方法的拟合效果最好,估算的R0值为3.49(95%CI:3.42~3.58)。在COVID-19流行初期,确诊人数呈现指数增长,采用EG方法通过疫情暴发初期的发病人数指数增长率与时间分布来估算的R0最为准确。目前,国内外多个团队对COVID-19的R0进行了模型预测,周涛等[13]利用截至1月26日凌晨确诊和疑似病例数等数据,采用SEIR仓室模型预测COVID-19早期的R0值在2.8~3.3之间。基于2019年12月到2020年1月期间425例确诊患者数据[1],参考SARS的一些参数,估计COVID-19的R0值为2.2(95%CI:1.4~3.9)。还有一些研究估算的R0值在2.1~3.6之间[14-18]。本研究估算的R0值高于之前的研究,可能因为随着纳入确诊病例数等数据的时间范围变长,在传染病流行初期处于潜伏期和疑似病人被确诊,病例数处于稳定增长的阶段,此时得到R0值更为准确。
湖北省多个城市分别于1月23-24日开始实施封城措施,在封城控制期间,EG方法估算COVID-19的R0值为2.95(95%CI:2.86~3.03),相较整体有明显的降低,同时也低于Wallinga等[11]估算重症急性呼吸综合征SARS的R0值(3.1~4.2)。尽管在湖北省采取封城措施之前,有一部分人已经离开了湖北,使封城的有效性降低,但是该措施仍在一定程度上有效减少了湖北省内各市区之间的感染以及省外的新增感染。在封城控制期间,公众的综合行为发生改变,开始佩戴口罩,减少外出等等。同时各专业技术机构、宣传系统和媒体大力开展科普宣传,提高了公众健康意识和自我防护能力,相关部门对疑似患者采取隔离措施及患者做好隔离治疗,进一步降低了COVID-19的传播速度。
本研究采用不同方法计算得到湖北省COVID-19的R0值,评估了COVID-19的传播能力,且对封城控制措施实施前后的R0值进行了对比。在传染病流行初期,适合采用EG方法估算的R0,采用封城措施后,R0值相较之前有明显的降低,说明封城的控制手段有效降低了病毒传播速率。该研究为进一步的疫情分析提供了重要参数,包括疫情控制措施的实施效果的评价、未来疫情流行趋势的预测等,同时也为控制措施的调整提供科学依据。
利益冲突 所有作者均声明不存在利益冲突
| [1] |
Li Q, Guan XH, Wu P, et al. Early transmission dynamics in Wuhan, China, of novel coronavirus-infected pneumonia[J]. N Engl J Med, available online 2020 Jan 29. DOI: 10.1056/NEJMoa2001316.
|
| [2] |
Hui DS, Azhar EIA, Madani TA, et al. The continuing 2019-nCoV epidemic threat of novel coronaviruses to global health-The latest 2019 novel coronavirus outbreak in Wuhan, China[J]. Int J Infect Dis, 2020, 91: 264-266. DOI:10.1016/j.ijid.2020.01.009 |
| [3] |
中华人民共和国国家卫生健康委员会卫生应急办公室.武汉市卫生健康委关于不明原因的病毒性肺炎情况通报[EB/OLR]. (2020-01-11)[2020-02-09]. http://www.nhc.gov.cn/xcs/yqtb/202001/1beb46f061704372b7ca41ef3e682229.shtml. Health Emergency Office, National Health Commission of the People's Republic of China. Emergency notification of unknown pneumonia reported by Wuhan Municipal Health Commission[EB/OLR]. (2020-01-11)[2020-02-08]. http://www.nhc.gov.cn/xcs/yqtb/202001/1beb46f061704372b7ca41ef3e682229.shtml. |
| [4] |
World Health Organization. WHO, Disease outbreak news, 2020. Novel Coronavirus-China: Disease outbreak news[EB/OL]. (2020-01-12)[2020-02-09]. https://www.who.int/csr/don/12-january-2020-novel-coronavirus-china/en/.
|
| [5] |
中华人民共和国国家卫生健康委员会卫生应急办公室.新型冠状病毒肺炎疫情最新情况[EB/OLR]. (2020-02-08)[2020-02-08]. http://www.nhc.gov.cn/xcs/xxgzbd/gzbd_index.shtml. Health Emergency Office, National Health Commission of the People's Republic of China. The latest situation of new coronavirus pneumonia[EB/OLR]. (2020-02-08)[2020-02-08]. http://www.nhc.gov.cn/xcs/xxgzbd/gzbd_index.shtml. |
| [6] |
Roy M, Anderson RM, Robert M, et al. Infectious diseases of humans; dynamics and control[M]. OxfordUS: Oxford University Press.
|
| [7] |
Obadia T, Haneef R, Bo?lle PY. The R0 package:a toolbox to estimate reproduction numbers for epidemic outbreaks[J]. BMC Medical Informatics and Decision Making, 2012, 12(1): 147. DOI:10.1186/1472-6947-12-147 |
| [8] |
Wallinga J, Lipsitch M. How generation intervals shape the relationship between growth rates and reproductive numbers[J]. Proc Biol Sci, 2007, 274(1609): 599-604. DOI:10.1098/rspb.2006.3754 |
| [9] |
White LF, Pagano M. A likelihood-based method for real-time estimation of the serial interval and reproductive number of an epidemic[J]. Stat Med, 2008, 27(16): 2999-3016. DOI:10.1002/sim.3136 |
| [10] |
Bettencourt LM, Ribeiro RM. Real time bayesian estimation of the epidemic potential of emerging infectious diseases[J]. PLoS One, 2008, 3(5): e2185. DOI:10.1371/journal.pone.0002185 |
| [11] |
Wallinga J, Teunis P. Different epidemic curves for severe acute respiratory syndrome reveal similar impacts of control measures[J]. Am J Epidemiol, 2004, 160(6): 509-516. DOI:10.1093/aje/kwh255 |
| [12] |
Nikbakht R, Baneshi MR, Bahrampour A, et al. Comparison of methods to Estimate Basic Reproduction Number (R0) of influenza, Using Canada 2009 and 2017-18 A (H1N1) Data[J]. J Res Med Sci, 2019, 24: 67. DOI:10.4103/jrms.JRMS_888_18 |
| [13] |
Zhou T, Liu QH, Yang ZM, et al. Preliminary prediction of the basic reproduction number of the Wuhan novel coronavirus 2019-nCoV[EB/OL]. (2020-01-30)[2020-02-08]. https://arxiv.org/ftp/arxiv/papers/2001/2001.10530.pdf.
|
| [14] |
Read JM, Bridgen JRE, Cummings DA, et al. Novel coronavirus 2019-nCoV: early estimation of epidemiological parameters and epidemic predictions[EB/OL]. (2020-01-24)[2020-02-08]. https://www.medrxiv.org/content/10.1101/2020.01.23.20018549v1.full.pdf.
|
| [15] |
Zhao S, Ran JY, Ran JJMusa S, et al. Preliminary estimation of the basic reproduction number of novel coronavirus (2019-nCoV) in China, from 2019 to 2020:A data-driven analysis in the early phase of the outbreak[J]. Int J Infect Dis, . bioRxiv, 2020, 92: 214-217. DOI:10.1016/j.ijid.2020.01.050 |
| [16] |
Zhao S, Musa SS, Lin QY, et al. Estimating the unreported number of novel coronavirus (2019-nCoV) cases in china in the first half of January 2020:a data-driven modelling analysis of the early outbreak[J]. J Clin Med, 2020, 9(2): 388. DOI:10.3390/jcm9020388 |
| [17] |
Imai N, Cori A, Dorigatti I, et al. Report 3: Transmissibility of 2019-nCoV[EB/OL]. (2020-01-24)[2020-02-08]. https://www.imperial.ac.uk/media/imperial-college/medicine/sph/ide/gida-fellowships/Imperial-2019-nCoV-transmissibility.pdf.
|
| [18] |
Wu Joseph T, Leung K, Leung G M. Nowcasting and forecasting the potential domestic and international spread of the 2019-nCoV outbreak originating in Wuhan, China: a modelling study[J]. Lancet, available online 31 Jan 2020. DOI: 10.1016/S0140-6736(20)30260-9.
|
 2020, Vol. 41
2020, Vol. 41