文章信息
- 高乐, 于树青, 周庆欣, 马峻岭, 詹思延, 孙凤.
- Gao Le, Yu Shuqing, Zhou Qingxin, Ma Junling, Zhan Siyan, Sun Feng
- 我国结直肠癌筛查循证指南关键问题清单的构建
- Construction of key question list in the evidence-based guidelines for colorectal cancer screening in China
- 中华流行病学杂志, 2020, 41(2): 267-272
- Chinese Journal of Epidemiology, 2020, 41(2): 267-272
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2020.02.022
-
文章历史
收稿日期: 2019-04-10
2. 北京大学肿瘤医院暨北京市肿瘤防治研究所流行病学研究室 100141;
3. 北京大学循证医学中心 100191
2. Department of Cancer Epidemiology, Peking University Cancer Hospital and Institute, Beijing 100141, China;
3. Center of Evidence-based Medicine and Clinical Search, Peking University, Beijing 100191, China
结直肠癌(colorectal cancer,CRC)是发达国家的高发癌症之一。美国、加拿大和澳大利亚等国家已提出了CRC防控策略[1-3],如早诊、筛查、改变生活方式等,也针对CRC筛查制订了相应的高质量筛查指南,并在指南的指导下,开展了大规模的筛查项目[4]。过去几十年中,美国、加拿大、澳大利亚等国家的CRC筛查取得了显著的效果[5-6],CRC的发病与死亡情况都在逐年改善,这很大程度上得益于筛查指南的良好执行[7-8]。
但是,我国的CRC疾病负担却在日益加重。据WHO数据显示,2018年我国CRC发病率与死亡率均高于世界平均水平;与美国、澳大利亚等发达国家相比,CRC发病率明显偏低,但死亡率却与之相当[9]。同时,根据我国癌症登记中心数据[10-18],1989-2015年,CRC发病率与死亡率持续上升,目前仍是我国疾病负担较重的前五位癌症之一。在CRC防控方面,我国有多部CRC筛查共识意见颁布[19-21],但其推荐意见存在一些差异,给实际决策增加了难度。近年来,我国也在逐步开展CRC筛查项目,如“城市癌症早诊早治项目”以及在部分省市设立的CRC筛查试点。
上述证据表明,我国尚未对CRC筛查形成可达成共识的明确过程,也缺乏系统性证据整合方式,即我国尚未形成高质量的CRC筛查指南,且CRC筛查参与人数少、覆盖范围窄,防控形势依然严峻。因此,有必要建立适合我国国情的系统、完善的指南制订体系,来形成高质量的筛查指南,并推荐其运用于临床实践中。本研究旨在通过参考国外高质量CRC筛查指南,提炼并补充CRC筛查循证指南关键问题清单,为指南制订提供一个较为清晰的思路。
研究方法1.系统综述:本研究在前期研究的基础上,对所有纳入的CRC筛查指南进行了是否为循证指南的判断。按照WHO指南制订标准[22],对循证指南做出如下定义:形成研究问题、进行文献系统综述、评价证据质量并给出推荐强度等级。同时符合上述3个步骤者为循证指南。对筛选出的循证指南的基本信息、推荐意见形成过程、关键问题及其回答方法进行整理。对于关键问题的结局指标,根据各指南纳入考虑频率将其划分为主要结局和次要结局。
2. Delphi专家论证:根据对已有循证指南关键问题的梳理,形成关键问题清单,通过Delphi法进行专家论证,形成最终清单。
(1)专家选择:消化道肿瘤或流行病及循证医学专家,对CRC筛查或循证指南的制订有一定了解(专家对问卷各条目的平均熟悉程度在“一般”及以上)。函询专家一部分为国内已有CRC筛查指南专家组成员(通过论著收集邮箱信息),另一部分为中国医师协会循证医学专业委员会成员。在人数方面,以15~50人左右为宜[23],通过一次性邮件发送问卷链接。
(2)统计学分析:①专家一般信息:年龄、职称等;②专家积极系数:问卷的有效回收率;③专家意见集中程度:各条目“重要性”百分比,通常大于满分的75%表明意见较为集中,可考虑纳入最终框架;④专家意见协调程度:各条目“重要性”得分的四分位数间距、标准差和变异系数;⑤专家权威程度:主要通过专家自评得到。运用专家权威系数(Cr)对专家的权威程度进行判断。该系数可通过专家对各条目的判断依据(Ca)和专家对各条目的熟悉程度(Cs)进行计算。计算公式为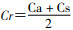
1.文献筛选结果:数据库检索共得到36 097篇文献,经过筛选后得到英文指南29篇,中文指南3篇。补充检索网站以及搜索引擎得到中英文指南共14篇。经过对上述46部指南的判断,本研究总计纳入8部符合定义的循证指南。
2.循证指南推荐内容:6部指南对一般风险人群的筛查方式进行了推荐[26-36]。加拿大预防保健工作组(Canadian Task Force on Preventive Health Care,CTFPHC)和美国预防服务工作组(U.S. Preventive Services Task Force,USPSTF)制订的指南对不同年龄段人群筛查给出了对应的推荐强度说明,同时也给出了不同的筛查方式及筛查间隔推荐,但并未对各筛查方式的推荐强度给出明确意见。推荐筛查年龄大多为50~75岁,筛查方式主要为基于粪便的检测(粪潜血试验、粪便免疫化学检测、粪便DNA)、结肠镜、可曲乙状结肠镜、CT结肠镜等;筛查间隔方面,粪便检测多为每1~3年1次,各种结肠镜筛查间隔较长,通常为每5~10年1次。这些循证指南间还存在一定的差异,如CTFPHC不推荐将结肠镜作为一种筛查工具,而其余大多数指南均对结肠镜筛查进行了推荐;不同工具的推荐筛查间隔也存在一定差异。此外,仅韩国的指南提到了根据筛查结果确定后续的监测间隔[28]。
共有4部循证指南针对高风险人群进行了推荐[30-33],但各指南对高危人群进行推荐时的分类略有不同。3部指南主要关注了有家族史的人群[30-32],1部还对有炎症性肠病个人史的高风险人群进行了推荐[33]。暂无指南针对腺瘤性息肉和无柄锯齿状息肉个人史进行推荐。
3.各循证指南关键问题:本研究定义的循证指南中的关键步骤之一是进行系统的文献检索,因此这些指南主要证据体是系统综述和(或)Meta分析。在这些指南中,关键问题的制订基本按照PICO原则制订。在筛查人群选择方面,各指南考虑的主要问题集中在筛查起止年龄、CRC患病风险(一般风险人群和高风险人群)、以及不同性别、种族、经济条件下筛查结果的差异等;在筛查工具的选择方面,各指南考虑的筛查工具不尽相同;在比较组方面,主要是筛查与不筛查或者是其他筛查工具进行比较;在结局方面,各循证指南主要关注流行病学情况、筛查的获益、筛查的风险、人群偏好、费用等方面。
4.关键问题清单的构建:根据对循证指南的系统梳理,形成了我国CRC筛查循证指南关键问题初步清单(表 2),结合各环节的结局指标,通过专家咨询,确定各条目的重要性,最终形成能够为我国CRC筛查循证指南制订所用的关键问题清单。
5. Delphi法的可靠性评估:
(1)专家一般信息:34名有效函询专家的平均年龄为42.97岁,其中17名专家的专业方向为流行病学或循证医学,其余专家来自肿瘤学、消化学、外科学、内镜学等临床领域。各专家的专业技术职称分布较为均匀;大多数专家(64.71%)的最高学历为博士,其次为硕士(29.41%);从事相关领域的年限分布也较为均匀;约一半的专家报告对该问卷内容整体熟悉程度为一般熟悉,其余专家的熟悉程度为较熟悉及熟悉。
(2)专家积极系数:流行病与循证医学领域专家有效问卷回收率为37.78%;临床领域专家有效问卷回收率为14.29%。
(3)专家意见集中及协调程度:见表 2。各条目重要性的平均值均大于满分的75%,所有20个小条目均符合纳入要求;专家对各条目重要性评分的变异系数在0.08~0.27之间,均<0.3,表明专家的意见较为集中。
(4)专家权威程度:经过计算,专家判断系数为0.87,对各条目的平均熟悉程度为0.75,计算得出Cr=0.81>可接受值(0.70),表明接受函询的专家权威程度较高。
6.关键问题清单介绍:所有6个维度20个小条目经过专家咨询均较为重要,且专家意见较为集中,关键问题框架无变动,因此未进行第二轮专家咨询。各条目内容见表 2。其中维度4筛查方法是指南制订过程中很重要的一部分内容,是对筛查的具体评价。
讨论本研究在国外已有循证筛查指南的基础上,拟定了可运用于我国CRC筛查循证指南制订的关键问题清单,清单包含流行病学问题、人群风险分类、筛查起止年龄、筛查方法、实施相关情况及参与指南制订人员确定,共6个维度20个小条目。国外现有的8部循证指南少有将维度1、2、5和6纳入关键问题考虑,其中仅4部指南考虑了维度3,且极少将维度4涉及的获益风险整体评价纳入考虑,也没有指南将在本土进行筛查的特殊性纳入关键问题考虑,但对于常见的研究问题如筛查有效性、安全性、准确性等方面,大多数指南进行了考虑。而本研究形成的关键问题清单对已有循证指南进行了补充,考虑的内容更为全面。
虽然CRC筛查已达成一定共识,但仍存在许多争议,如筛查年龄、部分筛查方法以及亚太地区人群CRC风险等[34]。此外,有学者总结了我国现有研究中的CRC筛查依从率,范围从9%~30%不等[35];同时对可能的影响因素进行了分析提出,筛查供方的作用不能被忽视。在筛查实施的过程中,一部高质量的指南能够指导医疗工作者在实践中给出合适的推荐意见,这也会在一定层面上增加筛查的参与率。因此,未来我们需要制订适合我国国情的CRC筛查循证指南,以达到降低CRC发病率和死亡率的目的。
我国CRC的疾病负担日益严峻,CRC筛查指南的质量也亟待提高。我国CRC筛查指南的制订应该严格遵循被广泛认可的指南制订流程,如WHO指南制订手册[22]等。在制订我国CRC筛查循证指南时,可以先提出关键问题,对现有的高质量指南进行梳理,挑选能够回答上述关键问题(如维度3及维度4的大部分条目等)的指南进行改编[36];对于无法通过已有指南解决的关键问题(如维度4的条目6及条目9等),需要进行原始文献的系统综述,最终形成明确的推荐意见。
本研究的优势在于通过专家论证的方式,确立了CRC筛查循证指南关键问题清单,为后续我国癌症筛查循证指南的制订提供了一个较为清晰的思路,有助于CRC筛查循证指南乃至癌症筛查领域循证指南制订的工作推进。同时本研究也存在局限性。在进行Delphi专家论证时,由于未事先确定专家组、仅根据已有指南的专家组成员选择临床专家以及采用邮件形式进行调查等原因,应答率较低,研究结果的效力有待进一步提高;此外,由于条件所限,仅基于国外文献经临床及流行病学专家进行论证,未考虑对利益相关者(循证指南制订者、指南用户、卫生政策制订者、目标人群等)进行调查,其适用性可能存在一定不足。
综上所述,本研究为CRC筛查指南制订提供了较为系统的关键问题检索目标,该清单也适用于其他癌症筛查循证指南的制订,但需要在文献检索过程中,根据不同癌症的特异性,确定其特殊的风险分类及研究结局,修订为有针对性的检索策略。
利益冲突 所有作者均声明不存在利益冲突
| [1] |
Key Statistics for Colorectal Cancer[EB/OL].[2019-05-17]. https://www.cancer.org/cancer/colon-rectal-cancer/about/key-statistics.html.
|
| [2] |
Colorectal cancer statistics-Canadian Cancer Society[EB/OL].[2019-05-17]. https://www.cancer.ca/en/cancer-information/cancer-type/colorectal/statistics/?region=on#.
|
| [3] |
Bowel cancer statistics|Bowel cancer[EB/OL].[2019-05-17]. https://bowel-cancer.canceraustralia.gov.au/statistics.
|
| [4] |
Major D, Bryant H, Delaney M, et al. Colorectal cancer screening in Canada:results from the first round of screening for five provincial programs[J]. Curr Oncol, 2013, 20(5): 252-257. DOI:10.3747/co.20.1646 |
| [5] |
Colorectum Statistics|American Cancer Society-Cancer Facts & amp, Statistics[EB/OL].[2019-05-16]. https://cancerstatisticscenter.cancer.org/?_ga=2.174320481.212990873.1557108444-1452973440.1545395435#!/cancer-site/Colorectum.
|
| [6] |
Bowel cancer statistics|Bow[EB/OL].[2019-05-16]. https://bowel-cancer.canceraustralia.gov.au/statistics.
|
| [7] |
Colorectal Cancer Screening|Cancer Trends Progress Report[EB/OL].[2019-05-16]. https://progressreport.cancer.gov/detection/colorectal_cancer.
|
| [8] |
Cancer Screening-National Bowel Cancer Screening Program-Fact sheet[EB/OL].[2019-05-17]. http://www.cancerscreening.gov.au/internet/screening/publishing.nsf/Content/nbcsp-fact-sheet.
|
| [9] |
Cancer[EB/OL].[2018-12-13]. https://www.who.int/en/news-room/fact-sheets/detail/cancer.
|
| [10] |
陈万青, 郑荣寿, 曾红梅, 等. 1989-2008年中国恶性肿瘤发病趋势分析[J]. 中华肿瘤杂志, 2012, 34(7): 517-524. Chen WQ, Zheng RS, Zeng HM, et al. Trend analysis and projection of cancer incidence in China between 1989 and 2008[J]. Chin J Oncol, 2012, 34(7): 517-524. DOI:10.3760/cma.j.issn.0253-3766.2012.07.010 |
| [11] |
曾红梅, 郑荣寿, 张思维, 等. 1989-2008年中国恶性肿瘤死亡趋势分析[J]. 中华肿瘤杂志, 2012, 34(7): 525-531. Zeng HM, Zheng RS, Zhang SW, et al. Trend analysis of cancer mortality in China between 1989 and 2008[J]. Chin J Oncol, 2012, 34(7): 525-531. DOI:10.3760/cma.j.issn.0253-3766.2012.07.011 |
| [12] |
陈万青, 张思维, 郑荣寿, 等. 中国2009年恶性肿瘤发病和死亡分析[J]. 中国肿瘤, 2013, 22(1): 2-12. Chen WQ, Zhang SW, Zheng RS, et al. Report of cancer incidence and mortality in China, 2009[J]. China Cancer, 2013, 22(1): 2-12. DOI:10.11735/j.issn.1004-0242.2013.01.A2012315 |
| [13] |
陈万青, 张思维, 曾红梅, 等. 中国2010年恶性肿瘤发病与死亡[J]. 中国肿瘤, 2014, 23(1): 1-10. Chen WQ, Zhang SW, Zeng HM, et al. Report of cancer incidence and mortality in China, 2010[J]. China Cancer, 2014, 23(1): 1-10. DOI:10.11735/j.issn.1004-0242.2014.01.A001 |
| [14] |
陈万青, 郑荣寿, 曾红梅, 等. 2011年中国恶性肿瘤发病和死亡分析[J]. 中国肿瘤, 2015, 24(1): 1-10. Chen WQ, Zheng RS, Zeng HM, et al. Report of cancer incidence and mortality in China, 2011[J]. China Cancer, 2015, 24(1): 1-10. DOI:10.11735/j.issn.1004-0242.2015.01.A001 |
| [15] |
陈万青, 郑荣寿, 张思维, 等. 2012年中国恶性肿瘤发病和死亡分析[J]. 中国肿瘤, 2016, 25(1): 1-8. Chen WQ, Zheng RS, Zhang SW, et al. Report of cancer incidence and mortality in China, 2012[J]. China Cancer, 2016, 25(1): 1-8. DOI:10.11735/j.issn.1004-0242.2016.01.A001 |
| [16] |
陈万青, 郑荣寿, 张思维, 等. 2013年中国恶性肿瘤发病和死亡分析[J]. 中国肿瘤, 2017, 26(1): 1-7. Chen WQ, Zheng RS, Zhang SW, et al. Report of cancer incidence and mortality in China, 2013[J]. China Cancer, 2017, 26(1): 1-7. DOI:10.11735/j.issn.1004-0242.2017.01.A001 |
| [17] |
陈万青, 李贺, 孙可欣, 等. 2014年中国恶性肿瘤发病和死亡分析[J]. 中华肿瘤杂志, 2018, 40(1): 5-13. Chen WQ, Li H, Sun KX, et al. Report of cancer incidence and mortality in China, 2014[J]. Chin J Oncol, 2018, 40(1): 5-13. DOI:10.3760/cma.j.issn.0253-3766.2018.01.002 |
| [18] |
郑荣寿, 孙可欣, 张思维, 等. 2015年中国恶性肿瘤流行情况分析[J]. 中华肿瘤杂志, 2019, 41(1): 19-28. Zheng RS, Sun KX, Zhang SW, et al. Report of cancer epidemiology in China, 2015[J]. Chin J Oncol, 2019, 41(1): 19-28. DOI:10.3760/cma.j.issn.0253-3766.2019.01.005 |
| [19] |
房静远. 中国大肠肿瘤筛查、早诊早治和综合预防共识意见[J]. 胃肠病学和肝病学杂志, 2011, 20(11): 979-995. Fang JY. Consensus on colorectal cancer screening, early diagnosis, early treatment and comprehensive prevention in China[J]. Chin J Gastroenter Hepatol, 2011, 20(11): 979-995. DOI:10.3969/j.issn.1006-5709.2011.11.001 |
| [20] |
中国抗癌协会大肠癌专业委员会中国结直肠肿瘤早诊筛查策略制订专家组. 中国结直肠肿瘤早诊筛查策略专家共识[J]. 中华胃肠外科杂志, 2018, 21(10): 1081-1086. China Cancer Association Colorectal Cancer Professional Committee Expert Group on Early Diagnosis and Screening Strategies for Colorectal Cancer in China. Expert Consensus on Early Diagnosis and Screening Strategies for Colorectal Tumors in China[J]. Chin J Gastrointest Surg, 2018, 21(10): 1081-1086. DOI:10.3760/cma.j.issn.1671-0274.2018.10.001 |
| [21] |
李鹏, 王拥军, 陈光勇, 等. 中国早期结直肠癌及癌前病变筛查与诊治共识[J]. 中国实用内科杂志, 2015, 35(3): 211-227. Li P, Wang YJ, Chen GY, et al. Consensus on screening and treatment of early colorectal cancer and precancerous lesions in China[J]. Chin J Prac Intern Med, 2015, 35(3): 211-227. |
| [22] |
WHO. WHO handbook for guideline development[M]. 2nd ed. Geneva: WHO, 2014.
|
| [23] |
李颖.应用Delphi法对辽宁省高职护理专业课程设置的重构[D].沈阳: 中国医科大学, 2009. Li Y. Restructuring of curriculum design for the nursing of higher vocational education in Liaoning province by Delphi method[D]. Shenyang: China Medical University, 2009. http://cdmd.cnki.com.cn/article/cdmd-10159-2009162444.htm |
| [24] |
田会东, 王静. 基于Delphi法构建临床药师核心能力指标体系的研究[J]. 中国现代应用药学, 2019, 36(2): 236-239. Tian HD, Wang J. Study on using Delphi method constructing the core competence index system of clinical pharmacists[J]. Chin J Mod Appl Pharm, 2019, 36(2): 236-239. DOI:10.13748/j.cnki.issn1007-7693.2019.02.023 |
| [25] |
叶莎莎, 潘志刚, 刘湾湾, 等. 应用Delphi法确定社区全科医生对非瓣膜性心房颤动患者抗凝治疗的知信行问卷内容[J]. 中国全科医学, 2018, 21(33): 4118-4126. Ye SS, Pan ZG, Liu WW, et al. General practitioners' KAP questionnaire on anticoagulation in patients with nonvalvular atrial fibrillation using Delphi method[J]. Chin Gen Prac, 2018, 21(33): 4118-4126. DOI:10.12114/j.issn.1007-9572.2018.00.295 |
| [26] |
Bibbins-Domingo K, Grossman DC, Curry SJ, et al. Screening for colorectal cancer:US Preventive Services Task Force recommendation statement[J]. JAMA, 2016, 315(23): 2564-2575. DOI:10.1001/jama.2016.5989 |
| [27] |
Bacchus CM, Dunfield L, Gorber SC, et al. Recommendations on screening for colorectal cancer in primary care[J]. CMAJ, 2016, 188(5): 340-348. DOI:10.1503/cmaj.151125 |
| [28] |
Lee BI, Hong SP, Kim SE, et al. Korean guidelines for colorectal cancer screening and polyp detection[J]. Clin Endosc, 2012, 45(1): 25-43. DOI:10.5946/ce.2012.45.1.25 |
| [29] |
Alsanea N, Almadi MA, Abduljabbar AS, et al. National guidelines for colorectal cancer screening in Saudi Arabia with strength of recommendations and quality of evidence[J]. Ann Saudi Med, 2015, 35(3): 189-195. DOI:10.5144/0256-4947.2015.189 |
| [30] |
Guidelines: Colorectal cancer/-Cancer Guidelines Wiki[EB/OL].[2019-03-12]. https://wiki.cancer.org.au/australia/Guidelines:Colorectal_cancer/.
|
| [31] |
Sung JJY, Ng SC, Chan FKL, et al. An updated Asia Pacific consensus recommendations on colorectal cancer screening[J]. Gut, 2015, 64(1): 121-132. DOI:10.1136/gutjnl-2013-306503 |
| [32] |
Leddin D, Lieberman DA, Tse F, et al. Clinical practice guideline on screening for colorectal cancer in individuals with a family history of nonhereditary colorectal cancer or adenoma:the Canadian Association of Gastroenterology Banff Consensus[J]. Gastroenterology, 2018, 155(5): 1325-1347. DOI:10.1053/j.gastro.2018.08.017 |
| [33] |
SIGN 126 Diagnosis and management of colorectal cancer[EB/OL].[2019-03-12]. https://www.sign.ac.uk/sign-126-diagnosis-and-management-of-colorectal-cancer.html.
|
| [34] |
王振军, 付李缘. 大肠癌筛查共识与争议[J]. 临床外科杂志, 2018, 26(10): 721-723. Wang ZJ, Fu LY. Consensus and controversy of colorectal cancer screening[J]. J Clin Surg, 2018, 26(10): 721-723. DOI:10.3969/j.issn.1005-6483.2018.10.001 |
| [35] |
陈宏达, 卢明, 代敏. 我国结直肠癌人群筛查参与率现状及影响因素探讨[J]. 华西医学, 2018, 33(12): 1455-1459. Chen HD, Lu M, Dai M. Current status of participation rate in population-based colorectal cancer screening programs in China and its associated factors[J]. West Chin Med J, 2018, 33(12): 1455-1459. DOI:10.7507/1002-0179.201812094 |
| [36] |
胡晶, 陈茹, 谢雁鸣, 等. 科学和规范的改编临床实践指南[J]. 中国循证儿科杂志, 2012, 7(3): 226-230. Hu J, Chen R, Xie YM, et al. Scientific and normative adaptation of clinical practice guidelines[J]. Chin J Evid Based Pediatr, 2012, 7(3): 226-230. DOI:10.3969/j.issn.1673-5501.2012.03.014 |
 2020, Vol. 41
2020, Vol. 41




