文章信息
- 郑英杰, 蔡倩莹, 范伟, 张淼.
- Zheng Yingjie, Cai Qianying, Fan Wei, Zhang Miao.
- 因果思维在效应估计若干问题中的应用
- The application of causal thinking in several issues in estimation of effects
- 中华流行病学杂志, 2019, 40(10): 1314-1323
- Chinese Journal of Epidemiology, 2019, 40(10): 1314-1323
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2019.10.026
-
文章历史
收稿日期: 2019-05-14
流行病学是研究同质群体中“异乎寻常”的现象及其发生原因的科学。几乎所有的流行病学研究均不满足于对现象的发现与描述,揭示产生这一现象或结果的原因是研究者孜孜以求的目标。原因与结果总是按恒定的因先果后的单向时序(时间序),并以因对果产生影响(因果序)为特征而紧密地联系在一起,这种关系即因果关系或因果律[1]。因对果产生的影响程度,为因果效应(效应)。因又是前一因的果,果又是后一果的因,延续不断,推动客观世界事物的发生发展。因此,谈因不谈果,或谈果不谈因,均不恰当。因果推断(causal inference)是一个确立因果关系是否存在及其效应大小的过程。
流行病学常被认为擅长因果推断,主要关注疾病病因的研究,至今已形成了许多从简单到复杂的疾病病因模型,如朴素的单因论(瘴气理论、微生物学说等)及复杂的多因论(三角模型、轮状模型、社会生态模型、病因链/网、充分病因模型等)。总体上,这些模型为病因推断提供了概念性框架,指明了病因研究的大致方向,但存在以下问题:①涉及因果推断的关键信息,常常停留在文字描述上,模型内各因素之间的关系总体模糊;②充分病因模型仅适合于理论研究;③缺乏有效、可行的因果语言和工具。
在因果推断上,传统思维的方向是从数据到结论,系不完全确定——归纳法的产物。基于数据获得的显著关联,在排除各种偏倚对关联的影响后,结合病因“标准”[2-3],予以是否存在因果关系的结论(图 1)。这些标准中仅“因变引起果变”系因果标准[2],时间序为必要而非充分条件;其余几乎都是统计学标准(关联强度、重复性等)或间接证据(实验证据、相似性等),既非必要亦非充分。类似的做法见于采用关联的不可折叠性来判定混杂是否存在,从未成功[4]。混杂的因果结构仅有一种,而不可折叠性则可有多种因果结构。这种不以大自然因果律作为唯一金标准的做法,必然不容易成功。

|
| 图 1 因果推断:“新”思维与传统思维的对比 |
在逻辑推理上,当前发表的研究,总是在认可已获得的显著关联基础上,努力地寻找各种支持性依据;然而,研究的局限性总会提及可能存在的偏倚对研究结果的影响,从而形成了推理谬论[5]:既然存在影响关联的可能性,则说明已获得的显著关联存在着不确定性,忽略这些偏倚对效应估计的影响,而专注于对所获得的效应值的解释,可能得出误导性结论。
1、因果思维与因果推断概述因果思维是一种基于因果律(时间序和因果序),以果为特性,以因为因素,逐步深入分析研究问题的思维方法[6-8]。近年来,以“虚拟事实模型和潜在结局模型及其图形版(有向无环图、因果图)和公式版(结构方程模型)”为标志的因果革命[4, 9-13],提供了一种认识因果关系的全新语言、工具和思维,这种思维帮助我们提升了对流行病学理论和方法的认识[14-19];结合应用性研究中的数据产生机制所形成的因果框架,可正确指导我们认识研究问题,发现存在的不足,并提出针对性的解决方案。这种研究策略具有更广泛的应用领域,适用于所有涉及因果关系的研究,包括疾病和非疾病事件(如参与研究的意愿、测量有效性等)。
因果革命的新思维提出以下做法[7-9](图 1):对既往认识及研究问题(或假设),及其研究设计具体实施过程所反映的数据产生机制,通过诸如因果图等工具,以透明的语言、直观地运用变量编码既往的认识和科学假设,代表着我们对大自然存在因果律的认识,根据因果图规则可推导出这些变量间的逻辑与概率关系,特别是识别可以检验的假设及预测干预下的变化[12]。在此基础上,进行研究设计、变量测量,并在因果图及其因果规则的指导下获得调整变量的充分子集,至少可得到一个暂定的因果关联估计[4]。若我们对因果关系有新的认识,因果图的可塑性有助于这种透明关系的重建。这种从因果关系出发,结合研究设计及数据产生机制,来推断因果关联是否存在,系演绎法的思维,可让我们重新认识流行病学理论和方法。
本文从因果新思维的角度,围绕效应估计的若干问题,从效应与关联的关系、变量及其测量版的时序关系、动态人群自然图景、易感人群的形成、研究人群的选择、协变量和病例类型对效应估计的影响等方面,考察新思维如何帮助我们重新认识流行病学理论、方法及其应用。
2、效应与关联的关系理论上,效应是不可识别的。要认识效应,首先需对代表因与果的变量进行测量,接着通过计算这两个变量(测量因与测量果)之间存在的关联,以此来判定效应是否存在及大小,这是认识因果关系的必由之路。我们采用因果图来进行说明,变量在全文的表示方法——以大写字母代表真实变量,其测量版变量以同名字母加上标“*”表示,变量下标数字代表不同测量时间点。
假定暴露E和结局D代表着两个不同的事件,ME(或MD)代表除了E(或D)外所有影响E*(或D*)的其他因素,并且ME与MD相互独立(图 2A)[19]。若E→D的确存在,则E*-D*间的关联是以E为混杂子的混杂路径,即E*←E→D→D*,所产生的结果[20]。图 2A中无其他开放路径干扰E*-D*的关联估计,因此,E*-D*间的关联可正确反映E-D间的效应,这正是因果推断所需要的。基于因果新思维,从效应推断关联,简洁易懂。
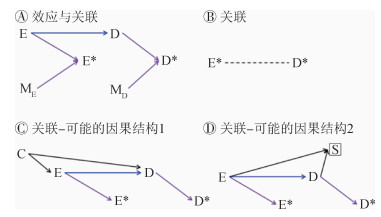
|
| 注:E和E*:真实的和测量的暴露变量;D和D*:真实的和测量的结局变量;ME和MD分别代表除了E和D外所有影响E*和D*的其他因素;C为混杂子;S为碰撞子,加框代表调整。蓝色单箭头代表拟研究的暴露-结局效应;其他单箭头代表箭头两侧存在着因果律;“------”代表存在关联 图 2 效应与关联的因果结构 |
实际研究中,我们仅能获得E*-D*间的关联(图 2B),可由E-D间的效应结构所致(图 2A);然而,亦可由更多的其他结构引起(图 2C、D)。因此,E*-D*间的关联实际上是因果效应和非因果效应及其两者的组合而产生的。能否区分因果和非因果关联,是我们进行正确因果推断的关键。
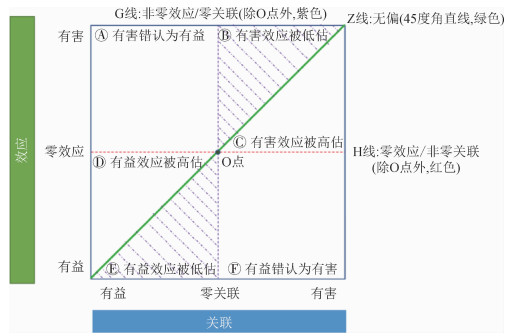
对比效应值与关联值之间的大小可发现,二者关系可能出现6种情形(图 3):(1)完全一致或无偏:仅出现在Z线,包括零效应与零关联相一致的情况(图 3中O点),这是我们研究所期望的结果;(2)不一致或偏倚,具体可分为以下5种情形:①方向逆转:有害效应将被错认为有益(图 3A),或有益效应将被错认为有害(图 3F);②效应被高估:有害(或有益)效应被估计过高,即出现了比效应值更大的关联值(图 3C和E),或偏倚远离无效值[21];③效应被低估:有害(或有益)效应被估计过低,即出现了比效应值更小的关联值(图 3B和D),或偏倚趋向无效值[21];④零效应将被错判为非零关联(图 3H线,不含O点),从而得出有益或有害的结果;⑤非零效应被错判为零关联(图 3G线,不含O点),可表现为有益或有害,难以判断其真实的因果关系。
|
| 图 3 效应值与关联值对比的情形 |
由上可见,效应与关联的关系复杂。若无法获得正确的关联结果,将给后续的疾病预防控制带来较大的不确定性,甚至是灾难性结果,如方向逆转、零效应的非零关联等情形。因此,针对因果关系研究的所有努力都应围绕尽可能获得接近Z线的关联值进行。
3、因果思维在效应估计中的应用(1)变量间的时序关系:
时间序是因果关系最根本的特性之一,也是我们进行因果思维的基础。据此可推断出3个结论:①同时发生的变量之间不可能存在着因果关系,为零效应。显然,变量不能对其自身产生因果关系,具体实例见表 1;②发生时间在后的变量不可能对发生时间在前的变量产生效应;③发生时间在前的变量可能对发生时间在后的变量产生效应,具体实例见表 2。上述①和②的时间序和因果序明确;然而③中时间序明确但因果序却只存在着可能性,这将给后续的因果关系判断带来困难:因其无法区分到底是时间连贯性(如从白天到黑夜)还是真正的因果律。尽管如此,在进行具体的效应研究时,变量间的时间序对判断变量之间是否存在着因果序仍具有重要的价值。
(2)因与果变量及其测量版的时序关系:
因或果事件的发生通常时间很短甚至是一瞬间,如癌症的具体启动时点——单个癌细胞的出现,但癌症的确诊则取决于其病情进展程度与筛查/诊断技术的性能。由图 2A可见,若暴露和结局不是针对同一属性,如乙肝母婴传播中,母亲和婴儿均进行HBsAg的测定,为同一属性情形,暴露E或结局D与E*或D*的时间序和因果序清楚(图 4①和②)。

|
| 注:E和E*:真实的和测量的暴露变量;D和D*:真实的和测量的结局变量。暗红色单箭头代表非研究效应所需的额外路径,可导致偏倚;其他单箭头代表箭头两侧存在着因果律 图 4 暴露E和结局D及其测量版(E*和D*)之间的时序关系 |
对变量间的关系,若E→D的确存在,则其关系亦清楚(图 4③)。然而,因E先于D、D先于D*,故D*→E不成立。此外,D影响E*,则只通过D*产生影响(图 4B⑤),如运动状况与阿尔茨海默症关系的病例对照研究,患者患病情况(D)只有在其被诊断后(D*),获知患病的个体可能将影响其过去运动状况的回忆测量(E*)。E*不可能影响D,如电子数据库中的变量值不能影响现实世界疾病的真实发生。同样地,E影响D*有2种情形:①通过D的影响,即E→D→D*;②通过E*影响D*(图 4A④),如日光浴(E*)导致皮肤晒伤,而更可能就诊,从而导致皮肤癌的诊断(D*)率提高,这是检出偏倚的结构。由此可见,E和D间不存在反向时序,而E*和D*的“反向时序”(我们通常认为的)则是可能的,即D*先于E*的情形[22-23]。因此,反向时序实际上定义于暴露和结局的测量水平。
(3)暴露和结局间关系的测量与研究设计:
假设有一个样本量足够大的易感人群,在t0时间暴露为E0,经过足够长时间的随访观察后,在t1时间出现感兴趣的结局D1,暴露E0影响结局D1发生的因果关系见图 5A。假定有足够多的资源对整个人群进行测量,并且研究目标是E0-D1的效应。为简单起见,假定暴露/结局均为二分类(1=有,0=无),各变量的测量无偏并且为独立性机制,混杂已得到有效的控制。我们将暴露(和/或结局)的测量时机定义为研究起点。因E0和D1发生后方可对其进行测量,依据研究起点与E0和D1之间的时序关系,E0的测量可发生在3个时间[24](图 5):E0之后和D1之前、D1之时和D1之后;而D1的测量只有一个时间段:D1之后,或(t1,t1+⊿t]。显然,应假定E0→E1及E1→E2必须同时成立(E0→E2是可能的,为简单起见,暂时不考虑这种情形);若上述关系不成立,则E1和E2无法通过E0与D1形成路径,因果研究将无法进行。基于此,我们建立了暴露和结局的因果图(图 5B,C,D)。
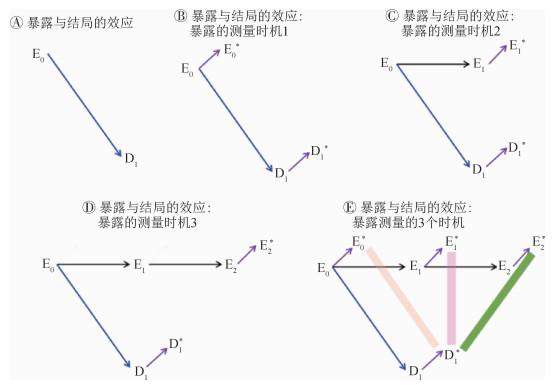
|
| 注:E0、E1和E2代表不同时间点的真实暴露,E0*、E1*和E2*分别为其测量版变量;D1和D1*:真实的和测量的结局变量;蓝色单箭头代表拟研究的暴露-结局效应;其他单箭头代表箭头两侧存在着因果律。图E中3种不同颜色分别对应于3种设计估计的关联 图 5 因与果及其测量时机所形成的研究设计的因果图 |
图 5B中,E0的测量在时间区间(t0,t1)进行,E0-D1间的效应以E0*-D1*间的关联来估计,此为前瞻性队列研究(prospective cohort study,PCS)的因果图;因E0*先于D1*,这为E0*→D1*的可能成立创造条件,如检出偏倚、霍桑效应等[25-26]。
图 5C中,E1和D1的测量同时进行的,因此E1*-D1*的效应为零,即E1*→D1*不可能成立;E0-D1间的效应以E1*-D1*间的关联来估计,此为横断面研究(cross-sectional study,CSS)的因果图[27]。
图 5D中,在获知病例(D1*=1)的情况下,选择非病例作为对照(D1*=0)。虽然对照的选择通常不早于病例,但对E2的测量一般与病例同时进行。通常t1+⊿t<t2,即D1*先于E2*,这为D1*→E2*的成立创造条件,如回忆偏倚等。E0-D1间的效应以E2*-D1*间的关联来估计,此即为病例对照研究(case control study,CCS)的因果图[28]。
然而,CSS难以保证人群中的病例不知道自己可能患病的情形,其回忆偏倚亦难以避免。同样地,虽然CCS中的病例通常已优先获知其患病,但有些CCS,如慢性乙肝感染与肝癌关系的研究中,在肝癌诊断的同时,其血清标本亦已采集——在时序上暴露与结局的测量表现为同时性。因此,CCS有时难以与CSS区别开来。在进行CSS和CCS的时候,应仔细分析暴露与结局及其测量版的时序关系。
由上可见,基于易感人群,上述3种设计理论上均围绕E0-D1间的效应进行,通过PCS可直接估计,而CSS需要满足E0→E1,及CCS需要满足E0→E2(或E0→E1及E1→E2)方可估计这种效应。因此,CSS和CCS需考虑暴露随时间的变化规律来确定其可行性,可存在以下3种情形:①不随时间发生变化的暴露变量,如性别、出生日期、血型、SNPs等,因E0=E1=E2,则三者均可直接估计E0-D1间的效应。②不同时间点暴露变量之间明确存在着因果关系,如研究以慢性乙肝感染为暴露,对E0的估计是以其后续时间点该暴露(如E1或E2)来进行的,因此,E1(或E2)的暴露分布可能与E0不同,进而影响效应估计值的大小。③暴露变量不满足E0→E1或E0→E2时,CSS或CCS不合适于因果关系研究。
我们将3种设计方法综合绘制于图 5E,并进行了设计特征的比较(表 3):虽然3种设计均估计同一效应,但PCS优越性最根本的特点是,其无需假设同一暴露不同时间点间存在着因果律,而这种假设则是CSS和CCS进行因果关系研究所必需的;在该假设成立的条件下(如上述①和②的情形),三者均可进行因果关联的估计。因此,在推断因果关系上3种设计各有优劣,单纯地认为队列研究优于其他2种设计(或CCS优于CSS)值得商榷。应结合具体研究问题进行具体分析。
(4)动态人群的自然图景:
易感是针对拟研究结局而言的,即易感的个体具有发生拟研究结局的可能性。实际研究时,暴露已持续地在研究者将面临的人群(或靶人群)中影响着结局的发生;该人群除了仍处于易感的个体外,还包括已出现过拟研究结局的个体及易感性发生改变的个体,如感染甲肝病毒后的个体一般都具有终身免疫,已不可能再次发生甲型肝炎。
人群的动态变化使得建立因果研究用易感人群更为复杂。以疾病首次发生为例,疾病自然史通常具有以下特征:①易感人群中已排除死亡者及不可能发生拟研究结局者;②唯有易感者才可能发病;③唯有发病者才可能康复,康复者的易感性可能已不同于其发病前;④死亡只发生一次,死亡个体后续任何事件均不可能发生(排他性);⑤失访/移出事件使得疾病、康复、死亡等其他相关事件的认定可能存在缺失;⑥唯有疾病首次发生的个体,才有再发生的可能(本文不赘述再发事件的情形)。
基于上述特征,假定有一个易感个体,在足够长的时限内,对于首次发病事件而言将发生以下6种可能情形(图 6):①持续保持易感;②易感-死亡;③易感-发病-患病;④易感-发病-患病-死亡;⑤易感-发病-患病-康复;⑥易感-发病-患病-康复-死亡。死亡可以出现在整个自然史的各个时期,如发病前、病程内、康复后。若发病前死亡,死因显然与疾病无关;若病程内和康复后死亡,则发病与死亡时间序清楚但仍不能准确判断其因果序,如发病后出现交通意外而死亡,显然与疾病无关。因此,死亡将干扰疾病发生等相关事件/状态的估计。

|
| 图 6 动态人群首发疾病自然史模式图 |
移入和移出人群可根据其移入或移出时的状态,决定着其未来可能发生的事件(图 6):显然,情形②、④和⑥均死亡,不可能发生移出;移出时个体若为情形①,则其未来的结局可能为上述6种情形的任何一种;移出时个体若为情形③,则其未来结局可有4种情形,③~⑥;移出时个体若为情形⑤,则其未来结局可有2种情形,⑤和⑥。移入者未来结局的情形,按照上述移入时的状态,可能发生对应的未来结局。
综上,我们绘制了动态人群首发疾病自然史模式图:6种疾病模式与人群移入、移出交织地影响着动态人群疾病的发生发展,这是研究者实施研究前将面临的人群自然图景。因死亡者的排他性、康复者的易感性改变、失访/移出者后续事件的不确定性等情形的存在,使得暴露与结局(疾病)间的关系研究尤为复杂。
(5)易感人群的建立与选择:
实际研究中,研究者将从靶人群中剔除已出现结局、不可能出现结局,如免疫者或死亡者。死亡者的排除容易,已出现结局者一般较为容易,而不可能出现结局者则较难。对已出现结局者,通常在基线招募人群时,采用主要针对结局的筛检和/或诊断等策略和措施,对结局进行识别后予以排除,从而获得的未出现结局的人群作为研究人群,其实质上是易感人群的替代(图 7)。

|
| 注:E0和E1代表不同时间点的真实暴露,E1*分别为其测量版变量;D1和D1*、D2和D2*分别为结局在两个时间点的真实的和测量的结局变量;蓝色单箭头代表拟研究的暴露-结局效应;其他单箭头代表箭头两侧存在着因果律。S1=0代表研究人群限制于非病例 图 7 前瞻性队列易感人群的建立:基线结局排除 |
在假想易感人群的基础上,暴露(E0)影响着结局(D1)的发生。在合适的策略识别D1后,所有可被识别的病例(D1*=1)将被排除,即只有非病例(D1*=0)的存活者才组成一个易感人群,纳入研究(S1=0)。此时,我们可获得E1*-D2*间的关联,作为对E0-D1间效应的替代估计(图 7)。
值得指出的是,若E0→D1成立,排除病例(D1*=1)将同时改变E1和D2的分布,E0-D1间效应与E1-D2间的效应可能不同,值得深入研究。即使这样,几乎所有研究仍然无法得以识别临床前、处于不可识别期的结局者,这种基线的残留结局将导致暴露-结局间的时序颠倒[29],加上死亡及不可能发生结局者的影响,默认该研究人群具备稳态人群的特征,成为所有因果关系用研究人群的基本假设[30-31]。
(6)研究人群的选择及协变量的影响:
资源的有限决定着研究设计效率提高的必要性。若在效率、方差和/或偏倚3方面权衡可以接受的前提下[32],我们通常会对源人群(病例与非病例,暴露与非暴露人群)进行选择以形成研究人群,如CSS采用简单随机抽样、CCS和PCS采用匹配策略等。然而,这种选择并不改变图 5B、C、D的基本结构。
同样地,干扰因素如混杂子等对暴露-结局间效应估计的影响,情形类似——虽然我们只是列出暴露与结局的因果图。以混杂子C-1结构为例(图 8),一般来说,PCS和CCS同时测量暴露和混杂子,即分别为E0*和C0*、E2*和C2*;而CSS同时测量暴露、结局和混杂子,即分别为E1*、D1*和C1*。由图 8可见,混杂子以替代形式发挥着作用,混杂子C-1在PCS、CCS和CSS分别以C0、C1和C2(假设三者均为C-1的效应变量)来替代,并以其测量版(C0*、C1*和C2*)分别计算上述各自的关联[见3(3)部分]。因此,类似于不同时间的暴露[见3(3)部分],3种设计均需假定混杂子具备在不同时点间的真实值存在着因果关系,否则,因果关系研究同样地无法进行——我们无法控制混杂子的替代者,因已不存在自C-1开始至C0、C1和C2的路径,后者的替代身份无法成立。

|
| 注:E0、E1和E2代表不同时间点的真实暴露,E0*、E1*和E2*分别为其测量版变量;D1和D1*分别为在真实的和测量的结局变量;C-1为混杂子,C0、C1和C2代表不同时间点的真实混杂,C0*、C1*和C2*分别为其测量版变量。蓝色单箭头代表拟研究的暴露-结局效应;其他单箭头代表箭头两侧存在着因果律。3种不同颜色分别对应于3种设计估计的关联 图 8 混杂结构影响因果关系及其测量的因果图 |
(7)新病例与旧病例对效应估计的影响:
疾病的发生,即从无病状态向有病状态的转变,通常发生时间是短暂或一瞬间的,之后可处于一定时间的疾病状态;疾病从启动到结束,如死亡、康复等的整个过程即是病程(图 9)。病例发生时,或病程起点,即被识别或诊断,这类病例即新发(生)病例(图 9②A点);此后,在病程上任何时候进行的第一次诊断,即为新发(现)病例(图 9③B、④C和⑤D,疾病已发生,只不过是首次被识别/诊断),这两部分病例组成了新病例。若病例已完成了首次诊断(图 9,⑥B和⑦B),在后续病程上再次或多次被识别(图 9⑥C、⑦C和⑦D),则这种病例被称为旧病例。习惯上将新病例和旧病例合并称为现患病例,即处于病程上的个体们。

|
| 注:圆点代表发病——病程起点,A-D为诊断时机。绿色虚线代表个体的易感期,黑色实线代表整个病程 图 9 新病例与旧病例及其被识别 |
病例的诊断是疾病病因推断的关键,一般认为新病例在因果推断上优于旧病例。疾病发生后,通常一开始不可识别,经过一段时间后,逐渐发展为疾病的可识别阶段,这为我们诊断疾病奠定基础。由此可见,对疾病的识别或测量是疾病自然史与研究者通过合适的策略对其进行测量之间的相互作用的过程,我们对疾病的定义是建立在疾病的发生(首发)与其测量时机之间的关系上(图 9)。2015年笔者在浙江德清新安镇发现一名女性,79岁,自诉体健,无既往疾病史和诊疗史;体检发现,其收缩压为180 mmHg(1 mmHg=1.33 kPa),舒张压为110 mmHg,因此,将其判定为新发现病例。由此可见,对疾病病例不同类型的定义是建立在我们如何测量及测量次数的基础上,病例的“新”与“旧”并不真实反映其所处的病程长短。
以CSS中进行病例的两次测量为例(图 10),在病例(D1=1)发生后,其第一次被识别为疾病(D1*=1,即新病例);在D1*=1的病例中,若第二次被识别为同一疾病(D2*=1,即旧病例);若D1*=0的非病例在第二次被识别为病例(D2*=1),则此时病例为新病例;若D1*=1的病例在第二次诊断时未被识别或未经历第二次诊断,则不能将其判定为旧病例(D2*=0)。因D1*=1的个体更可能地被判定为D2*=1,故D1*→D2*成立(图 10B、C、D)。若不论是新病例还是旧病例,疾病可导致更多的死亡(S2=1或S3=1),则通常只能观察到存活的病例人群(S2=0和S3=0)。实际研究时,人群病例由单独的D1*=1、单独的D2*=1(新病例)和D1*=D2*=1(旧病例)并且均为存活者这3部分病例组成。我们考虑以下不同情形对效应估计的影响:①若研究只考虑新病例(图 10A),并且有理由认为所有的新病例均在其死亡之前被观察和测量,则其效应估计同图 5C,无奈曼偏倚(neyman bias)[33]。②若研究只考虑旧病例(图 10B),并且有理由认为所有的旧病例均在其死亡之前被观察和测量(S3=1的情形被忽略),而新病例发生一定比例的死亡(S2=1的情形不可忽略),此时效应估计为E2*-D2*,但研究人群限制于S2=0和D1*=D2*=1,即只含有旧病例的存活人群,因此将可能发生奈曼偏倚。③若研究同时考虑新病例和旧病例(图 10C),并且有理由认为所有的旧病例均在其死亡之前被观察和测量(S3=1的情形被忽略),此时效应估计仍为E2*-D2*,但研究人群限制于S2=0,因此仍将可能发生奈曼偏倚。④若研究同时考虑新病例和旧病例(图 10D),但新(或旧)病例发生一定比例的死亡(S3=1的情形不可忽略),此时效应估计仍为E2*-D2*,但研究人群限制于S2=0和S3=0,因此仍将可能发生奈曼偏倚。
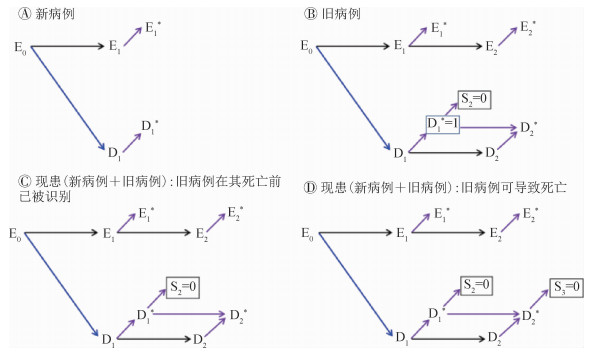
|
| 注:E0、E1和E2代表不同时间点的真实暴露,E1*和E2*分别为其测量版变量;D1和D1*、D2和D2*分别为结局在两个时间点的真实的和测量的结局变量;S2=0和S3=0代表研究人群限制于存活者。蓝色单箭头代表拟研究的暴露-结局效应;其他单箭头代表箭头两侧存在着因果律 图 10 新病例与旧病例的因果图 |
前文提及,除了新发(生)病例外,新发(现)病例只是根据病例在其整个病程中被首次诊断时的情形,因此,认为所有的新病例均在其死亡之前被首次诊断不太可能成立。同样地,所有的旧病例均在其死亡之前被观察和测量到也不太可能成立。病程起点至病例被识别的这段时间即潜隐期(latent period,LP):对同一个体而言,其作为旧病例的LP显然长于其作为新病例的LP;但对不同病例而言,其相互间的LP大小并不容易判定,如上述德清女性高血压的例子。由此看来,新病例在因果推断上优于旧病例的观点值得商榷。人群中上述3种病例的不同构成使得采用CSS进行因果推断更为复杂。虽然我们只讨论了CSS中病例不同类型对效应估计的可能影响,从疾病识别策略的相似性来说,上述讨论对PCS和CCS同样地适用。
4.结语:现实世界是多元交互的复杂世界,因果律是最为基本、更为广泛的关系,推动世界发展的动力。以因果律为根基,借助于因果革命的理论、方法与工具,首先建立一个因果关系的框架作为研究蓝图,接着借用科研设计所提供的技术路线,最后以数据分析方法作为实现认识因果律的工具。这种从传统思维到因果新思维的转变,帮助我们重新认识流行病学理论、方法及其应用,这种认识扎实了流行病学的基本概念,丰富了学科内涵,基于新思维已发展了多种效应识别的设计方法及识别和控制偏倚的策略,如阴性结局(或暴露)对照法、工具变量法及其变体、孟德尔随机化设计等[14, 34-41]。应加强对因果新思维的认识与应用,并将其注入诸如大数据、真实世界、人工智能、数据挖掘、神经网络、机器学习等研究中。
利益冲突 所有作者均声明不存在利益冲突
志谢 感谢李意杰在作图过程中给予的帮助
| [1] |
Shahar E, Shahar DJ. Marginal structural models:much ado about (almost) nothing[J]. J Eval Clin Pract, 2013, 19(1): 214-222. DOI:10.1111/j.1365-2753.2011.01757.x |
| [2] |
Susser M. What is a cause and how do we know one? A grammar for pragmatic epidemiology[J]. Am J Epidemiol, 1991, 133(7): 635-648. DOI:10.1093/oxfordjournals.aje.a115939 |
| [3] |
Hill AB. The environment and disease:association or causation?[J]. Proc Roy Soc Med, 1965, 58: 295-300. DOI:10.1177/003591576505800503 |
| [4] |
Pearl J, Mackenzie D. The book of why:the new science of cause and effect[M]. London: Penguin, 2019.
|
| [5] |
Lash TL, Fox MP, Fink AK. Applying quantitative bias analysis to epidemiologic data[M]. New York: Springer, 2009.
|
| [6] |
Lipton R, Ødegaard T. Causal thinking and causal language in epidemiology:it's in the details[J]. Epidemiol Perspect Innov, 2005, 2: 8. DOI:10.1186/1742-5573-2-8 |
| [7] |
Glymour MM, Hamad R. Causal thinking as a critical tool for eliminating social inequalities in health[J]. Am J Public Health, 2018, 108(5): 623. DOI:10.2105/AJPH.2018.304383 |
| [8] |
Kaufman JS, Poole C. Looking back on "causal thinking in the health sciences"[J]. Annu Rev Public Health, 2000, 21: 101-119. DOI:10.1146/annurev.publhealth.21.1.101 |
| [9] |
Pearl J. Causal diagrams for empirical research[J]. Biometrika, 1995, 82(5): 669-688. DOI:10.1093/biomet/82.4.669 |
| [10] |
Greenland S, Brumback B. An overview of relations among causal modelling methods[J]. Int J Epidemiol, 2002, 31(5): 1030-1037. DOI:10.1093/ije/31.5.1030 |
| [11] |
Pearl J. Causality:Models, Reasoning, and Inference[M]. 2nd ed. Cambridge: Cambridge University Press, 2009.
|
| [12] |
Bareinboim E, Pearl J. Causal inference and the data-fusion problem[J]. Proc Natl Acad Sci USA, 2016, 113(27): 7345-7352. DOI:10.1073/pnas.1510507113 |
| [13] |
郑英杰, 赵耐青. 有向无环图:语言、规则及应用[J]. 中华流行病学杂志, 2017, 38(8): 1140-1144. Zheng YJ, Zhao NQ. Directed acyclic graphs:languages, rules and applications[J]. Chin J Epidemiol, 2017, 38(8): 1140-1144. DOI:10.3760/cma.j.issn.0254-6450.2017.08.029 |
| [14] |
Pearce N, Richiardi L. Commentary:three worlds collide:Berkson's bias, selection bias and collider bias[J]. Int J Epidemiol, 2014, 43(2): 521-524. DOI:10.1093/ije/dyu025 |
| [15] |
Mansournia MA, Jewell NP, Greenland S. Case-control matching:effects, misconceptions, and recommendations[J]. Eur J Epidemiol, 2018, 33(1): 5-14. DOI:10.1007/s10654-017-0325-0 |
| [16] |
Mansournia MA, Higgins JP, Sterne JA, et al. Biases in randomized trials:a conversation between trialists and epidemiologists[J]. Epidemiology, 2017, 28(1): 54-59. DOI:10.1097/EDE.0000000000000564 |
| [17] |
Infante-Rivard C, Cusson A. Reflection on modern methods:selection bias-a review of recent developments[J]. Int J Epidemiol, 2018, 47(5): 1714-1722. DOI:10.1093/ije/dyy138 |
| [18] |
Hernán MA, Hernández-Diáz S, Robins JM. A structural approach to selection bias[J]. Epidemiology, 2004, 15(5): 615-625. DOI:10.1097/01.ede.0000135174.63482.43 |
| [19] |
Hernán MA, Cole SR. Invited commentary:causal diagrams and measurement bias[J]. Am J Epidemiol, 2009, 170(8): 959-962. DOI:10.1093/aje/kwp293 |
| [20] |
Shahar E. Causal diagrams for encoding and evaluation of information bias[J]. J Eval Clin Pract, 2009, 15(3): 436-440. DOI:10.1111/j.1365-2753.2008.01031.x |
| [21] |
Gustafson P, Greenland S. Misclassification[M]//Ahrens W, Pigeot I. Handbook of epidemiology. New York: Springer; 2014: 639-658.
|
| [22] |
Sattar N, Preiss D. Reverse causality in cardiovascular epidemiological research:more common than imagined?[J]. Circulation, 2017, 135(24): 2369-2372. DOI:10.1161/CIRCULATIONAHA.117.028307 |
| [23] |
Kramer MS, Moodie EE, Dahhou M, et al. Breastfeeding and infant size:evidence of reverse causality[J]. Am J Epidemiol, 2011, 173(9): 978-983. DOI:10.1093/aje/kwq495 |
| [24] |
郑英杰, 赵耐青, 何一宁. 客观世界的因果关系:基于有向无环图的结构解析[J]. 中华流行病学杂志, 2018, 39(1): 90-93. Zheng YJ, Zhao NQ, He YN. Causality in objective world:directed acyclic graphs-based structural parsing[J]. Chin J Epidemiol, 2018, 39(1): 90-93. DOI:10.3760/cma.j.issn.0254-6450.2018.01.019 |
| [25] |
Mangione-Smith R, Elliott MN, McDonald L, et al. An observational study of antibiotic prescribing behavior and the Hawthorne effect[J]. Health Serv Res, 2002, 37(6): 1603-1623. DOI:10.1111/1475-6773.10482 |
| [26] |
Horwitz RI, Feinstein AR. Alternative analytic methods for case-control studies of estrogens and endometrial cancer[J]. N Engl J Med, 1978, 299(20): 1089-1094. DOI:10.1056/NEJM197811162992001 |
| [27] |
Shahar E, Shahar DJ. Causal diagrams and the cross-sectional study[J]. Clin Epidemiol, 2013, 5: 57-65. DOI:10.2147/CLEP.S42843 |
| [28] |
Shahar E, Shahar DJ. Causal diagrams and the logic of matched case-control studies[J]. Clin Epidemiol, 2012, 4: 137-144. DOI:10.2147/CLEP.S31271 |
| [29] |
刘丽丽, 何一宁, 蔡倩莹, 等. 现实队列研究中暴露与结局的时序关系[J]. 中华流行病学杂志, 2018, 39(6): 858-861. Liu LL, He YN, Cai QY, et al. Exposure-preceding-outcome regarding time sequence among cohort studies in real world[J]. Chin J Epidemiol, 2018, 39(6): 858-861. DOI:10.3760/cma.j.issn.0254-6450.2018.06.031 |
| [30] |
Freeman J, Hutchison GB. Prevalence, incidence and duration[J]. Am J Epidemiol, 1980, 112(5): 707-723. DOI:10.1093/oxfordjournals.aje.a113043 |
| [31] |
Vandenbroucke JP, Pearce N. Incidence rates in dynamic populations[J]. Int J Epidemiol, 2012, 41(5): 1472-1479. DOI:10.1093/ije/dys142 |
| [32] |
Shahar E, Shahar DJ. Causal diagrams and three pairs of biases[M]//Lunet N. Epidemiology-current perspectives on research and practice. http://www.intechopen.com/books/epidemiology-current-perspectives-on-research-and-practice/causaldiagrams-and-three-pairs-of-biases:InTech; 2012: 31-62.
|
| [33] |
Sackett DL. Bias in analytic research[J]. J Chronic Dis, 1979, 32(1/2): 51-63. DOI:10.1016/0021-9681(79)90012-2 |
| [34] |
Arnold BF, Ercumen A. Negative control outcomes:a tool to detect bias in randomized trials[J]. JAMA, 2016, 316(24): 2597-2598. DOI:10.1001/jama.2016.17700 |
| [35] |
Jackson LA, Jackson ML, Nelson JC, et al. Evidence of bias in estimates of influenza vaccine effectiveness in seniors[J]. Int J Epidemiol, 2006, 35(2): 337-344. DOI:10.1093/ije/dyi274 |
| [36] |
Greenland S. An introduction to instrumental variables for epidemiologists[J]. Int J Epidemiol, 2000, 29(4): 722-729. DOI:10.1093/ije/29.4.722 |
| [37] |
Hernán MA, Robins JM. Instruments for causal inference:an epidemiologist's dream?[J]. Epidemiology, 2006, 17(4): 360-372. DOI:10.1097/01.ede.0000222409.00878.37 |
| [38] |
Lawlor DA, Harbord RM, Sterne JAC, et al. Mendelian randomization:using genes as instruments for making causal inferences in epidemiology[J]. Stat Med, 2008, 27(8): 1133-1163. DOI:10.1002/sim.3034 |
| [39] |
Brito C, Pearl J. Generalized instrumental variables[C]//Proceedings of the eighteenth conference on uncertainty in artificial intelligence. Alberta, Canada: Morgan Kaufmann Publishers Inc., 2002: 85-93.
|
| [40] |
Pearce N, Vandenbroucke JP, Lawlor DA. Causal inference in environmental epidemiology:old and new approaches[J]. Epidemiology, 2019, 30(3): 311-316. DOI:10.1097/EDE.0000000000000987 |
| [41] |
Glymour MM, Mayeda ER, Selby VN. Commentary:selection bias in clinical epidemiology:causal thinking to guide patient-centered research[J]. Epidemiology, 2016, 27(4): 466-468. DOI:10.1097/EDE.0000000000000473 |
 2019, Vol. 40
2019, Vol. 40





