文章信息
- 屠丽红, 林声, 张驰, 袁政安, 张曦, 陈敏, 陈洪友, 潘浩.
- Tu Lihong, Lin Sheng, Zhang Chi, Yuan Zheng'an, Zhang Xi, Chen Min, Chen Hongyou, Pan Hao.
- 上海市2013-2016年门诊腹泻患者弯曲菌流行特征及耐药研究
- Epidemiological characteristics and antibiotic resistance of Campylobacter spp. among diarrhea outpatients in Shanghai, 2013-2016
- 中华流行病学杂志, 2019, 40(8): 900-903
- Chinese journal of Epidemiology, 2019, 40(8): 900-903
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2019.08.006
-
文章历史
收稿日期: 2019-03-08
弯曲菌病(Campylobacteriosis)是由弯曲菌属(Campylobacter spp.)细菌感染引起的一系列疾病的总称,其中最常见的是由感染该菌所致的腹泻[1]。弯曲菌感染引起的腹泻是许多发达国家最常见的急性细菌性肠道传染病,在美国弯曲菌引起的腹泻病例数仅次于沙门菌,且许多国家的弯曲菌感染率呈上升趋势[2-4]。本研究依托上海市腹泻病综合监测网络,在23家哨点医院肠道门诊开展腹泻患者中弯曲菌检测。对分离自腹泻患者粪便标本中的弯曲菌进行药敏试验,为了解上海市弯曲菌的流行特征及耐药情况提供数据。
材料与方法1.标本来源:2013年7月至2016年12月,选择上海市23家哨点医院(一级医院9所、二级医院7所、三级医院7所)作为腹泻病监测点医院。根据2010年监测点医院肠道门诊的腹泻病例数和医院分配样本量的比值,确定各监测点医院1 : 3至1 : 20不等的抽样比例,按照不同抽样比例确定病例[5]。监测点医院肠道门诊进行病例资料收集和粪便标本采集。腹泻病例定义为排便≥3次/d,伴粪便性状的改变。选取病例均为肠道门诊散发病例,不包含食源性暴发或聚集性事件相关病例。
2.主要试剂和仪器:Cary-Blair运输培养基、无血弯曲菌选择性琼脂平板、哥伦比亚血琼脂平板、1%马尿酸钠、3%过氧化氢溶液由上海市CDC培养基供应中心配制,孔径0.45 μm的47 mm滤膜购自Millipore公司,氧化酶试剂、API CAMPY鉴定试剂盒购自法国生物梅里埃公司,空肠弯曲菌/结肠弯曲菌核酸双色荧光PCR试剂盒购自上海辉睿生物科技有限公司,弯曲菌药敏板条购自美国TREK诊断有限公司。2.5 L和3.5 L微需氧产气袋购自ThermoFisher有限公司,2.5 L和7 L厌氧罐购自日本三菱瓦斯化学株式会社。ANOXOMAT MARK Ⅱ微需氧发生器购自荷兰MART公司,光学显微镜购自蔡司公司。
3.分离培养:用无菌棉拭采集急性期腹泻患者新鲜粪便标本,插入Cary-Blair运输培养基,24 h内运送至区CDC实验室进行检测。采用直接膜过滤法对标本进行弯曲菌分离检测[6]。将腹泻患者粪便棉拭洗脱于0.5 ml无菌生理盐水中,将孔径0.45 μm的47 mm滤膜放置于无血弯曲菌选择性琼脂平板上,将洗脱液滴加于滤膜上,37 ℃静置30~45 min,除去滤膜,于42 ℃微需氧培养24~48 h,挑取灰色、湿润、沿划线生长,不规则圆形,有金色光泽的可疑菌落转种到哥伦比亚血琼脂平板上纯化培养,42 ℃微需氧培养24 h,进行进一步鉴定。
4.菌株鉴定:参照《感染性腹泻诊断标准》WS 271-2007中弯曲菌检验方法进行弯曲菌鉴定[7],革兰染色镜检为革兰阴性,呈小逗点状,氧化酶试验阳性、过氧化氢酶试验阳性,并用API CAMPY试剂盒及PCR鉴定为空肠弯曲菌或结肠弯曲菌,PCR鉴定方法按照试剂盒说明书操作。
5.药物敏感试验:研究根据美国CDC的National Antimicrobial Resistance Monitoring System for Enteric Bacteria(NARMS)推荐的药物[8],采用微量肉汤稀释法对分离鉴定的弯曲菌进行药敏实验,具体操作按照弯曲菌药敏板条试剂盒说明书。抗菌药物为阿奇霉素、环丙沙星、红霉素、庆大霉素、四环素、萘啶酸、泰利霉素、克林霉素。质控菌株空肠弯曲菌ATCC33560为上海市CDC中心实验室提供,结果判断按照NARMS标准,空肠弯曲菌折点为阿奇霉素≥0.5 μg/ml、环丙沙星≥1 μg/ml、红霉素≥8 μg/ml、庆大霉素≥4 μg/ml、四环素≥2 μg/ml、萘啶酸≥32 μg/ml、泰利霉素≥8 μg/ml、克林霉素≥1 μg/ml,结肠弯曲菌折点为阿奇霉素≥1 μg/ml、环丙沙星≥1 μg/ml、红霉素≥16 μg/ml、庆大霉素≥4 μg/ml、四环素≥4 μg/ml、萘啶酸≥32 μg/ml、泰利霉素≥8 μg/ml、克林霉素≥2 μg/ml[8]。
6.统计学分析:采用Excel 2010和Epi Info 7软件进行统计学分析。计数资料用例数和百分比表示,组间比较采用χ2检验,双侧检验以P<0.05为差异有统计学意义。
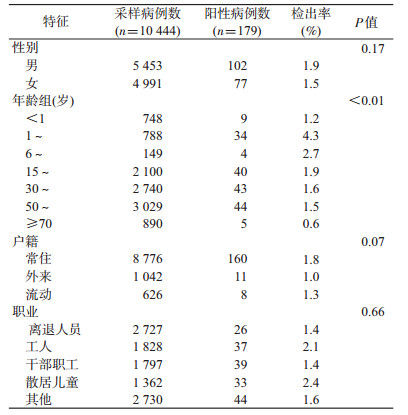
结果1.基本情况:10 444例采样病例中,男性5 453例(52.2%),女性4 991例(47.8%);以15~69岁(7 869例,75.34%)为主;职业包括离退人员、工人、干部职工、散居儿童。见表 1。
2.菌株检测情况及阳性病例人群分布:10 444例腹泻患者的粪便肛拭标本中共检出弯曲菌179株,平均阳性率为1.7%,空肠弯曲菌占94.4%(169/179),结肠弯曲菌占5.6%(10/179)。2013-2016年弯曲菌检出率依次为0.3%(6/1 868)、1.9%(43/2 235)、1.9%(64/3 375)和2.2%(66/2 966)。检出的179例弯曲菌感染病例中,男性病例检出率为1.9%,女性病例检出率为1.5%,但差异无统计学意义;1~岁组的检出率最高(4.3%),组间差异有统计学意义(P<0.01);不同户籍和职业间差异无统计学意义。见表 1。
3.地区和时间分布:市区哨点医院弯曲菌检出率为1.8%(124/6 888),郊区医院检出率1.5%(55/3 556)(P=0.34),差异无统计学意义。弯曲菌在4-6月和10-12月检出率高,1-3月的平均检出率为1.4%,4-6月为3.5%,7-9月为0.9%,10-12月为1.8%,差异有统计学意义(P<0.01)。其中以2014年5月(7.8%)和2016年5月(5.0%)最高,见图 1。

|
| 图 1 2013-2016年上海市人源弯曲菌检出率分布 |
4.临床症状:179例弯曲菌感染病例中,90.5%病例首发症状为腹泻,粪便性状以稀软便居多,占40.8%,水样便占39.1%。有3.3%病例存在发热症状,1.7%病例有呕吐症状。
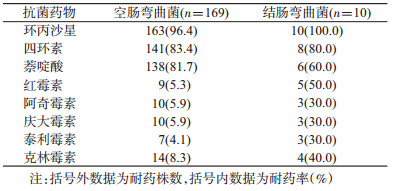
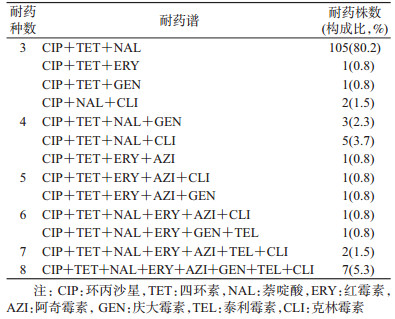
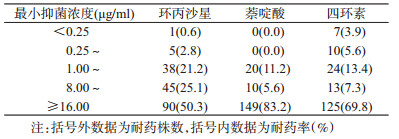
5.菌株耐药情况:空肠弯曲菌对环丙沙星、四环素和萘啶酸耐药率高,对红霉素、阿奇霉素、庆大霉素、泰利霉素、克林霉素部分耐药。结肠弯曲菌的耐药率高于空肠弯曲菌,见表 2。179株弯曲菌中,有131株菌株(73.2%)对≥3种抗菌药物存在多重耐药,其中对CIP+TET+NAL耐药有105株(80.2%),为主要的耐药谱,见表 3。179株弯曲菌对环丙沙星、萘啶酸、四环素抑菌液浓度≥16 μg/ml的耐药率为50.3%、83.2%、69.8%,见表 4。
2013-2016年上海市门诊腹泻患者弯曲菌监测显示,上海市门诊腹泻患者弯曲菌的平均阳性率为1.7%,以空肠弯曲菌感染为主,略低于北京市部分地区的检出率[9-10],可能因检测方法不同所致。弯曲菌的生长需要微需氧环境,对空气中的O2、N2和CO2比较敏感,温度、pH值、营养等因素变化会导致弯曲菌进入非可培养状态(VBNC)[11],而本研究在检测过程中存在部分标本运送时间超过24 h、运送过程中标本保存温度偏高、培养气体环境不稳定等问题,检测标本中的弯曲菌或已进入VBNC,无法恢复到可培养状态,使得弯曲菌检测阳性率偏低。同时部分腹泻患者感染菌量不大,本研究使用的直接膜过滤法在过滤过程中会损失部分弯曲菌,也可能导致弯曲菌检测阳性率偏低。2018年上海市2家弯曲菌平均阳性率低于2.0%的区CDC试点对标本使用中国CDC推荐的加强过滤培养方法[9-10],阳性率确有提升,平均阳性率可达8%左右。本研究仅初步描述了上海市人源弯曲菌检测的本底情况,为后续改进检测方法后的人源弯曲菌检测研究提供依据。
本研究显示弯曲菌可感染所有年龄段人群,高发于<5岁儿童,男女童比例约为1.3 : 1。弯曲菌感染与职业、户籍、地区分布无统计学关联。从月份分布来看,全年均可检出弯曲菌,以4-6月和10-12月检出较高,5月检出率最高为7.8%,与北京市部分地区的高峰有重叠[9-10]。
弯曲菌感染导致的腹泻属于自限性,但免疫力低下及症状严重的患者常需要抗菌药物治疗。随着抗菌药物在人群及养殖业的使用,弯曲菌对多种抗菌药物的耐药率显著增加。本研究显示,上海市人源空肠弯曲菌对环丙沙星、四环素和萘啶酸耐药率均>81.0%。人源结肠弯曲菌比空肠弯曲菌耐药情况严重,对进行检测的抗菌药物的耐药率均>30.0%,对环丙沙星的耐药率甚至达到了100.0%。179株人源弯曲菌中多重耐药情况严重,有73.2%的人源弯曲菌存在多重耐药,其中5.3%菌株同时对8种抗菌药物耐药,对环丙沙星、四环素、萘啶酸多重耐药菌占80.2%,为主要多重耐药谱。本研究显示2013-2016年上海市腹泻患者分离的弯曲菌对喹诺酮类药物(环丙沙星、萘啶酸)和四环素的耐药率高,≥16 μg/ml的耐药率为50.3%、83.2%、69.8%,略低于顾一心等[12]的研究数据(>85.0%)。目前我国治疗弯曲菌感染尤其儿童腹泻的首选药物是大环内酯类抗菌药物,红霉素是治疗弯曲菌感染的主要药物[13]。本研究显示上海市人源弯曲菌对大环内酯类药物(红霉素、阿奇霉素、泰利霉素)耐药率为5.3%、5.9%、4.1%,仍以敏感为主,但仍需要长期开展监测和研究。弯曲菌的耐药情况已成为了全球弯曲菌病预防控制及临床治疗面临的重要问题,美国CDC已将耐氟喹诺酮类和大环内酯类弯曲菌列为影响公共卫生的耐药威胁之一[14]。弯曲菌的耐药性的产生主要由基因水平转移和耐药基因获得引起[15],但本研究中尚未深入开展对弯曲菌耐药基因及其相关影响因素的研究。在后续研究中,上海市将持续开展弯曲菌耐药监测,并对耐药株开展耐药相关基因检测和传播机制、影响因素等研究,为弯曲菌治疗和防控等提供科学依据。
利益冲突 所有作者均声明不存在利益冲突
| [1] |
Altekruse SF, Stern NJ, Fields PI, et al. Campylobacter jejuni-an emerging foodborne pathogen[J]. Emerg Infect Dis, 1999, 5(1): 28-35. DOI:10.3201/eid0501.990104 |
| [2] |
Ravel A, Pintar K, Nesbitt A, et al. Non-food-related risk factors of campylobacteriosis in Canada:a matched case-control study[J]. BMC Public Health, 2016, 16: 1016. DOI:10.1186/s12889-016-3679-4 |
| [3] |
Clark CG, Berry C, Walker M, et al. Genomic insights from whole genome sequencing of four clonal outbreak Campylobacter jejuni assessed within the global C. jejuni population[J]. BMC Genomics, 2016, 17: 990. DOI:10.1186/s12864-016-3340-8 |
| [4] |
吴蜀豫, 张立实, 冉陆. 弯曲菌及弯曲菌病的流行现状[J]. 中国食品卫生杂志, 2004, 16(1): 58-61. Wu SY, Zhang LS, Ran L. Epidemiology of campylobacter and campylobacteriosis[J]. Chin J Food Hyg, 2004, 16(1): 58-61. DOI:10.3969/j.issn.1004-8456.2004.01.021 |
| [5] |
黎健, 胡家瑜, 吴寰宇, 等. 上海市2013年8月至2014年7月腹泻病例病原学监测研究[J]. 中华流行病学杂志, 2015, 36(10): 1099-1103. Li J, Hu JY, Wu HY, et al. Etiological surveillance for diarrhea in Shanghai from August 2013 to July 2014[J]. Chin J Epidemiol, 2015, 36(10): 1099-1103. DOI:10.3760/cma.j.issn.0254-6450.2015.10.014 |
| [6] |
屠丽红, 陈洪友, 陈敏. 上海市2014年腹泻患者弯曲菌分离、毒力基因检测及分子分型结果[J]. 上海预防医学, 2015, 27(6): 311-314. Tu LH, Chen HY, Chen M. Campylobacter spp. isolation, its toxin genes detection and molecular subtyping in diarrhea patients in Shanghai in 2014[J]. Shanghai J Prev Med, 2015, 27(6): 311-314. DOI:10.19428/j.cnki.sjpm.2015.06.003 |
| [7] |
卫生部. WS 271-2007感染性腹泻诊断标准[S].北京: 人民卫生出版社, 2007. Administration of Health. Diagnostic criteria for infectious diarrhea[S]. Beijing: People's Medical Publishing House, 2007. |
| [8] |
USCDC. Antimicrobial agents used for susceptibility testing of Campylobacter isolates[EB/OL].[2019-02-28]. https://www.cdc.gov/narms/antibiotics-tested.html.
|
| [9] |
王云霞, 刘海波, 史文凤, 等. 北京市房山区空肠弯曲菌检测与感染现状[J]. 公共卫生与预防医学, 2018, 29(6): 71-73. Wang YX, Liu HB, Shi WF, et al. Laboratory detection and infection status of Campylobacter jejuni in Fangshan, Beijing[J]. J Pub Health Prev Med, 2018, 29(6): 71-73. DOI:10.3969/j.issn.1006-2483.2018.06.018 |
| [10] |
王彦波, 李颖, 李湛. 北京市顺义区370份腹泻病例中弯曲菌监测结果[J]. 首都公共卫生, 2018, 12(4): 211-213. Wang YB, Li Y, Li Z. The surveillance result of Campylobacter detection in 370 diarrhea patients in Shunyi district of Beijing[J]. Capit J Public Health, 2018, 12(4): 211-213. DOI:10.16760/j.cnki.sdggws.2018.04.017 |
| [11] |
王为, 王蓓蕾, 胡桂学, 等. 空肠弯曲菌在环境压力条件下的生存机制和可培养性研究进展[J]. 肉类研究, 2011, 25(5): 37-39. Wang W, Wang BL, Hu GX, et al. Recent advances in research on survival mechanisms and culturability of Campylobacter jejuni under stress conditions[J]. Meat Res, 2011, 25(5): 37-39. DOI:10.3969/j.issn.1001-8123.2011.05.009 |
| [12] |
顾一心, 何利华, 刘红莹, 等. 空肠弯曲菌耐药谱特征分析[J]. 疾病监测, 2013, 28(4): 314-318. Gu YX, He LH, Liu HY, et al. Drug susceptibility of Campylobacter jejuni isolated in China[J]. Dis Survil, 2013, 28(4): 314-318. DOI:10.3784/j.issn.1003-9961.2013.4.018 |
| [13] |
Luangtonkum T, Jeon B, Han J, et al. Antibiotic resistance in Campylobacter:emergence, transimission and persistence[J]. Future Microbiol, 2009, 4(2): 189-200. DOI:10.2217/17460913.4.2.189 |
| [14] |
USCDC. Antibiotic resistance threats in the United States[EB/OL]. (2013-07-14)[2019-02-28]. http://www.cdc.gov/drugresistance/threat-report-2013/.
|
| [15] |
白瑶, 叶淑瑶, 李凤琴. 弯曲菌耐药机制研究进展[J]. 中华预防医学杂志, 2018, 52(10): 1072-1077. Bai Y, Ye SY, Li FQ. Overview of resistance mechanisms in Campylobacter[J]. Chin J Prev Med, 2018, 52(10): 1072-1077. DOI:10.3760/cma.j.issn.0253-9624.2018.10.021 |
 2019, Vol. 40
2019, Vol. 40