文章信息
- 殷召雪, 任泽萍, 荆刚, 刘丹, 张坚, 王卓群, 张梅, 翟屹, 宋鹏坤, 赵艳芳, 庞邵杰, 米生权, 赵文华.
- Yin Zhaoxue, Ren Zeping, Jing Gang, Liu Dan, Zhang Jian, Wang Zhuoqun, Zhang Mei, Zhai Yi, Song Pengkun, Zhao Yanfang, Pang Shaojie, Mi Shengquan, Zhao Wenhua.
- 老年人肾健康相关膳食模式与认知障碍关系的队列研究
- A cohort study on the association between dietary patterns which benefit for normal kidney function and the cognitive performance in the Chinese elderly
- 中华流行病学杂志, 2019, 40(4): 427-432
- Chinese Journal of Epidemiology, 2019, 40(4): 427-432
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2019.04.011
-
文章历史
收稿日期: 2018-09-27
2. 山西省疾病预防控制中心慢病所, 太原 030012;
3. 山西省临猗县疾病预防控制中心, 临猗 044100;
4. 中国疾病预防控制中心营养与健康所, 北京 100050;
5. 中国疾病预防控制中心慢性非传染性疾病预防控制中心, 北京 100050;
6. 首都医科大学附属北京天坛医院国家神经系统疾病临床医学研究中心, 北京 100070;
7. 国家粮食局科学研究院粮食品质营养研究所, 北京 100037;
8. 北京联合大学健康与环境学院 100101
2. Division for Non-communicable Disease Control, Shanxi Provincial Center for Disease Control and Prevention, Taiyuan 030012, China;
3. Linyi County Center for Disease Control and Prevention of Shanxi Province, Linyi 044100, China;
4. Institute for Nutrition and Health, Chinese Center for Disease Control and Prevention, Beijing 100050, China;
5. Center for Chronic and Non-communicable Disease Control and Prevention, Chinese Center for Disease Control and Prevention, Beijing 100050, China;
6. Beijing Tiantan Hospital, Capital Medical University, China National Clinical Research Center for Neurological Diseases, Beijing 100070, China;
7. Institute of Grain Quality and Nutrition, Academy of State Administration of Grain, Beijing 100037, China;
8. College of Health and Environment, Beijing Union University, Beijing 100101, China
伴随我国人口老龄化形势的加剧,阿尔茨海默病和痴呆症的流行也逐渐成为一个重要的公共卫生问题,但目前尚无治疗阿尔茨海默病的有效药物,研究认为全球超过1/3的阿尔茨海默病及其前期的认知功能受损是可以通过改善生活方式来预防的[1],从膳食营养角度开展干预是减缓认知受损进程、预防阿尔茨海默病很具前景的方向。相对于某种营养素或食物,膳食模式更能反映膳食营养的健康作用[2],很多研究也发现膳食模式对于认知功能具有明显的影响,比如地中海膳食模式不但可降低阿尔茨海默病的发病风险,还可减缓痴呆前症状到痴呆的发展进程[3]。采用降秩回归法(reduced rank regression,RRR)选择特定生物指标为反应变量,能够提取与所选生物指标相关的特定类型的膳食模式,通过研究该类型膳食模式与认知功能的关系,有助于探索膳食模式与健康结局之间关系的可能生物机制,如Ozawa等[4]用RRR提取了中老年人炎性膳食模式,发现以“红肉、加工肉和油炸食物摄入较多,全谷物摄入较少”为特征的炎性膳食模式与认知功能降低关系明显。但该方法在国内应用较少[5]。肾功能受损也是老年人常见的慢性疾病,研究表明膳食模式会明显影响肾功能水平[6],肾功能水平也是影响认知功能的重要因素[7],提示肾功能水平可能是膳食与认知功能之间关系的重要途径。因此本研究以肾小球滤过率(estimated glomerular filtration rate,eGFR)为反应变量,采用RRR提取能够最大程度解释eGFR变异的膳食模式,这种膳食模式评分与eGFR水平两者之间具有正向的关联,由于eGFR水平是反映肾功能的指标,可以反映肾的健康水平,因而将这种膳食模式命名为肾健康相关膳食模式。通过分析肾健康相关膳食模式评分与认知功能的关系,探索肾功能在膳食模式与认知功能关系中的可能作用。
对象与方法1.研究对象:数据来自山西营养与慢性病家庭队列,该队列建于2002年并于2015年进行第一次随访,收集调查对象社会人口学特征、生活方式及患病状况,评估了认知功能,并采集空腹静脉抗凝血样测定血浆TG、TC、肌酐和尿素氮等指标[5, 8]。2017年对2015年参加调查的4个县(晋城市阳城县、忻州市五寨县、晋中市和顺县和运城市临猗县)的1 003名≥60岁老年人进行健康结局专项随访,并再次评估认知功能及其变化。除去死亡和由于搬迁、无法联系等各种原因导致的失访、拒访,共随访到存活老年人784名。去除认知功能评定不完整和估计eGFR缺失者,共有712名老年人纳入本研究。其中2015年随访时认知功能正常的对象有638人。
2.研究方法:山西营养与慢性病家庭队列通过食物频率法(FFQ)收集了40种食物/食物组的摄入情况。根据食物种类及归属,对研究对象2015年40种食物/食物组进行分类,形成24种食物组,将所有食物的摄入频率转化为每天摄入次数,每天摄入次数乘以每次摄入量即为每种/组食物的摄入量,随后对摄入量数据进行标准化。RRR是通过建立摄入食物变量的线性函数来解释反应变量(如营养素摄入、生物标志物测量等)的变异,采用已有的研究发现,提取出最大程度解释反应变量变异的膳食模式,找到影响反应变量的食物种类,可为进一步通过膳食干预预防疾病提供建议,有助于在分析膳食模式与健康结局的关系的同时分析可能的机制。采用RRR,选取eGFR作为反应变量,可提取肾健康相关的膳食模式。
3.相关指标定义和诊断标准:采用国际上广泛使用的简易精神状态量表(Mini Mental State Evaluation,MMSE)测定认知功能,该量表可测定定位、识别、计算能力、记忆能力及语言能力,总分30分,得分越高认知功能越好。由于教育程度是认知功能非常重要的影响因素,本研究中采用基于教育程度的认知受损的评定标准[9],即:未受过教育者认知受损标准为MMSE ≤19,接受教育1~6年者认知受损标准为MMSE≤22,接受教育>6年者为MMSE≤26,否则定义为认知正常。认知功能MMSE评分降低≥3分判定为认知功能下降[10],研究表明这是判定认知功能下降较为可靠的标准。婚姻状况分为是否在婚,不在婚包括离婚、丧偶或从未结婚。采用身体活动频率和强度计算总代谢当量值,根据总代谢当量值是否高于研究人群总代谢当量值的均值确定身体活动是否不足。血压测量3次取其均值用于高血压判定,标准:SBP≥140 mmHg(1 mmHg=0.133 kPa)或DBP≥90 mmHg,或者报告已诊断的高血压,或者报告正服用降压药。糖尿病判定标准:FPG≥7.0 mmol/L,或报告已诊断为糖尿病。BMI=体重/身高2,按BMI≥28 kg/m2定义为肥胖。采用Katz量表评价日常生活自理能力(activities of daily living,ADL),如果“洗澡、穿衣、大小便、室内活动、憋住大小便和吃饭”6项活动中,有一项需要帮助,则定义为ADL受损[11]。高胆固醇血症定义为TC≥6.22 mmol/L,高TG血症定义为空腹TG≥2.26 mmol/L[12]。eGFR由肾病膳食改良(modification of diet in renal disease,MDRD)研究公式计算[13]:男性:eGFR(ml/min/1.73 m2)=186×(血肌酐/88.4)-1.154×(Age)-0.203;女性:eGFR(ml/min/1.73 m2)=186×(血肌酐/88.4)-1.154×(Age)-0.203×0.742。肾功能受损定义为eGFR<90 ml/min/1.73 m2,其中60 ml/min/1.73 m2≤eGFR<90 ml/min/1.73 m2为轻度受损,30 ml/min/1.73 m2≤eGFR<60 ml/min/1.73 m2为中度受损,eGFR<30 ml/min/1.73 m2为重度受损[14]。
4.统计学分析:通过t检验或χ2检验比较认知功能是否下降两组对象特征的差异。RRR提取膳食模式可通过SAS软件PLS过程的选项(Method=RRR)来实现。24类食物的因子负荷代表每个食物组对肾健康相关膳食模式贡献的大小和方向。膳食模式因子负荷与标准化的食物摄入量相乘即得膳食模式评分,针对每个个体,计算所得膳食模式评分。
按肾健康相关膳食模式评分的三分位数将研究对象分为3组(<P33.3、P33.3~、≥P66.6),分析不同三分位数组下研究对象的特征和食物摄入量,并采用广义线性模型进行趋势分析。将分组设置哑变量后,采用logistic回归,调整年龄、能量摄入水平、性别(男性=对照)、教育程度(未受过教育=对照)、吸烟(否=对照)、饮酒(否=对照)、身体活动不足(身体活动足=对照)、高血压(无=对照)、糖尿病(无=对照)、中风(无=对照)、肥胖(否=对照)、ADL失能(否=对照)、高TC(否=对照)、高TG(否=对照)。通过logistic回归,采用2015-2017年队列分析肾健康相关膳食模式与认知功能下降之间的关系,进行趋势分析。进一步以2015年认知功能正常者为研究对象,分析肾健康相关膳食模式与2年后认知受损发生之间的关系。
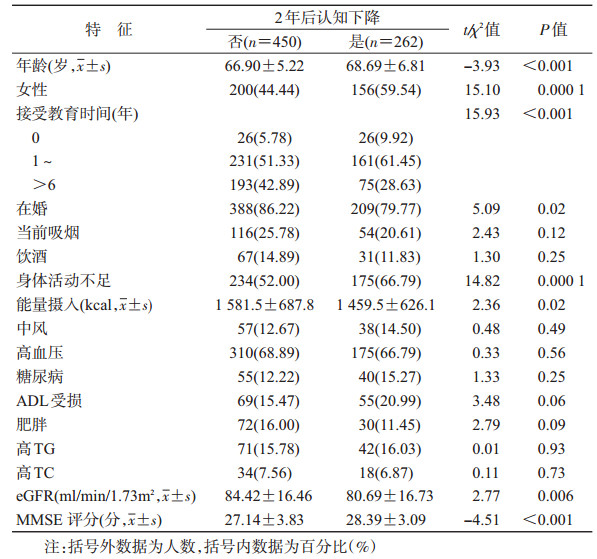
结果1.一般特征:与2017年认知功能未下降者相比,认知下降者在基线时(2015年)年龄偏大,女性比例较高,身体活动不足比例较高(P<0.001);接受教育时间较少(P<0.001),在婚状态的比例和能量摄入水平均较低(P<0.01);估计的eGFR较低。见表 1。
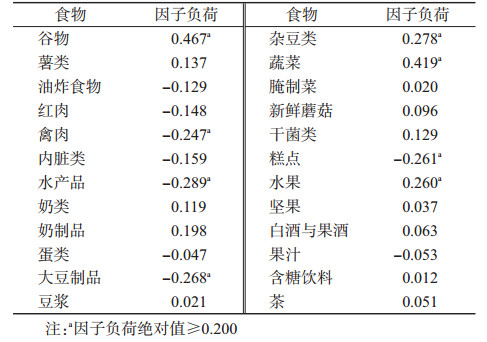
2.肾健康相关膳食模式提取:采用RRR,选择eGFR对数值作为反应变量,提取能够最大程度解释eGFR的膳食模式(肾健康相关膳食模式),该种模式摄入谷物、杂豆类、蔬菜和水果较多,肉类、水产品、大豆制品等食物摄入较少,见表 2。该膳食模式解释食物变异为8.77%,可解释反应变量的变异为12.44%。
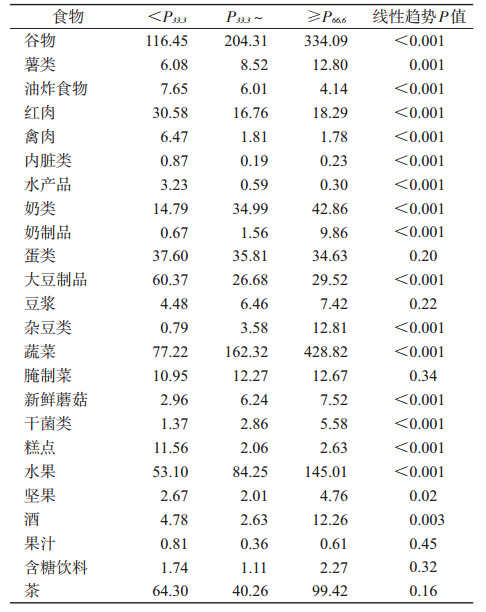
3.肾健康相关膳食模式评分不同三分位数组食物摄入量:与肾健康相关膳食模式平均<P33.3组相比,该模式较高分位数组研究对象女性比例较低(线性趋势P<0.01),身体活动不足和ADL受损的比例较低(线性趋势P<0.01),eGFR水平较高(线性趋势P<0.01)。随着肾健康相关膳食模式评分升高,谷物、蔬菜、杂豆类和水果等食物摄入明显增多,如蔬菜人均日摄入量从<P33.3组的77 g升高至≥P66.6组的429 g,水果从<P33.3组的53 g升至145 g。禽肉水产等肉类及大豆制品摄入量明显较低,肾健康相关模式评分<P33.3组每人每日肉类摄入量大约在40 g,而在≥P66.6组摄入量仅约21 g。见表 3。
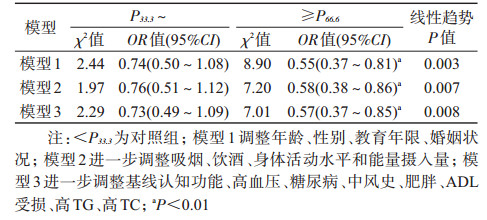
4.肾健康相关膳食模式与2年后认知下降风险之间的关系:logistic回归分析表明,调整多个混杂因素之后,肾健康相关膳食模式与2年后认知功能下降风险明显负相关(P<0.01)。与该膳食模式评分<P33.3组相比,调整年龄、性别、教育年限、婚姻状况、吸烟、饮酒、身体活动水平、能量摄入量、中风史、ADL受损、高TG和TC后,该膳食模式评分≥P66.6组2年后发生认知下降的风险明显较低,OR值(95%CI)为0.57(0.37~0.85),而且随着评分升高,认知下降的风险具有显著的线性下降趋势(P=0.007)。见表 4。
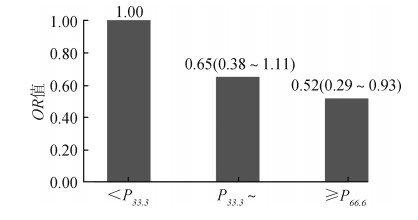
5.认知正常者中肾健康相关膳食模式与2年后发生认知受损的关系:logistic回归分析表明,在2015年认知功能正常者中,调整多个混杂因素之后,肾健康相关膳食模式与2年后认知受损明显负相关(P<0.05)。与该膳食模式评分<P33.3组相比,调整混杂因素(同以上模型3)后,≥P66.6组2年后发生认知受损的风险明显降低(P<0.05),OR值(95%CI)为0.52(0.29~0.93),而且随着膳食模式评分升高,各组风险具有显著的线性下降趋势(P=0.01),见图 1。
|
| 图 1 认知正常者肾健康相关膳食模式与2年后认知受损发生风险关系的logistic回归分析 |
本研究选择eGFR作为反应变量通过RRR提取了肾健康相关膳食模式,其特征是谷物、蔬菜、杂豆类和水果摄入较多,而肉类、大豆制品等食物摄入较少。肾健康相关膳食模式从食物的角度较大程度地解释了eGFR的变异,高于之前研究中RRR所提取膳食模式对反应变量的解释比例[4-5]。本研究结果显示,肾健康相关膳食模式评分较高者2年后发生认知下降的风险明显较低,在基线认知功能正常的老年人中,肾健康相关膳食模式评分较高者2年后认知受损的发生风险也明显较低。这可能有以下两方面的解释:首先,蔬菜水果和谷物类食物对于认知功能受损具有重要的认知保护作用。Meta分析结果显示,水果和蔬菜摄入可使认知受损和痴呆风险降低20%,剂量反应关系分析表明,每天多摄入100 g的水果和蔬菜,可使认知受损风险降低13%[15]。这可能与蔬菜水果中含有大量抗氧化物质、抗炎性物质有关。Ozawa等[4]提取到的炎性膳食模式评分较高的人推理能力降低更为明显,而且认知功能降低更快,而谷物摄入较少是其重要特征,提示谷物摄入可能有助于认知功能的保护。其次,蔬菜水果和谷物摄入较多而肉类甜食较少的膳食可能有助于保护eGFR水平[6],蛋白质摄入较多与肾功能降低明显相关[16],而肾功能受损会明显增加认知功能受损风险。已有研究表明肾功能受损者发生认知障碍的风险会明显升高[7],其原因可能包括小血管病、尿毒素导致的神经元损伤[17]。
本研究结果显示,肾健康相关膳食模式与本项目组之前报道的血压相关膳食模式不同[5],二者的膳食组成和相对量有所不同,而且所解释的生物指标及与认知功能的关联也是不同的。血压相关膳食模式解释的是研究人群的血压水平,与认知受损风险明显正相关;而肾健康相关膳食模式解释的是研究对象eGFR水平,因而与认知功能之间的关系是不同的。
本研究的优势在于用RRR提取了与肾健康相关的膳食模式,并分析其与认知功能受损的关系,这种膳食模式最大程度解释了eGFR的变异,对于初步探索膳食与认知功能关系的机制具有重要意义。尽管这种膳食模式不能代表研究人群中实际的膳食模式,但该膳食模式的主要特点与我们之前采用因子分析法在该人群实际提取到的“谷物蔬果”膳食模式的特点类似[8],因此,可以认为本研究采用RRR提取到的肾健康相关膳食模式仍具有重要的公共卫生意义。
本研究存在一定的局限性。MMSE是目前应用最为广泛的认知功能筛查量表,能够反映总体认知功能,但由于该量表敏感性偏低,因而在评估认知功能水平上可能会出现假阴性,进而会低估膳食模式与认知功能下降或受损之间的关联。
综上所述,肾健康相关膳食模式评分与认知下降风险和认知受损风险均明显负相关,坚持肾健康相关膳食模式,多摄入谷物、蔬菜、水果等食物,可能有助于维护认知功能,该结论仍需更多干预性研究进行验证。
利益冲突 所有作者均声明不存在利益冲突
| [1] |
Livingston G, Sommerlad A, Orgeta V, et al. Dementia prevention, intervention, and care[J]. Lancet, 2017, 390(10113): 2673-2734. DOI:10.1016/S0140-6736(17)31363-6 |
| [2] |
殷召雪, 赵文华. 膳食模式是营养与健康的关键[J]. 中华健康管理学杂志, 2017, 11(1): 3-6. Yin ZX, Zhao WH. Dietary pattern:the key for nutrition and health[J]. Chin J Health Manage, 2017, 11(1): 3-6. DOI:10.3760/cma.j.issn.1674-0815.2017.01.002 |
| [3] |
Solfrizzi V, Panza F. Mediterranean diet and cognitive decline. A lesson from the whole-diet approach:What challenges lie ahead?[J]. J Alzheimers Dis, 2014, 39(2): 283-286. DOI:10.3233/JAD-130831 |
| [4] |
Ozawa M, Shipley M, Kivimaki M, et al. Dietary pattern, inflammation and cognitive decline:The Whitehall Ⅱ prospective cohort study[J]. Clin Nutr, 2017, 36(2): 506-512. DOI:10.1016/j.clnu.2016.01.013 |
| [5] |
殷召雪, 任泽萍, 徐小刚, 等. 基于降秩回归的血压相关膳食模式与老年人认知受损的关系[J]. 中华流行病学杂志, 2018, 39(6): 781-785. Yin ZX, Ren ZP, Xu XG, et al. Association between blood pressure related dietary patterns and identified cognitive performance in the elderly Chinese-a study by reduced rank regression method[J]. Chin J Epidemiol, 2018, 39(6): 781-785. DOI:10.3760/cma.j.issn.0254-6450.2018.06.017 |
| [6] |
Lin J, Fung TT, Hu FB, et al. Association of dietary patterns with albuminuria and kidney function decline in older white women:a subgroup analysis from the nurses' health study[J]. Am J Kidney Dis, 2011, 57(2): 245-254. DOI:10.1053/j.ajkd.2010.09.027 |
| [7] |
Wei YD, Wei YK, Zhu JM. Early markers of kidney dysfunction and cognitive impairment among older adults[J]. J Neurol Sci, 2017, 375: 209-214. DOI:10.1016/j.jns.2017.01.071 |
| [8] |
Yin ZX, Chen J, Zhang J, et al. Dietary patterns associated with cognitive function among the older people in underdeveloped regions:Finding from the NCDFaC study[J]. Nutrients, 2018, 10(4): 464. DOI:10.3390/nu10040464 |
| [9] |
Yin ZX, Yan ZR, Liang YJ, et al. Interactive effects of diabetes and impaired kidney function on cognitive performance in old age:a population-based study[J]. BMC Geriatr, 2016, 16: 7. DOI:10.1186/s12877-016-0193-6 |
| [10] |
Tombaugh TN. Test-retest reliable coefficients and 5-year change scores for the MMSE and 3MS[J]. Arch Clin Neuropsychol, 2005, 20(4): 485-503. DOI:10.1016/j.acn.2004.11.004 |
| [11] |
Katz S, Ford AB, Moskowitz RW, et al. Studies of illness in the aged:The index of ADL:A standardized measure of biological and psychosocial function[J]. JAMA, 1963, 185(12): 914-919. DOI:10.1001/jama.1963.03060120024016 |
| [12] |
中国成人血脂异常防治指南修订联合委员会. 中国成人血脂异常防治指南:2016年修订版[J]. 中华健康管理学杂志, 2017, 11(1): 7-28. Joint Committee Issued Chinese Guideline for the Management of Dyslipidemia in Adults. 2016 Chinese guideline for the management of dyslipidemia in adults[J]. Chin J Health Manage, 2017, 11(1): 7-28. DOI:10.3760/cma.j.issn.1674-0815.2017.01.101 |
| [13] |
Levey AS, Bosch JP, Lewis JB, et al. A more accurate method to estimate glomerular filtration rate from serum creatinine:a new prediction equation[J]. Ann Intern Med, 1999, 130(6): 461-470. DOI:10.7326/0003-4819-130-6-199903160-00002 |
| [14] |
National Kidney Foundation. K/DOQI clinical practice guidelines for chronic kidney disease:evaluation, classification, and stratification[J]. Am J Kidney Dis, 2002, 39(2 Suppl 1): S1-266. |
| [15] |
Jiang X, Huang J, Song DQ, et al. Increased consumption of fruit and vegetables is related to a reduced risk of cognitive impairment and dementia:meta-analysis[J]. Front Aging Neurosci, 2017, 9: 18. DOI:10.3389/fnagi.2017.00018 |
| [16] |
Martin WF, Armstrong LE, Rodriguez NR. Dietary protein intake and renal function[J]. Nutr Metab (Lond), 2005, 2: 25. DOI:10.1186/1743-7075-2-25 |
| [17] |
Bugnicourt JM, Godefroy O, Chillon JM, et al. Cognitive disorders and dementia in CKD:the neglected kidney-brain axis[J]. J Am Soc Nephrol, 2013, 24(3): 353-363. DOI:10.1681/ASN.2012050536 |
 2019, Vol. 40
2019, Vol. 40