文章信息
- 宁铁林, 郑敏娜, 李龙, 柏建芸, 赵璇, 郭燕, 杜向瑞, 程绍辉.
- Ning Tielin, Zheng Minna, Li Long, Bai Jianyun, Zhao Xuan, Guo Yan, Du Xiangrui, Cheng Shaohui.
- 天津市男男性行为人群HIV-1急性期感染研究
- Study on acute HIV-1 infection in men who have sex with men in Tianjin
- 中华流行病学杂志, 2018, 39(11): 1472-1476
- Chinese Journal of Epidemiology, 2018, 39(11): 1472-1476
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2018.11.010
-
文章历史
收稿日期: 2018-05-14
2. 300070 天津医科大学
2. Tianjin Medical University, Tianjin 300070, China
HIV-1急性期感染是指从感染HIV到抗体出现阳转之间的过程,大约持续1个月左右,虽然存在时间较短,但由于病毒在这段时间大量复制,且常规方法难以检出,因而具有很强的传染性。研究显示,通过性接触感染病例中约50%是由处于HIV-1急性期和早期感染性伴所传播[1]。MSM作为HIV感染的高危人群,性活跃程度高且多性伴和无保护肛交行为普遍,极易导致HIV-1急性期感染传播。近年来,我国HIV男男性传播比例逐年上升,但有关MSM中HIV-1急性期感染研究的报道相对较少,了解该人群HIV-1急性期感染特征和流行状况,并采取针对性的干预措施,对艾滋病防治具有重要公共卫生意义。
对象与方法1.研究对象:将年龄≥16岁,最近6个月内与男性发生过口交或肛交性行为的MSM作为研究对象。2015年10月至2016年10月依托天津市主要的4个MSM人群志愿者工作组,通过网络招募和滚雪球方式动员其参与检测。
2.研究方法:对每名研究对象采集静脉血3~5 ml,EDTAK3抗凝,现场进行HIV抗体快速检测,随后将血样离心分离血浆。初筛阳性样本按照《全国艾滋病检测技术规范》(2015年修订版)标准流程进行复检和最终确证。初筛阴性样本在48 h内进行HIV-1 RNA集合核酸检测,对阳性病例测定其病毒载量值,补充进行HIV四代ELISA检测和P24 ELISA检测,同时开展流行病学信息调查,重新采血进行第二次核酸检测及CD4+T淋巴细胞计数(CD4)和CD8+T淋巴细胞计数(CD8)。依照《艾滋病和艾滋病病毒诊断标准(WS 293-2008)》,将HIV抗体初筛阴性,两次核酸检测阳性病例定义为HIV-1急性期感染。
3.试验检测:使用HIV抗体快速检测试剂盒(广州万孚生物技术股份有限公司)对样品进行初筛,采用HIV四代ELISA检测试剂盒(北京万泰生物药业有限公司)及原快速检测试剂盒对初筛阳性样品进行复检,确证试验使用Genelab Diagnostics HIV BLOT 2.2 Western试剂盒(新加坡MP公司)过夜法检测。HIV-1 RNA集合核酸检测使用罗氏全自动病毒载量检测系统(COBAS AmpliPrep/COBAS TaqMan HIV-1 Test,version 2.0),每24份样品组成一个集合,阳性集合逐级拆分至单个样本后经病毒载量测定做最终判定,病毒载量最低检出限为20拷贝数/ml。采用流式细胞仪(BD公司FACSCanto Ⅱ)四色荧光标记方法(CD3/CD8/CD45/CD4)检测CD4和CD8。使用HIV四代ELISA检测试剂盒(北京万泰生物药业有限公司)和P24 ELISA检测试剂盒(北京科跃中楷生物技术有限公司)同时检测HIV-1急性期感染者首次采集样本。以上试验均严格按照说明书进行操作和质量控制。
4.统计学分析:对于计量资料以(x±s)加以描述,利用Graphpad Prism 7.0软件进行统计学处理,使用Kolmogorov-Smirnov法检验变量是否服从正态分布,呈正态分布且方差不齐数据使用Welch法对两组样本差异性进行校正t检验,非正态分布数据采用Mann-Whitney U检验,构成比和不同检测方法灵敏度比较使用χ2检验。检验水准α=0.05,双侧检验。
结果1. HIV-1急性期感染:共招募MSM 3 016例,HIV抗体快速检测阳性193例,确证阳性179例,不确定7例,阴性7例。HIV抗体快速检测阴性2 823例,核酸检测阳性18例,其中1例经流行病学调查为既往阳性,17例为HIV-1急性期感染。研究对象HIV-1感染率为6.53%(197/3 016),HIV-1急性期感染率为0.56%(17/3 016)。
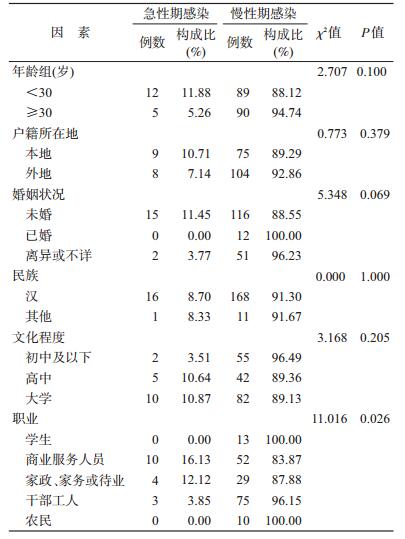
2. HIV-1急性期感染与慢性期感染的人口学特征比较:17例HIV-1急性期感染者年龄(32.6±10.4)岁,30岁以下占70.59%(12/17),本市户籍占52.94%(9/17),未婚者居多,占88.24%(15/17),汉族为主,占94.12%(16/17),大学文化程度者占58.82%(10/17),多数为商业服务人员,占58.82%(10/17)。经χ2检验,HIV-1急性期与慢性期感染者除职业构成差异具有统计学意义(χ2=11.016,P=0.026)外,在年龄、户籍、婚姻状况、民族和文化程度变量构成差异均无统计学意义(P>0.05),见表 1。
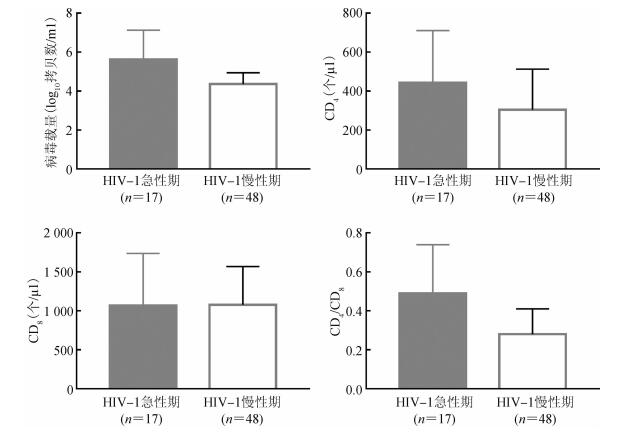
3. HIV-1急性期与慢性期感染者CD4、CD8及病毒载量比较:17例HIV-1急性期感染样本的病毒载量为(5.63±1.50)log10拷贝数/ml,CD4为(442.82±268.17)个/μl,CD8为(1 069.65±668.22)个/μl,CD4/CD8比值为(0.49±0.25)。对随机抽取的48例慢性期感染样本进行测定,病毒载量为(4.36±0.58)log10拷贝数/ml,CD4为(304.54±208.76)个/μl,CD8为(1 077.10±491.26)个/μl,CD4/CD8比值为(0.28±0.13)。HIV-1急性期感染样本与慢性期感染样本相比,病毒载量差异具有统计学意义(U=148,P<0.01),CD4差异具有统计学意义(U=272,P=0.042),CD8差异无统计学意义(t=0.042,P=0.967),CD4/CD8比值差异有统计学意义(t=3.147,P=0.005),见图 1。
|
| 图 1 天津市男男性行为人群HIV-1急性期感染与慢性期感染的CD4、CD8及病毒载量结果分析 |
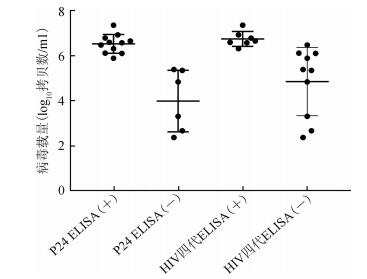
4. P24 ELISA与HIV四代ELISA检测结果比较:17例HIV-1急性期感染样本中P24 ELISA检出阳性11例,病毒载量为(6.53±0.42)log10拷贝数/ml;阴性6例,病毒载量为(3.99±1.37)log10拷贝数/ml,经检验两组间差异具有统计学意义(t=4.440,P=0.005);HIV四代ELISA检出阳性7例,病毒载量为(6.75±0.33)log10拷贝数/ml,阴性10例,病毒载量为(4.85±1.52)log10拷贝数/ml,经检验两组间差异具有统计学意义(t=3.821,P=0.003),见图 2,提示两种方法的检测结果均与样品中病毒载量水平存在关联。本研究中P24 ELISA和HIV四代ELISA未检出样品病毒载量最高值分别为5.39 log10拷贝数/ml和6.48 log10拷贝数/ml,提示相比P24 ELISA,HIV四代ELISA对更高病毒载量水平的样品仍无法获得检出,灵敏度存在不足。进一步对两种方法进行χ2检验,结果显示,对于HIV-1急性期感染样本,P24 ELISA灵敏度高于HIV四代ELISA(Fisher精确检验法,P=0.017)。
|
| 图 2 天津市男男性行为人群HIV-1急性期感染研究两种方法检测结果比较 |
早期发现和早期治疗是减少和控制艾滋病传播的重要手段[2-4],调查发现,天津市MSM人群HIV-1急性感染率为0.56%,感染者血浆中病毒载量为(5.63±1.50)log10拷贝数/ml,高于国外研究结果[5],处于高病毒血症阶段,虽然急性感染期血浆病毒载量水平不能预示疾病进程,但一些前瞻性研究表明,在急性期开始抗病毒治疗可以取得更好的治疗效果,甚至有望达到功能性治愈[6],Chun等[7]发现,如果治疗在抗体阳转前或之中开始,当抗病毒治疗停止后,免疫系统会在一定程度上得以保留,并且血中病毒载量会持续降低。高病毒血症是急性期感染的重要特征,诊断前的高危性行为被认为是造成HIV传播增加的关键因素[8],而本研究所发现的HIV-1急性期感染者多为青壮年,正处于性活跃期,虽然与慢性期感染者在年龄构成的差异无统计学意义,但有报道认为,与处于HIV慢性感染期相比,急性期和早期感染者同时拥有的性伴数量更多[9-10],因此从疾病传播的角度来讲,急性期感染者行为学因素导致的危害更甚于高病毒血症所带来的预期风险[11]。HIV大量复制导致宿主免疫功能紊乱是HIV-1急性期感染的重要特征,具有极高的传播风险,在艾滋病高危人群中开展HIV-1急性期感染检测是提高感染发现的重要途径,加强HIV核酸检测具有重要的公共卫生意义。
本研究显示,HIV-1急性期感染者体内CD4数量高于慢性期感染者,而CD8则基本持平。Robb等[12]在非洲和泰国的研究发现,在HIV-1急性期感染的病毒复制高峰期,CD4和CD8会分别发生下降和上升,随后虽可逐渐恢复,但难以回到初始水平,这与本研究结果不符,推测或与招募的研究对象所处感染时间不同有关,本研究发现的17例急性期感染者可能感染时间更短。既往研究认为,淋巴细胞亚型在感染初始至病毒血症出现之前变化并不明显,而病毒血症高峰则会发生剧烈波动,因此CD4/CD8比值倒置往往发生在原发感染14 d之后,急性期CD8大量增殖使得CD4/CD8比值多<0.5[13]。本研究中虽然全部急性期感染者均出现CD4/CD8比值倒置,但仅有约一半的比值<0.5,且病毒载量水平远高于慢性期感染,提示在HIV-1急性期感染病毒复制迅速且持续时间短暂,受细胞毒性淋巴细胞效应影响,机体免疫系统遭到破坏,但严重程度存在差异,因此,对于近期有过高危性行为的MSM来说,出现CD4/CD8比值倒置的结果,无论比值高低都应该引起高度怀疑。
一些研究发现,40%~90%的HIV-1急性期感染者会出现临床症状,但这些症状通常存在时间较短且非特异性[14-16],因此核酸检测仍然是早期发现感染者的重要手段[17]。美国已将HIV-1 RNA检测纳入急性期感染检测指南[18],近年来即时检测HIV-1 RNA技术的发展更为扩大急性期感染筛查提供了可能[19],然而昂贵的成本限制了核酸检测在发展中国家推广使用。WHO的HIV检测服务指南[20]建议艾滋病高危人群应每年至少检测1次HIV,抗体快速检测作为许多国家用于MSM社区筛查的主要方法,虽然具有操作简便、结果及时等优势,但仍无法满足急性期感染检测需要。本研究结果显示,在17例HIV抗体快速检测阴性的急性期感染样本中,7例HIV四代ELISA结果阳性,11例P24 ELISA检测阳性,提示P24抗原是HIV-1急性期感染的重要标志物,针对P24抗原成分检测可以大大提高急性期感染发现概率,而P24 ELISA试剂相比于HIV四代ELISA试剂,检测灵敏度更高,可为资源有限地区制定MSM人群HIV-1急性期感染筛查策略提供参考。但由于本研究样本数量有限,且未涵盖HIV阴性样本,因而尚无法对其特异度进行评价,在MSM人群中的应用效果有待进一步深入研究。
综上所述,MSM人群HIV-1急性期感染风险较高,采用P24 ELISA试剂可提高HIV-1急性期感染的检测灵敏度。加强HIV核酸检测是提高感染发现的重要途径。
利益冲突 无
| [1] |
Brenner BG, Roger M, Routy JP, et al. High rates of forward transmission events after acute/early HIV-1 infection[J]. J Infect Dis, 2007, 195(7): 951-959. DOI:10.1086/512088 |
| [2] |
Sanders EJ, Wahome E, Power KA, et al. Targeted screening of at-risk adults for acute HIV-1 infection in sub-Saharan Africa[J]. AIDS, 2015, 29 Suppl 3: S221-230. DOI:10.1097/QAD.0000000000000924 |
| [3] |
Miller WC, Rosenberg NE, Rutstein SE, et al. Role of acute and early HIV infection in the sexual transmission of HIV[J]. Curr Opin HIV AIDS, 2010, 5(4): 277-282. DOI:10.1097/COH.0b013e32833a0d3a |
| [4] |
Ratmann O, Van Sighem A, Bezemer D, et al. Sources of HIV infection among men having sex with men and implications for prevention[J]. Sci Transl Med, 2016, 8(320): 320ra2. DOI:10.1126/scitranslmed.aad1863 |
| [5] |
Robb ML. Viral dynamics and immune response in acute infection and their impact on viral set-point[C]//AIDS vaccine 2012 conference. Boston, United States of America: AIDS, 2012.
|
| [6] |
Grijsen ML, Steingrover R, Wit FWNM, et al. No treatment versus 24 or 60 weeks of antiretroviral treatment during primary HIV infection:the randomized Primo-SHM trial[J]. PLoS Med, 2012, 9(3): e1001196. DOI:10.1371/journal.pmed.1001196 |
| [7] |
Chun TW, Justement JS, Moir S, et al. Decay of the HIV reservoir in patients receiving antiretroviral therapy for extended periods:implications for eradication of virus[J]. J Infect Dis, 2007, 195(12): 1762-1764. DOI:10.1086/518250 |
| [8] |
Attia S, Egger M, Müller M, et al. Sexual transmission of HIV according to viral load and antiretroviral therapy:systematic review and meta-analysis[J]. AIDS, 2009, 23(11): 1397-1404. DOI:10.1097/QAD.0b013e32832b7dca |
| [9] |
Rekart ML, MacIntosh J. Acute primary HIV infection[J]. CMAJ, 2011, 183(11): 1280. DOI:10.1503/cmaj.101605 |
| [10] |
Epstein H, Morris M. Concurrent partnerships and HIV:an inconvenient truth[J]. J Int AIDS Soc, 2011, 14(1): 13. DOI:10.1186/1758-2652-14-13 |
| [11] |
Eaton JW, Hallett TB, Garnett GP. Concurrent sexual partnerships and primary HIV infection:a critical interaction[J]. AIDS Behav, 2011, 15(4): 687-692. DOI:10.1007/s10461-010-9787-8 |
| [12] |
Robb ML, Eller LA, Kibuuka H, et al. Prospective study of acute HIV-1 infection in adults in east Africa and Thailand[J]. N Engl J Med, 2016, 374(22): 2120-2130. DOI:10.1056/NEJMc1609157 |
| [13] |
Musey L, Hughes J, Schacker T, et al. Cytotoxic-T-cell responses, viral load, and disease progression in early human immunodeficiency virus type 1 infection[J]. N Engl J Med, 1997, 337(18): 1267-1274. DOI:10.1056/NEJM199710303371803 |
| [14] |
Dybul M, Fauci AS, Bartlett JG, et al. Guidelines for using antiretroviral agents among HIV-infected adults and adolescents, recommendations of the panel on clinical practices for treatment of HIV[EB/OL]. Centers for Disease Control and Prevention(US). (2002-05-17)[2018-04-01]. https://www.cdc.gov/MMWR/preview/mmwrhtml/rr5107a1.htm.
|
| [15] |
Wood E, Kerr T, Rowell G, et al. Does this adult patient have early HIV infection? The rational clinical examination systematic review[J]. JAMA, 2014, 312(3): 278-285. DOI:10.1001/jama.2014.5954 |
| [16] |
Braun DL, Kouyos RD, Balmer B, et al. Frequency and Spectrum of unexpected clinical manifestations of primary HIV-1 infection[J]. Clin Infect Dis, 2015, 61(6): 1013-1021. DOI:10.1093/cid/civ398 |
| [17] |
赵璇, 程绍辉, 郑敏娜, 等. 病毒载量检测对HIV抗体确证实验结果不确定样本的辅助诊断研究[J]. 中华流行病学杂志, 2016, 37(7): 992-995. Zhao X, Cheng SH, Zheng MN, et al. Study of auxiliary diagnostic value of viral load test for samples with indeterminate HIV antibody detection results[J]. Chin J Epidemiol, 2016, 37(7): 992-995. DOI:10.3760/cma.j.issn.0254-6450.2016.07.017 |
| [18] |
Branson B, Owen SM, Wesolowski LG, et al. Laboratory testing for the diagnosis of HIV infection: updated recommendations[EB/OL]. Centers for Disease Control and Prevention(US). (2017-06-27)[2018-04-01]. https://stacks.cdc.gov/view/cdc/23447.
|
| [19] |
Garrett NJ, Drain PK, Werner L, et al. Diagnostic accuracy of the point-of-care Xpert HIV-1 viral load assay in a South African HIV clinic[J]. J Acquir Immune Defic Syndr, 2016, 72(2). DOI:10.1097/QAI.0000000000000978 |
| [20] |
World Health Organization. Consolidated guidelines on HIV testing services[EB/OL]. (2015-07-14)[2018-04-30]. http://www.who.int/hiv/pub/guidelines/hiv-testing-services/en/.
|
 2018, Vol. 39
2018, Vol. 39