文章信息
- 郑志刚, 耿文奎, 陆珍珍, 李剑军, 周崇兴, 杨文敏.
- Zheng Zhigang, Geng Wenkui, Lu Zhenzhen, Li Jianjun, Zhou Chongxing, Yang Wenmin.
- 艾滋病病毒与结核分枝杆菌双重感染对死亡的影响
- Impact of HIV and Mycobacterium tuberculosis co-infection on related mortality
- 中华流行病学杂志, 2018, 39(10): 1362-1367
- Chinese Journal of Epidemiology, 2018, 39(10): 1362-1367
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2018.10.014
-
文章历史
收稿日期: 2018-03-05
2. 530028 南宁, 广西壮族自治区疾病预防控制中心办公室;
3. 530021 南宁, 广西壮族自治区卫生和计划生育委员会防治艾滋病办公室
2. General Affairs Offices, Guangxi Zhuang Autonomous Region Center for Disease Control and Prevention, Nanning 530028, China;
3. Special Office of AIDS Prevention and Treatment, Guangxi Zhuang Autonomous Region Commission of Health and Family Planning, Nanning 530021, China
结核病和艾滋病是导致死亡最多的传染病。HIV及结核分枝杆菌(Mycobacterium tuberculosis,MTB)双重感染是死亡的影响因素。2016年WHO估计全球新报告1 040万结核病病例,约10%合并HIV感染,全球同期共有3 670万人感染HIV,虽然53.00%接受抗病毒治疗(antiretroviral therapy,ART),仍有40.00%死于结核病相关疾病[1]。HIV感染能缩短MTB感染的潜伏期,容易导致活动性结核病和加速发病[2-3];MTB感染可加快HIV感染者及艾滋病患者(HIV/AIDS)的疾病与死亡进程[4-5]。中国结核病疫情居全球第二位,占全球结核病负担的10.00%,且有4亿人口潜伏感染MTB。监测数据显示,广西壮族自治区(广西)每年新报告HIV/AIDS约1万例,结核病近4万例,54.00%的HIV/AIDS处于晚发现阶段[CD4+T淋巴细胞计数(CD4)≤200个/μl][6]。广西每年HIV/MTB双重感染患者报告数占比超过全国的1/3。有研究认为广西HIV/AIDS的MTB感染率为9.00%~11.00%[7-8]。本研究利用跨系统大数据分析方法,交叉核对广西2011年HIV/AIDS登记队列(HIV/AIDS队列)的治疗、随访、综合信息和结核病患者登记队列(结核病队列)信息,系统测量HIV/AIDS的MTB感染率以及结核病患者的HIV感染率,分析HIV/MTB双重感染患者流行特征及死亡风险。
对象与方法1.研究对象:从中国疾病预防控制信息系统的艾滋病综合防治信息系统和结核病病例报告系统分别收集2011年广西HIV/MTB双重感染患者。将HIV/AIDS登记队列筛查发现的结核病患者及结核病队列检测HIV发现的HIV/AIDS纳入分析队列。纳入标准:①HIV/AIDS队列中被诊断为结核病的患者,包括肺结核和肺外结核患者;②结核病患者队列检出HIV被诊断为HIV/AIDS;③HIV/AIDS队列年龄≥18周岁,结核病队列年龄≥15周岁。排除标准:①未筛查结核的HIV/AIDS;②不明确HIV状态的结核病患者;③外籍。
2.研究方法:
(1) HIV/MTB双重感染诊断:2011年新报告的HIV/AIDS中,采集痰、支气管灌洗液、胸水、脑脊液等涂片抗酸染色阳性,或培养后有MTB生长,或病理检查证实,结合影像学及临床症状体征确定结核病。按知情同意原则,对结核病患者抽取血标本,用ELISA法检测HIV抗体,初筛阳性者再抽取一份血标本,送确证实验室确定是否感染HIV。
(2) 基础信息收集:收集整理2011年广西HIV/AIDS的治疗、随访、治疗信息,交叉核对结核病新报告患者基本信息;统计分析HIV/AIDS队列MTB感染率,结核病队列HIV感染率,病死率,死亡平均年龄,从诊断艾滋病到死亡时间间隔,以及CD4和患者晚发现情况等。为了保护患者隐私,分析数据删除了患者的姓名、报告ID和地址等涉及患者隐私信息。
(3) 随访期限:从HIV/AIDS队列筛查到的MTB阳性患者,随访期限从2011年1月1日至2015年12月31日;从结核病队列检测发现的HIV阳性患者,随访期限从2011年1月1日至2011年12月31日。
(4) 核心指标定义和应用:①HIV/MTB双重感染:患者感染HIV同时感染MTB;包括从HIV/AIDS队列筛查的MTB阳性患者,及从结核病队列检测的HIV阳性患者。②诊断到死亡时间间隔:指HIV/MTB双重感染患者从确诊艾滋病开始,到死亡的时间间隔,主要评价抗结核病治疗和ART开展情况及效果。③HIV/MTB晚发现:指患者报告时CD4<200个/μl者,用于评价患者早发现能力。
3.统计学分析:描述性流行病方法描述HIV/MTB双重感染患者基本特征,计算HIV/AIDS队列MTB感染率,结核病报告队列HIV感染率;用四格表χ2检验对比分析单纯感染HIV者、单纯感染MTB者和HIV/MTB双重感染病死率的差异;采用Cox比例风险回归模型分析HIV/MTB、单纯感染HIV、单纯感染MTB者的死亡风险。模型自变量包括单纯感染HIV者(赋值1),HIV队列的双重感染者(赋值2),单纯感染MTB者(赋值3)以及结核病报告队列的双重感染者(赋值4)。用SPSS 23.0和R3.2.2软件进行统计学分析。检验水准α=0.05,双侧检验。
结果1.一般情况:2011年广西的HIV/AIDS队列14 293例,感染MTB 2 533例,HIV/AIDS的MTB感染率为17.72%;结核病队列42 205例,感染HIV 2 351例,结核病患者HIV感染率为5.57%。HIV/AIDS感染MTB者1年病死率为15.16%(384/2 533),单纯感染HIV者1年病死率为13.63%(1 603/11 760);HIV/AIDS队列中HIV/MTB双重感染患者男女性别比为2.37:1,与单纯感染HIV者男女性别比例相当;结核病报告队列中HIV/MTB男女性别比为1.88:1,单纯感染MTB者男女性别比为2.68:1。两队列的HIV/MTB双重感染均以汉族、农民为主(表 1)。
2.晚发现情况:HIV/MTB双重感染者确诊艾滋病时CD4的M=116 (IQR:30.0~290.7)个/μl;单纯感染HIV者确诊艾滋病时CD4的M=224(IQR:65.0~379.0)个/μl。有CD4值HIV/MTB双重感染者中,64.13%(785/1 224)确诊艾滋病时CD4<200个/μl;49.36%(3 138/6 357)的单纯感染HIV者确诊艾滋病时CD4<200个/μl。两者差异有统计学意义(χ2=89.09,P<0.000 1)。
3.死亡和死亡风险:结核病队列有859例HIV阳性者死亡,死亡年龄15~89(53.20±34.71)岁;单纯感染MTB者死亡668例,死亡年龄19~93(64.12±29.45)岁;从诊断结核病到死亡时间为5.72(5.72±4.79)个月;47.73%(410/859)HIV/MTB双重感染患者在诊断结核病2个月内死亡。5年随访期内,HIV/AIDS队列有1 071例HIV/MTB双重感染死亡,死亡年龄18.84~90.47(56.69±31.06)岁;单纯感染HIV者,死亡年龄17.45~96.99(58.00±31.40)岁。结核病患者感染HIV的1年病死率为36.54%(859/2 351),单纯感染MTB者为3.45%(668/39 854);与单纯感染MTB者相比,HIV/MTB双重感染病死率显著升高(χ2=7 727.18,P<0.000 1)。HIV/AIDS感染MTB者1年病死率为15.16%(384/2 533),单纯感染HIV者病死率为11.22%(1 603/11 760);与单纯感染HIV者相比,HIV/MTB双重感染者病死率差异有统计学意义(χ2=4.07,P=0.04)。
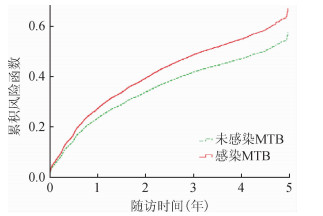
Cox比例风险回归模型分析结果显示,随访5年时,HIV/MTB双重感染死亡风险是单纯感染HIV者的1.17倍(95%CI:1.09~1.25),Waldχ2检验显示两者死亡风险差异有统计学意义(χ2=20.04,P<0.000 1)(图 1);随访12个月,HIV/MTB双重感染者死亡风险是单纯感染MTB者的25.68倍(95%CI:22.66~29.10);Waldχ2检验显示两者死亡风险差异有统计学意义(χ2=2 590.49,P<0.000 1)(图 2)。
|
| 图 1 单纯感染艾滋病病毒、艾滋病病毒/结核分枝杆菌双重感染随访5年的死亡风险 |

|
| 图 2 单纯感染结核分枝杆菌、艾滋病病毒/结核分枝杆菌双重感染12个月内死亡风险 |
4.抗病毒治疗和抗结核治疗:抗病毒治疗和抗结核治疗覆盖率不高是HIV/MTB双重感染死亡的主要原因。在HIV/AIDS队列发现的结核病患者中,开始ART比例为60.05%,结核病治愈率为15.48%,27.48%完成疗程;在结核病队列发现的HIV/AIDS中,47.90%开始ART,结核病治愈率及结核治疗完成疗程率分别为19.70%、37.26%(表 2)。
本研究采用跨系统大数据分析方法,交叉核对HIV/AIDS治疗、随访、综合信息和结核病报告患者队列后发现,HIV/AIDS报告队列感染MTB的比例、结核病报告队列感染HIV的比例均高于医院住院患者筛查结果[7-8],也高于前期单系统报告结果[9]。主要原因是本研究采用了交叉串联核对方法,将单个系统诊断为HIV/MTB双重感染者填补到其他系统,多系统交叉核对,最终结果纠正了住院患者选择偏倚和单系统报告偏倚可能,合理反映了广西HIV/AIDS报告队列MTB感染率以及结核病报告队列HIV感染率。本研究有24 849例(58.88%)结核病登记者接受HIV检测,阳性比例为9.46%(2 351/24 849)。广西结核病患者检测HIV比例和2016年全球57%相当,但仍低于30个HIV/MTB双重感染高负担国家66%检测水平,接受检测者HIV阳性感染率亦低于全球15%水平[1]。
患者知道自身HIV感染状态可以减少传播HIV的高危行为,及早接受HIV咨询、ART等服务以取得病毒抑制效果。病毒抑制不但可以提升个人机体免疫功能,减少死亡,而且可以显著减少HIV传播的机会[10-12],患者晚发现很大程度削弱这些方面的效果,并导致更大范围HIV传播[13]。本研究发现广西HIV/MTB双重感染患者倾向于较晚才被诊断,比例高于全国35%水平[6],亦高于广西同年单纯感染HIV者49%水平。一方面原因是合并感染MTB会显著加快HIV/AIDS疾病进程[4-5],另一方面和采取的检测策略有很大关系。国内有学者发现,与自愿检测咨询策略相比,医疗服务者提供检测和咨询策略导致晚发现优势比超过1.37倍[14]。广西艾滋病患者大部分因机会性感染就诊,或因手术检测HIV才被发现,也是晚发现比例高的主要原因之一。因此,艾滋病防治规划应该注意提高自愿咨询检测和强制检测比例,关注高危人群主动检测和筛查,才能提高患者早发现比例。
ART和抗结核治疗是减少HIV阳性人群中结核病发病和死亡危险的关键干预因素。研究表明,ART可以减少65%联合感染个体发展为活动性结核病的概率,并与淋巴细胞CD4计数无关[15];本研究HIV/AIDS队列发现的结核病患者ART比例60.05%,结核病治愈率和完成疗程率之和为42.96%,结核病登记队列发现的HIV/AIDS开始ART比例为47.90%,结核病治愈率和完成疗程率之和为56.96%,均显著低于2016年全球双重感染患者ART和抗结核治疗水平[1],导致广西HIV/MTB双重感染死亡风险高于单纯感染HIV或MTB者。另外,需要考虑HIV/MTB双重感染患者ART后免疫重建炎症综合征(immune reconstitution inflammatory syndrome,IRIS)导致结核病临床治疗转归恶化的可能。对于HIV/MTB双重感染患者,抗结核治疗病情稳定后,随着ART开展和免疫系统功能改善,伴随着CD4升高可以导致致死性大范围炎症反应发生,导致结核病症状重新恶化,如淋巴结肿大、脓肿形成、浆膜炎和X线影像恶化,增加HIV/MTB双重感染者死亡的可能[16]。目前IRIS和HIV/MTB双重感染者死亡之间的关系并不清楚,相关研究有待进一步开展。HIV/MTB双重感染者和单纯感染HIV者、单纯感染MTB者死亡差异有统计学意义,但还受到治疗方案、CD4等因素影响。下一步研究的方向是开展分层分析,在相同层内比较双重感染和单纯感染HIV者、单纯感染MTB者死亡差别,提供更合理的分析结果。
本研究尚有不足。一是限于资料可及程度,无法将结核病分层为肺结核和肺外结核进行更细致的分析;二是限于篇幅,未对ART、抗结核病治疗对死亡的影响展开分析;三是由于资料收集原因,未能分析IRIS对HIV/MTB双重感染者死亡的影响。
本研究利用跨系统大数据串联、交叉核对分析方法,纠正了HIV/MTB双重感染报告偏倚和患者选择偏倚,提高了敏感度,真实反映了广西严重的HIV/MTB双重感染疾病负担。HIV/AIDS患者MTB感染率为17.72%;结核病登记患者HIV感染率为5.57%;64.13%HIV/MTB双重感染诊断艾滋病时属晚发现;结核病患者感染HIV者1年病死率为36.54%,HIV/AIDS感染MTB者1年病死率为15.16%,均高于单纯感染MTB者或者单纯感染HIV者;HIV/MTB双重感染者随访5年的死亡风险是单纯感染HIV者的1.17倍,HIV/MTB双重感染者随访12个月的死亡风险是单纯感染MTB者的25.68倍,死亡风险均高于单纯感染MTB者或单纯感染HIV者。
综上所述,广西HIV/MTB双重感染者死亡、发病占报告艾滋病患者比例较高,病死率及死亡风险明显高于单纯感染HIV者及单纯感染MTB者。HIV/MTB双重感染是值得关注的重大公共卫生问题,应尽快提高抗病毒治疗覆盖率和抗结核治愈率;针对HIV感染者,应加强早发现和早治疗MTB感染。
利益冲突: 无
| [1] |
World Health Organization. Global tuberculosis report 2017[EB/OL]. Geneva: World Health Organization, (2017-12-01)[2018-02-01]. http://www.who.int/tb/publications/global_report/en/.
|
| [2] |
Selwyn PA, Hartel D, Lewis VA, et al. A prospective study of the risk of tuberculosis among intravenous drug users with human immunodeficiency virus infection[J]. N Engl J Med, 1989, 320(9): 545-550. DOI:10.1056/NEJM198903023200901 |
| [3] |
Corbett EL, Charalambous S, Moloi VM, et al. Human immunodeficiency virus and the prevalence of undiagnosed tuberculosis in African gold miners[J]. Am J Respir Crit Care Med, 2004, 170(6): 673-679. DOI:10.1164/rccm.200405-590OC |
| [4] |
López-Gatell H, Cole SR, Hessol NA, et al. Effect of tuberculosis on the survival of women infected with human immunodeficiency virus[J]. Am J Epidemiol, 2007, 165(10): 1134-1142. DOI:10.1093/aje/kwk116 |
| [5] |
Badri M, Ehrlich R, Wood R, et al. Association between tuberculosis and HIV disease progression in a high tuberculosis prevalence area[J]. Int J Tuberc Lung Dis, 2001, 5(3): 225-232. |
| [6] |
金霞, 熊燃, 王丽艳, 等. 2010-2014年我国HIV感染病例的晚发现情况分析[J]. 中华流行病学杂志, 2016, 37(2): 218-221. Jin X, Xiong R, Wang LY, et al. Analysis on the 'late diagnosis' (LD) phenomena among newly identified HIV/AIDS cases in China, 2010-2014[J]. Chin J Epidemiol, 2016, 37(2): 218-221. DOI:10.3760/cma.j.issn.0254-6450.2016.02.014 |
| [7] |
Gao L, Zhou F, Li XW, et al. HIV/TB co-infection in mainland China:a Meta-analysis[J]. PLoS One, 2010, 5(5): e10736. DOI:10.1371/journal.pone.0010736 |
| [8] |
崔哲哲, 林玫, 蓝如束, 等. 2010-2011年广西结核菌/艾滋病病毒双向筛查及治疗监测结果分析和评价[J]. 重庆医学, 2013, 42(3): 326-328. Cui ZZ, Lin M, Lan RS, et al. Analysis and evaluation on TB/HIV co-infection and treatment monitoring results in Guangxi province from 2010 to 2011[J]. Chongqing Med, 2013, 42(3): 326-328. DOI:10.3969/j.issn.1671-8348.2013.03.034 |
| [9] |
郑志刚, 梁旭, 崔哲哲, 等. 广西2010-2013年TB/HIV双重感染患者登记变化趋势分析[J]. 中国艾滋病性病, 2015, 21(7): 585-588. Zheng ZG, Liang X, Cui ZZ, et al. Contribution analysis on the trend of registration of tuberculosis and human immunodeficiency virus co-infection patients, 2010-2013, Guangxi[J]. Chin J AIDS STD, 2015, 21(7): 585-588. DOI:10.13419/j.cnki.aids.2015.07.11 |
| [10] |
Cohen MS, Chen YQ, McCauley M, et al. Antiretroviral therapy for the prevention of HIV-1 transmission[J]. N Engl J Med, 2016, 375(9): 830-839. DOI:10.1056/NEJMoa1600693 |
| [11] |
Rodger AJ, Cambiano V, Bruun T, et al. Sexual activity without condoms and risk of HIV transmission in serodifferent couples when the HIV-positive partner is using suppressive antiretroviral therapy[J]. JAMA, 2016, 316(2): 171-181. DOI:10.1001/jama.2016.5148 |
| [12] |
Bavinton B, Grinsztejn B, Phanuphak N, et al. HIV treatment prevents HIV transmission in male serodiscordant couples in Australia, Thailand and Brazil[C]//Presentation at the 9th IAS Conference on HIV Science (IAS 2017). Paris, France: Abstract TUAC0506LB, 2017.
|
| [13] |
Mark G, Crepaz N, Senterfitt JW, et al. Meta-analysis of high-risk sexual behavior in persons aware and unaware they are infected with HIV in the United States:implications for HIV prevention programs[J]. J Acquir Immune Defic Syndr, 2005, 39(4): 446-453. DOI:10.1097/01.qai.0000151079.33935.79 |
| [14] |
Cheng WB, Tang WM, Han ZG, et al. Late presentation of HIV infection:prevalence, trends, and the role of HIV testing strategies in Guangzhou, China, 2008-2013[J]. Biomed Res Int, 2016, 1631878. DOI:10.1155/2016/1631878 |
| [15] |
Suthar AB, Lawn SD, del Amo J, et al. Antiretroviral therapy for prevention of tuberculosis in adults with HIV:a systematic review and Meta-analysis[J]. PLoS Med, 2012, 9(7): e1001270. DOI:10.1371/journal.pmed.1001270 |
| [16] |
Meintjes G, Lawn SD, Scano F, et al. Tuberculosis-associated immune reconstitution inflammatory syndrome:case definitions for use in resource-limited settings[J]. Lancet Infect Dis, 2008, 8(8): 516-523. DOI:10.1016/S1473-3099(08)70184-1 |
 2018, Vol. 39
2018, Vol. 39




