文章信息
- 吴守丽, 高敏, 郑健, 颜苹苹, 严延生.
- Wu Shouli, Gao Min, Zheng Jian, Yan Pingping, Yan Yansheng.
- 引起HIV抗体不确定结果的非特异性反应影响因素分析
- Analysis on influencing factors that leading to nonspecific responses to indeterminate results of HIV antibodies
- 中华流行病学杂志, 2018, 39(9): 1255-1260
- Chinese Journal of Epidemiology, 2018, 39(9): 1255-1260
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2018.09.021
-
文章历史
收稿日期: 2018-06-11
2. 350004 福州, 福建医科大学公共卫生学院;
3. 350001 福州, 福建省人兽共患病研究重点实验室
2. School of Public Health, Fujian Medical University, Fuzhou 350004, China;
3. Fujian Province Key Laboratory of Zoonosis Research, Fuzhou 350001, China
随着HIV检测覆盖面不断扩大,样本来源更加复杂,HIV抗体不确定检出率越来越多[1]。这不仅给实验室检测和疫情管理带来困扰,而且也给受检者带来沉重的心理负担,甚至会延误治疗。产生HIV抗体不确定反应性条带大致可分为两大类:①特异性反应条带:主要与HIV感染有关,包括HIV感染早期(窗口期)、艾滋病终末期、病毒变异、机体免疫严重缺陷导致机体对HIV产生免疫逃逸等;②非特异性反应条带:主要与其他生物学因素有关,包括其他病毒或细菌感染、自身免疫性疾病、特殊生理状态、接种疫苗等[2]。根据《全国艾滋病检测技术规范》(2015年修订版)建议对HIV抗体不确定者进行HIV-1核酸试验或2~4周后随访[3]。如果HIV-1核酸试验结果阴性且2~4周后随访免疫印迹法(WB)条带无进展或更少,可推断该不确定结果可能是由非特异性反应引起的。国内外已有相关文献报道[4-7],感染人T淋巴细胞白血病病毒(human T-cell leukemia virus,HTLV)、梅毒螺旋体(treponema pallidum,TP)、HCV、HBV以及体内抗核抗体(antinuclear antibody,ANA)、甲胎蛋白(alpha-fetoprotein,AFP)升高等因素有可能会引起HIV抗体不确定非特异性反应的产生。本研究对福建省2015-2016年各艾滋病确证实验室检出的HIV抗体不确定样本进行了相关生物学因素研究,旨在发现引起HIV抗体不确定结果非特异性反应的相关影响因素,为HIV鉴别诊断和防治策略提供参考依据。
对象与方法1.研究对象:①HIV抗体不确定组:来源于2015-2016年福建省各艾滋病确证实验室,经WB确证为HIV抗体不确定样本,HIV核酸检测阴性,且经过2~4周随访WB条带无进展。排除HIV核酸检测阳性或经过2~4周随访WB条带有进展,最终判为HIV抗体阳性的不确定样本。②普通人群对照组:同期福建省经HIV抗体筛查检测为阴性的普通人群样本。排除HIV抗体筛查结果阳性或不确定的样本。③确证阴性对照组:为HIV抗体初筛阳性,但确证阴性的样本。排除HIV抗体确证阳性、不确定或经随访抗体转阳的样本。
2.研究方法:
(1)研究设计:采用病例对照研究设计,将HIV抗体不确定组和普通人群对照组按照性别、年龄进行成组匹配,以消除其可能引起的混杂因素的影响。为了进一步消除受检人群类型及构成可能对结果的影响,将HIV抗体不确定组和确证阴性对照组按照性别、年龄、受检人群类型及构成进行匹配。样本量估计根据相关文献[7],TP等影响因素在不确定人群中估计暴露率为8.02%,在普通人群中估计暴露率为0.20%,估算病例组和对照组的最少样本量分别为68例和136例。病例组110例,对照组226例,符合本研究所需的样本量。
(2)实验室检测方法:HIV抗体确证试验:所有送检样本均使用HIV抗原抗体检测试剂(北京万泰生物药业股份有限公司)进行复检,复检试验有反应的样本,进行WB确证试验(MP生物医学亚太私人有限公司),按照全国艾滋病检测技术规范要求和试剂说明书操作。结果判断标准:①HIV抗体阳性诊断标准:检测出2条env带(gp160/gp41和gp120)及1条gag带(p17、p24、p55)或pol带(p31、p51、p66);②HIV抗体阴性诊断标准:无HIV抗体特异条带;③HIV抗体不确定诊断标准:出现HIV抗体特异条带,但是不满足HIV抗体阳性诊断标准。HIV核酸检测:采用HIV-1核酸定量检测试剂盒(PCR-荧光探针法,中山大学达安基因股份有限公司),具体操作参照试剂盒说明书。
其他指标检测:采用ELISA法分别检测HBsAg(北京万泰生物药业有限公司)、抗-HCV抗体(北京万泰生物药业有限公司)、TP抗体(厦门英科新创科技有限公司)、ANA(美国宙斯科技公司)、HTLV抗体(北京万泰生物药业有限公司)、AFP(郑州安图生物工程股份有限公司)的含量。操作步骤和结果判断按照各试剂盒说明书。
3.统计学分析:应用SPSS 17.0软件进行统计学分析,采用χ2检验和多因素非条件logistic回归分析引起HIV抗体不确定结果的非特异性反应的影响因素。检验水准α=0.05,双侧检验。
结果1.样本基本特征:共收集HIV抗体不确定样本210例,经HIV核酸检测为阴性且经过随访WB条带无进展者共110例,占52.38%,其中男性占51.82%(57/110),女性占48.18%(53/110),年龄(35.50±12.56)岁。样本主要来源于无偿献血者、孕产妇、其他就诊者、检测咨询者、术前检查和其他受检者,占全部样本来源的92.73%(102/110)。普通人群样本共226例,其中男性占51.77%(117/226),女性占48.23%(109/226),年龄(37.07±15.11)岁。对HIV抗体不确定组与普通人群对照组在年龄、性别构成进行均衡性检验,两组间均衡可比,差异无统计学意义(P > 0.05)。
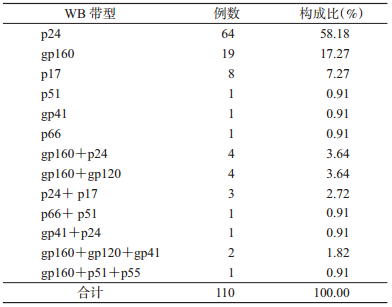
2. HIV抗体不确定样本WB带型模式:110例HIV抗体不确定样本,共出现13种WB带型模式,最常见的是p24单条带占58.18%(64/110),其次是gp160单条带占17.27%(19/110),p17单条带占7.27%(8/110),其余10种带型呈散在分布,所占比例较小。见表 1。
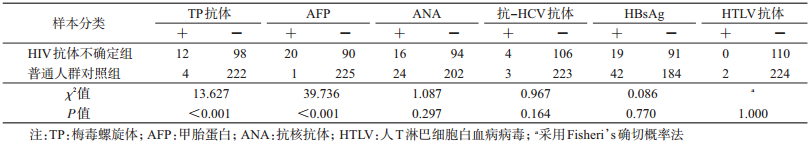
3.引起HIV抗体不确定的非特异性反应影响因素:HIV抗体不确定组中TP抗体阳性率为10.91%(12/110),高于普通人群对照组1.77%(4/226),两组差异有统计学意义(χ2=13.627,P < 0.001);HIV抗体不确定组中AFP阳性率为18.18%(20/110),高于普通人群对照组0.44%(1/226),两组差异有统计学意义(χ2=39.736,P < 0.001)。而ANA、HBsAg、抗-HCV抗体、HTLV抗体在HIV抗体不确定组和普通人群对照组间差异无统计学意义(χ2值分别为1.087、0.086、0.967,Fisheri’s确切概率法,P值均 > 0.05)。见表 2。
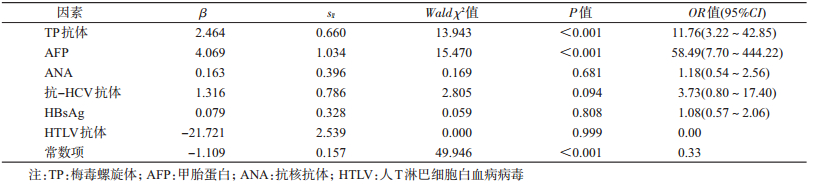
对各影响因素进行多因素非条件logistic回归分析,结果显示,TP抗体阳性人群引起HIV抗体不确定结果的非特异性反应的风险是TP抗体阴性人群的11.76倍,AFP阳性人群引起HIV抗体不确定非特异性反应的风险是AFP阴性人群的58.49倍。见表 3。
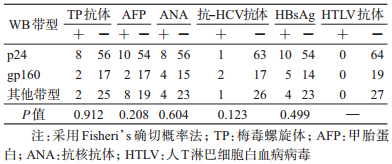
分析HIV抗体不确定样本中不同带型与各影响因素的关系结果显示:HIV抗体不确定样本中TP抗体、AFP、ANA、抗-HCV抗体或HBsAg阳性检出率在不同带型样本分布中差异均无统计学意义。见表 4。
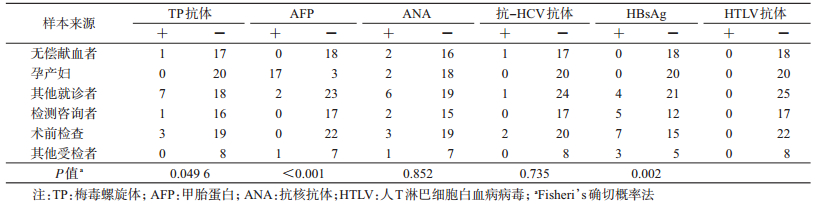
进一步分析HIV抗体不确定样本中不同受检人群与各影响因素的关系,HIV抗体不确定样本中TP抗体、AFP、HBsAg阳性检出率在不同受检人群的差异有统计学意义(Fisheri’s确切概率法,P值均 < 0.05),其中来自其他就诊者的HIV抗体不确定样本TP抗体阳性检出率最高,达到28.00%(7/25);孕产妇的HIV抗体不确定样本AFP阳性检出率最高,达到85.00%(17/20)。ANA、HCV和HTLV抗体阳性检出率在不同受检人群中差异无统计学意义(Fisheri’s确切概率法,P值均 > 0.05)。见表 5。
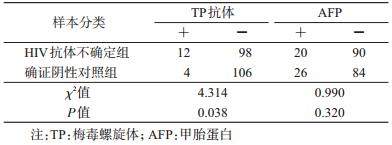
本研究发现,有统计学意义的两个影响因素TP抗体和AFP阳性检出率在不同受检人群中有差异。为排除受检人群类型和构成的混杂因素可能影响,本研究按照HIV抗体不确定样本性别、年龄、受检人群类型及构成进行优化匹配,筛选110例HIV抗体确证阴性样本作为确证阴性对照组,同时进行TP抗体和AFP检测。见表 6。经过受检人群类型和构成匹配后,HIV抗体不确定组的TP抗体阳性率(10.91%)仍高于确证阴性对照组(3.64%),两组差异有统计学意义(χ2=4.314,P < 0.05);然而HIV抗体不确定组的AFP阳性率(18.18%)略低于确证阴性对照组(23.64%),两组差异无统计学意义(χ2=0.990,P > 0.05)。由此可见,来自孕产期检查的HIV抗体不确定样本AFP阳性检出率高,主要与其本身特殊生理状况有关,而与HIV抗体不确定非特异性反应无关。
近年来,HIV抗体不确定结果检出率越来越多,据报道4%~20%的样品经过HIV初筛和复检阳性后WB确证为“HIV抗体不确定”,影响不确定结果的因素复杂且尚不清楚,转归以实验室出现非特异反应为主[8]。本研究收集210例HIV抗体不确定样本,排除HIV核酸检测阳性或2~4周随访HIV-1抗体转阳后,共发现110例(占52.4%)HIV抗体不确定者。由非特异性反应所引起的HIV抗体不确定结果比例相当大,实验室检测者和临床医生对于HIV抗体不确定结果解读应非常慎重,必要时可进行HIV-1核酸试验加以排除,避免给受检者造成不必要的心理负担。
HIV抗体不确定样本出现的WB条带模式不尽相同,带型不同其预示着转归结局也不同。一些研究显示,WB单条带尤其是gag带其非特异性反应可能性较大,而出现env带预示HIV感染可能性大[9-11]。本研究结果显示HIV抗体不确定样本中共出现13种WB带型模式,不管gag带还是env或pol带均有可能出现非特异性反应,但是gag带出现非特异性反应的概率比较大。值的注意的是,各国家/国际组织推荐的HIV-1抗体阳性判定标准不同,如WHO推荐至少出现2条env带[12],美国CDC推荐出现p24、gp41、gp120、gp160中任何2条带[13],美国红十字会推荐出现env、gag、pol各1条带[13]。如按照上述各类标准判定,本研究就有少数病例会被误判为HIV-1抗体阳性,这将给受检者带来身心伤害或者不必要的医疗纠纷。为慎重起见,HIV-1抗体阳性判定标准除了要严格按照试剂盒说明书规定的判定标准外,对于临界阳性条带的样本需结合流行病学史或HIV核酸补充试验或进一步随访复检等结果谨慎判定,以免造成假阳性。
引起HIV抗体不确定非特异性反应的原因十分复杂,不同研究得出的结论也不一样,这可能与每个研究所选择的研究对象、对照组选择及研究设计不同有关。有些研究显示HIV抗体不确定的出现与其他反转录病毒、分枝杆菌、疟原虫等感染、自身免疫相关疾病、特殊情况如怀孕或疫苗接种等有关,此外,如果实验操作或判读不当以及试剂盒质量有问题均有可能引起HIV抗体不确定[14]。本研究最初结果显示HIV抗体不确定样本中TP抗体阳性率和AFP水平高于对照人群。但进一步分析发现HIV抗体不确定样本中TP抗体、AFP、HBsAg阳性检出率在不同受检人群中结果不一样,其中20例孕产妇检查就有18例AFP检出阳性,经查阅文献发现孕产妇本身体内AFP就比正常人高,尤其是到了孕中期或孕晚期[15]。为此,本研究通过对受检人群类型和构成进行优化匹配后,发现两组中AFP阳性检出率差异并无统计学意义,提示应注意对照组的选择偏倚。
经过受检人群类型和构成优化匹配后HIV抗体不确定样本组中TP抗体阳性率仍高于确证阴性对照组,提示TP抗体阳性可能是HIV抗体不确定非特异性反应发生的影响因素,但仍需加大样本进一步进行证实。另外,本研究发现HBsAg、HCV抗体、ANA、HTLV抗体在两组样本间检出率差异并无统计学意义,这提示HBV、HCV、HTLV感染或ANA抗体水平升高不一定是引起HIV抗体不确定非特异性反应的影响因素。此外,进一步分析发现,HIV抗体不确定样本中TP抗体、AFP、ANA、HCV抗体和HBsAg阳性检出率在不同带型样本分布中差异均无统计学意义,该结果预示这些影响因素不会与特定的WB条带发生反应。
本研究存在不足。对象类型和构成可能存在混杂因素,应注意对照组的选择偏倚,避免研究结果受到研究样本量和对照组人群选择的影响。下一步研究可加大样本量,优化对照组的选择,以便获取更为可靠的信息。
综上所述,引起WB非特异性反应的影响因素较为复杂,TP抗体阳性可能是HIV抗体不确定非特异性反应发生的影响因素,其参与非特异性反应的具体成分及反应机制尚不清楚,有待于进一步研究。孕妇中AFP阳性检出率高主要与其本身特殊生理状况有关,而与HIV抗体不确定非特异性反应无关。
利益冲突: 无
| [1] |
彭瑾瑜, 贺健梅, 江洋, 等. 湖南省2008-2012年HIV抗体不确定结果分析[J]. 中国艾滋病性病, 2014, 20(4): 240-243. Peng JY, He JM, Wang Y, et al. The analysis on indeterminate results of HIV antibodies from 2008 to 2012 in Hunan province[J]. Chin J AIDS STD, 2014, 20(4): 240-243. DOI:10.13419/j.cnki.aids.2014.04.010 |
| [2] |
高敏, 吴守丽, 严延生. HIV抗体不确定的影响因素及其检测方法的研究进展[J]. 中国艾滋病性病, 2016, 22(4): 308-311. Gao M, Wu SL, Yan YY. Review of theinfluence factors and detection methods regarding indeterminate result of HIV antibodies by WB test[J]. Chin J AIDS STD, 2016, 22(4): 308-311. DOI:10.13419/j.cnki.aids.2016.04.28 |
| [3] |
中国疾病预防控制中心. 全国艾滋病检测技术规范(2015年修订版)[J]. 中国病毒病杂志, 2016, 6(6): 401-427. Chinese Center for Disease Control and Prevention. National Guideline for Detection of HIV/AIDS (2015 revised)[J]. Chin J Viral Dis, 2016, 6(6): 401-427. DOI:10.16505/j.2095-0136.2016.06.001 |
| [4] |
Cremonezi D, de Mesquita PE, Romão MM, et al. Prevalence of indeterminate human immunodeficiency virus Western Blot results in pregnant women attended at a public hospital in Presidente Prudente, Brazil[J]. Braz J Infect Dis, 2005, 9(6): 506-509. DOI:10.1590/S1413-86702005000600009 |
| [5] |
Guan M. Frequency, causes, and new challenges of indeterminate results in Western blot confirmatory testing for antibodies to human immunodeficiency virus[J]. Clin Vaccine Immunol, 2007, 14(6): 649-659. DOI:10.1128/CVI.00393-06 |
| [6] |
Tesoro-Cruz E, Hernández-González R, Kretschmer-Schmid R, et al. Cross-reactivity between caprine arthritis-encephalitis virus and type 1 human immunodeficiency virus[J]. Arch Med Res, 2003, 34(5): 362-366. DOI:10.1016/j.arcmed.2003.08.001 |
| [7] |
高凯, 文芳, 徐慧芳, 等. 影响蛋白印迹法检测HIV抗体结果的生物学因素分析[J]. 热带医学杂志, 2009, 9(9): 1073-1075. Gao K, Wen F, Xu HF, et al. Biological factors affecting the determination of HIV antibody[J]. J Trop Med, 2009, 9(9): 1073-1075. |
| [8] |
殷方兰, 钟培松, 张永, 等. HIV抗体不确定结果影响因素的分析及对策[J]. 中国皮肤性病学杂志, 2015, 29(9): 978-980. Yin FL, Zhong PS, Zhang Y, et al. Study on factors and measures of the indeterminate results of human immunodeficiency virus in Western blot[J]. Chin J Dermatovenereol, 2015, 29(9): 978-980. DOI:10.13735/j.cjdv.1001-7089.201408151 |
| [9] |
李燕, 梁彩云, 高凯, 等. HIV抗体不确定患者的随访转归及相关生物学因素[J]. 中华预防医学杂志, 2011, 45(10): 916-919. Li Y, Liang CY, Gao K, et al. Follow-up and outcome as well as the related biological factors on the cases with indeterminate HIV antibody level[J]. Chin J Prev Med, 2011, 45(10): 916-919. DOI:10.3760/cma.j.issn.0253-9624.2011.10.014 |
| [10] |
曹栋卿, 胡雪娜, 赵丹燕. HIV抗体不确定样品的随访结果[J]. 浙江预防医学, 2015, 27(1): 68-70. Cao DQ, Hu XN, Zhao DY. Follow-up results of the cases with indeterminate HIV antibody[J]. Zhejiang J Prev Med, 2015, 27(1): 68-70. DOI:10.19485/j.cnki.issn1007-0931.2015.01.020 |
| [11] |
王海, 蒋文雅, 顾松叶. HIV抗体不确定样本的特征与确证策略研究[J]. 中国卫生检验杂志, 2013, 23(15): 3068-3071, 3074. Wang H, Jiang WY, Gu SY. Serological characteristics and confirmation strategy of indeterminate HIV antibody samples[J]. Chin J Health Lab Technol, 2013, 23(15): 3068-3071, 3074. |
| [12] |
World Health Organization. AIDS:proposed WHO criteria for interpreting Western Blot assays for HIV-1, HIV-2, and HTLV-Ⅰ/HTLV-Ⅱ[J]. Bull World Health Organ, 1991, 69(1): 127-129, 131-133. |
| [13] |
Centers for Disease Control (CDC). Interpretation and use of the western blot assay for serodiagnosis of human immunodeficiency virus type 1 infections[J]. MMWR Suppl, 1989, 38(7): 1-7. |
| [14] |
马仲慧, 陈兵, 常浩, 等. 非HIV感染者蛋白印迹试验不确定及假阳性结果的原因[J]. 中国艾滋病性病, 2017, 23(6): 571-574. Ma ZH, Chen B, Chang H, et al. Reasons of indeterminate and false-positive results by a confirmatory human immunodeficiency virus Western Blot testing in the uninfected people[J]. Chin J AIDS STD, 2017, 23(6): 571-574. DOI:10.13419/j.cnki.aids.2017.06.28 |
| [15] |
Miao ZY, Liu X, Shi TK, et al. First trimester, second trimester, and integrated screening for Down's syndrome in China[J]. J Med Screen, 2012, 19(2): 68-71. DOI:10.1258/jms.2012.011145 |
 2018, Vol. 39
2018, Vol. 39