文章信息
- 彭瑾瑜, 郑军, 贺健梅, 江洋, 姚栋, 陈曦.
- Peng Jinyu, Zheng Jun, He Jianmei, Jiang Yang, Yao Dong, Chen Xi.
- 湖南省首次诊断2例非输入性HIV-2感染病例与流行病学个案调查
- Diagnostic and epidemiological features of the first two HIV-2 indigenous infections in Hunan province
- 中华流行病学杂志, 2018, 39(8): 1077-1081
- Chinese journal of Epidemiology, 2018, 39(8): 1077-1081
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2018.08.012
-
文章历史
收稿日期: 2017-12-25
2. 410004 长沙市疾病预防控制中心
2. Changsha Center for Disease Control and Prevention, Changsha 410004, China
HIV主要有两种型别,HIV-1和HIV-2,氨基酸水平上的同源性为40%~60%。HIV-1是引起全球艾滋病流行的病毒,相对于HIV-2,致病性更强,传播效率更高,病程进展更快[1-2]。HIV-2主要在西非和中非流行,其他国家有散发报道。我国的福建省、上海市和广州市等地有过输入性病例的报道,但尚未发现本地的非输入性病例[3-5]。我们从长沙市一名服刑人员检出HIV-2感染,并发现了与其有关联的另一例感染病例,现将结果报告如下。
对象与方法1.研究对象:①病例1,男,服刑人员,入监时体检诊断“HIV抗体不确定”并出现了HIV-2型特异性条带,2次复查结果一致,分别于2017年4月10日、5月9日和9月4日抽取静脉EDTA抗凝血10 ml,检测CD4+T淋巴细胞(CD4)计数后分成全血、淋巴细胞富集液和血浆,-70 ℃保存待检。②病例2,女,长沙市人,自2016年起,两次HIV检测结果为“HIV抗体不确定”并出现了HIV-2型特异性条带,9月11日抽取静脉EDTA抗凝血10 ml,处理方式和保存条件同前。
对2例疑似HIV-2患者进行流行病学个案调查,包括人口学特征、性接触史、输(供)血史、毒品使用史、出入境史、既往接受医疗服务情况等。
2.实验室检测:
(1)HIV血清学检测:严格按照《全国艾滋病检测技术规范(2015年修订版)》[6]的HIV抗体检测策略与程序分别对病例的血清或血浆进行了多次HIV抗体筛查与确证试验。HIV抗体初筛试剂为第4代HIV-1/2抗原抗体ELISA试剂盒(北京万泰生物药业股份有限公司;珠海丽珠试剂股份有限公司)。确证试剂分别采用了3种试剂,用于诊断HIV-1的HIV 1+2型抗体检测试剂盒(HIV BLOT 2. 2)(新加坡MP生物医学亚太有限公司,MP试剂)和IMT HIV-1/2 Blot试剂(上海英旻泰生物技术有限公司,IMT试剂),可用于同时诊断HIV-1和HIV-2的(HIV 1+2)抗体确证试剂盒(条带免疫法)(德国Mikrogen GmbH公司,Mikrogen试剂)。所用试剂均在有效期内,结果判读按照试剂盒说明书。
(2)HIV核酸检测:HIV-1核酸定量试剂为Cobas TaqMan HIV-1 Test v2. 0(美国罗氏分子诊断公司),检测样本为血浆1 ml,检测灵敏度为20 IU/ml,仪器为COBAS TaqMan 96分析仪。HIV(1+2型)核酸定性试剂为Cobas TaqScreen MPX Test,version 2.0(美国罗氏分子诊断公司),检测样本为血浆1 ml,仪器为COBAS S201系统。定性试剂可检测HIV-1 M组、O组RNA和HIV-2 RNA,但不能区分鉴别。
(3)HIV-2的基因检测:采用天根生化科技(北京)有限公司生产的RNA提取试剂盒(离心柱型)提取血浆中HIV的RNA,设计两对引物通过巢式PCR扩增HIV-2的保守区gag区,扩增产物经1%琼脂糖凝胶电泳30 min,根据Marker位置判断出目的条带正确后送测序公司测序,与已公布的HIV-2基因组比对序列结果。引物序列:外侧引物H1:5′- AGA GGC TGG CAG ATT GAG C-3′和H2:5′- CAA GAC GGA GTT TCT CGC G-3′;内侧引物H3:5′- GAG GTT CTC TCC AGC ACT AGC A-3′和H4:5′- TAG GAG CAC TCG TCG TGG T-3′。PCR反应条件:第一轮扩增:50 ℃ 30 min,94 ℃ 5 min;94℃ 10 s,55 ℃ 30 s,72 ℃ 30 s,30个循环;72℃ 7 min。第二轮扩增:94 ℃ 5 min;94 ℃ 10 s,55 ℃ 30 s,72 ℃ 30 s,30个循环;72 ℃ 7 min。测序引物为H3。
(4)CD4检测:采用美国BD公司生产的FACSCalibur流式细胞仪和相关试剂。
结果1.流行病学调查:病例1,男,汉族,1959年2月出生,四川省攀枝花市人,初中文化,退休工人,从2013年一直居住在长沙市芙蓉区。2016年底因家庭纠纷,警务人员调解过程中发生袭警而入狱。在入监体检时HIV检测结果连续2次为“HIV抗体不确定”并出现HIV-2型的特异性条带。自诉身体健康,无吸毒史,无手术史和输/献血史,有短暂出国史(自述1992年在德国劳务输出,管理严格,无性接触史)。有3次婚史,已经证实最后一任妻子的HIV结果为阴性。承认与病例2从2013年一直保持情人关系,直至入狱,另外还承认和其他2名女性也存在婚外性关系,但已经失去联系。最近一次CD4计数结果为131个/μl,诊断为艾滋病,无其他临床疾病。
病例2,女,汉族,1962年12月出生,湖南省长沙市人,高中文化,退休工人,离异后再婚,自诉身体健康,无吸毒史,无手术史和输/献血史,无出国史,现任丈夫HIV检测结果为阴性。2013年起与病例1发生婚外性关系,无其他性伴。2014年7月14日献血时血液合格,证实当时还未感染HIV。2016年7月,因脚痛住院检查发现HIV抗体阳性,在长沙市CDC检测为“HIV抗体不确定”,后2017年1月在湖南省CDC检测仍为“HIV抗体不确定”。两次结果都有HIV-2型的特异性条带。CD4计数结果为2 527个/μl,无其他临床疾病。
病例2献血证显示在2014年献血时未感染HIV,自述2013年至今,仅与两位男性发生过性关系,即本人配偶与病例1。依据病例1为艾滋病患者且与病例2之间存在性接触史,可以推断病例2的HIV-2感染来源于病例1。病例1感染来源不明确,需要进一步调查。
2. HIV血清学检测:采用3种方法。
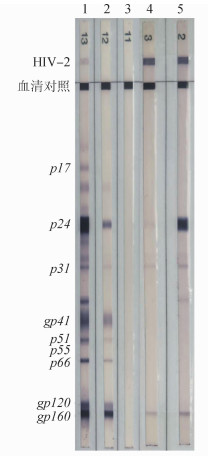
(1)免疫印迹法一:采用IMT试剂,病例1和病例2的条带都为p24、p31、p51、p66、gp160和HIV-2条带,判定为“HIV抗体不确定”,见图 1。
|
| 注:上海英旻泰生物技术有限公司IMT HIV-l/2Blot试剂盒; 1=强阳性对照, 2=弱阳性对照, 3=阴性对照, 4=病例1, 5=病例2, 6=HIV-1阳性 图 1 免疫印迹法一检测条带 |
(2)免疫印迹法二:采用MP试剂,病例1和病例2的条带都为p24、p31、gp160和HIV-2条带,也判定为“HIV抗体不确定”,见图 2。
|
| 注:新加坡MP生物医学亚太有限公司的HIV1+2型抗体检测试剂盒(HIV BLOT 2.2);1=强阳性对照, 2=弱阳性对照, 3=阴性对照, 4=病例1, 5=病例2 图 2 免疫印迹法二检测条带 |
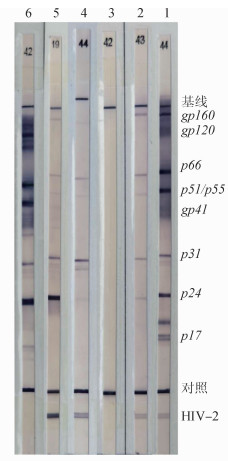
(3)条带免疫法:采用Mikrogen试剂,病例1条带为gp41(+/-)、p51(+/-)、p31、p24(+/-)、gp105和gp36,病例2条带为gp120(+/-)、gp41(+/-)、p51、p31、p24、p17(+/-)、gp105和gp36,满足判定标准,都可以诊断为“HIV-2抗体阳性”,见图 3和表 1。图 3的5泳道是典型的HIV-1阳性感染者,6泳道是MP试剂诊断的“HIV-1抗体不确定并有HIV-2特异性条带”,在Mikrogen试剂中gp36显示强度比gp41弱很多,同时出现了gp120、p51、p31(+/-)、p24(+/-),按说明书可以诊断为“HIV-1抗体阳性”。

|
| 注:德国Mikrogen GmbH的HIV1+2抗体确证试剂盒; 1=阴性对照, 2=阳性对照, 3=病例1, 4=病例2, 5=HIV-1阳性, 6=HIV-1抗体不确定+gp36 图 3 条带免疫法检测条带 |
3. HIV核酸检测:病例1的HIV-1病毒载量结果为“低于检测限”,而HIV(1+2型)核酸定性结果为“核酸反应阳性”。这说明病例1可能感染的是HIV-2,而不是HIV-1。
4. HIV-2 gag区测序:病例1的3份和病例2的2份不同时间样本分别做了RNA提取和扩增,同时加上HIV-1阳性血清作为对照检测引物扩增的特异性。从凝胶电泳中可以看出,仅病例1和2的标本出现了片段约为300 bp的条带,而HIV-1阳性血清标本未出现该条带,说明该片段是HIV-2特异性扩增产物。扩增产物送公司测序,序列结果在美国国立生物技术信息中心(National Center for Biotechnology Information,NCBI)网址上进行核苷酸BLAST比对,相似度≥90%的都是HIV-2毒株,超过50株以上,其中与HIV-2 isolate LA36GomM毒株的相似度达到98%,见图 4。由序列分析结果可以进一步证实,病例1和病例2样品中有HIV-2毒株的特异性片段。

|
| 注:HN HIV-2 01A和HN HIV-2 01B是病例1不同时间的样品, HN HIV-2 02是病例2样本, HIV-2 iso LA36是HIV-2 isolate LA36GomM序列 图 4 病例1和病例2 HIV-2 gag区扩增产物的测序比较 |
5. CD4检测:病例1的2017年4月10日、5月9日和9月4日3次不同时间的CD4计数分别为118、129和131个/μl,已经处于艾滋病晚期。病例2的9月11日的CD4计数为2 527个/μl。
讨论HIV-2已经发现了30多年,但在我国过去报道的少数病例都是输入性病例,均有国外性接触史[3-5],国内本地感染病例未见报道,这是国内首次诊断的本地感染HIV-2病例。对病例进行个案流行病学调查,判断病例1通过性接触感染了病例2,而病例1无国外性接触史,可以排除国外输入性感染可能,由于其所处环境和性关系复杂,感染源头还需进一步调查取证。我们推断在湖南省HIV-2已经发生了本地2代、3代传播,其人群规模和危害不详,这是对湖南省甚至我国艾滋病疫情防控的一次重大挑战。
我国的艾滋病疫情以HIV-1为主要感染型别,很少出现HIV-2感染,确证试剂都以诊断HIV-1为主,缺少对HIV-2的诊断试剂。邱茂锋等[7]分析了16例HIV-2可疑样品,用免疫印迹试剂、线性免疫试剂和核酸试验分别检测,全部为HIV-1感染,而非HIV-2感染。说明国内的HIV检测工作中,出现的HIV-1/HIV-2混合感染的样品,多半是HIV-2的假阳性结果。此次,为避免出现以往研究中血清学诊断的不确定,我们依据文献设计了HIV-2 gag保守区引物,进行基因扩增测序,结果与国际流行株比对,证实为HIV-2感染。虽然HIV-2没有HIV-1传播的那样广泛,致病力也低于HIV-1,感染HIV-2同样也能发展成为艾滋病[8]。而一些可有效抑制HIV-1的药物如非核苷类反转录酶抑制剂和蛋白酶抑制剂对于HIV-2治疗无效[9]。因此,区分HIV-1和HIV-2对于临床治疗十分重要。现在我国经济高速发展,与国际沟通交流频繁便利,人口的流动性与日俱增,在非洲部分地区流行的HIV-2被带入中国并在国内传播很难避免,所以HIV-2毒株在中国本地病例的出现应引起足够的重视。
综上所述,湖南省首次诊断2例非输入性HIV-2感染病例表明,HIV-2已在我国存在,将对我国艾滋病的预防、诊断和治疗提出了严峻的挑战。
利益冲突: 无
| [1] | Campbell-Yesufu OT, Gandhi RT. Update on human immunodeficiency virus (HIV)-2 infection[J]. Clin Infect Dis, 2011, 52(6): 780–787. DOI:10.1093/cid/ciq248 |
| [2] | Popper SJ, Sarr AD, Travers KU, et al. Lower human immunodeficiency virus (HIV) type 2 viral load reflects the difference in pathogenicity of HIV-1 and HIV-2[J]. J Infect Dis, 1999, 180(4): 1116–1121. DOI:10.1086/315010 |
| [3] |
严延生, 郑兆双, 陈舸, 等. 我国首例HIV-2感染者的确认[J]. 中国性病艾滋病防治, 2000, 6(1): 16–18.
Yan YS, Zheng ZS, Chen G, et al. Confirmation of the first HIV-2 case in China[J]. J Chin AIDS/STD Prev Cont, 2000, 6(1): 16–18. DOI:10.13419/j.cnki.aids.2000.01.008 |
| [4] |
邵一鸣, 戴玉琳, 邢辉, 等. HIV-1和HIV-2混合感染的发现[J]. 中华实验和临床病毒学杂志, 1999, 13(4): 383–385.
Shao YM, Dai YL, Xing H, et al. HIV-1 and HIV-2 mixed infection was found[J]. Chin J Exp Clin Virol, 1999, 13(4): 383–385. DOI:10.3760/cma.j.issn.1003-9279.1999.04.022 |
| [5] |
高凯, 李燕, 梁彩云, 等. 广州市发现首例HIV-1/HIV-2混合感染[J]. 华南预防医学, 2006, 32(1): 17–19.
Gao K, Li Y, Liang CY, et al. The identification of first HIV-1/HIV-2 mixed infection in Guangzhou[J]. South Chin J Prev Med, 2006, 32(1): 17–19. DOI:10.3969/j.issn.1671-5039.2006.01.005 |
| [6] |
中国疾病预防控制中心. 全国艾滋病检测技术规范(2015年修订版)[M]. 北京: 中国疾病预防控制中心, 2015: 8–38.
Chinese Center for Disease Control and Prevention.National guideline for detection of HIV/AIDS (2015 revised edition)[M]. Beijing: Chinese Center for Disease Control and Prevention, 2015: 8–38. |
| [7] |
邱茂锋, 孙显光, 蒋岩, 等. 不同人类免疫缺陷病毒2型检测方法的比较研究[J]. 中华检验医学杂志, 2006, 29(1): 61–64.
Qiu MF, Sun XG, Jiang Y, et al. A comparing study of various detection methods for human immunodeficiency virus type 2[J]. Chin J Lab Med, 2006, 29(1): 61–64. DOI:10.3760/j:issn:1009-9158.2006.01.020 |
| [8] | Tchounga B, Ekouevi DK, Balestre E, et al. Mortality and survival patterns of people living with HIV-2[J]. Curr Opin HIV AIDS, 2016, 11(5): 537–544. DOI:10.1097/COH.0000000000000299 |
| [9] | Ekouevi DK, Balestre E, Coffie PA, et al. Characteristics of HIV-2 and HIV-1/HIV-2 dually seropositive adults in West Africa presenting for care and antiretroviral therapy:the IeDEA-West Africa HIV-2 cohort study[J]. PLoS One, 2013, 8(6): e66135. DOI:10.1371/journal.pone.0066135 |
 2018, Vol. 39
2018, Vol. 39



