文章信息
- 付建光, 施超, 沙丹, 石平, 鲍昌俊, 艾静.
- Fu Jianguang, Shi Chao, Sha Dan, Shi Ping, Bao Changjun, Ai Jing.
- 江苏省一起胃肠炎暴发疫情中分离的诺如病毒基因特征分析
- Genetic characterization of norovirus isolated in an outbreak of gastroenteritis in Jiangsu province
- 中华流行病学杂志, 2018, 39(1): 72-74
- Chinese journal of Epidemiology, 2018, 39(1): 72-74
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2018.01.015
-
文章历史
收稿日期: 2017-06-21
2. 214002 无锡市疾病预防控制中心
2. Wuxi Prefecture Center for Disease Control and Prevention, Wuxi 214002, China
诺如病毒是引起急性胃肠炎暴发和散发的主要病原体。诺如病毒感染是自限性的,但是在老年人、儿童及免疫功能障碍人群中会引起严重感染,甚至危及生命,在发展中国家每年约有20万<5岁儿童死于诺如病毒感染[1]。2016年12月在江苏省无锡市某小学出现了诺如病毒的暴发疫情,本研究对送检肛拭子标本的部分RNA依赖的RNA聚合酶(聚合酶)及衣壳蛋白区(VP1)进行了测序分析,以明确其基因特征信息。
材料与方法1.标本来源与核酸提取:2016年12月16-27日江苏省无锡市某小学出现了一起急性胃肠炎暴发疫情,共计发病43例,无死亡病例。初步检测为诺如病毒感染所致,将诺如病毒检测阳性肛拭子标本10份低温(4 ℃)运送至江苏省CDC,由病毒实验室进行病毒核酸提取,试剂盒采用美国ABI公司的5X Mag MAXTM-96 Viral Isolation Kit,提取方法参照说明书操作。
2.检测方法:提取的病毒核酸用美国Invitrogen公司的Superscript Ⅲ cDNA synthesis kit反转录为cDNA,然后利用日本TaKaRa公司的PrimeScriptTM One Step RT-PCR Kit分别扩增聚合酶序列及完整衣壳蛋白序列,引物及反应条件参照文献[2]。PCR产物用1.5%的琼脂糖凝胶电泳,阳性产物送生工生物工程(上海)股份有限公司测序。
3.序列分析:利用BioEdit及Mega 7.0软件对PCR产物进行比对,按照邻接法构建系统进化树,确定聚合酶及VP1的基因型别,并用SimPlot软件对可能的重组位点进行分析。
结果1.系统进化分析:基于聚合酶及VP1核苷酸序列的系统进化分析显示,本研究分离的诺如病毒聚合酶区为GⅡ.Pg型别,与参考株间的同源性为98.7%;VP1区为GⅡ.1型别,与参考株(美国株)间的同源性为99.4%。综合2个区的型别推测该暴发毒株可能为罕见型别的重组毒株(图 1)。

|
| 注:▲为本研究暴发毒株,编号相同的为同一暴发毒株 图 1 江苏省一起胃肠炎暴发中分离的诺如病毒聚合酶及衣壳蛋白系统进化树 |
2.重组分析:为了找到可能的重组位点,利用SimPlot软件对序列进行分析,结果显示,该暴发毒株为重组毒株,可能重组位点在VP1的5 106位点。而参考株的开放读码框架(open reading frame,ORF)1与ORF2之间重叠区为5 091~5 110位核苷酸,因此重组位点处于重叠区内,这一区域也是诺如病毒的重组热点区域(图 1)。
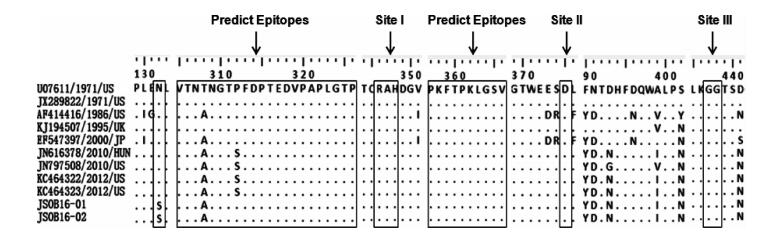
3.氨基酸变异位点分析:诺如病毒VP1的氨基酸位点变异分析显示,共有变异位点48个,占VP1序列535个氨基酸残基的8.97%,其中结构区S区有7个氨基酸残基突变,另外41个氨基酸残基突变集中在高变区P区。如图所示,绝大多数变异属于无义突变,毒株的假定抗原表位(Predict Epitopes)及受体结合位点(SiteⅠ~Ⅲ)均未出现独特的变异,仅在132位氨基酸残基出现了N到S的变异(图 2)。
|
| 图 2 江苏省一起胃肠炎暴发中分离的诺如病毒GⅡ.1型衣壳蛋白区氨基酸变异位点分析 |
本研究结果显示,引起胃肠炎暴发的诺如病毒为GⅡ.g-GⅡ.1型别重组株。GⅡ.g基因型别诺如病毒可见于散发和暴发,世界多地有过报道,但总体检出率较低[3]。北京地区曾在散发标本中检出GⅡ.g-GⅡ.12型别的重组毒株[4]。诺如病毒基因组重组热点区域在ORF1~ORF2的交叠区,本研究结果显示,GⅡ.g-GⅡ.1重组变异株的假定重组位点也是位于该区域。重组改变了病毒的基因构成,新的聚合酶可能具有更强的活性,使病毒复制更活跃。诺如病毒VP1蛋白P区域的氨基酸残基易发生变异,这些变异有可能使得病毒抗原表位及受体结合位点出现改变,从而使病毒感染性增加,毒力增强,并逃避人群的固有免疫[5]。诺如病毒GⅡ.1基因型比较保守。抗原表位及受体结合位点的保守,使得GⅡ.1基因型别诺如病毒的抗原性与感染性很少改变,这也解释了GⅡ.1基因型别诺如病毒一直未出现大规模流行的原因。
利益冲突: 无
| [1] | Glass RI, Parashar UD, Estes MK. Norovirus gastroenteritis[J]. N Engl J Med, 2009, 361(18): 1776–1785. DOI:10.1056/NEJMra0804575 |
| [2] | Fu J, Ai J, Jin M, et al. Emergence of a new GⅡ. 17 norovirus variant in patients with acute gastroenteritis in Jiangsu, China, September 2014 to March 2015[J]. Euro Surveill, 2015, 20(24): 21157. DOI:10.2807/1560-7917.ES2015.20.24.21157 |
| [3] | Bruggink LD, Dunbar NL, Marshall JA. Emergence of GⅡ. Pg norovirus in gastroenteritis outbreaks in Victoria, Australia[J]. J Med Virol, 2016, 88(9): 1521–1528. DOI:10.1002/jmv.24511 |
| [4] | Sang SW, Zhao ZT, Suo JJ, et al. Report of recombinant norovirus GⅡ. g/GⅡ. 12 in Beijing, China[J]. PLoS One, 2014, 9(2): e88210. DOI:10.1371/journal.pone.0088210 |
| [5] | Currier RL, Payne DC, Staat MA, et al. Innate susceptibility to norovirus infections influenced by FUT2 genotype in a United States pediatric population[J]. Clin Infect Dis, 2015, 60(11): 1631–1638. DOI:10.1093/cid/civ165 |
 2018, Vol. 39
2018, Vol. 39


