文章信息
- 斗智, 江震, 潘品良, 宋炜路, 徐杰, 吴尊友.
- Dou Zhi, Jiang Zhen, Pan Pinliang, Song Weilu, Xu Jie, Wu Zunyou.
- 参比校正对中国15个大城市MSM人群HIV感染者病毒载量抽样调查结果的影响
- Effect of laboratory referencing on data analysis of community viral load in HIV positive MSM from 15 cities, China
- 中华流行病学杂志, 2017, 38(12): 1683-1687
- Chinese journal of Epidemiology, 2017, 38(12): 1683-1687
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2017.12.020
-
文章历史
收稿日期: 2017-01-20
2. 102206 北京, 中国疾病预防控制中心性病艾滋病预防控制中心参比实验室;
3. 102206 北京, 中国疾病预防控制中心性病艾滋病预防控制中心
2. Reference Laboratory, National Center for AIDS/STD Control and Prevention, Chinese Center for Disease Control and Prevention, Beijing 102206, China;
3. National Center for AIDS/STD Control and Prevention, Chinese Center for Disease Control and Prevention, Beijing 102206, China
随着我国各地HIV-1病毒载量(viral load,VL)检测在艾滋病临床辅助诊断、抗病毒治疗以及科研工作中的广泛应用,该项检测工作的实验室日益增多,加强监测HIV感染者群体VL水平[1],各地区间社区VL(Community viral load,CVL)水平比较日趋可行,但各地区采用不同的检测方法、检测试剂,检测结果的准确性和可靠性方面也有差异[2],一定程度上影响了CVL水平的可比性。本研究在参比校正的基础上,对我国2014-2015年15个大城市MSM感染者抽样调查人群的VL数据变化情况进行分析。
资料与方法1.资料来源:国家科技重大专项子项目“MSM人群扩大检测扩大治疗降低新发感染试点”为有效治疗MSM人群中HIV感染者(MSM感染者),预防继发传播、降低HIV新发感染。以MSM感染者VL作为评价干预效果的指标。VL数据来源于北京、上海、南京、杭州、武汉、重庆、昆明、西安、广州、南宁、乌鲁木齐、哈尔滨、长春、成都和天津15个大城市的样本,调查时间为2013年5月至2015年12月,在基线、干预后1年、干预后2年的3个时间点随机抽取4 050例MSM感染者,比较其VL的变化趋势。本研究目的是根据不同实验室检测方法做参比校正,分析15个大城市MSM感染者CVL水平。
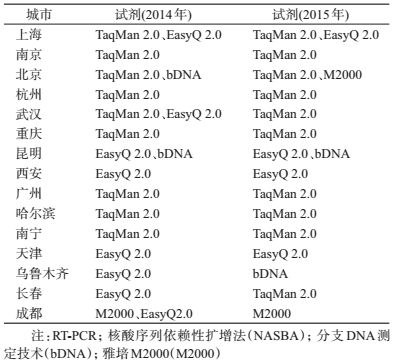
2.研究方法:2014-2015年,15个大城市VL检测及参比校正主要采用RT-PCR、核酸序列依赖性扩增法(NASBA)、分支DNA测定技术(bDNA)、雅培M2000(M2000)4种方法。各地VL检测试剂见表 1。
3.统计学分析:数据录入和整理采用Excel 2010软件,采用SPSS 17.0软件进行描述性统计分析,比较不同VL检测方法的校正参比关系。检验水准α=0.05。
结果1. CVL水平参比校正前后比较:以VL检测对数均数作为评估CVL水平的指标,采用TaqMan法作为参比标准,根据参比实验室的数据,对15个大城市VL实际检测方法进行参比校正。见表 2。
15个城市参比校正后的VL对数值高于校正前数值。2015年校正前后均值均低于2014年的对应值,结合各地的检测方法进一步分析:2014-2015年统一采用TaqMan检测试剂的城市有南京、杭州、武汉、重庆、广州、哈尔滨,以及统一采用EasyQ检测试剂的城市有西安、天津,均出现2015年校正前后的数据低于2014年校正前后数据,提示这些城市受检测的MSM感染者的VL水平呈下降趋势。2014年上海市24.8%的样本量采用EasyQ,75.2%的样本采用TaqMan进行检测;2015年分别为38.8%、61.2%。根据参比数据推算VL值≤106拷贝/ml,EasyQ检测值参比校正后上升,结合数据,可以大致判断检测人群VL水平呈下降趋势;北京、乌鲁木齐、长春、成都、昆明、南宁市在两个年度间出现检测方法更换或检测构成比的调整,影响对这些地区VL水平变化趋势的判断。
运用校正前后的数据,分别对15个城市的VL对数均值进行排序,差异极大。提示当前各地检测方法的差异以及更换,加之VL校正参数的稳定性,感染者样本人群CVL水平的横向不具有可比性。
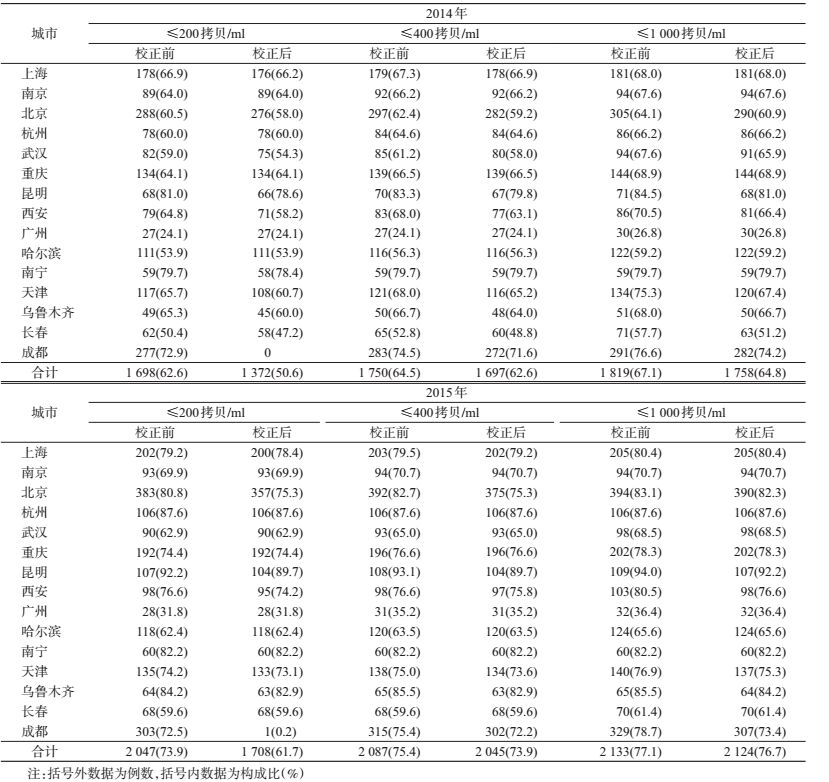
2. 15个城市MSM感染者VL抑制成功比例:参照美国CDC以及临床治疗标准,个体VL水平≤200拷贝/ml、≤400拷贝/ml、≤1 000拷贝/ml多作为VL抑制成功的标准。参比校正会带来具体数据的改变,影响对感染者中抑制成功人群比例的评估。见表 3。
以VL≤200拷贝/ml为抑制成功标准时,成都市参比前后差异较大。排除成都市,3种标准测算的成功抑制比例参比校正后的差异均有统计学意义(P值介于0.003~0.07)。从数值上比较,以VL≤400拷贝/ml或≤1 000拷贝/ml作为抑制成功评价标准,15个城市参比前后的成功抑制比例变化幅度在1%~4%。见表 4。
CVL水平的地区间比较受到实际VL水平、样本人群抽样偏差、实验室方法、实验室检测结果稳定性、参比系数稳定性等多因素的影响。本研究2014-2015年分别在国家艾滋病信息系统HIV感染者随访数据库中,随机抽取4 050例MSM感染者接受VL检测,以样本人群VL平均水平,估计CVL水平[1]。由于调查地区VL检测数据、检测方法都存在差异,本研究以TaqMan 2.0检测结果为参比标准,对bDNA、EasyQ、M2000三种VL检测值进行参比校正,根据15个城市CVL校正前后的变化情况,分析各地HIV感染者人群VL水平可比性。
1. VL检测方法的多样性,降低了地区间平均VL水平的可比性。调查城市采用多种VL检测方法,以VL检测值对数值均数作为评估CVL水平的指标,参比校正前后的数值变化较大,降低了地区间CVL水平比较的可行性。
2.保持检测方法的统一将增加年度间的可比性。在地区监测层面上,无论是采取何种检测方法,保持检测方法前后的统一,有助于本地区感染者VL水平的年度趋势比较。如果用于地区监测的样本来自于多个医疗卫生机构,需要尽可能保证不同机构样本人群构成比例在各年度基本接近[2]。
3.以VL≤400拷贝/ml或≤1 000拷贝/ml作为人群成功抑制标准进行地区间比较,稳定性较好。随着检测方法的不断更新,VL最低检测限(lower limit of detection,LLD)从1990年代的1 000拷贝/ml,降至2000年代的400拷贝/ml,降至最近50拷贝/ml及20拷贝/ml。随着检测能力、研究证据等多种因素的提升和发展,VL抑制成功的定义标准一直在变化,2010年,WHO将VL>1 000拷贝/ml定义为病毒学失败(Virological failure)[3]。此后,由于常规检测方法如RT-PCR的Cobas Amplicor HIV-1 Monitor 1.5等检测最低可信限为400拷贝/ml,有文献直接将VL≤400拷贝/ml界定为检测限以下(Undetectable),并将此标准等同于VL抑制成功[3-5]。2011年,美国CDC确定感染者VL≤200拷贝/ml为VL抑制成功(Suppressed),VL>200拷贝/ml为未成功抑制(Not suppressed);随后,VL≤200拷贝/ml的标准被认为是理想的VL抑制水平(Optimal suppression),计算该人群比例,用于地区间及年度比较[1]。除此之外,结合临床诊疗,VL还有不同的分类标准,如抗病毒治疗过程中连续两次VL>500拷贝/ml即为临床病毒学抑制失败[6]。2012年WHO指出VL<1 500拷贝/ml时感染者HIV传播性风险接近零[7]。应该考虑在众多的VL分类标准中,在参比校正的基础上,选择适宜稳定的标准进行地区间人群VL水平比较[8]。
总之,15个大城市MSM感染者VL成功抑制人群比例,经过参比校正前后的数据发生一定幅度的变化。以VL≤200拷贝/ml标准,个别城市数据在参比校正前后变化幅度较大,随着标准的放宽,参比前后的变化幅度减小,以VL≤400拷贝/ml或≤1 000拷贝/ml标准,参比前后较为稳定,抑制成功比例有1%~4%的变动幅度。本研究数据提示:以VL≤400拷贝/ml或≤1 000拷贝/ml标准,在VL检测方法多样化的现况下,不进行VL检测参比值校正,考虑1%~4%的变动幅度,地区间的初步比较是可行的。
志谢: 本文得到国家科技重大专项MSM人群艾滋病干预研究课题组的16个现场工作组成员(卢红艳、曾吉、王娟、于茂河、徐鹏、郭伟、梅淑娟、李雪静、李一、闫红梅、刘岩琳、庄鸣华、宁镇、沈晓沛、还锡萍、闫红静、张敏、朱正平、潘晓红、王懳、罗艳、张兴亮、蒋洪林、汤恒、刘普林、李艳、徐慧芳、程伟彬、钟斐、刘少础、蓝光华、陈怡、农全兴、李恬、龚毅、何勤英、范双凤、吴国辉、欧阳琳、闵向东、章任重、梁军、常文辉、贾华、卫晓丽、吴明旭、倪明建、李凡、李瑞兰、王新迪、王云霞等)工作支持,以及徐晓玉、任仙龙、陈军、曹巍和Nanci Nanyi Zhang的大力协助利益冲突: 无
| [1] | Center for Disease Control and Prevention. Guidance on community viral load:a family of measures, definitions, and method for calculation[DB/OL]. (2011-08-31)[2016-06-30]. http://www.incarecampaign.org/files/viral-suppression/community-viral-load-guidance/ |
| [2] |
蒋岩, 潘品良, 李敬云, 等. HIV-1病毒载量检测及质量保证指南(2007版)[EB/OL]. (2008-08-02)[2016-06-30]. 北京: 中国疾病预防控制中心性病艾滋病预防控制中心. http://www.chinaaids.cn/jszn/200808/t20080802_1099125.htm.
Jiang Y, Pan PL, Li JY, et al. The guideline of HIV-1 viral load testing and quality assurance (2007)[EB/OL]. (2008-08-02)[2016-06-30]. Beijing:National Center for AIDS/STD Control and prevention, China CDC. http://www.chinaaids.cn/jszn/200808/t20080802_1099125.htm. |
| [3] | World Health Organization. Antiretroviral therapy for HIV infection in adults and adolescents:recommendations for a public health approach-2010 revision[DB/OL]. (2010-08-01)[2016-06-17]. http://apps.who.int/iris/bitstream/10665/44379/1/9789241599764_eng.pdf. |
| [4] | Law MG, Woolley I, Templeton DJ, et al. Trends in detectable viral load by calendar year in the Australian HIV observational database[J]. J Int AIDS Soc, 2011, 14: 10. DOI:10.1186/1758-2652-14-10 |
| [5] | Terzian AS, Bodach SD, Wiewel EW, et al. Novel use of surveillance data to detect HIV-infected persons with sustained high viral load and durable virologic suppression in New York City[J]. PLoS One, 2012, 7(1): e29679. DOI:10.1371/journal.pone.0029679 |
| [6] | Landis RC, Branch-Beckles SL, Crichlow S, et al. Ten year trends in community HIV viral load in Barbados:implications for treatment as prevention[J]. PLoS One, 2013, 8(3): e58590. DOI:10.1371/journal.pone.0058590 |
| [7] | Mermin J, Ekwaru JP, Were W, et al. Utility of routine viral load, CD4 cell count and clinical monitoring among adults with HIV receiving antiretroviral therapy in Uganda:randomised trial[J]. BMJ, 2011, 343(7834). DOI:10.1136/bmj.d6792 |
| [8] | World Health Organization. Programmatic update:antiretroviral treatment as prevention (TASP) of HIV and TB[DB/OL]. (2012-06-01)[2016-06-17]. http://apps.who.int/iris/bitstream/10665/70904/1/WHO_HIV_2012.12_eng.pdf. |
 2017, Vol. 38
2017, Vol. 38