文章信息
- 陆蓓蓓, 谷少华, 王爱红, 葛挺, 王永, 李晓海, 许国章.
- Lu Beibei, Gu Shaohua, Wang Aihong, Ge Ting, Wang Yong, Li Xiaohai, Xu Guozhang.
- 宁波市气温对居民慢性阻塞性肺疾病每日死亡的影响
- Study on influence of air temperature on daily chronic obstructive pulmonary disease mortality in Ningbo
- 中华流行病学杂志, 2017, 38(11): 1528-1532
- Chinese Journal of Epidemiology, 2017, 38(11): 1528-1532
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2017.11.018
-
文章历史
收稿日期: 2017-03-20
2. 315010 宁波市医疗中心李惠利医院呼吸内科
2. Respiratory Department, Ningbo Medical Treatment Center Lihuili Hospital, Ningbo 315010, China
COPD在全世界具有较高的患病率和死亡率[1-3]。2013年我国死因监测数据显示,COPD已成为第三位死亡原因疾病[4]。预计到2020年,COPD将成为全球第三位死亡原因的疾病[5]。已有研究表明高温和低温均会导致COPD死亡危险增加[6-7],但气温对其影响也不尽相同,且定量评估暴露因素造成的人群归因风险相关研究较少。本研究利用宁波市2011-2016年日均气温和每日居民COPD死亡数,采用时间序列的分布滞后非线性模型(distributed lag non-linear model,DLNM),定量评价宁波市日均气温对人群COPD死亡的短期效应和归因风险。
资料与方法 (1) 资料来源2011年1月1日至2016年12月31日宁波市居民每日COPD死亡资料来自宁波市CDC死因登记报告信息系统,根据国际疾病伤害及死因分类标准(ICD-10)编码对资料进行整理,收集根本死因编码为J44死亡个案资料,资料包括性别、年龄、死亡日期等。2011-2012年气象资料下载自中国气象科学数据共享网站,2013-2016年气象资料由宁波市气象台提供,变量包括全市日均气温、日均相对湿度和日均气压。同期空气污染物日均浓度资料由宁波市环境监测中心提供,变量包括可吸入颗粒物(PM10)、二氧化硫(SO2)和二氧化氮(NO2),通过各个监测站点的数据求得全市算术平均值,作为人群污染物平均暴露量。
(2) 分析方法(1)气温的短期效应:为了同时拟合自变量的非线性效应和滞后效应,日均气温采用交叉基的形式纳入DLNM,参照文献[8]建立模型,考虑到每日的COPD死亡为小概率事件,并可能存在过度离散化,采用广义泊松回归(Quasi-Poisson)作为模型的链接函数,模型中控制湿度、气压、大气污染物、时间趋势、星期几效应等混杂因素的影响。计算方法:
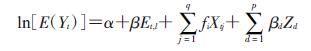
式中E(Yt)为观察到第t日死亡例数的期望值;β为日均气温的效应系数;Et, l为第t日日均气温,选择最长滞后时间为14 d;Xtj为暴露-反应关系中非线性的混杂因素,包括湿度、气压、大气污染物、时间趋势变量;fi为平滑函数(本文均使用自然立方样条函数);Zd为其他线性混杂因素,包括星期几效应等。气温的短期效应采用RR值表示。
(2)气温的归因风险:参照文献[9-10]评估气温对COPD死亡短期暴露的归因风险,结局指标包括归因死亡人数(attribute numbers,AN)和人群归因分值(attribute fraction,AF)。本文中AN表示由于气温短期暴露造成的超额死亡人数,AF表示AN占总人群死亡数的比例。计算方法:
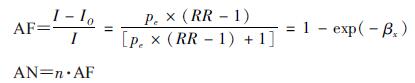
式中,I为全人群的死亡率;IO为未暴露人群中的死亡率;pe为人群暴露于研究因素的比例,此处假设为全人群暴露,pe为1;βx为气温的效应强度,高温和低温时暴露-反应关系为线性时,分别计算高温和低温时效应强度,表示为效应系数(β)和日均气温(x)的乘积;n为人群死亡数。
由于气温的效应具有滞后性,可认为第t天的风险是前一段时间暴露效应的累加,因此AF和AN的计算方法修正为:
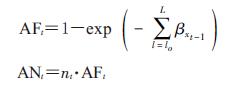
式中L为最长滞后时间,参考以往文献设定为14 d;nt为第t日的人群死亡数。
根据赤池信息准则(Akaike information criterion)最小的原则,调整气温最长滞后天数为14~30,时间变量自由度为每年3~8,观察模型稳定性,进行敏感性分析。
各气象指标和空气污染之间的相关性分析采用Spearman相关,分布滞后非线性模型运用R(3.3.1)软件中的“dlnm”工具包进行DLNM分析;P<0.05为差异有统计学意义。
结果 (1) 一般特征2011-2016年宁波市共监测到COPD死亡15 693例,日均7.16例,其中男性8 822例(56.20%),女性6 871例(43.80%),男女性别比1.28 : 1;≥65岁15 233例(97.07%),<65岁460例(2.93%)。研究期间日均气温为17.69 ℃,日均相对湿度为74.35%RH,日均大气压1 015.71 hPa。每日PM10、SO2、NO2平均浓度分别为81.71 μg/m3、20.54 μg/m3、44.12 μg/m3,PM10和NO2均超过《环境空气质量标准》GB 3095-2012中的二级浓度限值(表 1)。
日均气温和每日COPD死亡呈现一致的季节性波动,但与日均气温变化相反,随着日均气温逐渐升高,COPD死亡人数先下降后升高,每年COPD死亡人数均呈现冬春季高,夏秋季低的分布趋势(图 1)。

|
| 图 1 2011-2016年宁波市日均气温和每日慢性阻塞性肺疾病死亡人数的时间变化趋势 |
监测期间宁波市日均气温、日均相对湿度、日均气压及大气PM10、SO2、NO2日均浓度两两简单相关分析结果表明,除日均相对湿度分别与日均气温和NO2之间相关性无统计学意义外,其他气象指标与空气污染之间均存在相关关系,其中日均气温与其他指标间均呈负相关(表 2)。
(1)滞后作用:用日均气温的P2.5(2 ℃)和P97.5(32 ℃)分别代表宁波市极冷和极热温度,不同滞后天数(0 d和7 d)时不同气温(极冷和极热温度)对COPD死亡影响见图 2、3。显示COPD死亡当天即存在热效应,而COPD死亡前2 d未出现冷效应,但滞后时间均较长,滞后14 d仍表现为一定的危害作用。

|
| 图 2 宁波市日均气温不同滞后天数对慢性阻塞性肺疾病死亡的影响 |

|
| 图 3 宁波市不同滞后天数(0和7 d)时不同气温(冷、热效应)对慢性阻塞性肺疾病死亡的影响 |
(2)总效应:日均气温对COPD死亡的效应曲线为反“J”形,高温和低温均会增加COPD死亡风险(图 4)。通过模型预测获得最小死亡效应的温度(MMT)(25.5 ℃)作为参考值,不同温度(冷、热效应)相对于MMT计算的RR值分别代表COPD死亡的冷、热效应,分别计算滞后0、0~1 d、0~7 d、0~14 d的累积效应值。结果表明,COPD死亡存在明显的冷效应,14 d累积RR值达2.767(95%CI:1.950~3.928);而热效应呈现一定的收获效应,滞后14 d累积RR值为1.168(95%CI:1.036~1.315),见表 3。

|
| 注:MMT为最小死亡效应的温度,以25.5 ℃作为参考值 图 4 宁波市日均气温滞后14 d对慢性阻塞性肺疾病死亡累积效应 |
2011-2016年宁波市归因于气温暴露的COPD死亡人数为4 963(95%CI:3 469~6 027)例,人群归因分值为31.62%(95%CI:23.05%~38.89%)。其中高温(>25.5 ℃)和低温(<25.5 ℃)对COPD死亡的归因死亡人数分别为192(95%CI:59~324)例和4 772(95%CI:3 375~5 984)例,归因分值分别为1.22%(95%CI:0.30%~2.00%)和30.41%(95%CI:21.57%~37.91%)。
(6) 影响气温与COPD死亡关系的因素分析分别按性别和年龄(<65岁和≥65岁)分层,观察气温与COPD死亡的关系。分层分析显示不同性别COPD死亡前2 d均未出现冷效应,其中女性COPD死亡冷效应强度较男性平缓,但滞后时间较长,滞后14 d累积效应大于男性,分别为2.829(95%CI:1.674~4.782)和2.695(95%CI:1.667~4.357),而高温仅对女性人群存在热效应,当天为效应最大RR值为1.186(95%CI:1.063~1.324)。当日均气温为25.5 ℃时,≥65岁组COPD死亡的风险最低,在其两侧RR值随着日均气温的降低或升高而增加,滞后14 d累积冷效应和热效应分别为2.787(95%CI:1.954~3.976)和1.176(95%CI:1.032~1.341),而低温和高温对<65岁组COPD死亡均无影响。
讨论本研究利用DLNM模型分析宁波市气温和COPD死亡之间的非线性关系、滞后效应和归因风险。我国不同城市气温与每日死亡人数的关系曲线不尽相同,总体呈“U”、“W”、“J”形[6, 11-13]。宁波市气温与COPD死亡总暴露-反应关系呈反“J”形,与已有研究结果相似[6, 13]。从滞后效应和RR值的三维图可见在滞后1 d未出现冷效应,但低温存在较长的滞后期且作用较为明显。与相关研究结果一致[12, 14]。而本文分析表明,一次极端高温短期内即造成大量人群的死亡,暴露当天最高,出现明显的“收获效应”[6, 12],考虑COPD患者多为>65岁老年人群,高温导致脆弱性人群提前死亡。
不同地区人群对温度的耐受力不同,最适宜温度也不同,气温高于或低于该温度均可增加死亡风险。本研究发现,宁波市最适宜日均气温为25.5 ℃,而归因于气温暴露造成的COPD死亡风险为31.62%,明显高于归因于气温暴露人群总死亡风险(13.39%)[10],与Davie等[15]研究结果一致。且归因于低温效应的比例(30.42%)明显大于高温效应(1.22%)。考虑冷空气的吸入易引起呼吸道痉挛,而COPD呼吸道温度调节功能差,吸入空气温度增加量也低于正常人,加重呼吸道阻塞[16]。此外,低温还可直接激活细胞因子引起呼吸道炎症变化,引起外周血管收缩,血液分流,使肺有效通气容积减少[17],这些因素均易导致COPD病程的持续恶化[18-19]。低温期间要对患有COPD等呼吸系统疾病的人群采取持续的保护措施。
气温对不同性别COPD死亡影响不同,男性COPD死亡主要受低温影响,而女性COPD死亡既受低温又受高温影响,表明女性是高温季节COPD死亡的脆弱人群,与Yang等[11]研究广州市温度对不同性别热相关疾病死亡影响分析结果一致,考虑可能与不同性别生理机制差异有关。不论是低温还是高温对<65岁的人群影响不明显,但是低温和高温均可增加≥65岁人群COPD死亡风险,类似结果也见于其他研究[19-20]。这可能与老年人生理功能的衰退,对温度变化适应能力的降低有关;此外,≥65岁人群中COPD具有较高的患病率、多为合并有其他慢性病的老年人,因而对气温变化更敏感。鉴于≥65岁的老年人是冬季COPD死亡的高危人群,所以建议老年人在冬季应注意防寒保暖,预防COPD死亡的发生。
本研究由于观察时间较短,COPD死亡样本例数较少,特别是在分层分析时可信区间较宽。另外,时间序列分析是生态学研究,是基于人群而不是个体,可能存在生态学谬误。总之,本研究提示极端高温和低温会显著增加脆弱人群的死亡风险,随着全球极端天气事件的频繁发生,应建立适宜COPD等呼吸系统疾病的预警系统,加强健康宣教,制定相应的防护策略。
利益冲突: 无
| [1] | Adeloye D, Chua S, Lee C, et al. Global and regional estimates of COPD prevalence:systematic review and Meta-analysis[J]. J Glob Health, 2015, 5(2): 020415. DOI:10.7189/jogh.05-020415 |
| [2] | GBD 2013 Mortality and Causes of Death Collaborators. Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990-2013:a systematic analysis for the Global Burden of Disease Study 2013[J]. Lancet, 2015, 385(9963): 117–171. DOI:10.1016/S0140-6736(14)61682-2 |
| [3] |
包鹤龄, 方利文, 王临虹.
1990-2014年中国40岁及以上人群慢性阻塞性肺疾病患病率Meta分析[J]. 中华流行病学杂志, 2016, 37(1): 119–124.
Bao HL, Fang LW, Wang LH. Prevalence of chronic obstructive pulm-onary disease among community population aged ≥ 40 in China:a Meta-analysis on studies published between 1990 and 2014[J]. Chin J Epidemiol, 2016, 37(1): 119–124. DOI:10.3760/cma.j.issn.0254-6450.2016.01.026 |
| [4] |
中国疾病预防控制中心慢性非传染性疾病预防控制中心.中国死因监测数据集(2013)[M]. 北京: 科学普及出版社, 2015.
Center for Chronic Non-communicable Disease Prevention and Control, Chinese Center for Disease Control and Prevention.Database of death surveillance in China (2013)[M]. Beijing: Science Press, 2015. |
| [5] | GOLD Excutive Committee. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease (updated 2016)[EB/OL]. (2016-09-02)[2016-09-02]. http://www.goldcopd.com. |
| [6] | Liu LQ, Breitner S, Pan XC, et al. Associations between air temperature and cardio-respiratory mortality in the urban area of Beijing, China:a time-series analysis[J]. Environ Health, 2011, 10: 51. DOI:10.1186/1476-069X-10-51 |
| [7] | Schwartz J. Who is sensitive to extremes of temperature:a case-only analysis[J]. Epidemiology, 2005, 16(1): 67–72. DOI:10.1097/01.ede.0000147114.25957.71 |
| [8] | Gasparrini A, Armstrong B, Kenward MG. Distributed lag non-linear models[J]. Stat Med, 2010, 29(21): 2224–2234. DOI:10.1002/sim.3940 |
| [9] | Gasparrini A, Leone M. Attributable risk from distributed lag models[J]. BMC Med Res Methodol, 2014, 14: 55. DOI:10.1186/1471-2288-14-55 |
| [10] |
谷少华, 贺天锋, 陆蓓蓓, 等.
基于分布滞后非线性模型的归因风险评估方法及应用[J]. 中国卫生统计, 2016, 33(6): 959–962.
Gu SH, He TF, Lu BB, et al. Measures and application for attributable risk from distributed lag non-linear model[J]. Chin J Health Stat, 2016, 33(6): 959–962. |
| [11] | Yang J, Ou CQ, Ding Y, et al. Daily temperature and mortality:a study of distributed lag non-linear effect and effect modification in Guangzhou[J]. Environ Health, 2012, 11: 63. DOI:10.1186/1476-069X-11-63 |
| [12] |
李萌萌, 周脉耕, 张霞, 等.
济南市4个区气温对非意外死亡及死因别死亡的影响[J]. 中华流行病杂志, 2014, 35(6): 684–688.
Li MM, Zhou MG, Zhang X, et al. Impact of temperature on non-accidental deaths and cause-specific mortality in four districts of Jinan[J]. Chin J Epidemiol, 2014, 35(6): 684–688. DOI:10.3760/cma.j.issn.0254-6450.2014.06.015 |
| [13] | Kan HD, Jia J, Chen BH. Temperature and daily mortality in Shanghai:a time-series study[J]. Biomed Environ Sci, 2003, 16(2): 133–139. |
| [14] | Barnett AG, Hajat S, Gasparrini A, et al. Cold and heat waves in the United States[J]. Environ Res, 2012, 112: 218–224. DOI:10.1016/j.envres.2011.12.010 |
| [15] | Davie GS, Baker MG, Hales S, et al. Trends and determinants of excess winter mortality in New Zealand:1980 to 2000[J]. BMC Publ Health, 2007, 7: 263. DOI:10.1186/1471-2458-7-263 |
| [16] | Paredi P, Caramori G, Cramer D, et a1. Slower rise of exhaled breath temperature in chronic obstructive pulmonary disease[J]. Eur Respir J, 2003, 21(3): 439–443. DOI:10.1183/09031936.03.00061902 |
| [17] | Li MC, Li Q, Yang G, et al. Cold temperature induces mucin hypersecretion from normal human bronchial epithelial cells in vitro through a transient receptor potential melastatin 8(TRPM8)-mediated mechanism[J]. J Allergy Clin Immunol, 2011, 128(3): 626–634.e5. DOI:10.1016/j.jaci.2011.04.032 |
| [18] | Tseng CM, Chen YT, Ou SM, et al. The effect of cold temperature on increased exacerbation of chronic obstructive pulmonary disease:a nationwide study[J]. PLoS One, 2013, 8(3): e57066. DOI:10.1371/journal.pone.0057066 |
| [19] | Huang F, Zhao A, Chen RJ, et al. Ambient temperature and outpatient visits for acute exacerbation of chronic bronchitis in Shanghai:a time series analysis[J]. Biomed Environ Sci, 2015, 28(1): 76–79. DOI:10.3967/bes2015.008 |
| [20] | Monteiro A, Carvalho V, Oliveira T, et al. Excess mortality and morbidity during the July 2006 heat wave in Porto, Portugal[J]. Int J Biometeorol, 2013, 57(1): 155–167. DOI:10.1007/s00484-012-0543-9 |
 2017, Vol. 38
2017, Vol. 38





