文章信息
- 何彩丽, 程宁, 荣右明, 李海燕, 李娟生, 丁蛟, 胡晓斌, 蒲宏全, 任晓卫, 白亚娜.
- He Caili, Cheng Ning, Rong Youming, Li Haiyan, Li Juansheng, Ding Jiao, Hu Xiaobin, Pu Hongquan, Ren Xiaowei, Bai Yana.
- 金昌队列人群痛风发病危险因素的Cox回归分析
- Risk factors of gout in Jinchang cohort:a Cox regression analysis
- 中华流行病学杂志, 2017, 38(7): 897-901
- Chinese journal of Epidemiology, 2017, 38(7): 897-901
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2017.07.010
-
文章历史
收稿日期: 2017-01-13
2. 361009 厦门市莲花医院体检科;
3. 361000 厦门市湖里区疾病预防控制中心地方病与慢性病防治科
2. Basic Medical College, Lanzhou University, Lanzhou 730000, China;
3. Workers'Hospital of Jinchuan Group Co, Ltd, Jinchang 737100, China He Caili and Cheng Ning are the first authors who contributed equally to the article
近几十年来,痛风的发病率在世界范围内都在不断增加。2005-2012年瑞典总人群的痛风发病率增加了50%[1],美国20年间原发性痛风的发病率增加了2倍多[2],我国近15年来城市医院住院的痛风病例数也正在直线上升[3]。痛风与MS关系密切[4-5],给全球许多国家带来了沉重的社会经济负担。我国大多数文献报道的是痛风的患病情况,依据前瞻性队列研究其发病情况的资料仍然稀少。本研究报道了金昌队列人群痛风的发病率,并采用多因素Cox回归分析方法分析金昌队列人群中痛风发病的危险因素,为制定该人群痛风的防治措施提供科学依据。
对象与方法1.研究对象:以金昌队列基线资料中未患痛风的金昌公司职工作为研究对象,基线调查从2011年6月24日开始,随访从2013年1月24日开始,截止2015年11月24日,共观察研究对象33 153例,平均随访时间(2.29±0.54)年。其中男性20 142例,女性13 010例,平均年龄(46.39±12.81)岁。随访期间共有新发痛风病例277例。随访内容包括问卷调查、体格检查和实验室检测[6-10]。问卷主要内容:一般人口学特征、生活饮食习惯、慢性病现患状况、家族疾病史等;体格检查包括身高、体重、血压等;实验室检测包括FPG、TC、TG、HDL-C、LDL-C、尿酸(UA)、尿素氮(BUN)、肌酐(Cr)等。
2.流行病学调查:研究对象签署知情同意书后,由经过统一培训的调查人员获取流行病学资料;临床检验和疾病诊断:由金川集团职工医院专业人员完成。吸烟指每天至少吸1支,连续吸烟6个月以上;饮酒指平均每周至少饮1次,连续6个月以上;饮茶指每周至少饮3次,连续6个月以上;体育锻炼平均每周3次以上,每次锻炼时间超过30 min视为“经常”。吸烟指数=吸烟量(支/d)×吸烟年数(年);每周饮酒酒精含量=啤酒的瓶数×640(ml)×0.043(%v/v)+葡萄酒的两数×0.129×50(%v/v)+白酒的两数×0.45×50(%v/v)×频率(次/周)×0.8;饮茶指数=饮茶量(两/月)×饮茶年数(年)。
3.相关诊断标准:痛风:主要采用1977年美国风湿病学会(ACR)制订的痛风诊断标准和1985年制订的霍姆斯(Holmes)标准。将关节滑液和痛风结节中找到“尿酸盐结晶”作为诊断痛风的“金标准”。在条件受限的情况下,也可根据患者的临床特征作出诊断:即根据12条临床特征中具备≥6条(ACR标准第3条);或者根据患者同时具备高尿酸血症、有反复发作的急性单关节炎及无症状间歇期、秋水仙碱对缓解症状有效等几项条件(Holmes标准第3条)作出痛风诊断。本次研究中的痛风病例由具有临床诊断和治疗资质的金川集团职工医院(三甲医院)依据此标准诊断。BMI:在24~28 kg/m2为超重,BMI≥28 kg/m2为肥胖。FPG:在6.1~6.9 mmol/L为空腹血糖受损,FPG≥7.0 mmol/L为糖尿病。UA:男性>420 mmol/L,女性>357 mmol/L为高尿酸。血脂和血压分层详细参见2016年中国成人血脂异常防治指南[11]和2010年中国高血压防治指南[12]。
4.统计分析:利用EpiData 3.1软件建立数据库,并采用双录入进行数据录入的质量控制。采用SPSS 20.0软件进行数据分析:采用χ2检验比较金昌队列人群不同年龄不同性别分层下痛风的发病状况,采用多因素Cox回归分析影响该人群痛风发病的影响因素,运用对数线性模型进行交互作用分析,检验水准均为α=0.05。
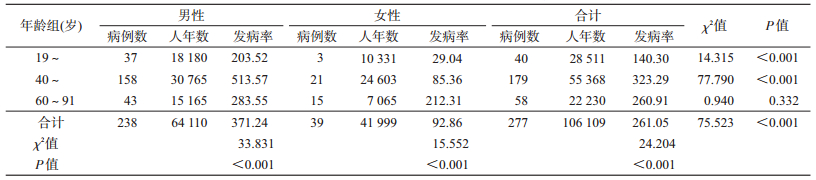
结果1.金昌队列人群痛风发病状况:总发病人数为277例,发病率为261.05/10万人年,其中男性新发痛风病例为238例,发病率为371.24/10万人年,女性新发痛风病例为39例,发病率为92.86/10万人年,男性痛风发病率远远高于女性,差异有统计学意义。该差异主要表现在60岁以前,随着年龄的增加,男女性痛风的发病率都呈现上升趋势,在40~59岁达到高值;60岁以后男性痛风发病率开始下降,女性痛风发病率持续上升,男女性痛风发病率差异无统计学意义。见表 1。
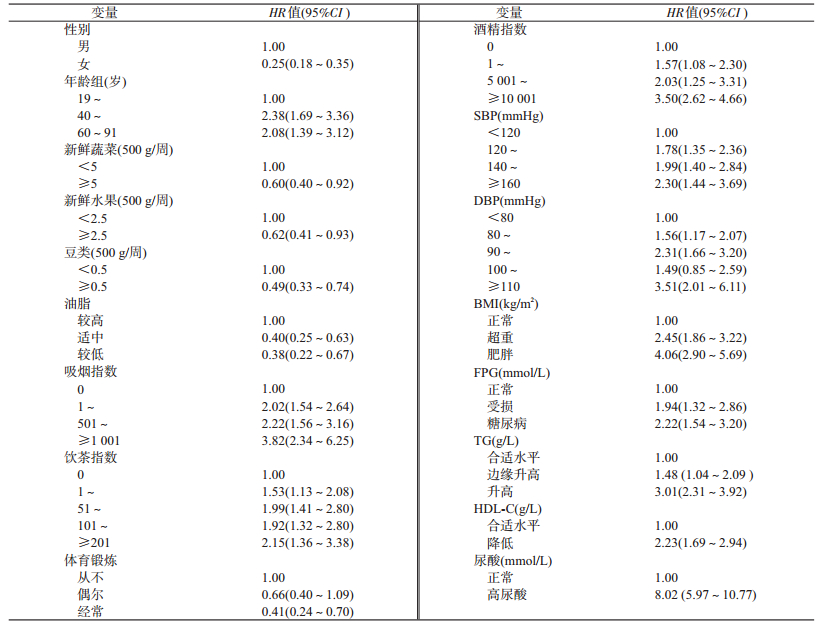
2.金昌队列人群痛风发病的单因素Cox回归结果:以生存时间t为横轴,对数生存率ln[-lnŜ(t)]为纵轴,绘制分类协变量各组别的生存曲线,协变量各组别对应的曲线平行,满足Cox回归模型的风险比例条件。对人口学特征、生活饮食习惯和实验室指标进行单因素Cox回归分析结果显示:性别、年龄、蔬菜摄入、水果摄入、豆类、油脂摄入、吸烟、饮酒、饮茶、体育锻炼、SBP、DBP、BMI、FPG、TG、HDL-C和UA有统计学意义(表 2)。
3.金昌队列人群痛风发病的多因素Cox回归结果:将单因素Cox回归分析中差异有统计学意义的变量纳入多因素Cox回归模型,进行痛风发病的影响因素研究。结果显示:年龄在40岁以上、酒精指数≥10 001、肥胖、糖尿病和高尿酸是痛风发病的危险因素,每周豆类摄入≥250 g,经常体育锻炼为痛风发病的保护性因素(表 3)。
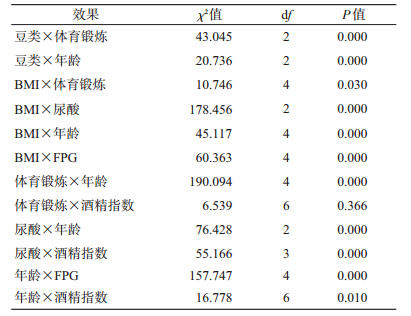
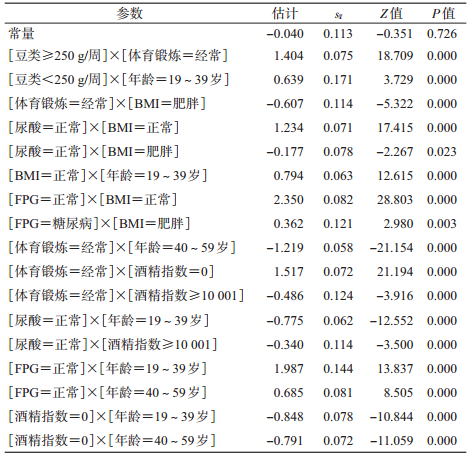
4.影响因素间的交互作用分析:将影响金昌队列人群痛风发病的7个因素引入对数线性模型,分析各因素之间可能存在的交互作用。先采用Model-Selection过程选择最佳的模型,再采用General过程得到具体的参数估计和检验结果。K阶效应检验结果显示,一阶效应(主效应)和二阶交互效应的似然比χ2和Pearson χ2检验有统计学意义(P<0.01)。因此在分层模型中定义最高阶为所有二阶(All 2-way),使用向后排除法逐步从检验概率大于标准值的效应中,淘汰拟合优度变化最小的效应,进行筛选显著效应项。二阶筛选结果显示(表 4):豆类×体育锻炼、豆类×年龄、BMI×体育锻炼、BMI×尿酸、BMI×年龄、BMI×FPG、体育锻炼×年龄、体育锻炼×酒精指数、尿酸×年龄、尿酸×酒精指数、年龄×FPG和年龄×酒精指数的交互作用有统计学意义(P<0.05),以这12个有统计学意义的二阶效应进行简约模型的参数估计。从表 5看出,经常体育锻炼与豆类(≥250 g/周)之间是协同作用,豆类(<250 g/周)与年龄在19~39岁之间是协同交互作用,经常体育锻炼与肥胖之间是拮抗作用,UA正常与肥胖之间是拮抗作用,年龄在19~39岁与BMI正常之间是协同作用,糖尿病与肥胖之间是协同作用,经常体育锻炼与年龄在40~59岁之间是拮抗作用,经常体育锻炼与酒精指数(≥10 001)之间是拮抗作用,UA正常与年龄在19~39岁之间是拮抗作用,UA正常与酒精指数(≥10 001)之间是拮抗作用,血糖水平正常与年龄在19~59岁之间是协同作用,不饮酒与年龄在19~59岁之间是拮抗作用。
本研究结果表明:① 40岁以上男性为痛风高发人群,男性高于女性,但在60岁以上男女性痛风发病水平相当,这可能与男性不良生活方式和雌激素促进肾脏对尿酸的排泄有关[13]。② 豆类是痛风发病的保护性因素,这可能是因为豆类属于植物性蛋白,大豆蛋白质与动物蛋白质中的氨基酸组成和相对比例不同,在功能及代谢方面有一定区别。而且在豆制品加工过程中,豆类植物含有的嘌呤大部分已遭到破坏,不会通过摄食进入人体内[14]。③ 经常进行体育锻炼,可以有效预防痛风的发生,这可能与体育锻炼能够减轻体重,增强组织对胰岛素的敏感性等有关[15]。④ 酒精摄入能够增加尿酸合成、减少尿酸排泄[16-18]。⑤ 肥胖能够增加尿酸合成,降低肾脏尿酸排泄[19],而且肥胖还能够导致胰岛素抵抗[20]。⑥ 糖尿病患者多存在胰岛素抵抗,而且长期高血糖可导致肾脏功能损害[21-22]。⑦ 高尿酸血症是痛风的重要生化标志,痛风的发生与高尿酸血症持续时间和程度有直接关系[13]。
交互作用分析结果显示,各影响因素之间存在协同或者拮抗的交互作用,而且各因素的不同分层之间交互作用的效果也有所不同,这提示我们在预防和控制痛风发病的过程中应该充分考虑各因素之间的联系,如体育锻炼和豆类摄入之间的协同作用,糖尿病和肥胖之间的协同作用,以及体育锻炼和肥胖之间的拮抗作用等,制定合理的预防措施,提高痛风防治的效果。
综上所述,培养良好的生活饮食习惯,定期进行体检,有利于预防和控制该职业人群痛风病的发生。
利益冲突: 无
| [1] | Dehlin M, Drivelegka P, Sigurdardottir V, et al. Incidence and prevalence of gout in Western Sweden[J]. Arthritis Res Ther, 2016, 18: 164. DOI:10.1186/s13075-016-1062-6 |
| [2] | Arromdee E, Michet CJ, Crowson CS, et al. Epidemiology of gout:is the incidence rising?[J]. J Rheumatol, 2002, 29(11): 2403–2406. |
| [3] |
杨岫岩, 唐福林, 尹培达.
21家医院痛风住院构成比15年变化趋势分析[J]. 中华流行病学杂志, 1996, 17(1): 10–12.
Yang XY, Tang FL, Yin PD. The trend of proportion among inpatients with gout in 21 hospitals during the past 15 years[J]. Chin J Epidemiol, 1996, 17(1): 10–12. |
| [4] | He, SJ, Chan C, Xie ZD, et al. The relationship between serum uric acid and metabolic syndrome in premenopausal and postmenopausal women in the Jinchang Cohort[J]. Gynecol Endocrinol, 2016, 33(2): 141–144. DOI:10.1080/09513590.2016.1214261 |
| [5] | Yang AM, Liu SM, Cheng N, et al. Dose-response analyses of uric acid and risk of type 2 diabetes in a Chinese occupational population:a cohort study and Meta-analysis[J]. Lancet Diab Endocrinol, 2016, 4: S22. DOI:10.1016/S2213-8587(16)30377-1 |
| [6] | Bai Y, Yang AM, Pu HQ, et al. Cohort Profile:The China metal-exposed workers cohort study (Jinchang Cohort)[J]. Int J Epidemiol, 2016. DOI:10.1093/ije/dyw223 |
| [7] | Bai YN, Yang AM, Pu HQ, et al. Nickel-exposed workers in China:a cohort study[J]. Biomed Environ Sci, 2014, 27(3): 208–211. DOI:10.3967/bes2014.042 |
| [8] | Cheng N, Ma L, Zheng TZ, et al. A retrospective cohort mortality study in Jingchuan of China-The largest nickel population in the world[J]. Int J Molecul Med, 2014, 34: S6. |
| [9] | Ma L, Bai YN, Pu HQ, et al. A retrospective cohort mortality study in Jinchang, the largest nickel production enterprise in China[J]. Biomed Environ Sci, 2014, 27(7): 567–571. DOI:10.3967/bes2014.088 |
| [10] |
白亚娜, 蒲宏全, 代敏, 等.
中国金昌队列研究进展[J]. 兰州大学学报:医学版, 2015, 41(6): 29-33–38.
Bai YN, Pu HQ, Dai M, et al. Study progress on China Jinchang Cohort[J]. Journal of Lanzhou University:Medical Sciences, 2015, 41(6): 29-33–38. DOI:10.13885/j.issn.1000-2812.2015.06.005 |
| [11] |
中国成人血脂异常防治指南修订联合委员会. 中国成人血脂异常防治指南(2016年修订版)[J]. 中国循环杂志, 2016, 31(10): 937-953. DOI: 10.3969/j.issn.1000-3614.2016.10.001.
The Guidelines for the Prevention and Control of adult Blood Lipid in China have been Revised Chinese guidelines on prevention and treatment of dyslipidemia in adults(2016 revision)[J]. Chin Circula J, 2016, 31(10):937-953. DOI:10.3969/j.issn.1000-3614.2016.10.001. |
| [12] |
刘力生.
中国高血压防治指南2010[J]. 中华高血压杂志, 2011, 19(8): 701–743.
Liu LS. 2010 Chinese guidelines for the management of hypertension[J]. Chin J Hypertens, 2011, 19(8): 701–743. DOI:10.16439/j.cnki.1673-7245.2011.08.009 |
| [13] |
陈日东, 白亚娜, 苏辉, 等.
金昌市职业人群痛风的影响因素分析[J]. 中国慢性病预防与控制, 2014, 22(6): 659–662.
Chen RD, Bai YN, Su H, et al. Analysis of influencing factors of gout in occupational crowd of Jinchang city[J]. Chin J Prev Contr Chron Dis, 2014, 22(6): 659–662. |
| [14] | MacFarlane LA, Kim SC. Gout:a review of nonmodifiable and modifiable risk factors[J]. Rheum Dis Clin North Am, 2014, 40(4): 581–604. DOI:10.1016/j.rdc.2014.07.002 |
| [15] |
张琳, 祝波, 孙琳, 等.
饮食与运动对痛风影响的研究[J]. 哈尔滨医科大学学报, 2013, 47(4): 360–362.
Zhang L, Zhu B, Sun L, et al. Effect of diet and movement on gout[J]. J Harbin Med Univ, 2013, 47(4): 360–362. DOI:10.3969/j.issn.1000-1905.2013.04.019 |
| [16] | Choi, HK, Atkinson K, Karlson EW, et al. Alcohol intake and risk of incident gout in men:a prospective study[J]. Lancet, 2004, 363(9417): 1277–1281. DOI:10.1016/s0140-6736(04)16000-5 |
| [17] | Faller J, Fox IH. Ethanol-induced hyperuricemia:evidence for increased urate production by activation of adenine nucleotide turnover[J]. N Engl J Med, 1982, 307(26): 1598–1602. DOI:10.1056/nejm198212233072602 |
| [18] | Sharpe CR. A case-control study of alcohol consumption and drinking behaviour in patients with acute gout[J]. Can Med Assoc J, 1984, 131(6): 563–567. |
| [19] | Choi HK, Atkinson K, Karlson EW, et al. Obesity, weight change, hypertension, diuretic use, and risk of gout in men:the health professionals follow-up study[J]. Arch Intern Med, 2005, 165(7): 742–748. DOI:10.1001/archinte.165.7.742 |
| [20] | Demarco MA, Maynard JW, Huizinga MM, et al. Obesity and younger age at gout onset in a community-based cohort[J]. Arthritis Care Res (Hoboken), 2011, 63(8): 1108–1114. DOI:10.1002/acr.20479 |
| [21] | Bhattacharjee N, Barma S, Konwar N, et al. Mechanistic insight of diabetic nephropathy and its pharmacotherapeutic targets:an update[J]. Eur J Pharmacol, 2016, 791: 8–24. DOI:10.1016/j.ejphar.2016.08.022 |
| [22] | Perez-Ruiz F, Aniel-Quiroga MA, Herrero-Beites AM, et al. Renal clearance of uric acid is linked to insulin resistance and lower excretion of sodium in gout patients[J]. Rheumatol Int, 2015, 35(9): 1519–1524. DOI:10.1007/s00296-015-3242-0 |
 2017, Vol. 38
2017, Vol. 38