文章信息
- 张顺祥, 杨品超, 蔡亚丽, 林莹, 邹宇华.
- Zhang Shunxiang, Yang Pinchao, Cai Yali, Lin Ying, Zou Yuhua.
- 基于社区慢性乙型肝炎抗病毒治疗策略成本效果分析
- Cost-effectiveness of community-based treatment of chronic hepatitis B in China
- 中华流行病学杂志, 2017, 38(7): 860-867
- Chinese journal of Epidemiology, 2017, 38(7): 860-867
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2017.07.004
-
文章历史
收稿日期: 2017-01-13
2. 510006 广州, 广东药科大学
2. Guangdong Pharmaceutical University, Guangzhou 510006, China
全球消除乙型肝炎(乙肝)纳入了联合国可持续发展规划并被成员国接受,WHO已经发布了具体的行动计划并在全球推广实施[1]。依托医疗卫生技术支持,采用公共卫生手段,阻断HBV传播,降低慢性乙肝(chronic hepatitis B,CHB)不良转归的发生率和死亡率,成为主要目标[2]。据此,提出了CHB基于社区治疗(community-based treatment)和预防性治疗(treatment as prevention)的理念[3]。WHO颁布的CHB防治指南中规定,各国应根据本地乙肝流行现状、实验室检测能力、药品及其供应、财政支持力度和医疗卫生的配置,不分性别、年龄、种族和社会经济地位,扩大HBV感染人群的抗病毒治疗,优先筛检出符合治疗指征的CHB患者,提供终身抗病毒治疗和效果监测[4],该规定体现了预防性治疗的理念。我国重大传染病社区综合防治方案和规程中,也提出了探索乙肝抗病毒社区适宜治疗模式,提高治疗可及性和规范化,降低乙肝病死率的策略[5]。由此可见,基于社区的CHB抗病毒治疗策略不同于临床治疗,不仅要靠临床医生在医院中实现,还应面向社区人群,使HBV感染者中符合治疗指征的CHB患者都得到抗病毒治疗。WHO对消除乙肝将要承受的经济负担评估发现,患者的检测和抗病毒治疗是最主要的构成部分[1]。我国是传统的乙肝高发区,消除乙肝将会承受巨量的公共卫生资源,基于社区CHB抗病毒治疗的经济学合理性如何,成为急需回答的问题。本研究以WHO有关规划和我国重大传染病社区综合防治方案为策略优化为依据[1-3],按照我国CHB防治指南确定抗病毒药物治疗和监测内容[6],遵循成本效果分析理论和方法构建经济学模型,旨在对我国基于社区CHB抗病毒治疗策略的成本效果和可支付性作出评价。
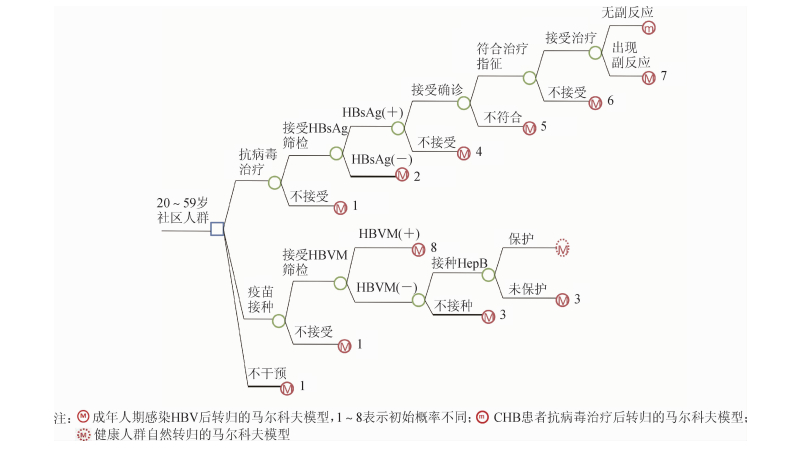
方法1.经济学模型的建立:以20~59岁人群为对象,构建了基于社区CHB抗病毒治疗决策分析马尔科夫模型(图 1)。基于社区CHB抗病毒治疗策略是指对20~59岁社区人群进行HBsAg筛检,阳性者进一步确诊,对符合治疗指征的CHB患者服用恩替卡韦,每天1次,每次0.5 mg,并终生用药,简称“抗病毒治疗”,为研究策略。分别以“疫苗接种”和“不干预”为对照策略,前者是指对社区人群进行HBV标志(HBVM,即抗-HBs、HBsAg和抗-HBc三项指标)筛检,阴性者按0-1-6月程序接种3剂10 μg乙肝疫苗,HBVM任一项阳性者不接种乙肝疫苗。“不干预”策略指不采取上述抗病毒治疗和疫苗接种措施。
|
| 图 1 我国基于社区CHB抗病毒治疗决策分析马尔科夫模型 |
“抗病毒治疗”策略中,考虑了人群筛检HBsAg依从性、HBsAg阳性率、确诊依从性、符合治疗指征的比例、接受恩替卡韦治疗的依从性和严重不良反应发生率6个影响因素(图 1)。“疫苗接种”策略中,考虑了人群接受HBVM筛检的依从性、HBVM的阳性率、乙肝疫苗全程接种率和抗-HBs阳转率等4个因素。图 1的结果节点分别连接了成年人期HBV感染转归、CHB患者抗病毒治疗后转归和人群自然转归的马尔科夫模型[7]。本研究以我国10万20~59岁人群为研究队列,计算其一生的成本和效果期望值,利用TreeAge Pro 2015软件完成模型的构建和运行。经济学模型的条件:接受恩替卡韦者均为CHB初治患者;一旦服用恩替卡韦,将终生接受治疗;未考虑恩替卡韦的耐药性。
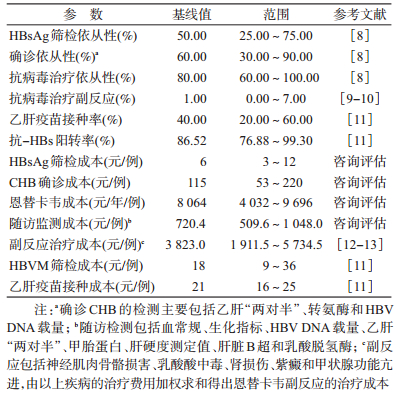
2.参数估计:本研究模型参数确定时,采用全国性调查和Meta分析结果,或咨询并参考国内外同类研究结果。基本参数包括HBsAg筛检依从性、确诊依从性和接受治疗的依从性[8],恩替卡韦抗病毒治疗副反应[9-10]、乙肝疫苗接种率和抗-HBs阳转率[11]。成本参数主要有HBsAg筛检成本、CHB确诊成本、恩替卡韦成本、随访监测成本和严重副反应治疗成本[12-13],HBVM筛检成本、乙肝疫苗接种成本和各型乙肝相关疾病的感染成本[14]。见表 1。按照年龄组引入模型的参数包括HBsAg阳性率[15]、符合治疗指征的比例[16]和HBVM阳性率[15]。见表 2。人群期望寿命来源于中国统计年鉴(2013年),贴现率取3%(0~6%)。乙肝相关疾病效用值、各类马尔科夫模型的初始概率和转移概率同文献[17]。依据参数的特征,设定乙肝相关疾病费用服从Gamma分布,其余参数均服从三角分布,完成了参数不确定性分析。
3.分析指标:
(1)成本:从全社会角度,抗病毒治疗策略的总成本包括筛检、确诊和抗病毒治疗成本(统称治疗成本)、未能阻断CHB不良转归所需要支付的直接和间接成本(统称疾病转归成本)。疫苗接种策略的免疫预防成本包括HBsAg筛检费和乙肝疫苗接种直接和间接费(统称免疫预防成本)和因感染HBV并转归为乙肝相关疾病所需要支付的直接和间接成本(统称感染成本)。从支付者角度,抗病毒治疗策略总成本仅纳入治疗成本,而疫苗接种策略的总成本仅考虑免疫预防成本。
(2)效果:计算了不同策略获得的质量调整生命年(quality adjusted life years,QALYs),计算公式: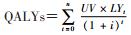
(3)成本效果分析指标:包括成本效果比(cost-effectiveness ratio,CER)和增量成本效果比(incremental cost-effectiveness ratio,ICER)。CER是策略成本(Cost,C)与效果(Effectiveness,E)之比,当研究策略与对照策略相互独立时计算该指标,表示单位效果所需要的成本[18-19]。本研究中,抗病毒治疗与疫苗接种策略比较时,采用CER指标。计算公式: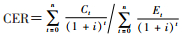
ICER是研究策略(A策略)与对照策略(B策略)成本差值与效果差值之比,适用于研究策略与对照策略相互排斥时,表示采用研究策略后,每多获得一个单位效果需要多投入的成本[18-19]。本研究中,抗病毒治疗和疫苗接种策略分别与不干预比较时,采用ICRE指标,计算公式:
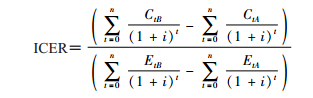
式中,n表示期望寿命,EtA和CtA、EtB和CtB分别表示A方案和B方案在第t年的效果和成本,i表示贴现率。
本研究成本效果阈值采用WHO建议的标准:ICER<0,表示研究策略获得健康收益的同时节省成本,最具成本效果价值;若0<ICER<人均GDP,则研究策略具有较高成本效果价值;若人均GDP<ICER<3倍人均GDP,则研究策略具有成本效果价值;而ICER>3倍人均GDP,则研究策略没有成本效果价值。以2013年我国人均GDP(43 320.1元)为对比参数。
4.敏感性分析:按照参数取值范围,逐个引入模型,获得相应的ICER,与参数基线值结果比较,绘制龙卷风图(Tornado Diagram),观察各参数对乙肝抗病毒治疗和疫苗接种策略经济学评估的影响大小,实现一维敏感性分析。概率敏感性分析时,采用蒙特卡洛模拟参数随机变动并运算1 000次,得到相应ICER值;在成本效果平面图中描绘ICER分布的成本效果散点图,根据95%散点所处象限位置和趋势,判断乙肝抗病毒治疗策略的经济学意义及其结果的可靠性。此外,本研究利用蒙特卡洛模拟运算结果,拟合抗病毒治疗策略的成本效果可接受曲线(cost-effectiveness acceptability curve,CEAC),获得不同支付意愿下研究策略具有成本效果的概率,对公众支付意愿和经济性的不确定性同步做出评估。
5.可支付性评价:为了评估基于社区CHB抗病毒治疗所需资金总量对策略实施的影响,本研究采取支付者角度的乙肝抗病毒治疗策略人均成本(简称支付成本)与队列人口总数相乘,获得实施该策略的总预算。以总预算为横坐标,乙肝抗病毒治疗策略可被支付的概率为纵坐标,绘制可支付线(affordability curve),表示支付成本在最小与最大范围变化时,在相应总预算范围内,该策略具有可支付性的概率[17]。本研究还对获得的CEAC与可支付线结果做出综合分析,拟合成本效果可支付曲线(cost-effectiveness affordability curves),同时分析支付意愿和总预算变化的不同情形下,乙肝抗病毒治疗策略同时具有经济性和可支付性的概率变化[17]。
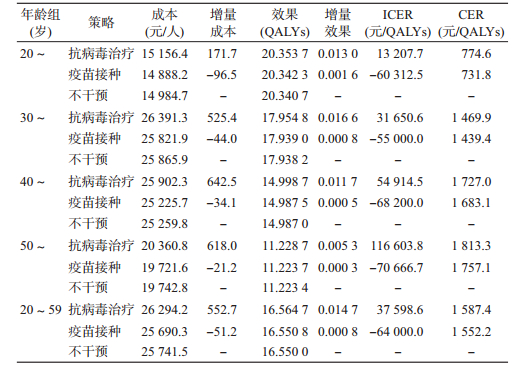
结果1.成本效果分析:我国20~59岁人群CHB抗病毒治疗策略成本效果分析结果见表 3。与不干预相比,在20~59岁及其各年龄组人群中,抗病毒治疗策略均增加成本,也可获得更多的效果;在20~、30~、40~、50~59和20~59岁人群中,ICER(/QALYs)分别为13 207.7、31 650.6、54 914.5、116 603.8和37 598.6元,均小于我国2013年3倍人均GDP(129 960.3元),表明抗病毒治疗策略每多获得一个QALYs需要额外投入,但符合成本效果原则;由于低年龄组人群ICER较小,提示抗病毒治疗策略应优先在低年龄人群中实施。
从表 3还可以看出,各年龄组人群采用乙肝疫苗接种策略时,均节省成本且能获得更多的效果。每多获得一个QALYs节省的成本,在20~、30~、40~、50~59和20~59岁年龄组人群中,分别为60 312.5、55 000.0、68 200.0、70 666.7和64 000.0元。这一结果表明,我国20~59岁各年龄组人群乙肝疫苗接种策略最具成本效果意义。
由表 3中CER可见,各年龄组人群中实施乙肝抗病毒治疗和疫苗接种策略,每获得一个QALYs需要投入的成本变动在731.8~1 813.3元,均小于我国2013年人均GDP(43 320.0元)水平,提示乙肝抗病毒治疗和疫苗接种策略具有较高成本效果意义。进一步分析发现,在各年龄人群中,乙肝疫苗接种策略的CER均低于抗病毒治疗策略,提示乙肝疫苗接种策略的经济学价值高于抗病毒治疗策略。提示我国20~59岁各年龄组人群乙肝防控策略是优先考虑对易感者接种乙肝疫苗,再对CHB患者实施抗病毒治疗。
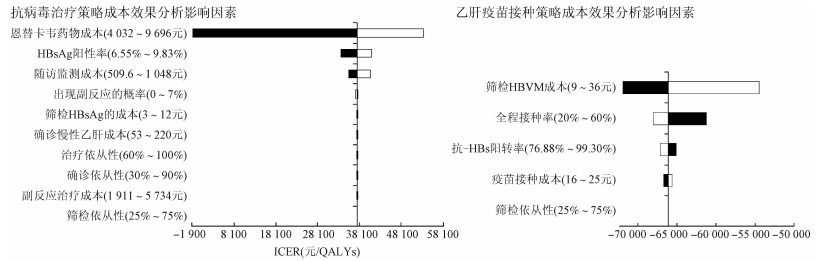
2.敏感性分析:按照设定的上下限取值,逐个改变模型中的主要参数,获得相应的ICER,与参数基线值时的ICER比较,获得影响策略经济学评价的主要因素。在20~59岁人群10个影响抗病毒治疗策略成本效果分析的参数中,恩替卡韦成本影响最为明显,成本降低可提高抗病毒治疗策略的成本效果价值,当恩替卡韦成本降低一半时,抗病毒治疗成为节省费用的策略。人群HBsAg阳性率和随访监测成本对抗病毒治疗策略也有一定影响,其他因素影响不明显。在20~59岁人群中,乙肝疫苗接种策略的主要影响因素为筛检HBVM成本和全程接种率,而抗-HBs阳转率、疫苗接种成本和筛检依从性影响较小。见图 2。
|
| 图 2 我国20~59岁人群乙肝抗病毒治疗和疫苗接种策略成本效果分析影响因素龙卷风图 |
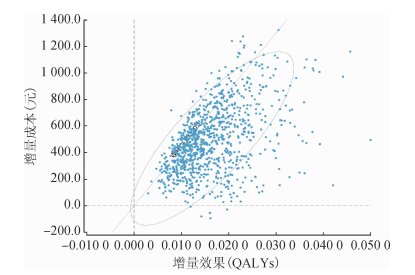
我国20~59岁人群CHB抗病毒治疗策略的概率敏感性分析结果见图 3,抗病毒治疗与不干预比较的增量效果与增量成本分别由横纵和纵轴表示,图中的每一个散点代表可能的ICER;由于95%的散点(椭圆内)位于成本效果第Ⅰ象限,说明抗病毒治疗策略获得更多的效果且均增加成本;由于参数在基线水平时计算的ICER(37 598.6)落在椭圆内,表明抗病毒治疗策略的基本经济学评价结论稳定可靠。
|
| 图 3 我国20~59岁人群乙肝抗病毒治疗策略成本效果散点图 |
我国20~59岁人群CHB抗病毒治疗策略的成本效果可接受曲线见图 4,如果没有支付意愿,抗病毒治疗策略无法实现。只有当支付意愿超过30 000元/QALYs,抗病毒治疗策略才具有成本效果意义。当支付意愿达到60 000元/QALYs时,抗病毒治疗策略具有成本效果的概率为100.0%,对比本研究成本效果阈值,提示在我国20~59岁人群中,乙肝抗病毒治疗策略的成本效果受公众支付意愿的影响不能忽视。

|
| 图 4 我国20~59岁人群乙肝抗病毒治疗策略成本效果可接受曲线 |
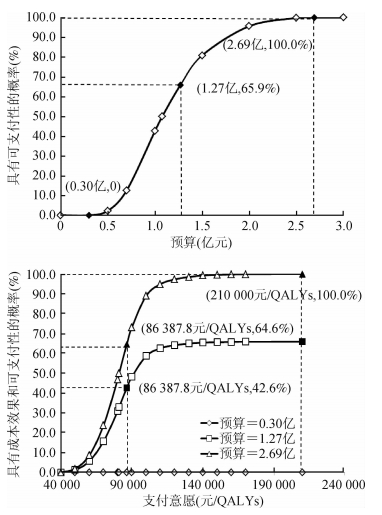
3.可支付性分析:我国20~59岁人群CHB抗病毒治疗策略成本效果可支付分析结果见图 5,以10万20~59岁队列人群计算,总预算低于0.30亿元时,抗病毒治疗策略没有可支付性。随着总投入的增加,该策略具有成本效果的概率增加;当总预算达到1.27亿元(参数取基线值)时,该策略具有成本效果的概率为65.9%;只有当总预算达到2.69亿元时,抗病毒治疗策略具有成本效果的概率才能达到100.0%,再增加支付意愿或预算,成本效果可支付性不变,可能会造成资源浪费。提示如果在10万例20~59岁人群中开展CHB抗病毒治疗,需要投入的总预算为2.69亿元。同时考虑了支付意愿和总预算对抗病毒治疗策略成本效果的影响,当总预算小于0.3亿元时,无论支付意愿如何,该策略均不能被实现。当总预算为1.27亿元时,尽管随着支付意愿增加,策略具有经济性及可支付性的概率增加,但最高只能达到42.6%。只有当总预算达到2.69亿元,本研究策略具有经济性及可支付性的概率随着支付意愿增加而升高。在同一个支付意愿下,总预算越高,乙肝抗病毒治疗策略具有经济性及可支付性的概率越高。
|
| 图 5 我国20~59岁人群CHB抗病毒治疗策略的成本效果可支付分析 |
本研究从多个角度探索了我国20~59岁人群CHB抗病毒治疗策略的经济学意义,发现该策略虽然符合成本效果原则,且低年龄组人群经济学效果更明显,但需要耗费较多的公共卫生资源。这一结论的依据:首先,与不干预比较,人群CHB抗病毒治疗策略需要增加投入,但可以收获更多的健康效果;用综合性指标ICER分析,即从每单位产出所需要的投入看,该策略虽然具有成本效果意义,但达不到最佳经济学效果。第二,不同年龄组人群CHB抗病毒治疗和乙肝疫苗接种策略成本效果分析显示,低年龄人群经济学效果更明显。第三,人群CHB抗病毒治疗策略经济学评价影响因素分析发现,各参数在一定范围变化时,基本结论稳定不变,抗病毒药物恩替卡韦的成本是最敏感的参数,当其价格降低一半后,抗病毒治疗成为最具经济学价值的策略;而且,该策略受支付意愿的影响不可忽略,与抗病毒治疗投入较高有关。最后,以10万队列人群计算,我国20~59岁人群CHB抗病毒治疗策略的总预算达到2.69亿元时才能完全实现,提示该策略需要较多公共卫生资源。对比类似成本效果分析的研究报道,发现人群CHB抗病毒治疗策略耗资较多为共同的特征。如Gray等[18]对移居加拿大的亚裔移民进行了CHB经济负担分析,发现损失生命年和承受的直接医疗费用均较高。Rossi等[20]的研究发现,对亚裔移民实施CHB抗病毒治疗策略时,虽然成本效果最优,但每获得一个QALYs需要的成本高达40 880加元。Buja等[21]在意大利移民中采用经济学模型研究发现,采用筛检后抗病毒治疗策略,每获得一个生命年需要的费用为676 709欧元。Hutton等[22]对美国管辖的亚太岛屿成年人乙肝防治策略研究发现,筛检后再治疗的ICER为36 088美元/QALYs。荷兰一项针对华裔成年人研究发现,筛检后再治疗1年的ICER为8 966欧元/QALYs[23]。这些研究结果均说明,基于社区CHB抗病毒治疗是一项耗资较多的策略。本研究完成的成本效果可接受曲线和可支付性分析,进一步明确了在我国实行基于社区CHB抗病毒治疗策略,作为传统的乙肝高流行区,与乙肝低流行水平的欧美等经济发达国家相比,将承受更为高昂的公共卫生资源总量。Nayagam等[24]注意到了中国实施基于社区CHB抗病毒治疗策略时,面临的资源总量限制问题,对8种抗病毒疗法进行经济学分析,发现恩替卡韦或替诺福韦单药疗法可以产生最大的QALYs,药物成本阈值分析发现,药价控制在每月195~460元,就能达到成本节省的最佳经济学效果,这与本研究结果基本一致。
我国20~59岁人群采取乙肝疫苗接种策略时,每获得一个QALYs可节省成本64 000.0元,而CHB抗病毒治疗策略每获得一个QALYs需要投入37 598.6元,提示前者的经济学价值明显高于后者。各年龄人群乙肝疫苗接种的CER均低于抗病毒治疗策略,表明乙肝疫苗接种策略的经济学价值高于抗病毒治疗策略。由于乙肝疫苗接种与人群CHB抗病毒治疗不是互相排斥的策略,因此,在我国20~59岁人群中实行CHB抗病毒治疗,与该人群乙肝疫苗接种同步进行,将产生更好的经济学效果。这个结果值得重视,因为乙肝疫苗接种目的是阻断HBV传播,而针对人群中CHB的抗病毒治疗,是为了降低乙肝不良转归的发生率和死亡率,这正好是WHO消除乙肝的主要目标。说明在我国为了消除乙肝,针对成年人采取措施时,应该将乙肝疫苗接种与人群抗病毒治疗同步考虑。虽然我国成年人乙肝疫苗接种指南已经出台,经济学评价结果已经明确了最优方案[23],但尚未成为公共卫生策略被实施。根据乙肝低流行区的研究结果[20, 22],消除乙肝仅考虑对高危人群进行HBV感染状况筛检和抗病毒治疗即可,而我国则需要采用明显不同的策略,即基于社区的乙肝疫苗接种与抗病毒治疗结合,这势必需要更多的公共卫生资源。
由Nayagam等[25]参与完成的WHO全球消除乙肝经济学模型公开发表,对冈比亚基于社区人群CHB筛检和抗病毒治疗策略的分析发现,ICER为511美元/QALYs,略高于该国人均GDP水平,具有成本效果意义。Lemoine等[26]在冈比亚开展了人群CHB筛查和抗病毒治疗策略可接受性研究,发现该策略的可行性良好,也印证了本文结果的可靠性。
本研究明确了我国乙肝成本效果分析中几个关键问题。一是ICER的适用条件,即当研究策略与比较策略为互斥关系时,应采用ICER。本研究基于社区CHB抗病毒治疗与不干预为互斥关系,采用了ICER为成本效果分析指标。而当研究策略与比较策略为独立关系时,如抗病毒治疗与乙肝疫苗接种相互独立,ICER不再适合而采用了CER作为评价指标[18-19]。二是成本效果阈值及其应用,即获得单位健康效果所耗费成本的最高额度应该是多少,这是对ICER和CER做出判断时的参比标准。由于我国缺乏专门的阈值研究结果,目前完成的成本效果分析均采用WHO推荐的阈值。三是成本效果象限的意义,这是成本效果分析理论和原理决定的,是概率敏感性分析的基础,也从一定程度上说明了与成本效益分析相比,为什么成本效果分析内容和方法更丰富、且应用更为广泛。四是支付意愿或经济学偏好(preference)对成本效果分析的影响,即公众或决策者在选择公共卫生策略时,由于受社会、经济、文化和伦理等影响,所持有的投资偏好对乙肝防治策略实施的影响,通过绘制成本效果可接受曲线,可以找到答案。五是可支付分析方法,即一项公共卫生策略获得的健康效果所需要的投入应在可控额度之内,同时必须让决策者明晰,该策略的总预算规模也应在在公共卫生资源的可控范围内。有关乙肝防治成本效果可接受曲线和可支付分析,读者可参阅本刊另一篇论文[17],由于该方法在国内研究报道较少,值得同行重视。
我国消除乙肝尚停留在研究的早期阶段,基于社区CHB抗病毒治疗内容尚需明确,经济学模型的参数、如慢性乙肝患者符合抗病毒治疗指证的比例等,需要权威性的调查结果和专家咨询来确定。
利益冲突: 无
| [1] | WHO. Combating hepatitis B and C to reach elimination by 2030:advocacy brief[EB/OL]. (2016-05)[2017-01-10]. http://www.who.int/hepatitis/publications/hep-elimination-by-2030-brief/en/. |
| [2] | WHO. Global health sector strategy on viral hepatitis, 2016-2021:towards ending viral hepatitis[EB/OL]. (2016-06)[2017-01-10]. http://apps.who.int/iris/bitstream/10665/246177/1/WHO-HIV-2016.06-eng.pdf?ua=1. |
| [3] | WHO. Prevention and control of viral hepatitis infection:framework for global action[EB/OL]. (2012)[2017-01-10]. http://www.who.int/hepatitis/publications/Framework/en/. |
| [4] | WHO. Guidelines for the prevention, care and treatment of persons with chronic hepatitis B infection[EB/OL]. (2015)[2017-01-10]. http://www.who.int/hepatitis/publications/hepatitis-b-guidelines/en/. |
| [5] | Ren JJ, Liu Y, Ren W, et al. Role of general practitioners in prevention and treatment of hepatitis B in China[J]. Hepatobiliary Pancreat Dis Int, 2014, 13(5): 495–500. DOI:10.1016/S1499-3872(14)60313-1 |
| [6] |
中华医学会肝病学分会, 中华医学会感染病学分会. 慢性乙型肝炎防治指南(2015更新版)[J]. 中华肝脏病杂志, 2015, 23(12): 888-905. DOI: 10.3760/cma.j.issn.1007-3418.2015.12.002.
Chinese Society of Hematology, Chinese Medical Association, Chinese Society of Infectious Diseases, Chinese Medical Association. The guideline of prevention and treatment for chronic hepatitis B:a 2015 update[J]. Chin J Hepatol, 2015, 23(12):888-905. DOI: 10.3760/cma.j.issn.1007-3418.2015.12.002. |
| [7] |
杨品超, 张顺祥, 林莹, 等.
我国乙型肝炎防治经济学评价马尔科夫模型的构建[J]. 中华流行病学杂志, 2017, 38(7): 845–852.
Yang PC, Zhang SX, Lin Y, et al. The development of Markov models for economic evaluation of strategies on hepatitis B vaccination and population-wide antiviral treatment in China[J]. Chin J Epidemiol, 2017, 38(7): 845–852. DOI:10.3760/cma.j.issn.0254-6450.2017.07.002 |
| [8] |
中国肝炎基金会. 全国肝炎诊疗现状调查报告[EB/OL]. (2015-12-18)[2017-01-10]. http://www.cfhpc.org/home/Details/2239.
China Foundation for Hepatitis Prevention and Control. Report on states of hepatitis diagnosis and trentment in China[EB/OL]. (2015-12-18)[2017-01-10]. http://www.cfhpc.org/home/Details/2239. |
| [9] |
冯铁柱, 岑枝梅.
核苷(酸)类似物治疗慢性乙型肝炎的不良反应荟萃[J]. 中华实验和临床感染病杂志:电子版, 2013, 7(1): 129–131.
Feng TZ, Cen ZM. Meta analysis on adverse reactions of nucleos(t)ide analogues as antiviral therapy for hepatitis B[J]. Chin J Exp Clin Infect Dis:Electron Ed, 2013, 7(1): 129–131. DOI:10.3877/cma.j.issn.1674-1358.2013.01.033 |
| [10] | Zhang MY, Zhu GQ, Shi KQ, et al. Systematic review with network Meta-analysis:comparative efficacy of oral nucleos(t)ide analogues for the prevention of chemotherapy-induced hepatitis B virus reactivation[J]. Oncotarget, 2016, 7(21): 30642–30658. DOI:10.18632/oncotarget.8907 |
| [11] |
肖和卫. 中国15岁以上人群乙型肝炎免疫预防的决策分析模型研究[D]. 长沙: 中南大学, 2011.
Xiao HW. Study on the decision-making model of the hepatitis B immunization among the people over 15 years old in China[D]. Changsha:Central South University, 2011. http://cdmd.cnki.com.cn/Article/CDMD-10533-1011179812.htm |
| [12] |
刘海艳.
用不同药物治疗甲亢的效果观察及经济学分析[J]. 当代医药论丛, 2014(14): 135–136.
Liu HY. Eeconomic analysis and effect observation for treatment of hyperthyroidism with different drugs[J]. Contemp Med Forum, 2014(14): 135–136. |
| [13] |
韩金芬, 何志旭, 张昌华.
特发性血小板减少性紫癜2种治疗方案比较及经济学评价[J]. 实用儿科临床杂志, 2012(3): 200–202.
Han JF, He ZX, Zhang CH. Clinical analysis and clinical economic evaluation of two treatments for children with idiopathic thrombocytopenic purpura[J]. J Appl Clin Pediatr, 2012(3): 200–202. DOI:10.3969/j.issn.1003-515X.2012.03.018 |
| [14] | Zhang S, Ma Q, Liang S, et al. Annual economic burden of hepatitis B virus-related diseases among hospitalized patients in twelve cities in China[J]. J Viral Hep, 2016, 23(3): 202–210. DOI:10.1111/jvh.12482 |
| [15] |
卫生部疾病预防控制局, 中国疾病预防控制中心. 全国人群乙型病毒性肝炎血清流行病学调查报告[M]. 北京: 人民卫生出版社, 2011.
Disease Control Bureau, Ministry of Health, China Disease Prevention and Control Center. The national report of seroepidemiologic investigation for hepatitis B in China[M]. Beijing:People's Medical Publishing House, 2011. |
| [16] | Fung J, Seto WK, Lai CL, et al. Profiles of HBV DNA in a large population of Chinese patients with chronic hepatitis B:implications for antiviral therapy[J]. J Hepatol, 2011, 54(2): 195–200. DOI:10.1016/j.jhep.2010.06.031 |
| [17] |
林莹, 张顺祥, 杨品超, 等.
中国乙肝母婴阻断策略的成本效果可支付分析[J]. 中华流行病学杂志, 2017, 38(7): 853–860.
Lin Y, Zhang SX, Yang PC, et al. Cost-effectiveness affordability on the strategy for preventing mother-to-child transmission of hepatitis B in China[J]. Chin J Epidemiol, 2017, 38(7): 853–860. DOI:10.3760/cma.j.issn.0254-6450.2017.07.003 |
| [18] | Gray A, Clarke PM, Wolstenholme JL, et al.Applied methods of cost-effectiveness analysis in health care[M]. New York: Oxford University Press, 2010: 3–30. |
| [19] |
孙利华.药物经济学[M]. 北京: 中国医药科技出版社, 2015: 68–71.
Sun LH.Pharmacoeconomics[M]. Beijing: China Medical Science Press, 2015: 68–71. |
| [20] | Rossi C, Schwartzman K, Oxlade O, et al. Hepatitis B screening and vaccination strategies for newly arrived adult Canadian immigrants and refugees:a cost-effectiveness analysis[J]. PLoS One, 2013, 8(10): e78548. DOI:10.1371/journal.pone.0078548 |
| [21] | Buja A, Martines D, Lobello S, et al. A cost-consequence analysis of hepatitis B screening in an immigrant population[J]. Ann Ist Super Sanita, 2015, 51(4): 327–335. DOI:10.4415/ANN_15_04_13 |
| [22] | Hutton DW, Tan D, So SK, et al. Cost-effectiveness of screening and vaccinating Asian and Pacific Islander adults for hepatitis B[J]. Ann Intern Med, 2007, 147(7): 460–469. DOI:10.7326/0003-4819-147-7-200710020-00004 |
| [23] | Veldhuijzen IK, Toy M, Hahné SJM, et al. Screening and early treatment of migrants for chronic hepatitis B virus infection is cost-effective[J]. Gastroenterology, 2010, 138(2): 522–530. DOI:10.1053/j.gastro.2009.10.039 |
| [24] | Nayagam S, Thursz M, Sicuri E, et al. Requirements for global elimination of hepatitis B:a modelling study[J]. Lancet Infect Dis, 2016, 16(12): 1399–1408. DOI:10.1016/S1473-3099(16)30204-3 |
| [25] | Nayagam S, Conteh L, Sicuri E, et al. Cost-effectiveness of community-based screening and treatment for chronic hepatitis B in The Gambia:an economic modelling analysis[J]. Lancet Glob Health, 2016, 4(8): e568–578. DOI:10.1016/S2214-109X(16)30101-2 |
| [26] | Lemoine M, Shimakawa Y, Njie R, et al. Acceptability and feasibility of a screen-and-treat programme for hepatitis B virus infection in The Gambia:the Prevention of Liver Fibrosis and Cancer in Africa (PROLIFICA) study[J]. Lancet Glob Health, 2016, 4(8): e559–567. DOI:10.1016/S2214-109X(16)30130-9 |
 2017, Vol. 38
2017, Vol. 38