文章信息
- 林莹, 张顺祥, 杨品超, 蔡亚丽, 邹宇华.
- Lin Ying, Zhang Shunxiang, Yang Pinchao, Cai Yali, Zou Yuhua.
- 乙型肝炎母婴阻断策略成本效果可支付性分析
- Cost-effectiveness and affordability of strategy for preventing mother-to-child transmission of hepatitis B in China
- 中华流行病学杂志, 2017, 38(7): 852-859
- Chinese journal of Epidemiology, 2017, 38(7): 852-859
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2017.07.003
-
文章历史
收稿日期: 2017-01-13
2. 510006 广州, 广东药科大学
2. Guangdong Pharmaceutical University, Guangzhou 510006, China
大力推广新生儿乙型肝炎(乙肝)疫苗接种,尽可能地使这一优先接种对象获得特异性乙肝免疫保护,从而控制人群中HBV传播,是我国20多年来采取的乙肝免疫预防策略,国际上统称为新生儿普种策略[1]。从2011年开始,我国启动了乙肝母婴阻断策略[2],即对所有孕妇先进行HBsAg筛查,阳性孕妇的新生儿出生24 h内注射100 IU乙肝免疫球蛋白(hepatitis B immune globulin,HBIG)的同时,完成第一剂10 μg乙肝疫苗接种,此后按照0-1-6方案接种第2和第3剂乙肝疫苗各10 μg;而HBsAg阴性孕妇的新生儿按照0-1-6方案完成3剂次10 μg乙肝疫苗接种。根据WHO消除乙肝倡议[3],降低乙肝母婴传播是消除人群HBV传播的关键。决策分析马尔科夫模型与成本效果分析结合,是评估乙肝免疫预防实际效果的有效方法。乙肝母婴阻断策略成本效果分析,一些国家和地区已有报道[4-5],我们也对中国乙肝母婴阻断可能选择的方案进行了成本效益分析[6],也对成本效果分析方法的适用性作了探讨[7],但我国正在实行的乙肝母婴阻断策略成本效果可支付性有待深入研究。由于我国乙肝母婴阻断为免费项目,公共财政资源必须具备可持续性,决策者既要了解该策略的成本效果价值,也需要清楚该策略的预算规模和耗资总量,即实施该策略是否存在经济压力,仅用传统的成本效果分析还不够,本研究引入成本效果可支付曲线(cost-effectiveness affordability curves)[8-9],对该策略实施效果及实施能力做出评价。
资料与方法1.经济学模型的建立:以2013年我国出生的1 640万新生儿(数据来源:2014年中国人口和就业统计年鉴)为研究对象,以乙肝母婴阻断为研究策略,不接种策略为对比策略,构建决策分析模型(decision analysis model),对孕妇HBsAg阳性率、免疫预防依从性、接种后结局等影响因素进行量化。马尔科夫模型(Markov model)部分,构建抗-HBs阳转、围产期感染和HBV易感3个马尔科夫模型,用于接受乙肝母婴阻断措施后终其一生所产生成本和效果的估算。利用TreeAge Pro 2015软件完成模型的构建和运转。见图 1。

|
| 图 1 中国现行乙肝疫苗接种策略决策分析马尔科夫模型 |
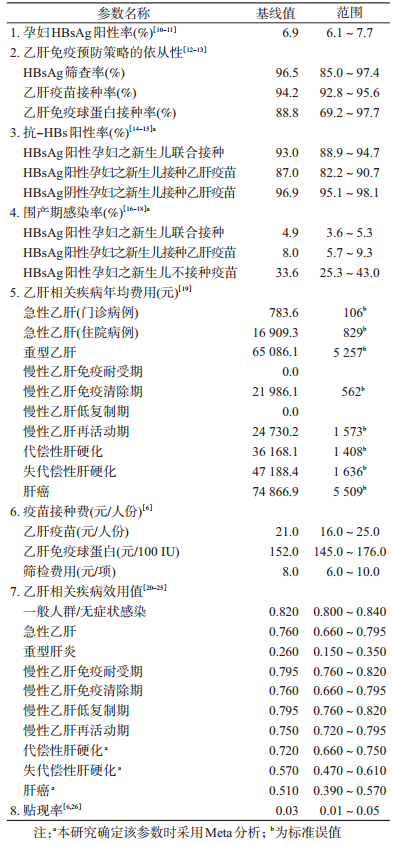
2.参数估计:模型参数确定遵循原则:选用全国性的调查结果或国家权威机构发布的数据;采用Meta分析,综合相关研究;咨询专家或参考国内外同类研究结果确定。主要参数共7类(表 1),概括为概率参数、效用值和费用参数。其中,概率参数包括孕妇HBsAg阳性率[10-11]、免疫预防接种率[12-13]、实施免疫预防后保护性抗体阳转率[14-15]、HBV围产期感染率[16-18]和乙肝相关疾病年均费用[19]。费用参数包括孕妇HBsAg的筛检费、乙肝疫苗和HBIG的接种费共3类[6]。效用值参数指乙肝相关疾病各状态的健康效用值[20-25],贴现率按照先前研究确定[6, 26]。
3.分析指标:① 成本:从全社会角度,总成本包括乙肝免疫预防直接和间接成本、因感染HBV并转归为乙肝相关疾病而接受治疗所需要支付的直接和间接成本[6]。从支付者角度,总成本仅纳入免疫预防成本,包括孕妇HBsAg筛检费、乙肝疫苗和HBIG的接种费,不接种策略不产生免疫成本。② 效果:以质量调整寿命年(QALYs)为效果指标,计算公式: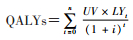
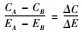
4.敏感性分析:① 一维敏感性分析:逐项改变模型中的主要参数,按照设定的上下限取值,获得相应的ICER,与参数基线值时的结果比较,绘制龙卷风图(Tornado Diagram)表示各参数对研究策略经济学评估的影响大小。② 概率敏感性分析:设定乙肝相关疾病费用服从Gamma分布,其余参数均服从三角分布,采用蒙特卡洛模拟参数随机变动并运算1 000次,得到相应ICER值。在成本效果平面图中描绘成本效果散点图,根据95%散点在成本效果平面图中所处象限位置,判断乙肝母婴阻断策略的经济学意义及其结果的可靠性。③ 成本效果可接受曲线(cost-effectiveness acceptability curve,CEAC):利用上述蒙特卡洛模拟运算结果,拟合CEAC,获得不同支付意愿下乙肝母婴阻断策略具有成本效果的概率,同时对经济性和公众支付意愿的不确定性做出评估[28]。
5.成本效果可支付性分析:为了评估研究策略所需资金总量对付诸实施的影响,本研究采取支付者角度的乙肝母婴阻断策略人均成本(支付成本)与队列人口总数相乘,获得实施该策略的年预算;因该策略为免费实施,该年预算可视为财政预算。以财政预算为横坐标,乙肝母婴阻断策略可被支付的概率为纵坐标,绘制可支付线(affordability curve),表示支付成本在最小与最大范围变化时,在相应财政预算范围内,该策略具有可支付性的概率[8]。本研究进一步对获得的CEAC与可支付线结果做出综合分析,拟合成本效果可支付曲线(cost-effectiveness affordability curves),同时分析支付意愿和财政预算变化的不同情形时,乙肝母婴阻断策略同时具有经济性和可支付性的概率变化。
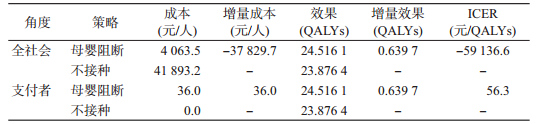
结果1.成本:根据本研究模型计算,从全社会角度看,实施乙肝母婴阻断策略时,我国2013年新生儿队列人群一生所承担的策略成本为4 063.5元/人,比不接种策略(41 893.2元/人)节省37 829.7元/人(表 2)。从支付者角度看,实施乙肝母婴阻断策略人均仅需要支付36.0元(表 2)。
2.效果:采取乙肝母婴阻断策略,全社会和支付者角度人均获得的QALYs均为24.516 1,与不接种相比,均增加0.639 7(表 2)。2013年的新生儿队列在不同乙肝免疫策略下的结局见表 3。与不接种比较,实施乙肝母婴阻断策略可减少HBV感染10 142 982例,避免有症状的急性乙肝903 720例,避免慢性乙肝2 120 692例;在避免发生的慢性乙肝中,包括肝硬化1 002 895例、肝细胞癌635 955例,合计避免乙肝相关死亡1 500 944例(表 3)。
3.成本效果分析:从全社会角度看,乙肝母婴阻断策略与不接种相比的ICER为-59 136.6元/QALYs,即每多获得一个QALYs可节省59 136.6元;根据本研究确定的成本效果阈值,提示乙肝母婴阻断策略能多获得效果并能节省成本,是具有成本效果价值的策略。从支付者角度分析(表 2),乙肝母婴阻断策略与不接种相比,ICER为56.3元/QALYs,即每获得一个QALYs需要多支付56.3元。结合本研究确定的成本效果阈值,ICER<人均GDP(4.33万元),提示乙肝母婴阻断策略具有较高成本效果价值(表 2)。
4.成本效果分析结果的可靠性:
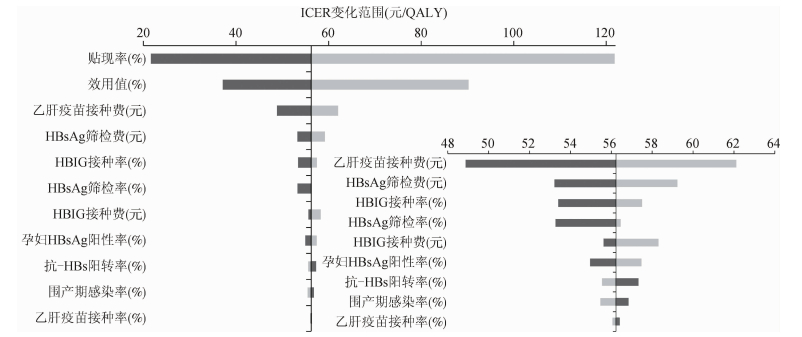
(1)从支付者角度看,一维敏感性分析结果显示,乙肝母婴阻断与不接种策略比较时,引入模型的11类参数中,贴现率、效用值对策略优化最为敏感;进一步对其他9类模型参数分析发现,乙肝疫苗接种费、HBsAg筛检费和HBIG接种率是策略优化最重要的影响参数,而乙肝疫苗接种率、抗-HBs阳转率和围产期感染率对策略优化的影响最小(图 2)。
|
| 图 2 乙肝母婴阻断与不接种策略比较的一维敏感性分析结果(支付者角度) |
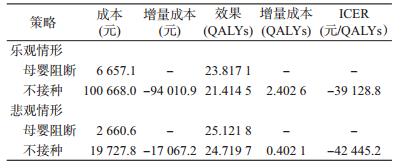
(2)从全社会角度分析,乙肝母婴阻断策略与不接种策略比较时,乐观和悲观情形下的ICER分别为-39 128.8元/QALYs和-42 445.2元/QALYs(表 4),根据成本效果阈值,两种情形与基线分析结论一致,即乙肝母婴阻断策略增加QALYs的同时节省成本,最具有成本效果价值。
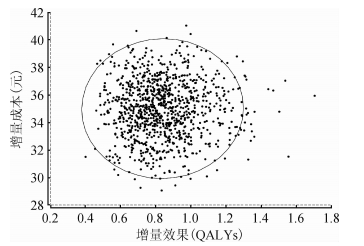
(3)乙肝母婴阻断与不接种策略比较的概率敏感性分析。从支付者角度分析,由蒙特卡洛模拟获得的1 000个ICER散点均落在第Ⅰ象限,根据本研究成本效果阈值,所有散点均小于我国当年人均GDP,提示乙肝母婴阻断策略具有较高成本效果价值。见图 3。
|
| 图 3 乙肝母婴阻断与不接种策略比较成本效果散点图(支付者角度) |
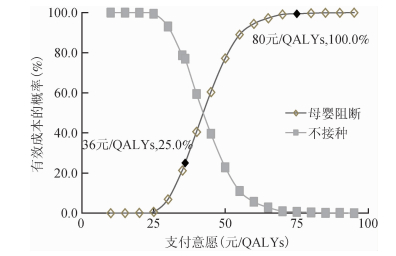
(4)乙肝母婴阻断与不接种策略比较的CEAC。随着支付意愿增加,实施乙肝母婴阻断策略获得高成本效果的概率递增,但支付意愿小于25元/QALYs时,乙肝母婴阻断策略不具有成本效果价值。支付意愿为36元/QALYs(本研究基线水平),策略具有成本效果的概率为25.0%。而支付意愿达到80元/QALYs时,该策略具有成本效果的概率达到100.0%。根据本研究成本效果阈值(人均GDP 4.33万元),我国乙肝母婴阻断策略具有经济学和可接受性。见图 4。
|
| 图 4 乙肝母婴阻断与不接种策略比较的成本效果可接受曲线(支付者角度) |
5.可支付性评价:与不接种相比,实施乙肝母婴阻断所需资金总量的潜在影响如何,由成本效果可支付线可见,年预算低于4.592亿元时,我国乙肝母婴阻断策略不具有可支付性,即该策略将无法实现(图 5)。随着年预算的增加,该策略具有可支付性的概率增大;当年预算为5.904亿元时(基线水平),策略具有可支付性的概率为68.0%。只有当年预算达到6.888亿元时,该策略可支付性的概率才能达到100.0%,之后再增加预算可支付性保持不变,即继续增加预算会造成资源浪费(图 6)。

|
| 图 5 乙肝母婴阻断与不接种策略比较的可支付曲线 |

|
| 图 6 乙肝母婴阻断与不接种策略比较的成本效果可支付曲线 |
本研究结果显示,我国实行的乙肝母婴阻断策略可节省成本,获得更多的健康效果。如果从全社会角度分析,即同时计算免疫预防成本和HBV感染风险成本,则接受乙肝母婴阻断的对象,终其一生所承担的人均成本为4 063.5元,与不接种相比,节省37 829.7元。按照2013年中国出生的1 640万新生儿计算,与不接种相比,HBV感染人数减少101.43万,其中减少慢性肝炎21.21万,减少乙肝相关死亡15.01万。实施乙肝母婴阻断策略,人均获得QALYs为24.516 1,与不接种相比,人均多获QALYs为0.639 7。
从成本效果分析结果,可以进一步明确上述结论。与不接种比较,乙肝母婴阻断策略的ICER分别为-59 136.6/QALYs,即每获得一个QALYs分别可节省59 136.6元,根据本研究成本效果阈值,提示中国实行乙肝母婴阻断是最具成本效果价值的策略。即使从支付者角度分析,乙肝母婴阻断策略与不接种比较时,ICER为56.3元/QALYs,仍然说明该策略具有较高成本效果价值。为了明确上述结论的可靠性,本研究采用一维、多情景和多维敏感性分析方法,不仅明确了本研究经济学模型中各个参数的影响大小,也发现上述结论稳定可靠,无论乐观或悲观情形下,无论参数在较大范围内如何改变,乙肝母婴阻断策略具有成本效果价值的结论不变。将稀缺的公共卫生资源投入到乙肝母婴阻断项目,这样的成本效果分析结果提供了最有力的证据,值得持续投入。WHO新近发布的全球消除乙肝倡议中,阻断HBV传播成为最重要的目标,而阻断乙肝母婴传播是阻断HBV传播最主要的方法之一[3]。因此,我国实行乙肝母婴阻断,不仅具有良好的经济学价值,也符合全球消除乙肝的要求。
本研究是将成本效果可支付分析用于乙肝免疫预防策略的探索。首先,成本效果分析回答的基本问题,就是乙肝母婴阻断策略是否具有经济学价值,通过ICER指标的计算,与成本效果阈值比较,就可以做出判断;项目具有经济学意义是公共财政投入的前提。其次,在概率敏感性分析的同时,除对经济学模型中主要参数的不确定性作出评价外,通过引入CEAC,明确支付意愿的影响。支付意愿是一个投资偏好的问题,作为福利性的公共卫生项目,乙肝母婴阻断的投资意愿如何,反映了公众对乙肝疫苗的认识水平,受社会、伦理和文化的影响。乙肝母婴阻断策略的实施,涉及对所有孕妇的HBsAg筛检和新生儿区别接种,在乙肝歧视现象尚存的环境下,有伦理学问题需要处理。因此,认识了公众支付意愿对乙肝母婴阻断策略实施的影响后,可有针对性地加强宣传,提高公众的接受程度。最后,公共卫生项目不仅要符合成本效益价值,项目的预算规模直接关系到能否实现财政支付,因为财政支付能力有限,不可能对所有符合经济学的项目都予以采纳,预算规模较小的项目更容易被接受;这就是成本效果可支付分析能够回答的问题[8-9, 29]。本研究结果表明,与不接种相比,年预算达到6.888亿元时,乙肝母婴阻断策略可支付性的概率就能完全实现,从我国现有的社会经济水平,并不会超出国家财政的支付能力。这一结论对我国政府持续地将资金投放到乙肝母婴阻断策略提供了有力的证据。
我国尚缺乏全国性的乙肝相关疾病健康效用值调查结果,这对本研究成本效果分析结果带来影响。本研究采用Meta分析,综合了不同地区的研究结果,重点考虑了包括中国在内的多国研究结果,作为本研究乙肝相关疾病健康效用值[20-25]。值得指出,全国6省12城市乙肝相关疾病经济负担调查,为乙肝免疫预防经济学分析提供了权威性成本计算参数[19],有必要开展全国性的乙肝相关疾病健康效用值调查,解决成本效果分析中效果的计算问题。我国成本效果分析阈值尚未确定,本研究采用WHO推荐的阈值标准。虽然我国也有学者研究认为,WHO的阈值符合我国实际,但鉴于该阈值不适合效果为QALYs的研究,因此我国急需适合自身国情的成本效果阈值标准。
利益冲突: 无
| [1] | Liao XY, Liang ZL. Strategy vaccination against Hepatitis B in China[J]. Hum Vaccin Immunother, 2015, 11(6): 1534–1539. DOI:10.4161/21645515.2014.980206 |
| [2] | Wang AL, Qiao YP, Wang LH, et al. Integrated prevention of mother-to-child transmission for human immunodeficiency virus, syphilis and hepatitis B virus in China[J]. Bull World Health Organ, 2015, 93(1): 52–56. DOI:10.2471/BLT.14.139626 |
| [3] | WHO. Combating hepatitis B and C to reach elimination by 2030:advocacy brief[EB/OL].(2016-05)[2017-01-10]. http://www.who.int/hepatitis/publications/hep-elimination-by-2030-brief/en/. |
| [4] | Barbosa C, Smith EA, Hoerger TJ, et al. Cost-effectiveness analysis of the national Perinatal Hepatitis B Prevention Program[J]. Pediatrics, 2014, 133(2): 243–253. DOI:10.1542/peds.2013-0718 |
| [5] | Chen SCC, Toy M, Yeh JM, et al. Cost-effectiveness of augmenting universal hepatitis B vaccination with immunoglobin treatment[J]. Pediatrics, 2013, 131(4): e1135–1143. DOI:10.1542/peds.2012-1262 |
| [6] |
石果, 张顺祥.
乙型肝炎病毒母婴传播阻断策略的决策分析及成本效益评价[J]. 中华流行病学杂志, 2013, 34(3): 273–278.
Shi G, Zhang SX. Decision tree and cost-benefit analysis on strategies related to preventing maternal-infantile transmission of hepatitis B virus infection[J]. Chin J Epidemiol, 2013, 34(3): 273–278. DOI:10.3760/cma.j.issn.0254-6450.2013.03.016 |
| [7] |
蔡亚丽, 张顺祥, 杨品超, 等.
乙型肝炎母婴阻断策略的成本效益和成本效果分析[J]. 中华流行病学杂志, 2016, 37(6): 846–851.
Cai YL, Zhang SX, Yang PC, et al. Cost-effectiveness and cost-benefit analysis on strategy for preventing mother-to-child transmission of hepatitis B virus[J]. Chin J Epidemiol, 2016, 37(6): 846–851. DOI:10.3760/cma.j.issn.0254-6450.2016.06.021 |
| [8] | Sendi PP, Briggs AH. Affordability and cost-effectiveness:decision-making on the cost-effectiveness plane[J]. Health Econ, 2001, 10(7): 675–680. DOI:10.1002/hec.639 |
| [9] | Kim SY, Salomon JA, Goldie SJ. Economic evaluation of hepatitis B vaccination in low-income countries:Using cost-effectiveness affordability curves[J]. Bull World Health Organ, 2007, 85(11): 833–842. |
| [10] |
林莹, 杨品超, 张顺祥, 等.
孕妇乙肝表面抗原流行率的Meta分析[J]. 医师在线, 2016, 2(1): 16–21.
Lin Y, Yang PC, Zhang SX, et al. Meta-analysis on the prevalence of hepatitis B surface antigen among pregnant women[J]. Doctors Online, 2016, 2(1): 16–21. |
| [11] |
石果, 张顺祥.
我国孕妇乙肝表面抗原阳性率的Meta分析[J]. 中国预防医学杂志, 2013, 14(1): 26–30.
Shi G, Zhang SX. Meta-analysis on the positive rate of hepatitis B surface antigen among pregnant women in China[J]. Chin Prev Med, 2013, 14(1): 26–30. |
| [12] | Cui FQ, Luo HM, Wang FZ, et al. Evaluation of policies and practices to prevent mother to child transmission of hepatitis B virus in China:results from China GAVI project final evaluation[J]. Vaccine, 2013, 31(Suppl 9): J36–42. DOI:10.1016/j.vaccine.2012.11.061 |
| [13] |
王富珍, 郑徽, 张国民, 等.
8个省(自治区)乙型肝炎病毒表面抗原阳性产妇筛查及新生儿免疫预防措施的调查[J]. 中国疫苗和免疫, 2014, 20(6): 523–528.
Wang FZ, Zheng H, Zhang GM, et al. Survey on hepatitis B virus surface antigen screening among pregnant women and prevention measures for newborns in 8 provinces or autonomous regions, China[J]. Chin J Vaccin Immun, 2014, 20(6): 523–528. |
| [14] | Kang WY, Ding ZR, Shen LP, et al. Risk factors associated with immunoprophylaxis failure against mother to child transmission of hepatitis B virus and hepatitis B vaccination status in Yunnan province, China[J]. Vaccine, 2014, 32(27): 3362–3366. DOI:10.1016/j.vaccine.2014.04.045 |
| [15] | Zhang L, Gui XE, Teter C, et al. Effects of hepatitis B immunization on prevention of mother-to-infant transmission of hepatitis B virus and on the immune response of infants towards hepatitis B vaccine[J]. Vaccine, 2014, 32(46): 6091–6097. DOI:10.1016/j.vaccine.2014.08.078 |
| [16] | Lin XF, Guo Y, Zhou AF, et al. Immunoprophylaxis failure against vertical transmission of hepatitis B virus in the Chinese population:a hospital-based study and a Meta-analysis[J]. Pediatr Infect Dis J, 2014, 33(9): 897–903. DOI:10.1097/INF.0000000000000315 |
| [17] | Beasley RP, Trepo C, Stevens CE, et al. The e antigen and vertical transmission of hepatitis B surface antigen[J]. Am J Epidemiol, 1977, 105(2): 94–98. DOI:10.1093/oxfordjournals.aje.a112370 |
| [18] | Stevens CE, Beasley RP, Tsui J, et al. Vertical transmission of hepatitis B antigen in Taiwan[J]. N Engl J Med, 1975, 292(15): 771–774. DOI:10.1056/NEJM197504102921503 |
| [19] | Zhang S, Ma Q, Liang S, et al. Annual economic burden of hepatitis B virus-related diseases among hospitalized patients in twelve cities in China[J]. J Viral Hep, 2016, 23(3): 202–210. DOI:10.1111/jvh.12482 |
| [20] | Levy AR, Kowdley KV, Iloeje U, et al. The impact of chronic hepatitis B on quality of life:a multinational study of utilities from infected and uninfected persons[J]. Value Health, 2008, 11(3): 527–538. DOI:10.1111/j.1524-4733.2007.00297.x |
| [21] | Jia YX, Cui FQ, Li L, et al. Comparison between the EQ-5D-5L and the EQ-5D-3L in patients with hepatitis B[J]. Qual Life Res, 2014, 23(8): 2355–2363. DOI:10.1007/s11136-014-0670-3 |
| [22] | Lu SQ, McGhee SM, Xie X, et al. Economic evaluation of universal newborn hepatitis B vaccination in China[J]. Vaccine, 2013, 31(14): 1864–1869. DOI:10.1016/j.vaccine.2013.01.020 |
| [23] | Che YH, You J, Chongsuvivatwong V, et al. Dynamics and liver disease specific aspects of quality of life among patients with chronic liver disease in Yunnan, China[J]. Asian Pac J Cancer Prev, 2014, 15(12): 4765–4771. DOI:10.7314/APJCP.2014.15.12.4765 |
| [24] | Lam ETP, Lam CLK, Lai CL, et al. Health-related quality of life of southern Chinese with chronic hepatitis B infection[J]. Health Qual Life Outcomes, 2009, 7: 52. DOI:10.1186/1477-7525-52 |
| [25] | Zhuang GH, Zhang M, Liu Y, et al. Significant impairment of health-related quality of life in mainland Chinese patients with chronic hepatitis B:a cross-sectional survey with pair-matched healthy controls[J]. Health Qual Life Outcomes, 2014, 12: 101. DOI:10.1186/1477-7525-12-101 |
| [26] | Yin J, Ji ZH, Liang PF, et al. The doses of 10μg should replace the doses of 5μg in newborn hepatitis B vaccination in China:a cost-effectiveness analysis[J]. Vaccine, 2015, 33(31): 3731–3738. DOI:10.1016/j.vaccine.2015.05.082 |
| [27] | Guilbert JJ. The world health report 2002-reducing risks, promoting healthy life[J]. Educ Health, 2003, 16(2): 230. DOI:10.1080/1357628031000116808 |
| [28] | Gray A, Clarke PM, Wolstenholme JL, et al.Applied methods of cost-effectiveness analysis in health care[M]. New York: Oxford University Press, 2010: 3–30. |
| [29] | Tu HAT, de Vries R, Woerdenbag HJ, et al. Cost-effectiveness analysis of hepatitis B immunization in Vietnam:application of cost-effectiveness affordability curves in health care decision making[J]. Value Health Regional Issues, 2012, 1(1): 7–14. DOI:10.1016/j.vhri.2012.03.007 |
 2017, Vol. 38
2017, Vol. 38