文章信息
- 郭玉双, 王嘉琪, 徐超, 刘雅宁, 贺晓慧, 魏强.
- Guo Yushuang, Wang Jiaqi, Xu Chao, Liu Yaning, He Xiaohui, Wei Qiang.
- 中国脊髓灰质炎网络实验室人员免疫接种状况及其影响因素分析
- Study on the immunization status and its influencing factors among workers from the polio network laboratories in China
- 中华流行病学杂志, 2017, 38(6): 737-739
- Chinese Journal of Epidemiology, 2017, 38(6): 737-739
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2017.06.009
-
文章历史
收稿日期: 2017-02-13
2. 100028北京市朝阳区太阳宫社区卫生服务中心;
3. 100124 北京市朝阳区社区卫生服务管理中心;
4. 100044 北京, 国家卫生和计划生育委员会医药卫生科技发展研究中心
2. Beijing Chaoyang District Taiyanggong Community Health Service Center, Beijing 100028, China;
3. Beijing Chaoyang District Community Health Service Management Center, Beijing 100124, China;
4. Development Center for Medical Science and Technology National Health and Family Planning Commission of People's Republic of China, Beijing 100044, China
脊髓灰质炎(脊灰)是目前全球第二个正在消灭的传染性疾病,目前其病例数已降至历史最低水平,全球流行脊灰野病毒的国家已从至少125个减至3个[1]。在消灭脊灰进程中,与弛缓性麻痹病例检测样本(可能含有脊灰病毒感染性材料)密切接触的实验室人员是必须关注的职业人群。对脊灰病毒实验室人员实施免疫预防策略,控制实验室工作人员可能出现的感染甚至传播,是消灭脊灰进程中及其之后不可或缺的重要环节。本文通过调查中国省级CDC脊灰网络实验室人员免疫状况,并分析其影响因素,为国家制定完善脊灰网络实验室人员相关免疫策略提供参考。
对象与方法1.样本资料:选取全国31个省、自治区、直辖市和新疆生产建设兵团CDC等32个省级脊灰网络实验室全部人员为调查对象。
2.调查方法:采用问卷调查了解调查对象人口学特征(年龄、性别、职称、学历、工作时间等)和免疫状况(基础免疫、工作后免疫以及不同频率接触弛缓性麻痹病例检测样本等人员的免疫状况)。
3.统计学分析:使用Excel软件录入数据,利用SAS软件进行分析。采用趋势χ2检验和确切概率法对免疫接种影响因素进行分析,以P<0.05为差异有统计学意义。
结果1.样本特征:共调查32个省级CDC脊灰网络实验室人员77人。其中男性28人(36.4%),女性49人(63.6%);20~岁年龄组16人(20.8%),30~岁组33人(42.8%),40~岁组19人(24.7%),≥50岁组9人(11.7%);初级职称者17人(22.0%),中级职称者30人(39.0%),副高职称者17人(22.1%),正高及以上职称者13人(16.9%);大专及以下学历10人(13.0%),本科及以上67人(87.0%)。
2.免疫接种状况:77人中完成脊灰疫苗基础免疫60人(77.9%),免疫状况不详17人(22.1%);参加实验室工作后完成疫苗接种者66人(85.7%),接种信息不完整11人(14.3%);在工作后明确完成疫苗接种的66人中,接种1剂次者21人(31.8%),2剂次者18人(27.3%),≥3剂次者27人(40.9%)。在每天和每周3~5次高频率接触含弛缓性麻痹病例检测样本的45名实验室人员中,有6人疫苗接种信息不完整,占高频率接触人数的13.3%,占11名接种信息不完整人数的54.5%。
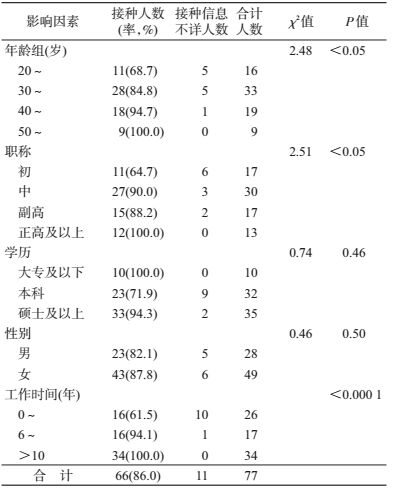
3.免疫接种影响因素:经统计学分析,影响免疫接种的因素包括年龄(χ2=2.48,P<0.05)、职称(χ2=2.51,P<0.05)、工作时间(P<0.000 1)、学历(χ2=0.74,P=0.46)、性别(χ2=0.46,P=0.50)。提示年龄、职称和工作时间与疫苗接种有统计学意义,其中年龄和职称与工作时间存在明显相关性,而工作时间是免疫接种情况的可能影响因素(表 1)。
目前我国脊灰网络实验室设置在各省级CDC,承担脊灰病毒细胞培养、病毒分离、中和定型及型内鉴定工作,其中包括对急性弛缓性麻痹病例、接触者、流动人口、健康人群及环境中样本的检测分析[2]。由于脊灰疫苗诱导抗体的浓度随着时间的推移而降低,甚至可能降低至检测阈值以下[3],而使密切接触的实验室人员具有感染的风险[4-6]。因此,遵循实验室生物安全管理规定,并适时进行预防接种是预防实验室脊灰野病毒获得性感染的重要手段[7-10]。
为预防控制脊灰实验室人员感染,美国CDC于2000年提出了关于实验室人员的脊灰免疫策略[11-12],推荐从事脊灰病毒研究的实验室人员按照“0-1-6”个月免疫程序接种3剂次脊灰灭活疫苗,即在任何时候开始接种第一剂次,间隔1~2个月接种第二剂次,与第一剂次间隔6~12个月接种第三剂次。我国病原微生物实验室生物安全管理条例中规定,从事高致病性病原微生物相关实验活动的实验室,应对实验室人员进行健康监测,必要时,对实验室人员预防接种,但未对接种的具体时间、种类、剂次等免疫规程做出具体要求。
本次调查显示,我国脊灰网络实验室人员免疫情况较好,已基本完成脊灰疫苗基础免疫和工作后免疫,接种疫苗种类以三价脊灰减毒活疫苗为主,且完成≥3剂次者占完成接种人员的41.0%,仅部分人员基础免疫情况不详及工作后接种情况记录不完整,主要集中在<40岁、中级职称以下、工作时间<5年的人员中。有资料表明,检测阈值以上的抗体水平与预防麻痹型脊灰的保护力有显著正相关[13]。
由于我国周边国家(巴基斯坦、阿富汗)存在输入脊灰野病毒疫情的风险[14],脊灰网络实验室人员在日常工作中仍有接触含有脊灰病毒感染材料的可能,因此借鉴国外相关免疫策略,在我国实验室生物安全管理现有措施基础上,应结合我国实际,制定完整规范的脊灰实验室工作人员免疫策略[15]。
利益冲突: 无
| [1] |
董少忠, 朱文兵.
Sabin株脊髓灰质炎灭活疫苗在全球消灭脊髓灰质炎最后阶段的作用[J]. 中华预防医学杂志, 2016, 50(12): 1032–1035.
Dong SZ, Zhu WB. The role of Sabin inactivated poliovirus vaccine in the final phase of global polio eradication[J]. Chin J Prev Med, 2016, 50(12): 1032–1035. DOI:10.3760/cma.j.issn.0253-9624.2016.12.003 |
| [2] |
王东艳, 张勇, 安洪秋, 等.
中国脊髓灰质炎实验室网络2007-2015年细胞敏感性监测与评价[J]. 中国疫苗与免疫, 2016, 22(2): 138–142.
Wang DY, Zhang Y, An HQ, et al. Monitoring and evaluation of the cell sensitivity in Chinese poliomyelitis laboratory network from 2007 to 2015[J]. Chin J Vacc Immun, 2016, 22(2): 138–142. |
| [3] |
世界卫生组织关于脊髓灰质炎疫苗的意见书[J].王真行, 邹力, 译.国际生物制品学杂志, 2016, 39(4):254-260. DOI:10.3760/cma.j.issn.1673-4211.2014.05.013.
WHO polio vaccines:WHO position papers[J]. Wang ZX, Zou L trans. Intern J Biolog, 2016, 39(4):254-260. DOI:10.3760/cma.j.issn.1673-4211.2014.05.013. |
| [4] | Buesching WJ, Neff JC, Sharma HM. Infectious hazards in the clinical laboratory:a program to protect laboratory personnel[J]. Clin Lab Med, 1989, 9(2): 351–361. |
| [5] | Sewell DL. Laboratory-associated infections and biosafety[J]. Clin Microbiol Rev, 1995, 8(3): 389–405. |
| [6] | Turnberg WL.Biohazardous waste:risk assessment, policy, and management[M]. New York: Wiley-Interscience, 1996. |
| [7] | Department of Health and Human Services. Biosafety in microbiological and biomedical laboratories[R]. 4th ed. Rockville, MD:Department of Health and Human Services, 1999. |
| [8] | Fleming DO, Hunt DL.Biological safety:principles and practices[M]. 3rd ed. Washington, DC: ASM Press, 2000. |
| [9] | Rusnak JM, Kortepeter MG, Hawley RJ, et al. Risk of occupationally acquired illnesses from biological threat agents in unvaccinated laboratory workers[J]. Bios Bioterr, 2004, 2(4): 281–293. DOI:10.1089/bsp.2004.2.281 |
| [10] | Clinical Laboratory Standards Institute. Clinical laboratory safety:approved guideline[R]. 2nd ed. NCCLS Document GP17-A2. Wayne PA:National Committee for Clinical Laboratory Standards, 2004. |
| [11] | Shimizu H, Yoshida H, Miyamura T. WHO global action plan for laboratory containment of wild polioviruses (2nd ed)[J]. Uirusu, 2005, 55(1): 161–178. DOI:10.2222/jsv.55.161 |
| [12] | Prevots DR, Burr RK, Sutter RW, et al. Poliomyelitis prevention in the United States:Updated Recommendations of the Advisory Committee on Immunization Practices (ACIP)[J]. MMWR, 2000, 49(RR-5): 12–15. DOI:10.1037/e548082006-001 |
| [13] | The World Health Organization about polio vaccine position papers (February 2014)[J]. Ning GJ trans[J]. Chin J Vacc Immun, 2014, 20(4): 376–380. |
| [14] |
余文周, 温宁, 汪海波, 等.
我国现阶段维持无脊髓灰质炎状态面临的挑战和对策[J]. 中国疫苗和免疫, 2013, 19(5): 468–471.
Yu WZ, Wen N, Wang HB, et al. Challenges and strategies on maintaining polio-free status in current period in China[J]. Chin J Vacc Immun, 2013, 19(5): 468–471. |
| [15] |
郭玉双, 魏强.
脊髓灰质炎病毒实验室工作人员免疫策略现状与展望[J]. 中国疫苗和免疫, 2016, 22(4): 473–475.
Guo YS, Wei Q. Status and prospect of immunization strategies among poliovirus laboratory staff[J]. Chin J Vacc Immun, 2016, 22(4): 473–475. |
 2017, Vol. 38
2017, Vol. 38