文章信息
- 徐嘉悦, 牟雨婵, 马原林, 张菊英.
- Xu Jiayue, Mou Yuchan, Ma Yuanlin, Zhang Juying.
- 成都市男男性行为人群艾滋病暴露前预防用药服药依从性分析
- Compliancy of pre-exposure prophylaxis for HIV infection in men who have sex with men in Chengdu
- 中华流行病学杂志, 2017, 38(5): 643-645
- Chinese Journal of Epidemiology, 2017, 38(5): 643-645
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2017.05.017
-
文章历史
收稿日期: 2016-10-24
据WHO估计,2015年底全球HIV新发感染者210多万例[1],MSM是艾滋病新发感染率最高的人群[2],中国的MSM感染情况不容乐观,新发感染从2007年的12.2%增至2011年的29.4%[3],总体感染率也从2012年6.7%,逐年上升至2015年8%[4],男男性行为已成为艾滋病传播的重要途径之一。艾滋病暴露前预防用药(pre-exposure prophylaxis,PrEP)被认为是目前具有应用前景的艾滋病预防策略,即服用抗病毒药物以降低易感人群经性传播感染HIV的风险。在泰国、法国和英国等进行的临床试验证明了PrEP的有效性和安全性,也指出药物的有效性很大程度上受研究对象依从性的影响[5-7]。在法国[6]和英国[7]进行的临床试验中,受试者依从性达到了100%,药物的有效性超过了90%;而在南非[8]和肯尼亚[9]的临床试验中,受试者依从性<40%,这两项试验均宣布无效。本研究利用在成都市开展的MSM人群PrEP临床试验数据,探讨该地MSM人群PrEP的依从性及影响因素,为PrEP在我国MSM人群中的推广提供参考依据。
对象与方法1.研究对象:采用非概率抽样法在成都市招募研究对象,纳入标准:① 签署知情同意书;② 年龄18~65岁;③ HIV阴性;④ 平均每2周≥1次性生活;⑤ 试验前1个月至少有1个及以上的同性伴侣;⑥ 愿意在指导下使用研究用药并服从随访安排;⑦ 愿意参加试验达96周。
2.研究方法:本研究设计为随机、平行对照临床干预研究,估算样本量为360人,将符合标准的受试者纳入研究队列,随机分为3组:① 时间组:每天口服替诺福韦(TDF)300 mg;② 事件组:在性行为前24~48 h口服一次TDF 300 mg,在性行为后加服一次TDF 300 mg,24 h内服药量不超过300 mg;③ 空白对照组:不服用任何药物。入组后每12周进行一次面对面随访,随访内容包括问卷填写、实验室检查和体格检查,同时向研究对象发放TDF。随访结束后,对收集的资料进行PrEP的服药依从性分析。随访地点为四川大学华西医学院附属第四医院。研究周期为2013年7月1日至2015年9月30日。
3.相关定义:PrEP依从性指有服药行为的研究对象自报按照方案服药的情况。(随访期间实际服药量/随访期间应服药量)×100%≥80%认为依从性好,否则认为依从性差。仅针对时间组和事件组(空白组和部分脱失者无服药信息),如果随访记录≥1次,进行服药依从性分析。
4.统计学分析:所有数据采用EpiData 3.1软件进行双录入,SAS 9.2软件数据整理及分析。社会人口学特征等变量的组间差异采用χ2检验。对PrEP的服药依从性进行统计描述,并对依从性影响因素进行单因素和多因素logistic回归分析,结合OR值(95%CI),P<0.10判断具有统计学意义。
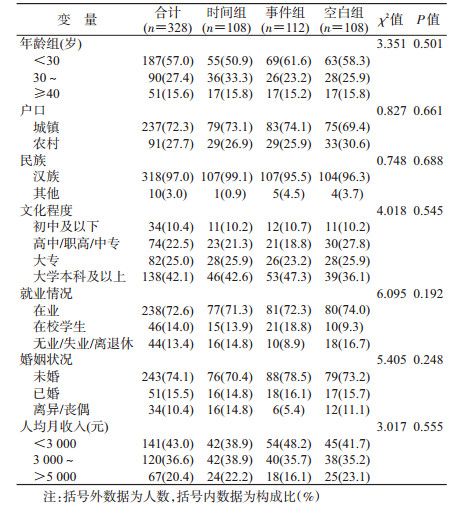
结果1.社会人口学特征:最终入组328人(时间组108人,事件组112人,空白组108人)。<30岁占57.0%,城镇户口占72.3%,汉族占97.0%,大学本科及以上文化程度占42.1%,未婚者占74.1%。人口学特征在时间组、事件组、空白组3组间的差异无统计学意义(χ2检验P>0.05),具有可比性。见表 1。
2. PrEP服药依从性及影响因素分析:141例研究对象(时间组71人,事件组70人)中依从性好的占41.8%(59/141),其中时间组的依从性好的占69.0%(49/71),事件组依从性好的占14.3%(10/70)。
将PrEP服药依从性设置为因变量(依从性好赋值=1,依从性差赋值=0),将PrEP服药依从性的可能影响因素作为自变量,进行单因素logistic回归分析,将单因素分析P≤0.2的自变量,以及用药方式等有专业意义的自变量纳入多因素logistic分析,采用逐步回归法,自变量的纳入标准=0.10,剔除标准=0.15。结果显示,用药方式和最近1个月男性性伴数是PrEP服药依从性的影响因素,与时间组比较,事件组的PrEP服药依从性较差(OR=0.07,95%CI:0.03~0.16);与最近1个月男性性伴数=1者比较,最近1个月男性性伴数≥2者的PrEP服药依从性较差(OR=0.44,95%CI:0.18~1.08)。见表 2。
目前,国际上比较确定的对PrEP服药的依从性有影响的因素包括MSM服药方式、对自身HIV感染的危险感知、婚姻状况等社会人口学特征[10]。本研究将以上因素纳入模型分析,结果显示,最近1个月男性性伴数和用药方式对服药的依从性有影响。最近1个月男性性伴数一定程度上可以反映近期MSM同性伴侣关系的稳定情况,可能伴侣较为稳定的MSM受到更多的社会支持,因此服药依从性较好。服药方式的影响可能因为时间组每日服药容易形成习惯,事件组要在性行为前后服药,形成间歇性的服药习惯更为困难。后续干预研究可通过电子盒监测、闹钟提醒或者其他方法来提高MSM的服药依从性。
每日服药组和高危行为前后服药组的整体服药依从性都不高,除了上述原因之外,由于PrEP的随机对照试验是在HIV阴性的MSM人群中开展,研究对象会综合考虑未感染HIV的情况下,服药对他们带来的风险和收益,包括舆论压力,如果被周围人发现服用PrEP,很有可能受到周围人的歧视或排斥,Gengiah等[11]研究也有相似研究结果。另外,部分研究对象会认为未感染HIV情况下,服药会对身体造成损伤,因此需要向研究对象充分解释PrEP给他们带来的益处。Marrazzo等[9]对研究对象的定性研究发现,参与者要先评估项目对他们的益处,与服药带来的不良反应等进行权衡,所以了解到参与者参加项目的动机,对提高服药的依从性有很大的帮助。
本研究有局限性,如样本量较小,失访率较高,样本的代表性不够;另外,通常自报的服药情况均好于实际服药情况,也可能带来报告偏倚。
利益冲突: 无
| [1] | World Health Organization. HIV department. Number of people newly infected with HIV over time[EB/OL]. (2011-11-01)[2017-03]. http://www.who.int/hiv/data/incidence_targets.PNG?ua=1. |
| [2] | van Griensven F, de Lind van Wijngaarden JW, Baral S, et al. The global epidemic of HIV infection among men who have sex with men[J]. Curr Opin HIV AIDS, 2009, 4(4): 300–307. DOI:10.1097/COH.0b013e32832c3bb3 |
| [3] |
中华人民共和国卫生部, 联合国艾滋病规划署, 世界卫生组织. 2011年中国艾滋病疫情估计报告[EB/OL]. (2011-11-01)[2017-03-01]. http://www.moh.gov.cn/cmsresources/mohyzs/cmsrsdocument/doc13944.pdf.
Ministry of Health of the People's Republic of China, The Joint United Nations Programme on HIV/AIDS, World Health Organization. Evaluation of AIDS epidemic in China in 2011[EB/OL].(2011-11-01)[2017-03-01]. http://www.moh.gov.cn/cmsresources/mohyzs/cmsrsdocument/doc13944.pdf. |
| [4] | The Joint United Nations Programme on HIV/AIDS. AIDSinfo. HIV prevalence in men who have sex with men[EB/OL].[2017-03]. http://aidsinfo.unaids.org/. |
| [5] | Choopanya K, Martin M, Suntharasamai P, et al. Antiretroviral prophylaxis for HIV infection in injecting drug users in Bangkok, Thailand (the Bangkok Tenofovir Study):a randomised, double-blind, placebo-controlled phase 3 trial[J]. Lancet, 2013, 381(9883): 2083–2090. DOI:10.1016/S0140-6736(13)61127-7 |
| [6] | Molina JM, Capitant C, Spire B, et al. On demand PrEP with oral TDF/FTC in MSM:results of the ANRS Ipergay trial[C]//Program and abstracts of the 2015 Conference on Retroviruses and Opportunistic Infections. Seattle, Washington:CROI. |
| [7] | McCormack S, Dunn DT, Desai M, et al. Pre-exposure prophylaxis to prevent the acquisition of HIV-1 infection (PROUD):effectiveness results from the pilot phase of a pragmatic open-label randomised trial[J]. Lancet, 2016, 387(10013): 53–60. DOI:10.1016/S0140-6736(15)00056-2 |
| [8] | van Damme L, Corneli A, Ahmed K, et al. Preexposure prophylaxis for HIV infection among African women[J]. N Engl J Med, 2012, 367(5): 411–422. DOI:10.1056/NEJMoa1202614 |
| [9] | Marrazzo JM, Ramjee G, Richardson BA, et al. Tenofovir-based preexposure prophylaxis for HIV infection among African women[J]. N Engl J Med, 2015, 372(6): 509–518. DOI:10.1056/NEJMoa1402269 |
| [10] | Corneli A, Wang M, Agot K, et al. Perception of HIV risk and adherence to a daily, investigational pill for HIV prevention in FEM-PrEP[J]. J Acquir Immune Defic Syndr, 2014, 67(5): 555–563. DOI:10.1097/QAI.0000000000000362 |
| [11] | Gengiah TN, Moosa A, Naidoo A, et al. Adherence challenges with drugs for pre-exposure prophylaxis to prevent HIV infection[J]. Int J Clin Pharm, 2014, 36(1): 70–85. DOI:10.1007/s11096-013-9861-1 |
 2017, Vol. 38
2017, Vol. 38