文章信息
- 李潇潇, 范华莹, 孙莉, 梁军成, 邓艳萍.
- Li Xiaoxiao, Fan Huaying, Sun Li, Liang Juncheng, Deng Yanping.
- 阿片类物质依赖者戒断期间机体免疫功能的变化以及济泰片干预的影响
- Changes and the impact on immune function of opioid-dependent subjects by Jitai tabelets during the withdrawal stage
- 中华流行病学杂志, 2017, 38(4): 531-536
- Chinese journal of Epidemiology, 2017, 38(4): 531-536
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2017.04.024
-
文章历史
收稿日期: 2016-08-10
2. 100044 北京大学人民医院科研处;
3. 100191 北京大学中国药物依赖性研究所
2. Department of Science and Research, Peking University People's Hospital, Beijing 100044, China;
3. National Institute on Drug Dependence, Peking University, Beijing 100191, China
长期滥用阿片类物质损害多种器官和系统,其中以对免疫功能的损伤最为常见。临床观察发现阿片类物质依赖者各种感染性疾病的发生率、肿瘤的发生和转移率明显高于普通人群[1],提示该群体的免疫功能受损。然而美沙酮等阿片类受体激动剂类戒毒药物对机体免疫功能的损伤并无修复作用,长期使用还可能加重免疫抑制[2]。戒毒中药具有低毒安全、无成瘾性、作用全面等特点,与西药相比,更能整体调节与成瘾相关的神经-内分泌-免疫网络,促进机体免疫功能的恢复。济泰片中的人参、当归、黄芪、红花、附子等成分均具有一定的免疫促进作用[3-6]。此外,动物实验证实济泰片能显著增强吗啡损伤小鼠单核-巨噬细胞的吞噬功能,增加血清血溶素的生成,显著抑制免疫器官的萎缩[7]。本研究通过观察阿片类物质依赖者脱毒前后血清中免疫球蛋白(IgA、IgG、IgM)、T细胞亚群(CD3+、CD4+、CD8+)以及细胞因子(IL-2、IL-4、IFN-γ)水平的变化,探讨戒断期间阿片类物质依赖者免疫功能的变化及济泰片干预的影响。
对象与方法1.研究对象:选择上海市公安局强制戒毒所收治的阿片类物质依赖者,符合DSM-Ⅳ阿片类物质依赖和阿片类物质戒断诊断标准,尿液吗啡定性检测阳性,末次使用毒品时间距入院为8~36 h,符合中医毒瘀互阻、脾肾不足、寒热错杂证辨证诊断标准,无重要器质性病变。本研究经北京大学医学部伦理委员会审核批准,受试者入组前均签署知情同意书。
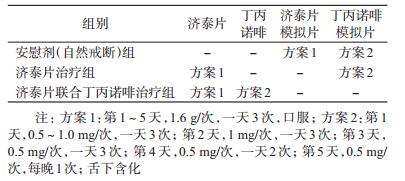
2.治疗方法:采用随机数字表(信封法随机分组,分配隐藏)将受试者随机分为3组,予双盲、双模拟、安慰剂平行对照试验。试验药:济泰片,每粒0.4 g,批号:0904010,由上海中药制药技术有限公司提供;联合用药:丁丙诺啡含片,每片0.5 mg,批号:090201,来源于天津药物研究院药业有限公司。模拟片与药片的外观、包装及厂家一致。治疗方案见表 1。选取同一地区年龄、性别相似的健康受试者30例作为正常对照组。
3.生物样本的检测:
(1)血样采集:于戒断前和戒断后第14天采集阿片类物质依赖者血样,检测血清中免疫球蛋白(IgA、IgG、IgM)、T细胞亚群(CD3+、CD4+、CD8+)以及细胞因子(IL-2、IL-4、IFN-γ)水平。同时采集正常对照组血样。
(2)免疫指标检测:采集外周静脉血3 ml,1 000×g 5 min,吸取上清液,免疫比浊法测IgG、IgA、IgM,具体操作步骤按试剂盒的说明进行。采用流式细胞术法检测外周血T细胞亚群和细胞内细胞因子的水平[8-9]。
4.统计学分析:统计学分析用SAS 9.13软件完成。符合正态分布和方差齐性的计量资料,组内比较采用配对t检验,两组间比较采用t检验,三组间比较采用方差分析或协方差分析;不符合正态分布和方差齐性的计量资料,组内和组间比较则采用非参数检验(秩和检验)。相关性分析采用直线相关或秩相关。P<0.05为差异有统计学意义。
结果1.免疫球蛋白和T细胞亚群检测:
(1)受试者一般情况:共入组阿片类物质依赖者112例,脱落3例,因入组时间>36 h、检测指标有缺失等原因剔除8例,确定纳入病例101例。正常对照组30例,其中男性21例,女性9例,年龄(42.47±7.00)岁。101例受试者的人口学资料与阿片类物质滥用情况见表 2,组间比较差异无统计学意义;各组分别与正常对照组进行比较,性别和年龄差异均无统计学意义(均P>0.05)。
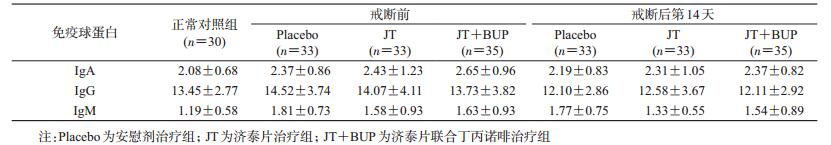
(2)戒断期间免疫球蛋白水平变化及药物干预影响:戒断前,101例阿片类物质依赖者的IgM水平为(1.67±0.87)g/L,高于正常对照组,差异有统计学意义(χ2=7.28,P=0.007 0);IgA、IgG水平在两组间的差异无统计学意义(P>0.05),见表 3。与戒断前相比,戒断后第14天安慰剂组受试者的IgA、IgG水平降低(IgA:S=142,P=0.008 9;IgG:t=7.20,P<0.000 1),与正常对照组的差异无统计学意义(P>0.05);IgM水平的波动较小(P>0.05),戒断第14天时仍高于正常对照组,差异有统计学意义(t=-3.40,P=0.001 2)。
与安慰剂相比,济泰片可使戒断期间IgG水平的降幅减小,差异有统计学意义(F=4.67,P=0.033 1);IgM水平的降幅增加,差异有统计学意义(F=5.05,0.026 9);戒断第14天时IgM恢复至正常水平(P>0.05)。济泰片联合丁丙诺啡则无类似优势(与安慰剂组相比,戒断前后IgG、IgM水平变化的差异均无统计学意义,P>0.05)。与安慰剂相比,药物干预(济泰片或济泰片联合丁丙诺啡)不影响戒断期间IgA的变化(均P>0.05)。
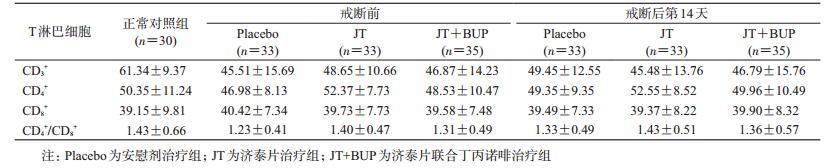
(3)戒断期间外周血T细胞亚群变化及药物干预影响:戒断前,101例阿片类物质依赖者CD3+ T细胞水平为(47.01±13.62)%,低于正常对照组,差异有统计学意义(χ2=25.89,P<0.000 1);阿片类物质依赖者的CD4+、CD8+T细胞水平及CD4+/CD8+比例,与正常对照组比较的差异均无统计学意义(均P>0.05),见表 4。安慰剂组CD3+、CD8+T细胞水平在戒断前后的差异均无统计学意义(均P>0.05);与戒断前相比,戒断后第14天CD4+ T细胞水平与CD4+/CD8+比例降低(CD4+ T淋巴细胞百分数:t=4.91,P<0.000 1;CD4+/CD8+比例:S=-147,P=0.006 5),但与正常对照组相比,差异均无统计学意义(均P>0.05)。
与安慰剂相比,济泰片或济泰片联合丁丙诺啡干预在戒断前后T细胞亚群的变化方面,差异均无统计学意义(均P>0.05)。
2.细胞内细胞因子检测:
(1)受试者一般情况:正常对照组20例,男女性别比为13/7,年龄(43.25±5.80)岁。在101例阿片类物质依赖受试者中有65人同时采集血样进行细胞因子检测,其中安慰剂组22例,济泰片组21例,济泰片联合丁丙诺啡组22例,一般情况组间比较的差异均无统计学意义(P>0.05)。各组分别与正常对照组比较,性别、年龄的差异均无统计学意义(P>0.05)。
(2)戒断期间细胞因子水平的变化及药物治疗的影响:戒断前,65例阿片类物质依赖受试者IL-2、IFN-γ及IL-4占CD3+CD8-细胞比例分别为(14.44±13.50)%、(20.23±15.10)%、(1.97±1.59)%,高于正常对照组,差异有统计学意义(IL-2:χ2=10.72,P=0.001 1;IFN-γ:χ2=12.55,P=0.000 4;IL-4:χ2=15.46,P<0.000 1);IFN-γ/IL-4比例为15.83±20.70,与正常对照组的差异无统计学意义(P>0.05)。与戒断前相比,戒断后第14天安慰剂(自然戒断)组仅IL-4水平恢复至正常水平[戒断前:(2.36±1.93)%,戒断后:(0.86±0.64)%],戒断前后差异有统计学意义(t=3.82,P=0.001 0),戒断后与正常对照组相比差异无统计学意义(P>0.05);IFN-γ/IL-4比例与戒断前相比升高约3.43倍(S=-115.50,P<0.000 1),高于正常对照组,差异有统计学意义(χ2=8.08,P=0.004 5)。
济泰片组IL-4占CD3+CD8-细胞比例自戒断前的(2.20±1.49)%下降至戒断后的(1.88±1.63)%,戒断前后相比差异有统计学意义(t=3.82,P=0.001 0),并且降幅小于安慰剂组,两组间的差异有统计学意义(F=4.50,P=0.038 2),戒断后IL-4水平高于正常对照组,差异有统计学意义(χ2=5.13,P=0.023 5)。戒断后IFN-γ/IL-4比例与戒断前相比升高1.63倍,戒断前后的差异有统计学意义(S=-115.50,P<0.000 1);但是升幅小于安慰剂组,两组间的差异有统计学意义(F=6.57,P=0.013 1)。济泰片联合丁丙诺啡则使戒断期间IL-4占CD3+CD8-细胞比例自(1.37±1.13)%升高至(2.11±2.06)%,涨幅约为0.54倍,IFN-γ/IL-4比例略有降低,但戒断后水平与正常对照组之间的差异无统计学意义(P>0.05),该变化有别于安慰剂组(IL-4:F=8.03,P=0.006 3;IFN-γ/IL-4比例:F=11.00,P=0.001 6)。戒断前后IL-2、IFN-γ变化趋势方面,药物干预组(济泰片或济泰片联合丁丙诺啡)与安慰剂组之间的差异无统计学意义(均P>0.05)。
3.相关性分析:戒断前,阿片类物质依赖者IgM水平与性别、年龄均存在相关性(性别:r=0.21,P=0.04;年龄:r=-0.32,P=0.001),CD4+T细胞水平、CD4+/CD8+比例与年龄存在相关性(CD4+T细胞水平:r=0.28,P=0.006;CD4+/CD8+比例:r=0.20,P=0.04);免疫球蛋白(IgA、IgG、IgM)与CD4+T细胞的水平与吸毒方式存在相关性(IgA:r=0.20,P<0.05;IgG:r=0.21,P=0.04;IgM:r=0.31,P=0.002;CD4:r=-0.23,P=0.02),CD8+T细胞水平与毒品近一周平均日用量呈负相关(r=-0.25,P=0.01)。
讨论阿片依赖人群存在严重的体液免疫功能降低或缺陷。早在1992年,Rouveix等[10]就发现阿片类物质可使机体B细胞活性降低。海洛因依赖者血清IgG、IgM水平的增高可能导致免疫损害[11]。本研究结果显示阿片类物质依赖者IgM水平高于正常对照组,而IgA、IgG水平与正常对照组相比差异无统计学意义。造成这种现象的原因比较复杂,可能与滥用物质本身、合并的病毒感染、慢性肝病或撤药所引起的应激反应等因素有关。目前关于海洛因依赖者的抗体水平研究报道的结论不一,这可能与观察对象的吸毒方式有关[12]。本研究结果显示,IgA、IgG、IgM与吸毒方式存在相关性,提示不同的吸毒方式可能影响免疫球蛋白水平。
以T细胞为代表的细胞免疫体系对免疫应答的启动、淋巴细胞的活化起重要作用,是反映阿片类物质对机体免疫系统影响的重要指标。既往研究报道阿片类物质依赖者外周血T细胞数量减少、增殖能力降低[13]。本研究发现戒断期间阿片类物质依赖者CD3+T细胞水平低于正常对照组,且直至第14天仍未恢复,证实了阿片类物质对免疫功能的抑制作用[14]。吸毒方式对T细胞亚群的水平也有一定的影响,静脉注射者T细胞数量和亚群比例较低[15]。本研究结果显示,CD4+T细胞与吸毒方式存在一定的相关性,与既往报道相符。
根据CD4+T细胞分泌的细胞因子谱不同,可将其分为Th1和Th2细胞。Th1细胞主要分泌IL-2、IFN-γ,参与细胞免疫;Th2细胞主要分泌IL-4、IL-6和IL-10等,辅助体液免疫应答,Th1/Th2的平衡在免疫反应中起重要作用。阿片类物质依赖者存在Th1/Th2功能紊乱,主要表现为Th1细胞功能降低,Th2细胞功能亢进[16-17],并且阿片类物质对Th1细胞的抑制程度与使用毒品剂量呈正相关[18-19]。本研究结果显示,阿片类物质依赖者的IL-2、IL-4、IFN-γ水平均高于正常对照组,戒断期间IL-2、IFN-γ水平升高,IL-4水平显著下降,导致IFN-γ/IL-4比例明显升高,提示Th1细胞介导的细胞免疫功能亢进,Th2细胞介导的体液免疫功能受抑,从而加重Th1/Th2平衡的偏移,可能与急性戒断所致的应激反应有关。
阿片类物质可损伤机体免疫功能,即使戒断期间给予药物治疗,这种损害在戒断后相当长的时间内仍难以恢复[20]。本研究结果显示,戒断后第14天阿片类物质依赖者各项免疫功能指标仍未完全恢复。
既往动物研究已从有效成分、组方角度,证实济泰片对免疫功能恢复的作用[3-7],临床研究亦证实济泰片较安慰剂组可促进纹状体中多巴胺转运体水平的有效恢复[21],血清皮质醇激素更快恢复至正常水平[22],从而进行成瘾相关的神经-内分泌-免疫网络调节,整体上促进机体恢复免疫功能。且与美沙酮相比,一年内预防复吸作用相似[23]。本研究证实,戒断期间给予济泰片可使异常升高的IgM更快地恢复至正常对照水平,并改善IL-4的明显下降和IFN-γ/IL-4比例的明显升高,从而降低Th1/Th2比值偏移。
中药戒毒历史悠久,其与西药联合用于脱毒治疗已被证实可更好地控制症状、降低复吸率、减少西药使用剂量等[24]。本研究结果显示,济泰片联合丁丙诺啡治疗可提高IL-2、IFN-γ和IL-4水平,降低Th1/Th2比值,同样有利于Th1/Th2平衡的恢复,且各指标的改善程度较济泰片单药治疗更大。该免疫学变化或可从一定程度上解释中西医联合治疗的优势。
综上所述,阿片类物质依赖者急性戒断后,体液免疫功能和细胞免疫功能均有一定程度的损害,且戒断第14天各项异常指标仍未恢复正常。脱毒期间给予济泰片或济泰片与丁丙诺啡联合治疗,对个别免疫指标有一定的修复作用,值得进一步深入研究。
利益冲突: 无
| [1] | Friedman H, Eisenstein TK. Neurological basis of drug dependence and its effects on the immune system[J]. J Neuroimmunol, 2004, 147(1/2): 106–108. DOI:10.1016/j.jneuroim.2003.10.022 |
| [2] | Chan YY, Yang SN, Lin JC, et al. Inflammatory response in heroin addicts undergoing methadone maintenance treatment[J]. Psychiatry Res, 2015, 226(1): 230–234. DOI:10.1016/j.psychres.2014.12.053 |
| [3] | Zheng X, Liang Y, Kang A, et al. Peripheral immunomodulation with ginsenoside Rg1 ameliorates neuroinflammation-induced behavioral deficits in rats[J]. Neuroscience, 2014, 256: 210–222. DOI:10.1016/j.neuroscience.2013.10.023 |
| [4] | Huang LF, Yao YM, Li JF, et al. The effect of Astragaloside Ⅳ on immune function of regulatory T cell mediated by high mobility group box 1 protein in vitro[J]. Fitoterapia, 2012, 83(8): 1514–1522. DOI:10.1016/j.fitote.2012.08.019 |
| [5] | Liu QY, Yao YM, Zhang SW, et al. Astragalus polysaccharides regulate T cell-mediated immunity via CD11c (high) CD45RB (low) DCs in vitro[J]. J Ethnopharmacol, 2011, 136(3): 457–464. DOI:10.1016/j.jep.2010.06.041 |
| [6] | Yang TH, Jia M, Zhou SY, et al. Antivirus and immune enhancement activities of sulfated polysaccharide from Angelica sinensis[J]. Int J Biol Macromol, 2012, 50(3): 768–772. DOI:10.1016/j.ijbiomac.2011.11.027 |
| [7] |
王宇华, 陶奕敏, 陈洁, 等.
济泰片对吗啡损伤小鼠免疫功能的影响[J]. 中国药物依赖性杂志, 2011, 20(1): 22–25.
Wang YH, Tao YM, Chen J, et al. Effects of Jitai tablets on immune function in morphine dependent mice[J]. Chin J Drug Depend, 2011, 20(1): 22–25. DOI:10.13936/j.cnki.cjdd1992.2011.01.001 |
| [8] | Choi HS, Ha SY, Kim HM, et al. The prognostic effects of tumor infiltrating regulatory T cells and myeloid derived suppressor cells assessed by multicolor flow cytometry in gastric cancer patients[J]. Oncotarget, 2016, 7(7): 7940–7951. DOI:10.18632/oncotarget.6958 |
| [9] |
周茂华, 王丁, 张建军, 等.
四色法流式细胞术测定淋巴细胞内细胞因子的方法学探讨[J]. 现代检验医学杂志, 2003, 18(4): 1–3.
Zhou MH, Wang D, Zhang JJ, et al. Determination of intracellular cytokines in human lymphocytes by four-color flow cytometry[J]. J Mod Lab Med, 2003, 18(4): 1–3. DOI:10.3969/j.issn.1671-7414.2003.04.001 |
| [10] | Rouveix B. Opiates and immune function. Consequences on infectious diseases with special reference to AIDS[J]. Therapie, 1992, 47(6): 503–512. |
| [11] | Cloak CC, Chang LD, O'Neil SP, et al. Neurometabolite abnormalities in simian immunodeficiency virus-infected macaques with chronic morphine administration[J]. J Neuroimmune Pharmacol, 2011, 6(3): 371–380. DOI:10.1007/s11481-010-9246-3 |
| [12] | Simonovska N, Zafirova-Ivanovska B, Babulovska A, et al. Influence of duration of heroin dependence on humoral immunologic indicators[J]. J Addict Med, 2016, 10(6): 448–452. DOI:10.1097/ADM.0000000000000259 |
| [13] | Singhal P, Kapasi A, Reddy K, et al. Opiates promote T cell apoptosis through JNK and caspase pathway//Friedman H, Klein TW, Madden JJ. Neuroimmune Circuits, Drugs of Abuse, and Infectious Diseases[M]. US:Springer, 2001:127-135. DOI:10.1007/0-306-47611-8_15. |
| [14] |
韦丽华, 方芳, 薛云松, 等.
海洛因依赖者几项细胞免疫指标的探讨[J]. 上海免疫学杂志, 2001, 21(5): 305–306.
Wei LH, Fang F, Xue YS, et al. Study on several cellular immune indexes in heroin addicts[J]. Shanghai J Immunol, 2001, 21(5): 305–306. DOI:10.3969/j.issn.1001-2478.2001.05.017 |
| [15] | Olin M, Choi K, Molitor TW. Morphine alters M. bovis infected microglia's ability to activate γδ T lymphocytes[J]. J Neuroimmune Pharmacol, 2011, 6(4): 578–584. DOI:10.1007/s11481-011-9308-1 |
| [16] |
和虹, 杨丽萍, 杨国军, 等.
海洛因依赖者Th1/Th2类细胞因子的变化[J]. 中国药物滥用防治杂志, 2005, 11(3): 131–133.
He H, Yang LP, Yang GJ, et al. The changes of Th1/Th2 type cytokines in heroin addicts[J]. Chin J Drug Abuse Prev Treat, 2005, 11(3): 131–133. DOI:10.3969/j.issn.1006-902X.2005.03.003 |
| [17] | Rivera-Amill V, Kumar R, Noel RJ Jr, et al. Short communication:Lack of immune response in rapid progressor morphine-dependent and SIV/SHIV-infected rhesus macaques is correlated with downregulation of TH1 cytokines[J]. AIDS Res Hum Retroviruses, 2010, 26(8): 919–922. DOI:10.1089/aid.2010.0012 |
| [18] | Nielsen DA, Hamon S, Yuferov V, et al. Ethnic diversity of DNA methylation in the OPRM1 promoter region in lymphocytes of heroin addicts[J]. Hum Genet, 2010, 27(6): 639–649. DOI:10.1007/s00439-010-0807-6 |
| [19] | Börner C, Warnick B, Smida M, et al. Mechanisms of opioid-mediated inhibition of human T cell receptor signaling[J]. J Immunol, 2009, 183(2): 882–889. DOI:10.4049/jimmunol.0802763 |
| [20] |
罗建强, 卢光祥, 闻心培, 等.
海洛因依赖者脱毒前后IL-1和TNF含量变化的研究[J]. 中国药物滥用防治杂志, 2004, 10(6): 327–329.
Luo JQ, Lu GX, Wen XP, et al. A study on the changes of cytokines (IL-1 and TNF) in serum of heroin abusers[J]. Chin J Drug Abuse Prev Treat, 2004, 10(6): 327–329. DOI:10.3969/j.issn.1006-902X.2004.06.007 |
| [21] | Liu Y, Han M, Liu XD, et al. Dopamine transporter availability in heroin-dependent subjects and controls:longitudinal changes during abstinence and the effects of Jitai tablets treatment[J]. Psychopharmacology (Berl), 2013, 230(2): 235–244. DOI:10.1007/s00213-013-3148-z |
| [22] | Fan HY, Sun L, Li XX, et al. Effects of Jitai tablet, a traditional Chinese medicine, on plasma adrenocorticotropic hormone and cortisol levels in heroin addicts during abstinence[J]. J Altern Complement Med, 2014, 20(7): 527–334. DOI:10.1089/acm.2012.0804 |
| [23] | Hao SQ, Zhao M, Zhang RW, et al. The effectiveness comparison of Jitai tablets versus methadone in community-based drug treatment:a 1-year follow-up study[J]. Addict Behav, 2013, 38(10): 2596–2600. DOI:10.1016/j.addbeh.2013.05.013 |
| [24] |
崔跃, 杨晓琳, 崔锆哲, 等.
中西医结合脱毒治疗的分析研究[J]. 中国现代药物应用, 2015, 9(15): 1–2.
Cui Y, Yang XL, Cui HZ, et al. Analysis and research of detoxification treatment by integrated traditional Chinese and Western medicines[J]. Chin J Mod Drug Appl, 2015, 9(15): 1–2. DOI:10.14164/j.cnki.cn11-5581/r.2015.15.001 |
 2017, Vol. 38
2017, Vol. 38