文章信息
- 熊为旻, 何斐, 肖仁栋, 俞婷婷, 张鑫, 刘志强, 徐秋萍, 蔡琳 .
- Xiong Weimin, He Fei, Xiao Rendong, Yu Tingting, Zhang Xin, Liu Zhiqiang, Xu Qiuping, Cai Lin .
- 人乳头瘤病毒感染与原发性肺癌相关性研究
- Association between human papillomavirus infection and lung cancer
- 中华流行病学杂志, 2016, 37(12): 1658-1661
- Chinese journal of Epidemiology, 2016, 37(12): 1658-1661
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2016.12.020
-
文章历史
收稿日期: 2016-07-13
自1979年Syrjänen[1]在支气管肺癌组织中发现HPV及上皮角化形态学改变后,HPV感染在肺癌发生发展中的作用引起广泛争议。既往研究显示肺癌中HPV感染率在0~78.3%[2]。由于正常肺组织难以获得,大部分研究仅检测肺癌组织中的HPV感染情况[3]。为了探索HPV感染与福建人群肺癌的关系,本研究检测匹配的肺癌和癌旁正常组织中HPV感染情况。
对象与方法1.研究对象:病例来源于福建医科大学附属第一医院胸外科2013年10月至2015年5月的原发性肺癌新发病例。行手术时切取肺部癌组织和癌旁正常组织作为自身对照,所有组织标本在术后10 min内放入冻存管存于-80 ℃冰箱。本研究经过福建医科大学伦理委员会批准,所有患者均签署知情同意书。
2.研究方法:
(1)资料收集:查阅患者的电子病历,收集临床信息(病理分型、临床分期、肿瘤发生部位、淋巴结转移等),同时面对面询问患者的吸烟饮酒情况。吸烟定义为累计吸烟 > 100支;吸烟包-年=每日吸烟支数÷20×吸烟年数;饮酒定义为每月饮酒精饮料至少1次[4]。
(2)样本检测:癌和癌旁组织的基因组DNA利用黏膜细胞DNA提取试剂盒(广东凯普生物科技股份有限公司)提取,采用DeNovix DS-11超微量紫外可见分光光度计对抽提的DNA产物的浓度及纯度进行定量测定。采用21种HPV分型检测试剂盒(广东凯普生物科技股份有限公司)检测HPV感染情况,包括15种高危型别(HPV16、18、31、33、35、39、45、51、52、53、56、58、59、66、68)和6种低危型别[HPV6、11、42、43、44、CP8304(81)]。
为防止交叉污染,整个过程分为3个独立区域:样品准备和DNA提取区、PCR扩增区以及导流杂交检测区。每张杂交膜上具有双质控点,Biotin点(DNA对照)及IC点(监测PCR反应的有效性)。同时检测宫颈细胞刷样品作为阴性和阳性对照。
3.统计学分析:应用SPSS 19.0软件进行数据分析。采用配对χ2检验比较肺癌与癌旁正常组织间HPV检出率差异。利用χ2检验或Fisher确切概率法分析不同性别、年龄、组织学类型、临床分期、淋巴结转移、吸烟和饮酒情况的HPV检出率差异。所有P值基于双侧检验,α=0.05。
结果1.一般特征:共有83例原发性肺癌病例,确诊年龄为38~82(58.9±9.8)岁,年龄M为60岁。其中鳞癌20例(24.1%)、腺癌55例(66.3%)、腺鳞癌5例(6.0%)、大细胞癌2例(2.4%)、小细胞癌1例(1.2%);47.0%的病例是非吸烟者,89.2%的病例是非饮酒者(表 1)。
2.肺癌组织和癌旁正常组织HPV感染状况:所有样本Biotin点及IC点同时显色。肺癌组织HPV阳性率为8.4%,7例HPV阳性的具体型别:3例HPV42,2例HPV51,1例HPV44,1例HPV35、42、44多重感染;癌旁正常组织HPV阳性率为7.2%,6例HPV阳性的具体型别:3例HPV42、1例HPV18、1例HPV6、1例HPV18、33多重感染。配对χ2检验结果显示,HPV检出率在肺癌与癌旁正常组织间差异无统计学意义(P > 0.999)。
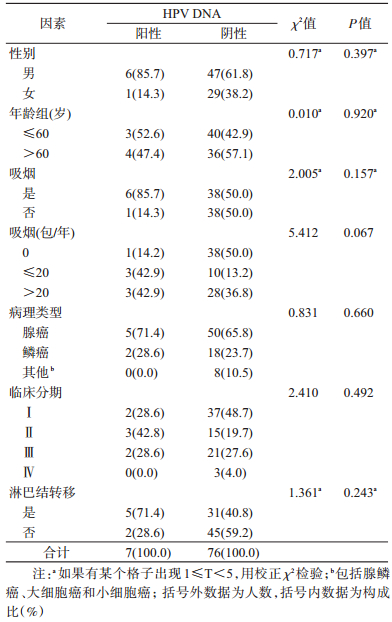
3.分层分析肺癌组织HPV感染状况:分层分析不同性别、年龄、吸烟、饮酒,不同病理类型、临床分期和淋巴结转移情况下肺癌组织HPV检出情况,χ2检验结果显示,差异均无统计学意义(P > 0.05),见表 2。
HPV是一种无包膜双链环状嗜上皮小DNA病毒,直径55 nm,由20面体衣壳包裹的基因组包括早期结构基因(E1-E8)和晚期结构基因(L1、L2)[5]。近半个世纪以来,科学家们对HPV的潜在致癌作用与各种癌症发生发展的关系进行了深入研究,有研究证明HPV与生殖系统癌症密切相关[6],但与非生殖恶性肿瘤的关系尚未阐明,尤其是呼吸系统恶性肿瘤。
本研究对83对匹配的肺癌和癌旁正常组织的HPV感染情况进行检测,结果显示,肺癌组织HPV阳性率为8.4%,癌旁正常组织HPV阳性率为7.2%,两者HPV阳性率差异无统计学意义。Galvan等[7]用相同原理的检测方法,在100对匹配的肺癌和癌旁正常组织中均未检测到HPV DNA,认为HPV与肺癌发生风险无关联。有研究报道,亚洲人群的肺癌组织HPV感染率为28.1%(95%CI:26.6%~30.3%)[8],调整年龄、性别、吸烟状况和肿瘤分期后,亚洲人群的肺癌组织HPV感染率为4.60%(95%CI:3.48%~5.73%),肺癌组织的HPV感染率高于正常肺组织(OR=3.86,95%CI:2.87~5.19)[9]。HPV感染与肺癌的关系及关联强度的差异可能与年龄、性别、吸烟状况、肿瘤分期和地区HPV感染率不同有关。
本研究进一步对不同性别、年龄、吸烟、饮酒、病理类型、临床分期和淋巴结转移情况下肺癌组织HPV检出情况进行分层分析,结果显示差异均无统计学意义(P > 0.05),与已有研究类似[9-10]。也有研究显示,吸烟肺癌患者相比非吸烟患者有更高的HPV感染率[11]。实验研究也显示烟草烟雾中的致癌物会增加HPV16/18的病毒合成以及与HPV16 E6/E7癌蛋白的相互作用,使肺细胞恶性增殖[12]。但Hasegawa等[8]对有关非吸烟非小细胞(型)肺癌(NSCLC)患者HPV感染率的研究进行系统综述显示,东亚地区吸烟NSCLC患者与非吸烟患者的HPV感染率差异无统计学意义(33.9% vs. 39.2%)。本研究未发现肺癌患者吸烟状态与HPV感染有明显关联,但还须加大样本进一步研究。有研究报道HPV感染与肺鳞癌关系密切[13],也有研究显示HPV阳性的肺癌组织均为腺癌[14]。但Zhai等[15]的Meta分析结果显示HPV感染、尤其是HPV16/18型别与肺鳞癌发生风险显著相关(OR=9.78,95%CI:6.28~15.22,P < 0.001),而与肺腺癌无关。研究者认为,吸烟可导致呼吸道正常柱状上皮鳞状化,HPV对鳞状上皮黏膜具有高度亲嗜性,能引起宿主黏膜异常增生[9]。本研究未发现不同组织病理类型HPV感染有明显差异,可能与样本较小和腺癌病例所占比例较大有关。
目前有关HPV与肺癌关系的研究结论仍不一致,可能的影响因素:①检测样本的不同(血液或组织);②样本的处理方法不同(新鲜冻存或石蜡包埋);③检测方法不同(PCR或ISH);④研究人群不同(年龄、性别、吸烟饮酒史、组织病理学类型、病理分期和种族等);⑤样本采集的时间点不同(在治疗措施前、中、后)。故本研究采取了下列措施以提高结果的可靠性:①标准化样本操作流程,手术后标本立即放入-80 ℃冰箱冻存,最大限度减少污染和核酸降解;②采用导流杂交法检测多种HPV型别,灵敏度及特异度均较高;③采用癌旁正常组织作对照,年龄、性别、吸烟饮酒史、组织病理学类型、临床分期和种族等均相同,不存在基本人口学资料不同的情况;④采集样本者均未在手术前采取放化疗措施。
本研究未发现HPV感染与肺癌的明显关联。由于样本量较小及病例对照研究本身的时序局限性,不能得出HPV感染与肺癌间的因果联系。为进一步探索在福建地区人群中,HPV感染与原发性肺癌发生风险关系,需要扩大样本量并采用更高级别的研究设计如巢式病例对照研究进行验证。
利益冲突: 无
| [1] | Syrjänen KJ. Condylomatous changes in neoplastic bronchial epithelium. Report of a case[J]. Respiration , 1979, 38(5) : 299–304. DOI:10.1159/000194095 |
| [2] | Srinivasan M, Taioli E, Ragin CC. Human papillomavirus type 16 and 18 in primary lung cancers-a meta-analysis[J]. Carcinogenesis , 2009, 30(10) : 1722–1728. DOI:10.1093/carcin/bgp177 |
| [3] | Syrjänen K. Detection of human papillomavirus in lung cancer:systematic review and meta-analysis[J]. Anticancer Res , 2012, 32(8) : 3235–3250. |
| [4] | Ribeiro KB, Levi JE, Pawlita M, et al. Low human papillomavirus prevalence in head and neck cancer:Results from two large case-control studies in high-incidence regions[J]. Int J Epidemiol , 2011, 40(2) : 489–502. DOI:10.1093/ije/dyq249 |
| [5] | Psyrri A, Boutati E, Karageorgopoulou S. Human papillomavirus in head and neck cancers:Biology, prognosis, hope of treatment, and vaccines[J]. Anticancer Drugs , 2011, 22(7) : 586–590. DOI:10.1097/CAD.0b013e328344ec44 |
| [6] | Zandberg DP, Bhargava R, Badin S, et al. The role of human papillomavirus in nongenital cancers[J]. CA Cancer J Clin , 2013, 63(1) : 57–81. DOI:10.3322/caac.21167 |
| [7] | Galvan A, Noci S, Taverna F, et al. Testing of human papillomavirus in lung cancer and non-tumor lung tissue[J]. BMC Cancer , 2012, 12 : 512. DOI:10.1186/1471-2407-12-512 |
| [8] | Hasegawa Y, Ando M, Kubo A, et al. Human papilloma virus in non-small cell lung cancer in never smokers:A systematic review of the literature[J]. Lung Cancer , 2014, 83(1) : 8–13. DOI:10.1016/j.lungcan.2013.10.002 |
| [9] | Ragin C, Obikoya-Malomo M, Kim S, et al. HPV-associated lung cancers:an international pooled analysis[J]. Carcinogenesis , 2014, 35(6) : 1267–1275. DOI:10.1093/carcin/bgu038 |
| [10] | Fei Y, Yang J, Hsieh WC, et al. Different human papillomavirus 16/18 infection in chinese non-small cell lung cancer patients living in wuhan, China[J]. Jpn J Clin Oncol , 2006, 36(5) : 274–279. DOI:10.1093/jjco/hyl017 |
| [11] | Carpagnano GE, Koutelou A, Natalicchio MI, et al. HPV in exhaled breath condensate of lung cancer patients[J]. Br J Cancer , 2011, 105(8) : 1183–1190. DOI:10.1038/bjc.2011.354 |
| [12] | Muñoz JP, González C, Parra B, et al. Functional interaction between human papillomavirus type 16 e6 and e7 oncoproteins and cigarette smoke components in lung epithelial cells[J]. PLoS One , 2012, 7(5) : e38178. DOI:10.1371/journal.pone.0038178 |
| [13] |
高志棣, 邵纬, 李黎, 等.
青岛地区人乳头状瘤病毒感染亚型与肺鳞状细胞癌的相关性[J]. 癌变·畸变·突变 , 2013, 25(2) : 111–114.
Gao ZD, Shao W, Li L, et al. The correlation between HPV infection subtype and lung squamous cell carcinoma in Qingdao region[J]. Carcinogen Teratogen Mut , 2013, 25(2) : 111–114. DOI:10.3969/j.issn.1004-616x.2013.02.007 |
| [14] | Joh J, Jenson AB, Moore GD, et al. Human papillomavirus (HPV) and merkel cell polyomavirus (mcpyv) in non small cell lung cancer[J]. Exp Mol Pathol , 2010, 89(3) : 222–226. DOI:10.1016/j.yexmp.2010.08.001 |
| [15] | Zhai K, Ding J, Shi HZ. HPV and lung cancer risk:a meta-analysis[J]. J Clin Virol , 2015, 63 : 84–90. DOI:10.1016/j.jcv.2014.09.014 |
 2016, Vol. 37
2016, Vol. 37