文章信息
- 鄢灵君, 陈法, 柳迪萌, 黄江峰, 刘芳萍, 伍俊锋, 刘凤琼, 叶佳增, 邱宇, 林李嵩, 何保昌 .
- Yan Lingjun, Chen Fa, Liu Dimeng, Huang Jiangfeng, Liu Fangping, Wu Junfeng, Liu Fengqiong, Ye Jiazeng, Qiu Yu, Lin Lisong, He Baochang .
- 饮茶、咖啡与口腔鳞状细胞癌发病关系的病例对照研究
- Tea, coffee intakes and risk of oral squamous cell carcinoma: a case-control study
- 中华流行病学杂志, 2016, 37(11): 1531-1535
- Chinese journal of Epidemiology, 2016, 37(11): 1531-1535
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2016.11.019
-
文章历史
收稿日期: 2016-05-25
2. 350004 福州, 福建医科大学附属第一医院口腔颌面外科
2. Department of Stomatology, the First Affiliated Hospital of Fujian Medical University, Fuzhou 350004, China
口腔鳞状细胞癌(OSCC)约占口腔癌的90%~95%[1],并具有局部转移率高,预后较差等特点[2-3]。茶、咖啡以及牛奶是日常生活常见饮料。近年来已有流行病学研究探讨饮茶、咖啡以及牛奶与OSCC的发病关系,但结果尚存在争议。其中一些研究认为饮茶、喝咖啡可降低口腔癌的发病风险[4-5],但也有研究显示两者与OSCC的发病并未存在关联[6-7]。目前有实验室研究发现牛奶可影响茶与咖啡在人体内的生物学功能[8-9],且牛奶在口腔癌发病中起保护作用[10],推测牛奶在研究饮茶、咖啡与OSCC的发病关系中可能起到一定的混杂作用。为此本研究在福建地区开展病例对照研究,以探讨经牛奶分层后饮茶、咖啡与OSCC发病的关系,为预防控制OSCC提供科学依据。
1、 对象与方法1.研究对象:源自2010年9月至2016年3月福建医科大学附属第一医院口腔颌面外科确诊的593例原发性OSCC新发病例,选取同期该医院体检人群及社区健康人群,按性别、年龄(±3岁)进行频数匹配作为对照组,共1 128例。病例组入选标准为①均经病理学确诊的OSCC新发病例,②均在福建地区居住10年以上,③年龄20~80岁;排除标准为①继发性和转移性的OSCC患者,②口腔炎症、口腔良性肿瘤的患者,③病情危重不能清晰回答问题者。对照组纳入标准为年龄20~80岁且在福建地区居住10年以上同期到该医院体检的健康人群和社区健康人群;排除标准为既往或现在有肿瘤疾病史及OSCC病例组的直系亲属。本研究已通过福建医科大学伦理委员会批准,所有研究对象均签署知情同意书。
2.研究方法:采用中国医学科学院肿瘤研究所和美国犹他大学流行病学专家联合编制的结构化调查问卷,由经统一培训合格的调查员面访所有入组的研究对象,主要包括一般情况(年龄、性别、职业、文化程度、身高、体重等)、吸烟史、饮酒史及饮茶(包括饮茶年龄、饮茶年限、每日饮茶量、饮茶浓度及温度等)、咖啡、牛奶史等。其中饮茶、咖啡、牛奶均是指每周至少饮1杯,且连续≥6个月。吸烟定义为累计吸烟量达到100支[11]。饮酒指每周至少1次,且连续6个月以上[12]。调查结束后,由专人负责调查表的审核,发现问题及时予以纠正,剔除不合格者。
3.统计学分析:采用EpiData 3.1软件进行数据双录入,经逻辑纠错,并随机抽样10%复查。采用χ2检验对病例组和对照组的一般人口学特征进行均衡性检验。应用非条件logistic回归模型计算经牛奶分层后,咖啡、饮茶及其相关变量与OSCC发病风险的调整OR及其95%CI并进行相乘交互作用分析,采用趋势性检验对有序分类变量进行趋势分析。运用Andersson等[13]编制的Excel计算表估算超额相对超危险度(RERI)、交互作用归因比(AP)、交互作用指数(SI)及其95%CI,评价因素间是否具有相加交互作用,如果两因素无相加交互作用,则RERI和API的可信区间应包含0,SI的可信区间应包含1。分析采用Stata 13.0软件。以P<0.05为差异有统计学意义。
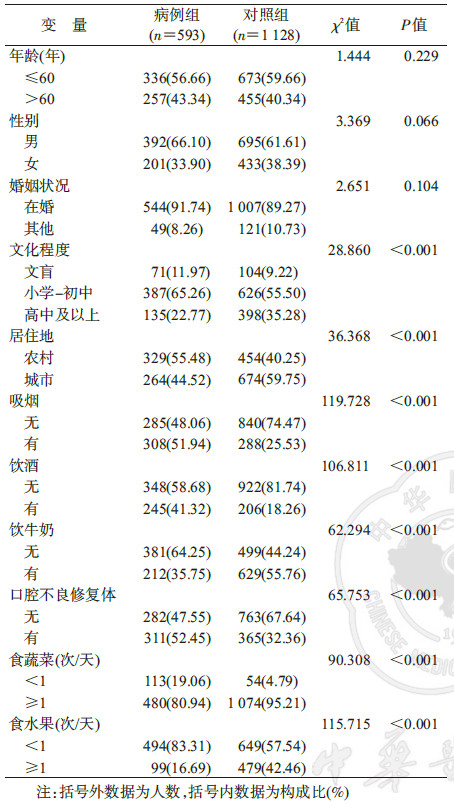
2、 结果1.一般情况:两组经均衡性检验在年龄、性别、婚姻状况等有可比性(P>0.05),但文化程度、居住地、吸烟、饮酒、饮牛奶、口腔不良修复体、食蔬菜和水果等分布差异有统计学意义(P<0.05),将这些因素纳入调整,进一步分析发现饮牛奶可降低OSCC的发病风险(aOR=0.69,95%CI:0.54~0.88),且饮牛奶在饮茶者与非饮茶者、饮咖啡和未饮咖啡者之间分布的差异均有统计学意义(χ2=4.36,P=0.037;χ2=4.01,P=0.045)。因此,饮牛奶可看作是饮茶、咖啡与OSCC关系研究中的混杂因素(表 1)。
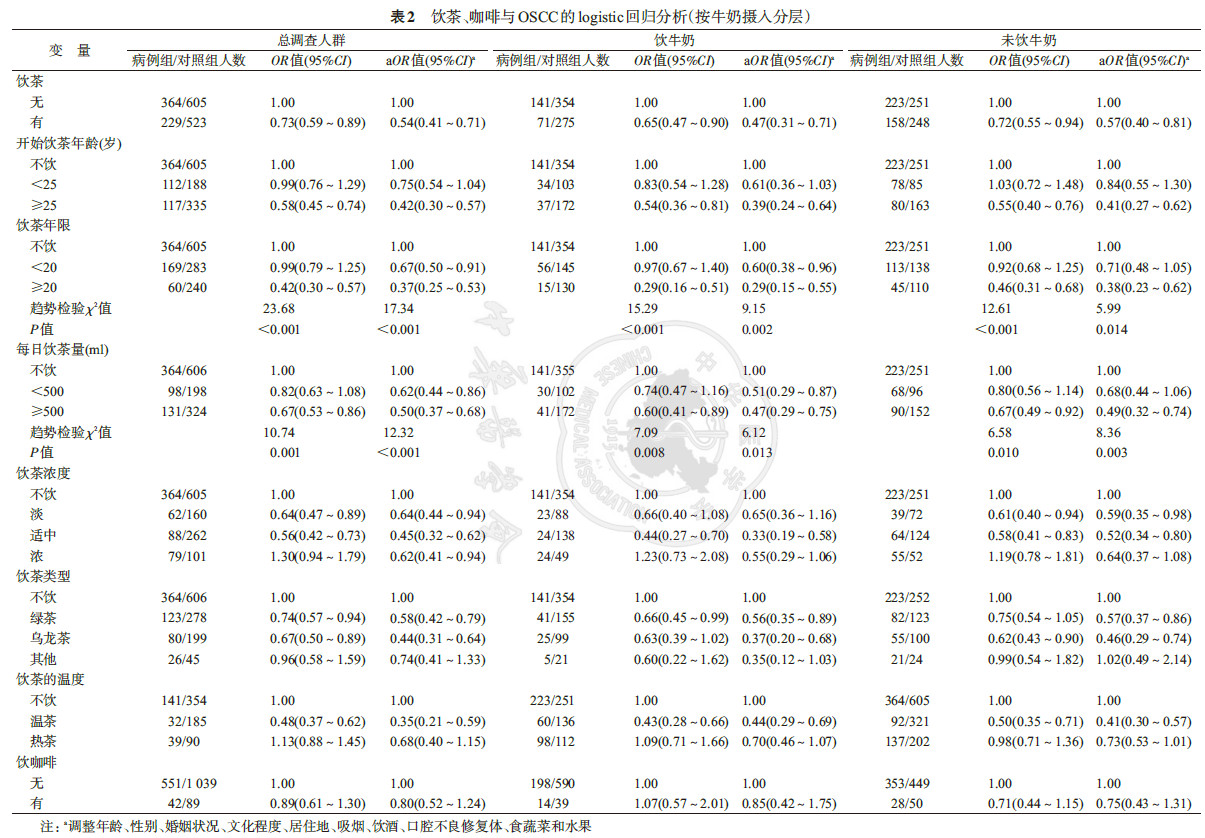
2.饮茶、咖啡与OSCC的关系:在总调查人群中,以及按牛奶摄入情况分层后,对饮茶、咖啡与OSCC的关系进行分析,经性别、年龄、文化程度、居住地、吸烟、饮酒、食蔬菜和水果等因素调整后,结果显示在总调查人群、饮牛奶和未饮牛奶人群中,与不饮茶者相比,饮茶者患OSCC的风险均显著降低,其aOR值及其95%CI分别为0.54(0.41~0.71)、0.47(0.31~0.71)和0.57(0.40~0.81)。进一步分析发现,开始饮茶年龄≥25岁、饮茶浓度适中、饮温茶、饮绿茶和乌龙茶在这三个人群中也均是OSCC的保护性因素,且在饮牛奶人群中各因素的保护作用更明显。此外,随着每日饮茶量的增加和饮茶年限延长,OSCC的发病风险也随之降低(趋势检验均P<0.05)。但未见饮咖啡与OSCC的发病存在关联(表 2)。
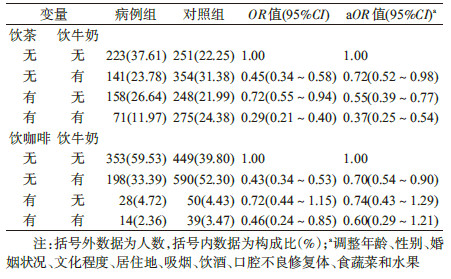
3.饮茶、咖啡与牛奶的相乘及相加交互作用:经相乘交互作用分析显示,饮茶与饮牛奶间存在相乘交互作用,其OR=0.42(95%CI:0.32~0.56)和aOR=0.52(95%CI:0.37~0.71),进一步叉生分析发现既饮茶又饮牛奶者,发生OSCC的风险最低,aOR=0.37(95%CI:0.25~0.54),但并未发现饮茶与饮牛奶间存在相加交互作用,RERI、API和SI值及其95%CI分别为0.10(-0.20~0.40)、0.27(-0.56~1.10)、0.86(0.58~1.30)。此外,研究中未发现饮咖啡与饮牛奶之间存在相乘及相加交互作用,其aOR、RERI、API和SI值及其95%CI分别为0.72(0.36~1.45)、0.15(-0.44~0.75)、0.26(-0.64~1.16)、0.72(0.20~2.56)。见表 3。
本文单因素研究结果表明饮茶与降低OSCC的发病风险相关,经潜在混杂因素调整后,仍显示饮茶对OSCC的发生起到保护作用,与Wang等[14]的研究结果一致。茶叶中富含多种活性物质(如茶多酚、黄酮醇),能够通过抗氧化、清除自由基以及抗炎症等途径降低患癌风险[15]。其中没食子儿茶素、没食子酸酯以及其他的多酚类能够通过活化P53基因进一步促进P21和Bax的表达来诱导肿瘤细胞周期停滞和凋亡,从而抑制肿瘤的发生[16]。以往有研究表明饮茶与口腔癌发病风险之间呈剂量-反应关系[17-18],本研究结果也显示随着饮茶年限和每日饮茶量的增加,OSCC的发病风险也随之降低。但本研究未发现开始饮茶年龄越早,其OSCC发病风险越低,可能与部分研究对象停止了饮茶的习惯,即造成饮茶年龄越早其饮茶年限不一定越长的现象。目前一些流行病学调查中也得出类似结果[17],但还未有相关的实验性研究解释其中原因。此外,本研究结果还显示饮茶浓度适中和饮用温茶是OSCC的保护性因素,与陈法等[19]研究结果一致。
茶与牛奶共饮是一种较为普遍的现象。本研究的交互作用结果显示饮茶与饮奶之间存在相乘交互作用(aOR=0.52,95%CI:0.37~0.71,P<0.001)。牛奶中含有的乳铁蛋白与茶多酚一样具有抗菌、抗氧化等多种生物活性功能。Mohan等[8]的细胞实验结果发现在茶多酚中加入乳铁蛋白,对舌鳞状细胞(CAL-27)增殖的抑制能力比茶多酚的单独作用强,Chandra等经动物实验也发现与茶多酚的单独作用相比,茶多酚与乳铁蛋白的共同作用能够更有效地抑制仓鼠颊囊癌的发生[20]。可能是由于茶多酚与乳铁蛋白的共同作用能进一步降低细胞中Bcl-2/Bax的比率,使线粒体产生的活性氧量升高,促进细胞色素C的大量释放至胞质继而激活半胱天冬酶-3(caspase-3),活化的caspase-3能够诱导细胞凋亡,从而抑制肿瘤的发生[21-22]。但本研究中并未发现饮茶与饮奶之间存在相加交互作用,其具体机制有待进一步研究。
已有研究显示咖啡中含有多种抗氧化和抗肿瘤成分,如绿原酸、咖啡酸、类黑精、咖啡醇等,且与口腔癌的发病呈负相关[6, 23]。但本研究并未发现饮咖啡与OSCC的发病有关联,这可能与本研究人群中饮咖啡的人所占比例太少有关。此外,本研究采用病例对照方法,难以避免回忆偏倚,但在问卷设计中对饮茶、咖啡等变量严格定义,调查中通过与饮茶、咖啡等习惯有联系的记忆目标协助研究对象进行联想回忆,在一定程度可能减少回忆偏倚。因此本文结果仍需扩大样本量及深入研究(特别是队列研究)加以验证。
综上所述,饮茶是OSCC发病的保护因素,且饮茶与饮牛奶之间存在相乘交互作用,适量饮茶、增加牛奶的摄入可在一定程度上降低OSCC的发病风险。
利益冲突: 无| [1] | Al-Jaber A, Al-Nasser L, El-Metwally A. Epidemiology of oral cancer in Arab countries[J]. Saudi Med J , 2016, 37(3) : 249–255. DOI:10.15537/smj.2016.3.11388 |
| [2] | León X, Ferlito A, Myer Ⅲ CM, et al. Second primary tumors in head and neck cancer patients[J]. Acta Otolaryngol , 2002, 122(7) : 765–778. DOI:10.1080/003655402/000028048 |
| [3] | Argiris A, Karamouzis MV, Raben D, et al. Head and neck cancer[J]. Lancet , 2008, 371(9625) : 1695–1709. DOI:10.1016/S0140-6736(08)60728-X |
| [4] | Radoï L, Paget-Bailly S, Menvielle G, et al. Tea and coffee consumption and risk of oral cavity cancer:results of a large population-based case-control study, the ICARE study[J]. Cancer Epidemiol , 2013, 37(3) : 284–289. DOI:10.1016/j.canep.2013.02.001 |
| [5] | Li YM, Peng J, Li LZ. Coffee consumption associated with reduced risk of oral cancer:a meta-analysis[J]. Oral Surg Oral Med Oral Pathol Oral Radiol , 2016, 121(4) : 381–389. DOI:10.1016/j.oooo.2015.12.006 |
| [6] | Hildebrand JS, Patel AV, McCullough ML, et al. Coffee, tea, and fatal oral/pharyngeal cancer in a large prospective US cohort[J]. Am J Epidemiol , 2013, 177(1) : 50–58. DOI:10.1093/aje/kws222 |
| [7] | Bundgaard T, Wildt J, Frydenberg M, et al. Case-control study of squamous cell cancer of the oral cavity in Denmark[J]. Cancer Causes Control , 1995, 6(1) : 57–67. DOI:10.1007/BF00051681 |
| [8] | Mohan KVPC, Gunasekaran P, Varalakshmi E, et al. In vitro evaluation of the anticancer effect of lactoferrin and tea polyphenol combination on oral carcinoma cells[J]. Cell Biol Int , 2007, 31(6) : 599–608. DOI:10.1016/j.cellbi.2006.11.034 |
| [9] | Tagliazucchi D, Helal A, Verzelloni E, et al. The type and concentration of milk increase the in vitro bioaccessibility of coffee chlorogenic acids[J]. J Agric Food Chem , 2012, 60(44) : 11056–11064. DOI:10.1021/jf302694a |
| [10] | Levi F, Pasche C, La Vecchia C, et al. Food groups and risk of oral and pharyngeal cancer[J]. Int J Cancer , 1998, 77(5) : 705–709. DOI:10.1002/(sici)1097-0215(19980831)77:5<705::aid-ijc8>3.0.co;2-z |
| [11] |
杨功焕, 马杰民, 刘娜, 等.
中国人群2002年吸烟和被动吸烟的现状调查[J]. 中华流行病学杂志 , 2005, 26(2) : 77–83.
Yang GH, Ma JM, Liu N, et al. Smoking and passive smoking in Chinese, 2002[J]. Chin J Epidemiol , 2005, 26(2) : 77–83. |
| [12] |
张林峰, 赵连成, 周北凡, 等.
男性饮酒与缺血性脑卒中发病关系的研究[J]. 中华流行病学杂志 , 2004, 25(11) : 954–957.
Zhang LF, Zhao LC, Zhou BF, et al. Alcohol consumption and incidence of ischemic stroke in male Chinese[J]. Chin J Epidemiol , 2004, 25(11) : 954–957. |
| [13] | Andersson T, Alfredsson L, Källberg H, et al. Calculating measures of biological interaction[J]. Eur J Epidemiol , 2005, 20(7) : 575–579. DOI:10.1007/s10654-005-7835-x |
| [14] | Wang W, Yang Y, Zhang W, et al. Association of tea consumption and the risk of oral cancer:a meta-analysis[J]. Oral Oncol , 2014, 50(4) : 276–281. DOI:10.1016/j.oraloncology.2013.12.014 |
| [15] | Fujiki H, Sueoka E, Watanabe T, et al. Primary cancer prevention by green tea, and tertiary cancer prevention by the combination of green tea catechins and anticancer compounds[J]. J Cancer Prev , 2015, 20(1) : 1–4. DOI:10.15430/jcp.2015.20.1.1 |
| [16] | Hastak K, Gupta S, Ahmad N, et al. Role of p53 and NF-κB in epigallocatechin-3-gallate-induced apoptosis of LNCaP cells[J]. Oncogene , 2003, 22(31) : 4851–4859. DOI:10.1038/sj.onc.1206708 |
| [17] | Chen F, He B, Hu Z, et al. Passive smoking and cooking oil fumes (COF) may modify the association between tea consumption and oral cancer in Chinese women[J]. J Cancer Res Clin Oncol , 2016, 142(5) : 995–1001. DOI:10.1007/s00432-016-2123-6 |
| [18] | Ide R, Fujino Y, Hoshiyama Y, et al. A prospective study of green tea consumption and oral cancer incidence in Japan[J]. Ann Epidemiol , 2007, 17(10) : 821–826. DOI:10.1016/j.annepidem.2007.04.003 |
| [19] |
陈法, 蔡琳, 何保昌, 等.
饮茶与非吸烟、非饮酒人群口腔癌的关系研究[J]. 中华预防医学杂志 , 2015, 49(8) : 683–687.
Chan F, Cai L, He BC, et al. Effect of tea on oral cancer in nonsmokers and nondrinkers:a case-control study[J]. Chin J Prev Med , 2015, 49(8) : 683–687. DOI:10.3760/cma.j.issn.0253-9624.2015.08.004 |
| [20] | Mohan KV, Letchoumy PV, Hara Y, et al. Combination chemoprevention of hamster buccal pouch carcinogenesis by bovine milk lactoferrin and black tea polyphenols[J]. Cancer Invest , 2008, 26(2) : 193–201. DOI:10.1080/07357900701511961 |
| [21] | Bhattacharyya A, Lahiry L, Mandal D, et al. Black tea induces tumor cell apoptosis by Bax translocation, loss in mitochondrial transmembrane potential, cytochrome c release and caspase activation[J]. Int J Cancer , 2005, 117(2) : 308–315. DOI:10.1002/ijc.21075 |
| [22] | Mohan KVPC, Devaraj H, Prathiba D, et al. Antiproliferative and apoptosis inducing effect of lactoferrin and black tea polyphenol combination on hamster buccal pouch carcinogenesis[J]. Biochim Biophys Acta , 2006, 1760(10) : 1536–1544. DOI:10.1016/j.bbagen.2006.06.009 |
| [23] | Biazevic MGH, Toporcov TN, Antunes JLF, et al. Cumulative coffee consumption and reduced risk of oral and oropharyngeal cancer[J]. Nutr Cancer , 2011, 63(3) : 350–356. DOI:10.1080/01635581.2011.536065 |
 2016, Vol. 37
2016, Vol. 37